文档内容
专练 9 氧化还原反应基本概念
一、选择题
1.[2024·浙江 1 月]汽车尾气中的 NO 和 CO 在催化剂作用下发生反应:2NO+
2CO=====2CO+N,下列说法不正确的是(N 为阿伏加德罗常数的值)
2 2 A
A.生成1 mol CO 转移电子的数目为2N
2 A
B.催化剂降低NO与CO反应的活化能
C.NO是氧化剂,CO是还原剂
D.N 既是氧化产物又是还原产物
2
答案:D
解析:由题给方程式可知,1 mol CO失去2 mol e-生成1 mol CO ,故生成1 mol CO
2 2
时转移电子的数目为2N ,A项正确;催化剂可以降低反应的活化能,提高反应速率,B
A
项正确;NO中N为+2价,N 中N为0价,N元素的化合价降低,发生还原反应,则NO
2
作氧化剂,N 为还原产物,同理可得,CO作还原剂,CO 为氧化产物,C项正确、D项错
2 2
误。
2.[2024·全国乙卷]下列应用中涉及到氧化还原反应的是( )
A.使用明矾对水进行净化
B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热
D.荧光指示牌被照发光
答案:C
解析:使用明矾对水进行净化的过程中,明矾电离出的铝离子发生水解生成氢氧化铝
胶体,氢氧化铝胶体粒子吸附水中的悬浮颗粒并沉降下来而水变得澄清,该过程中没有任
何一种元素的化合价发生变化,因此没有涉及到氧化还原反应,A不符合题意;雪天道路
上撒盐融雪,是因为雪遇到盐而使其熔点降低并熔化,该过程中没有任何一种元素的化合
价发生变化,因此没有涉及到氧化还原反应,B不符合题意;使用暖贴时,铁粉与空气中
的O 发生氧化还原反应,C符合题意;荧光指示牌被照发光,没有涉及到氧化还原反应,
2
D不符合题意;综上所述,本题选C。
3.[2022·北京卷]下列物质混合后,因发生氧化还原反应使溶液pH减小的是( )
A.向NaHSO 溶液中加入少量BaCl 溶液,生成白色沉淀
4 2
B.向NaOH和Fe(OH) 的悬浊液中通入空气,生成红褐色沉淀
2
C.向NaHCO 溶液中加入少量CuSO 溶液,生成蓝绿色沉淀[Cu (OH)CO]
3 4 2 2 3
D.向HS溶液中通入氯气,生成黄色沉淀
2
答案:D
解析:向NaHSO 溶液中加入少量BaCl 溶液,发生反应NaHSO +BaCl ===BaSO ↓
4 2 4 2 4
+NaCl+HCl,为非氧化还原反应,且溶液pH不变,A项错误;向NaOH和Fe(OH) 的
2
悬浊液中通入空气,发生氧化还原反应 4Fe(OH) +2HO+O===4Fe(OH) ,c(OH
2 2 2 3
-)增大,pH增大,B项错误;向NaHCO 溶液中加入少量CuSO 溶液,发生反应2Cu2++
3 4
4HCO===Cu (OH) CO↓+HO+3CO↑,为非氧化还原反应,C项错误;向HS溶液
2 2 3 2 2 2
中通入氯气,发生氧化还原反应HS+Cl===2HCl+S↓,且c(H+)增大,pH减小,D
2 2
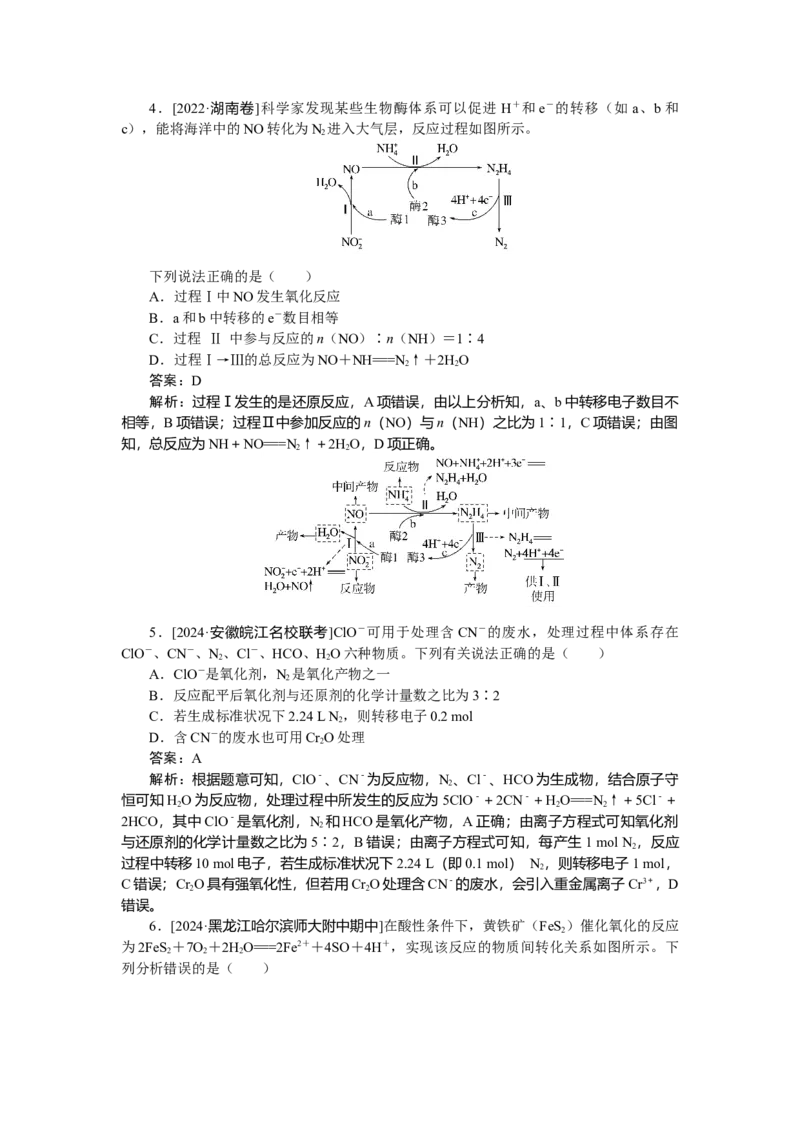
项正确。4.[2022·湖南卷]科学家发现某些生物酶体系可以促进 H+和e-的转移(如a、b和
c),能将海洋中的NO转化为N 进入大气层,反应过程如图所示。
2
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程 Ⅱ 中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N ↑+2HO
2 2
答案:D
解析:过程Ⅰ发生的是还原反应,A项错误,由以上分析知,a、b中转移电子数目不
相等,B项错误;过程Ⅱ中参加反应的n(NO)与n(NH)之比为1∶1,C项错误;由图
知,总反应为NH+NO===N ↑+2HO,D项正确。
2 2
5.[2024·安徽皖江名校联考]ClO-可用于处理含CN-的废水,处理过程中体系存在
ClO-、CN-、N、Cl-、HCO、HO六种物质。下列有关说法正确的是( )
2 2
A.ClO-是氧化剂,N 是氧化产物之一
2
B.反应配平后氧化剂与还原剂的化学计量数之比为3∶2
C.若生成标准状况下2.24 L N ,则转移电子0.2 mol
2
D.含CN-的废水也可用Cr O处理
2
答案:A
解析:根据题意可知,ClO-、CN-为反应物,N 、Cl-、HCO为生成物,结合原子守
2
恒可知HO为反应物,处理过程中所发生的反应为5ClO-+2CN-+HO===N ↑+5Cl-+
2 2 2
2HCO,其中ClO-是氧化剂,N 和HCO是氧化产物,A正确;由离子方程式可知氧化剂
2
与还原剂的化学计量数之比为5∶2,B错误;由离子方程式可知,每产生1 mol N ,反应
2
过程中转移10 mol电子,若生成标准状况下2.24 L(即0.1 mol) N ,则转移电子1 mol,
2
C错误;Cr O具有强氧化性,但若用Cr O处理含CN-的废水,会引入重金属离子Cr3+,D
2 2
错误。
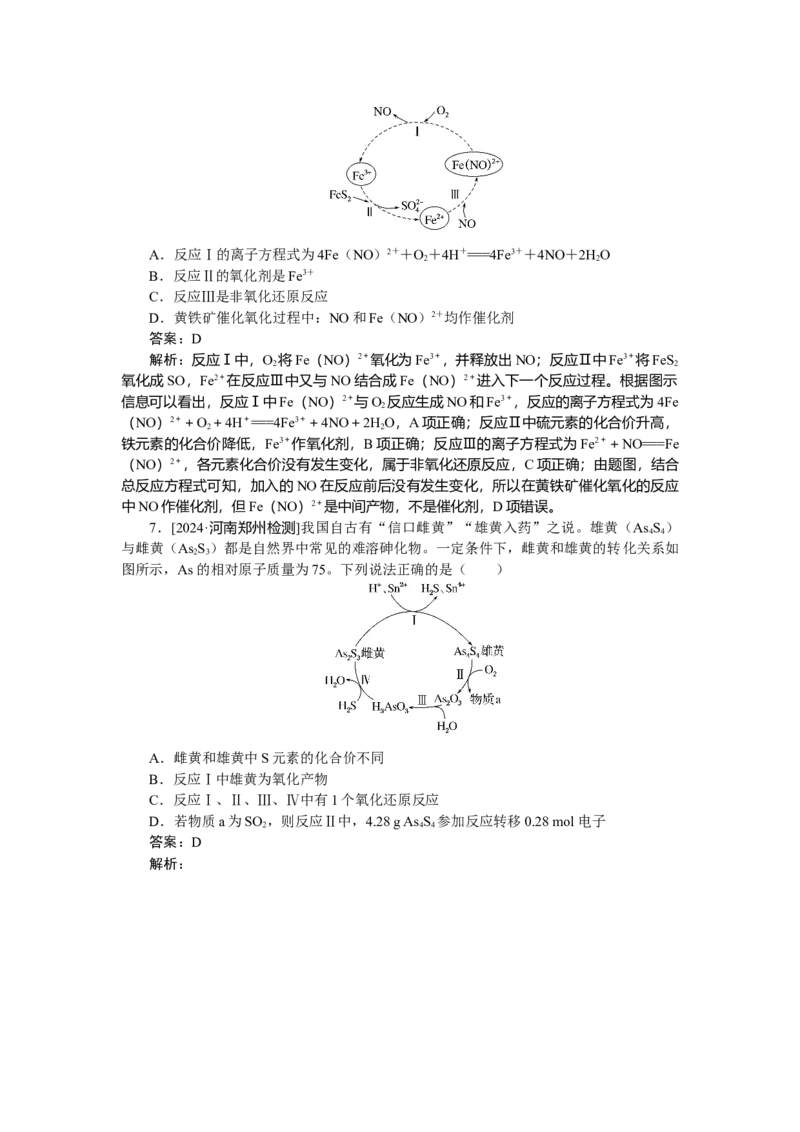
6.[2024·黑龙江哈尔滨师大附中期中]在酸性条件下,黄铁矿(FeS )催化氧化的反应
2
为2FeS +7O +2HO===2Fe2++4SO+4H+,实现该反应的物质间转化关系如图所示。下
2 2 2
列分析错误的是( )A.反应Ⅰ的离子方程式为4Fe(NO)2++O+4H+===4Fe3++4NO+2HO
2 2
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ⅲ是非氧化还原反应
D.黄铁矿催化氧化过程中:NO和Fe(NO)2+均作催化剂
答案:D
解析:反应Ⅰ中,O 将Fe(NO)2+氧化为Fe3+,并释放出NO;反应Ⅱ中Fe3+将FeS
2 2
氧化成SO,Fe2+在反应Ⅲ中又与NO结合成Fe(NO)2+进入下一个反应过程。根据图示
信息可以看出,反应Ⅰ中Fe(NO)2+与O 反应生成NO和Fe3+,反应的离子方程式为4Fe
2
(NO)2++O +4H+===4Fe3++4NO+2HO,A项正确;反应Ⅱ中硫元素的化合价升高,
2 2
铁元素的化合价降低,Fe3+作氧化剂,B项正确;反应Ⅲ的离子方程式为Fe2++NO===Fe
(NO)2+,各元素化合价没有发生变化,属于非氧化还原反应,C项正确;由题图,结合
总反应方程式可知,加入的NO在反应前后没有发生变化,所以在黄铁矿催化氧化的反应
中NO作催化剂,但Fe(NO)2+是中间产物,不是催化剂,D项错误。
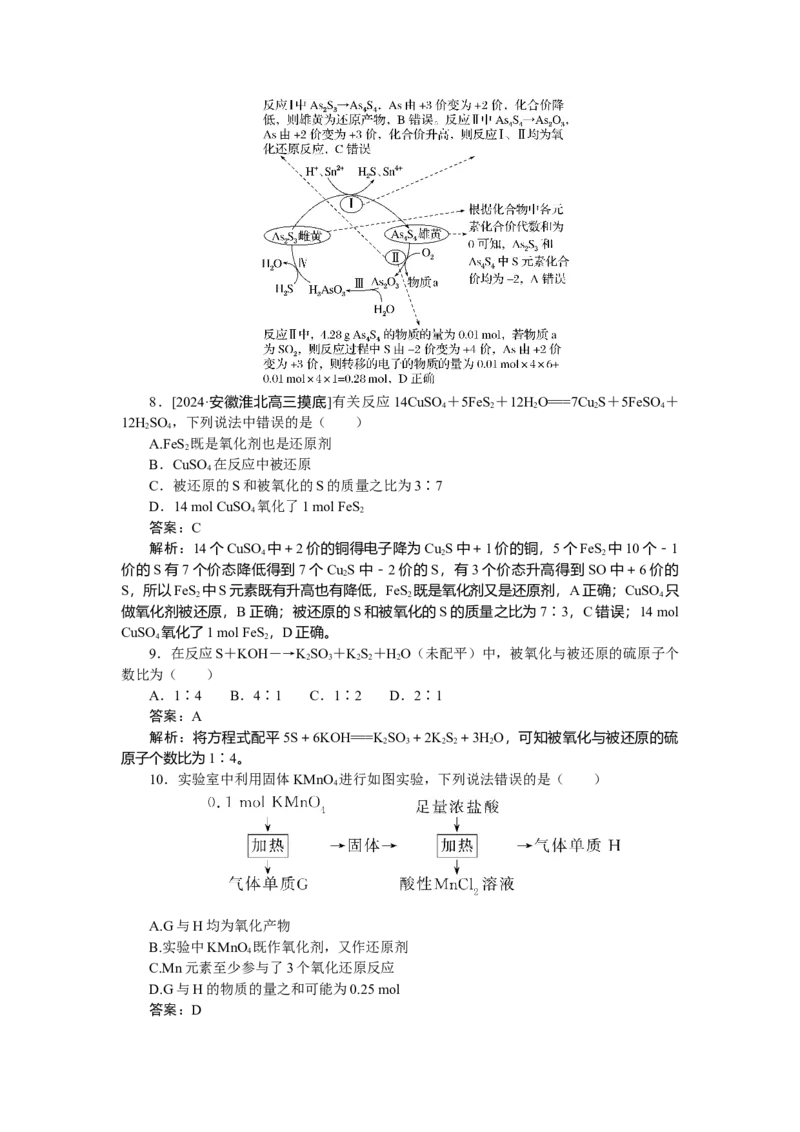
7.[2024·河南郑州检测]我国自古有“信口雌黄”“雄黄入药”之说。雄黄(As S )
4 4
与雌黄(As S )都是自然界中常见的难溶砷化物。一定条件下,雌黄和雄黄的转化关系如
2 3
图所示,As的相对原子质量为75。下列说法正确的是( )
A.雌黄和雄黄中S元素的化合价不同
B.反应Ⅰ中雄黄为氧化产物
C.反应Ⅰ、Ⅱ、Ⅲ、Ⅳ中有1个氧化还原反应
D.若物质a为SO ,则反应Ⅱ中,4.28 g As S 参加反应转移0.28 mol电子
2 4 4
答案:D
解析:8.[2024·安徽淮北高三摸底]有关反应14CuSO +5FeS +12HO===7Cu S+5FeSO +
4 2 2 2 4
12HSO ,下列说法中错误的是( )
2 4
A.FeS 既是氧化剂也是还原剂
2
B.CuSO 在反应中被还原
4
C.被还原的S和被氧化的S的质量之比为3∶7
D.14 mol CuSO 氧化了1 mol FeS
4 2
答案:C
解析:14个CuSO 中+2价的铜得电子降为Cu S中+1价的铜,5个FeS 中10个-1
4 2 2
价的S有7个价态降低得到7个Cu S中-2价的S,有3个价态升高得到SO中+6价的
2
S,所以FeS 中S元素既有升高也有降低,FeS 既是氧化剂又是还原剂,A正确;CuSO 只
2 2 4
做氧化剂被还原,B正确;被还原的S和被氧化的S的质量之比为7∶3,C错误;14 mol
CuSO 氧化了1 mol FeS ,D正确。
4 2
9.在反应S+KOH―→KSO +KS+HO(未配平)中,被氧化与被还原的硫原子个
2 3 2 2 2
数比为( )
A.1∶4 B.4∶1 C.1∶2 D.2∶1
答案:A
解析:将方程式配平5S+6KOH===K SO +2KS +3HO,可知被氧化与被还原的硫
2 3 2 2 2
原子个数比为1∶4。
10.实验室中利用固体KMnO 进行如图实验,下列说法错误的是( )
4
A.G与H均为氧化产物
B.实验中KMnO 既作氧化剂,又作还原剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25 mol
答案:D解析:KMnO 固体受热分解生成KMnO 、MnO 、O,KMnO 、MnO 均具有氧化性,
4 2 4 2 2 2 4 2
在加热条件下能与浓盐酸发生氧化还原反应,反应过程中Cl-被氧化为Cl,KMnO 、
2 2 4
MnO 被还原为MnCl ,因此气体单质G为O,气体单质H为Cl。加热KMnO 固体的反
2 2 2 2 4
应中,O元素化合价由-2升高至0被氧化,加热KMnO 、MnO 与浓盐酸的反应中,Cl
2 4 2
元素化合价由-1升高至0被氧化,因此O 和Cl 均为氧化产物,故A正确;KMnO 固体
2 2 4
受热分解过程中,Mn元素化合价降低被还原,部分O元素化合价升高被氧化,因此
KMnO 既是氧化剂也是还原剂,故B正确;Mn元素在反应过程中物质及化合价变化为
4
Mn元素至少参加了3个氧化还原反应,故C正确;每生成1 mol O 转移4 mol电子,
2
每生成1 mol Cl 转移2 mol电子,若KMnO 转化为MnCl 过程中得到的电子全部是Cl-生
2 4 2
成Cl 所失去的,则气体的物质的量最大,由2KMnO ~5Cl 可知,n(气体) =0.25
2 4 2 max
mol,但该气体中一定含有O,因此最终所得气体的物质的量小于0.25 mol,故D错误。
2
11.NaNO 是一种食品添加剂,它与酸性KMnO 溶液可发生反应:MnO+NO+
2 4
X―→Mn2++NO+HO(未配平)。下列叙述中正确的是( )
2
A.生成1 mol NaNO 需消耗0.4 mol KMnO
3 4
B.反应过程中溶液的pH减小
C.该反应中NO被还原
D.X可以是盐酸
答案:A
解析:反应过程中Mn从+7价被还原到+2价,N从+3价被氧化到+5价。根据得失
电子守恒可知反应中n(MnO)∶n(NO)=2∶5,根据反应前后电荷守恒、元素种类守
恒可知X为H+,将方程式配平可得方程式为:2MnO+5NO+6H+===2Mn2++5NO+
3HO。根据分析可知生成1 mol NaNO(即消耗1 mol NaNO)时需要消耗0.4 mol
2 3 2
KMnO ,A正确;反应进行的过程中消耗H+,pH增大, B错误;反应过程中NO化合价
4
升高,被氧化,C错误;若X为盐酸,在酸性条件下KMnO 会将Cl-氧化,反应式中产物
4
应出现Cl,与题目中条件不符,D错误。
2
12.已知:①SO +I+2HO===H SO +2HI;②向含有HCl、FeCl 和BaCl 的溶液中通
2 2 2 2 4 3 2
入足量的SO ,产生白色沉淀;③将FeCl 溶液滴在淀粉—KI试纸上,试纸变蓝色。现有
2 3
等物质的量的FeI、NaHSO 的混合溶液100 mL,向其中通入4.48 L(标准状况)氯气,然
2 3
后向反应后的溶液中滴加KSCN溶液,溶液呈微红色。下列有关说法正确的是( )
A.FeI 的物质的量浓度约为1 mol·L-1
2
B.完全反应时转移电子0.2 mol
C.通入氯气的过程中,首先被氧化的离子是Fe2+,最后被氧化的离子是I-
D.反应后,溶液中大量存在的离子有Na+、H+、SO和Fe3+
答案:A
解析:由①知,还原性强弱顺序为SO >I-;由②知,还原性强弱顺序为SO >Fe2+;由
2 2
③知,还原性强弱顺序为I->Fe2+,故还原性强弱顺序为SO >I->Fe2+,类比可得离子的还
2
原性强弱顺序为HSO>I->Fe2+。向混合溶液中通入Cl 的过程中,首先氧化HSO,然后氧
2化I-,最后氧化Fe2+,C错误;加入KSCN溶液,溶液呈微红色,说明有微量的Fe3+生成,
则有较多的Fe2+没有被氧化,D错误;HSO和I-均完全反应,Fe2+发生的反应可以忽略不
计,根据电子得失守恒得2n(FeI)+2n(NaHSO)=2×4.48 L÷22.4 L·mol-1,即n
2 3
(FeI)+n(NaHSO)=0.2 mol,由于溶质的物质的量相等,所以n(FeI)=0.1 mol,c
2 3 2
(FeI)=1 mol·L-1,A正确;转移电子的物质的量根据氯气计算得2×4.48 L÷22.4 L·mol
2
-1=0.4 mol,B错误;综上所述,本题选A。
13.将磁性氧化铁放入稀硝酸中可发生如下反应:3Fe O+28HNO===9Fe(NO )+
3 4 3 3 x
NO↑+14HO,下列判断合理的是( )
2
A.Fe(NO ) 中x为2
3 x
B.磁性氧化铁中的铁元素全部被氧化
C.稀硝酸在反应中只作氧化剂
D.反应中每生成0.4 mol还原产物,就有1.2 mol电子转移
答案:D
解析:根据氮元素守恒,则9x+1=28,解得x=3,A错误;反应中生成硝酸盐Fe
(NO ),磁性氧化铁中的铁元素化合价为+2、+3价,只有部分铁元素被氧化,B错误;
3 3
反应中生成硝酸盐Fe(NO ) 和NO,所以硝酸在反应中起氧化剂与酸的作用,C错误;
3 3
反应中只有氮元素被还原,氮元素化合价由+5价降低为+2价,还原产物为NO,所以生
成0.4 mol NO转移电子为0.4 mol×(5-2)=1.2 mol, D正确。
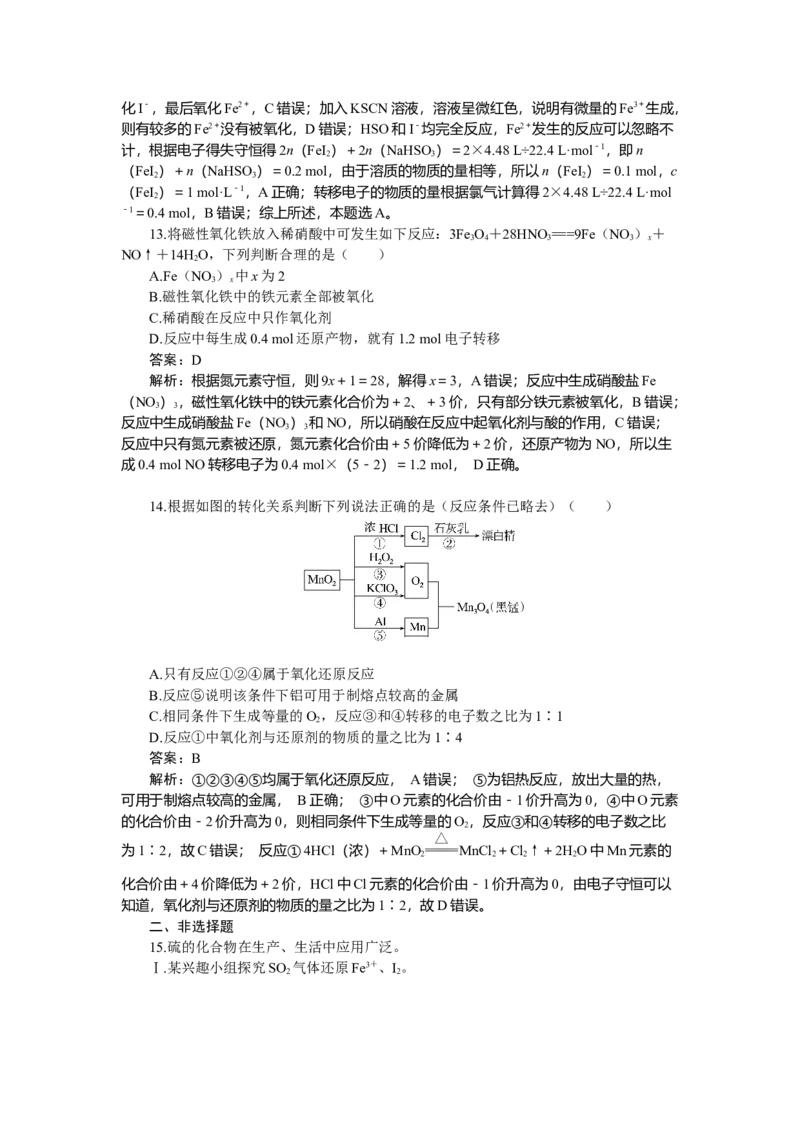
14.根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )
A.只有反应①②④属于氧化还原反应
B.反应⑤说明该条件下铝可用于制熔点较高的金属
C.相同条件下生成等量的O,反应③和④转移的电子数之比为1∶1
2
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
答案:B
解析:①②③④⑤均属于氧化还原反应, A错误; ⑤为铝热反应,放出大量的热,
可用于制熔点较高的金属, B正确; ③中O元素的化合价由-1价升高为0,④中O元素
的化合价由-2价升高为0,则相同条件下生成等量的O,反应③和④转移的电子数之比
2
为1∶2,故C错误; 反应①4HCl(浓)+MnO MnCl +Cl↑+2HO中Mn元素的
2 2 2 2
化合价由+4价降低为+2价,HCl中Cl元素的化合价由-1价升高为0,由电子守恒可以
知道,氧化剂与还原剂的物质的量之比为1∶2,故D错误。
二、非选择题
15.硫的化合物在生产、生活中应用广泛。
Ⅰ.某兴趣小组探究SO 气体还原Fe3+、I。
2 2(1)通入足量SO 后,装置B中的现象是
2
______________________________________;,装置C的作用是 。
(2)该小组同学认为SO 与FeCl 溶液发生的是氧化还原反应。
2 3
①写出SO 与FeCl 溶液反应的离子方程式:
2 3
________________________________________________________________________。
②请设计实验方案验证有Fe2+生成:
________________________________________________________________________。
Ⅱ.一些食品添加剂、抗氧化剂中含有焦亚硫酸钠(NaSO),大量的焦亚硫酸钠会损
2 2 5
伤细胞,具有生物毒性。
(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(NaSO)处理含铬酸性废
2 2 5
水(含有CrO),利用氧化还原反应,将六价铬还原为三价铬,SO被氧化为SO,该反应
2
中氧化剂与还原剂的物质的量之比为 。
(4)已知:NaSO 溶于水会生成NaHSO。检验NaSO 晶体在空气中已被氧化的实
2 2 5 3 2 2 5
验方法是_________________________________。
答案:
(1)溶液蓝色褪去 吸收多余的SO ,防止污染空气
2
(2)①2Fe3++SO +2HO===SO+2Fe2++4H+,②取A中反应后的溶液,向其中滴入
2 2
KSCN溶液,不变红,再加入新制的氯水,溶液变红(或其他合理答案)
(3)4∶3
(4)取少量NaSO 晶体于试管中,加入适量水溶解,滴入足量盐酸,振荡,再滴入
2 2 5
氯化钡溶液,有白色沉淀生成
解析:
(1)通入SO 后,与I 反应生成I-,所以蓝色消失;装置C是尾气处理装置。
2 2
(2)SO 与Fe3+反应生成SO和Fe2+,依据电荷守恒和原子守恒,即可写出方程式。
2
(3)CrO~Cr3+中Cr的化合价由+6到+3,得3 mol电子,SO~2SO中S的化合价
2
由+4到+6,失去4 mol电子,依据电荷守恒,CrO与SO的物质的量之比为4∶3。
2
(4) NaSO 晶体在空气中被氧化生成SO,滴入足量盐酸和氯化钡溶液,有白色沉
2 2 5
淀生成,证明NaSO 晶体被氧化。
2 2 5