文档内容
2010年潍坊市初中学业水平考试
化 学 试 题
2010.6
注意事项:
1.本试题分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。全卷满分为100分,考试时间
为90分钟。
2.答第1卷前务必将自己的姓名、准考证号、考试科目和试卷类型涂写在答题卡上。第Ⅰ
卷每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号(A、B、C、D)涂黑。如需改动,
必须先用橡皮擦干净,再改涂其它答案。
可能用到的相对原子质量:H1 C 12 N 14 O 16 Na 23 Mg 24 P 31 S 32
Cl 35.5 Fe 56 Zn 65
第Ⅰ卷 (选择题 共36分)
一、选择题 (本题包括18小题,每小题2分,共36分。每小题只有一个选项符合题意)
1.在我们的日常生活中涉及到许多变化。下列变化中不包含化学变化的是
A.用石灰浆涂抹墙壁后,表面有水珠生成
B.在口中咀嚼米饭或馒头时感到有甜味
C.用干冰做制冷剂进行人工降雨
D.绿色植物的光合作用
2.菜刀在生活中有重要应用。下列情况中,菜刀腐蚀由快到慢的是
①切青菜后用清水冲洗②切湿咸菜后未清洗③切肥猪肉后放置
A.①③② B.②①③ C.③①② D.③②①
3.物质的性质决定物质的用途。下列说法中,不合理的是
A.稀盐酸用于除铁锈 B.碳酸氢钠用于治疗胃酸过多
C.灯泡中充氮气以延长使用寿命 D.玻璃刀头上镶嵌的石墨用于切割玻璃
4.物质的分类非常重要。下列按酸、碱、盐的顺序排列的一组是
A.HSO、NaCO、NaCl B.Ca(OH) 、HCl、NaSO
2 4 2 3 2 2 4
C.NaOH、HCO、NaCl D.HSO、NaOH、NaCO
2 3 2 4 2 3
5.某品牌牛奶包装袋的营养成分表如下:
项目 每100g 营养参考值%
蛋白质 2.9g 5%
脂肪 3.6g 6%
碳水化合物 4.7g 2%
钠 60mg 3%
下列说法中,正确的是
A.脂肪是维持生命活动的重要供能物质
B.“碳水化合物”是指维生素,属于六大营养素之一
C.“钠”是指钠元素,其质量分数为60%
D.蛋白质是构成细胞的基本物质,它是由多种氨基酸混合组成
6.化学兴趣小组利用如图所示装置进行实验:打开弹簧夹,将液体 a滴入试
管①中与固体b接触,若试管②中的导管口没有气泡产生,则液体a和固
体b的组合可能是A.稀盐酸和碳酸钠 B.水和生石灰
C.锌和稀盐酸 D.水和硝酸铵
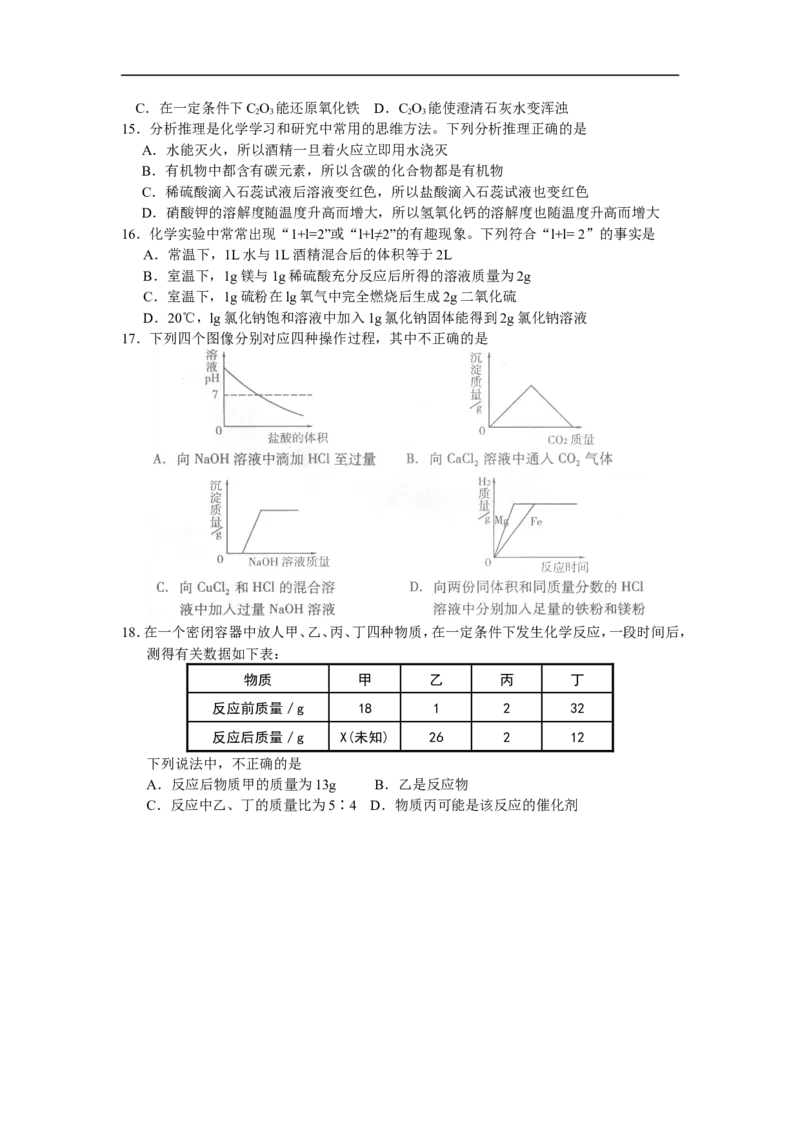
7.甲分子与乙分子反应生成丙分子的示意图如下:
下列说法中,不正确的是
A.物质甲是单质
B.丙分子中A、B原子个数比为3∶1
C.反应前后原子的个数没有改变,分子的个数也没有改变
D.根据质量守恒定律可推知,乙的化学式为A
2
8.下列实验操作或数据中,正确的是
9.物质X是一种重要的阻燃剂,工业上用三氧化二锑(Sb O)生产X,反应的化学方程式为:
2 3
Sb O+2H O=X+2H O(已配平),则X的化学式为
2 3 2 2 2
A.Sb O B.SbO C.HsbO D.HSbO
2 5 2 3 3 4
10.化学学习小组做实验时记录了下列实验现象,其中正确的是
A.细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成
B.红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
C.少量高锰酸钾固体溶于水可得到浅绿色溶液
D.在滴有石蕊的盐酸中逐滴加入氢氧化钠溶液,溶液颜色由蓝色逐渐变成红色
11.硫酸锰广泛用于医药、食品、造纸等行业。硫酸锰的溶解度曲
线如图所示。下列说法正确的是
A.硫酸锰的溶解度随温度的升高而增大
B.硫酸锰的溶解度随温度的升高而减小
C.100℃的硫酸锰饱和溶液升高温度时有晶体析出
D.硫酸锰饱和溶液的质量分数约为21.9%
12.通常情况下,下列选项中的两种物质之间不能发生化学反应的是
A.Cu与NaNO 溶液 B.CuO与稀HSO
3 2 4
C.稀HNO 与Mg(OH) D.NaCO 溶液与CaCl 溶液
3 2 2 3 2
13.鉴别下列各组物质,选用的试剂(在括号内)不合理的是
A.CO 和N(澄清石灰水)
2 2
B.Ca(OH) 溶液和NaOH溶液(稀盐酸)
2
C.NaOH溶液和稀HSO (pH试纸)
2 4
D.固体CaCO 和固体NaCO(水)
3 2 3
14.航天探测发现:金星是一个被浓密大气层包围的固体球,大气层的成分之一是三氧化二
碳(C O),实验证明它的化学性质与一氧化碳相似。下列关于三氧化二碳(C O)的说法中,不
2 3 2 3
正确的是
A.C O 中碳的化合价为+3价 B.C O 充分燃烧的产物是CO
2 3 2 3 2C.在一定条件下C O 能还原氧化铁 D.C O 能使澄清石灰水变浑浊
2 3 2 3
15.分析推理是化学学习和研究中常用的思维方法。下列分析推理正确的是
A.水能灭火,所以酒精一旦着火应立即用水浇灭
B.有机物中都含有碳元素,所以含碳的化合物都是有机物
C.稀硫酸滴入石蕊试液后溶液变红色,所以盐酸滴入石蕊试液也变红色
D.硝酸钾的溶解度随温度升高而增大,所以氢氧化钙的溶解度也随温度升高而增大
16.化学实验中常常出现“1+l=2”或“l+l≠2”的有趣现象。下列符合“l+l= 2”的事实是
A.常温下,1L水与1L酒精混合后的体积等于2L
B.室温下,1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
C.室温下,1g硫粉在lg氧气中完全燃烧后生成2g二氧化硫
D.20℃,lg氯化钠饱和溶液中加入1g氯化钠固体能得到2g氯化钠溶液
17.下列四个图像分别对应四种操作过程,其中不正确的是
18.在一个密闭容器中放人甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,
测得有关数据如下表:
物质 甲 乙 丙 丁
反应前质量/g 18 1 2 32
反应后质量/g X(未知) 26 2 12
下列说法中,不正确的是
A.反应后物质甲的质量为13g B.乙是反应物
C.反应中乙、丁的质量比为5∶4 D.物质丙可能是该反应的催化剂2010年潍坊市初中学业水平考试
化 学 试 题
2010.6
第Ⅱ卷 (非选择题 共64分)
注意:必须用蓝、黑色钢笔或圆珠笔答题,答案写在指定位置。
二、本题包括3小题(共34分)
19.(12分)2009年9月7日潍坊市政府与中国海洋石油总公司举行石油化工、盐化工一体
化工程启动仪式。石油化工生产中,可通过反应制得甲烷、乙烯、丙烯、苯等重要有机物。请回
答:
(1)有机物中都含有碳元素,碳元素的原子结构示意图是 。
(2)天然气(主要成分是甲烷)可做环保汽车的燃料,它完全燃烧的化学方程式是
。 可 燃 物 要 燃 烧 必 须 具 备 的 条 件 是
。
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下氮的氧
化物(用 NO 表示)与 CO 反应生成二氧化碳和氮气的化学方程式
x
。
(4)在一定条件下,丙烯(化学式为C H)像乙烯一样可以制得聚丙烯(缩写代号
3 8
PP)。上海世博会吉祥物海宝的填料是优质PP棉,聚丙烯属于 。
A.氧化物 B.聚合物 C.天然有机高分子材料
(5)自然界中消耗二氧化碳的主要途径是光合作用和海水吸收等,海水中的水与
二氧化碳反应的化学方程式是 ,用氢氧化钠溶液
吸收二氧化碳的化学方程式为 。
20.(12分)已知碱式碳酸铜[Cu (OH) CO]受热易分解、能与酸反应。孔雀石主要含
2 2 3
Cu (OH) CO ,还含少量 Fe、Si 的化合物。某学校化学研究小组以孔雀石为原料制备
2 2 3
CuSO ·5HO的流程如下:
4 2
请回答下列问题:
(1)流程中,X的化学式是 ;由溶液B获得CuSO·5HO,需要经过加热蒸发、
4 2
、过滤等操作。
(2) 若 通 过 置 换 反 应 由 溶 液 B 制 备 金 属 铜 , 反 应 的 化 学 方 程 式 是
。
若选用下列物质与氧化铜反应制备铜,写出反应的化学方程式:
①选用非金属单质 :
②选用氧化物 。
(3)工业上用焦炭在高温电炉中还原SiO:可得到含有少量杂质的Si和CO,反应的化学方程
式是
, 该反应类型为 。
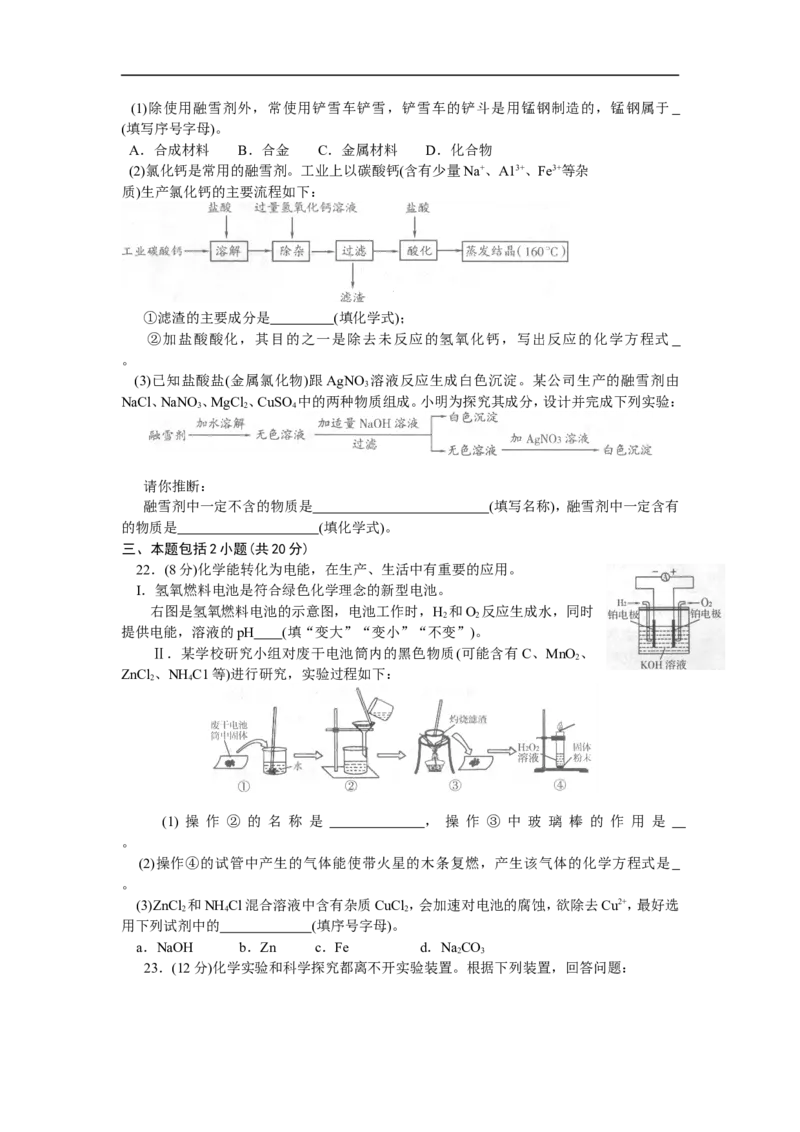
21.(10分)冬季,大雪覆盖路面,给交通造成很多麻烦,散撒融雪剂可以使雪很快融化,有效
地清除交通雪障。请回答:(1)除使用融雪剂外,常使用铲雪车铲雪,铲雪车的铲斗是用锰钢制造的,锰钢属于
(填写序号字母)。
A.合成材料 B.合金 C.金属材料 D.化合物
(2)氯化钙是常用的融雪剂。工业上以碳酸钙(含有少量Na+、A13+、Fe3+等杂
质)生产氯化钙的主要流程如下:
①滤渣的主要成分是 (填化学式);
②加盐酸酸化,其目的之一是除去未反应的氢氧化钙,写出反应的化学方程式
。
(3)已知盐酸盐(金属氯化物)跟AgNO 溶液反应生成白色沉淀。某公司生产的融雪剂由
3
NaCl、NaNO、MgCl 、CuSO 中的两种物质组成。小明为探究其成分,设计并完成下列实验:
3 2 4
请你推断:
融雪剂中一定不含的物质是 (填写名称),融雪剂中一定含有
的物质是 (填化学式)。
三、本题包括2小题(共20分)
22.(8分)化学能转化为电能,在生产、生活中有重要的应用。
I.氢氧燃料电池是符合绿色化学理念的新型电池。
右图是氢氧燃料电池的示意图,电池工作时,H 和O 反应生成水,同时
2 2
提供电能,溶液的pH (填“变大”“变小”“不变”)。
Ⅱ.某学校研究小组对废干电池筒内的黑色物质(可能含有C、MnO 、
2
ZnCl、NH C1等)进行研究,实验过程如下:
2 4
(1) 操 作 ② 的 名 称 是 , 操 作 ③ 中 玻 璃 棒 的 作 用 是
。
(2)操作④的试管中产生的气体能使带火星的木条复燃,产生该气体的化学方程式是
。
(3)ZnCl 和NH Cl混合溶液中含有杂质CuCl ,会加速对电池的腐蚀,欲除去Cu2+,最好选
2 4 2
用下列试剂中的 (填序号字母)。
a.NaOH b.Zn c.Fe d.NaCO
2 3
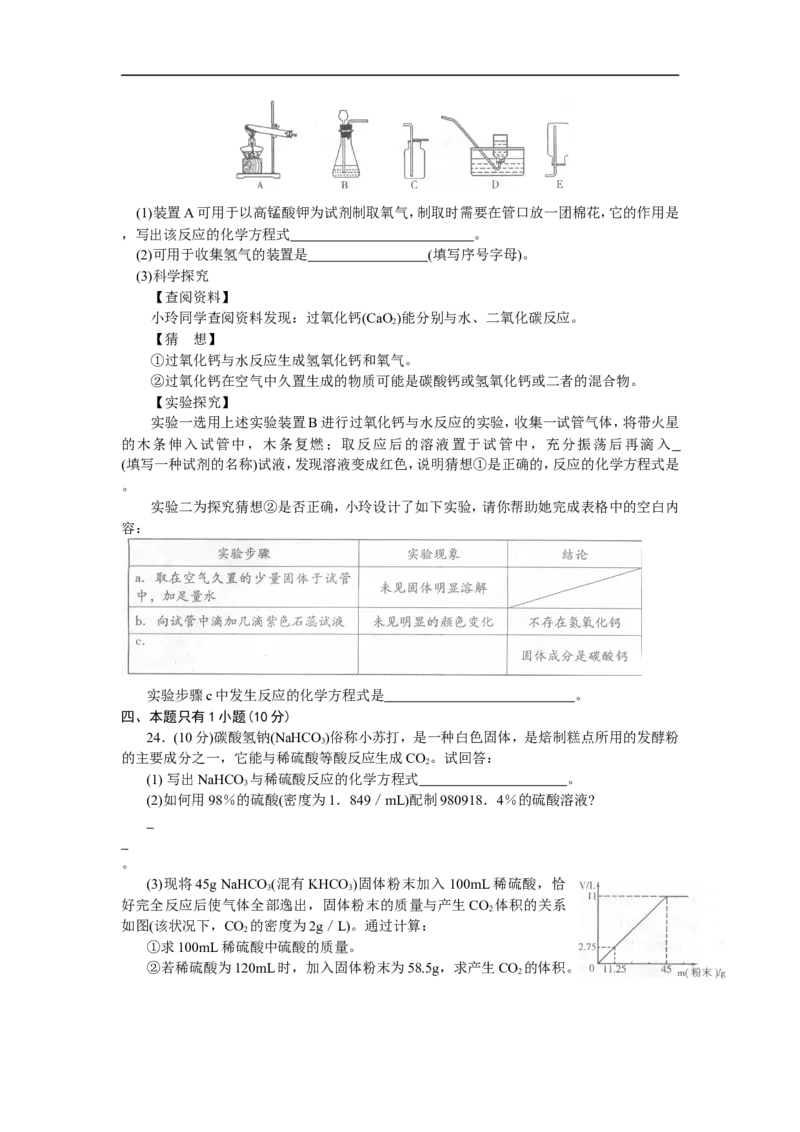
23.(12分)化学实验和科学探究都离不开实验装置。根据下列装置,回答问题:(1)装置A可用于以高锰酸钾为试剂制取氧气,制取时需要在管口放一团棉花,它的作用是
,写出该反应的化学方程式 。
(2)可用于收集氢气的装置是 (填写序号字母)。
(3)科学探究
【查阅资料】
小玲同学查阅资料发现:过氧化钙(CaO)能分别与水、二氧化碳反应。
2
【猜 想】
①过氧化钙与水反应生成氢氧化钙和氧气。
②过氧化钙在空气中久置生成的物质可能是碳酸钙或氢氧化钙或二者的混合物。
【实验探究】
实验一选用上述实验装置B进行过氧化钙与水反应的实验,收集一试管气体,将带火星
的木条伸入试管中,木条复燃;取反应后的溶液置于试管中,充分振荡后再滴入
(填写一种试剂的名称)试液,发现溶液变成红色,说明猜想①是正确的,反应的化学方程式是
。
实验二为探究猜想②是否正确,小玲设计了如下实验,请你帮助她完成表格中的空白内
容:
实验步骤c中发生反应的化学方程式是 。
四、本题只有1小题(10分)
24.(10分)碳酸氢钠(NaHCO )俗称小苏打,是一种白色固体,是焙制糕点所用的发酵粉
3
的主要成分之一,它能与稀硫酸等酸反应生成CO。试回答:
2
(1) 写出NaHCO 与稀硫酸反应的化学方程式 。
3
(2)如何用98%的硫酸(密度为1.849/mL)配制980918.4%的硫酸溶液?
。
(3)现将45g NaHCO(混有KHCO )固体粉末加入100mL稀硫酸,恰
3 3
好完全反应后使气体全部逸出,固体粉末的质量与产生CO 体积的关系
2
如图(该状况下,CO 的密度为2g/L)。通过计算:
2
①求100mL稀硫酸中硫酸的质量。
②若稀硫酸为120mL时,加入固体粉末为58.5g,求产生CO 的体积。
22010年潍坊市初中学业水平考试
化学试题(A)参考答案及评分标准
2010.6
说明:
1.化学专用名词出现错别字、元素符号有错误,都不得分。
2.化学方程式不配平、方程式中的化学式书写错误都不得分。化学方程式不写“↑”、
“↓”不扣分。
3.若考生在回答Ⅱ卷某些试题时出现其他答案,只要合理,表达清楚,同样给分。
第1卷 (选择题共36分)
一、选择题(每小题2分,共36分)
1.C 2.B 3.D 4.D 5.A 6.D 7.C 8.B 9.A
10.A 11.C 12.A 13.B 14.D 15.C 16.C 17.B 18.B
第Ⅱ卷(非选择题共64分)
二、本题包括3小题(共34分)
19.(12分)
(1) (1分)
点燃
(2)CH
4
+2O
2
CO
2
+2H
2
O(2分)
与氧气或空气接触(1分) 温度达到着火点(1分)
点燃
(3)2NO
2
+2xCO
2
N
2
+2XCO
2
(2分,无催化剂不扣分)
(4)B(1分)
(5)CO+H O == HCO(2分) 2NaOH+CO==NaCO+H O(2分)
2 2 2 3 2 2 3 2
20.(12分)
(1)H SO (2分) 冷却结晶(或结晶)(1分)
2 4
(2)Zn+CuSO==ZnSO+Cu(2分,其他合理答案也得分)
4 4
①2CuO+C 2Cu+CO↑或CuO+H △ C u+H O(2分)
2 2 2
②CuO+CO Cu+ CO↑(2分)
△ 2
(3)SiO+2C Si+2CO↑ (2分) 置换反应(1分)
2
21.(10分)
(1)BC(2分,每选对一项得1分,错选或多选不得分)
(2)①Al(OH) Fc(OH) (2分,每写对一项得1分,错写或多写不得分)
3 3
②Ca(OH) +2HCl==CaCl +2H O(2分)
2 2 2
(3)硫酸铜(2分) MgCl (2分)
2
三、本题包括2小题(共20分)
22.(8分)
I.变小(2分)Ⅱ.(1)过滤(1分) 搅拌,防止滤渣飞溅(迸溅)(1分) 转移固体(1分)
MnO 或催化剂
2
(2) 2HO ============= 2HO + O↑(2分)
2 2 2 2
(3)b(1分)
23.(12分)
(1)防止加热时高锰酸钾粉末进入导管(1分)
2KMnO △ K MnO +MnO+O ↑(2分)
4 2 4 2 2
(2)D E(2分,每选对一项得1分,错选或多选不得分)
(3)酚酞(1分) 2CaO+2H O=2Ca(OH) +O ↑(2分,未配平扣1分)
2 2 2 2
CaCO+2HCl=CaCl +CO↑+H O(2分)
3 2 2 2
四、本题只有1小题(10分)
24.(10分)
(1)2NaHCO+H SO=Na SO+2CO ↑+2H O(2分)
3 2 4 2 4 2 2
(2)将100mL98%的HSO 沿着烧杯内壁慢慢倒入796mL水中,同时用玻璃棒不断搅拌。
2 4
(得分要点:100mL浓硫酸得1分,796mL水得1分,浓HSO 倒入水中得1分,共3分)
2 4
(3)解:①m(CO) ==11L×2g/L=22 g(1分)
2
设硫酸溶液中HSO 的质量为x。
2 4
由(1)式得:HSO ~ 2CO
2 4 2
98 88
x 22g
x= (2分)
②与120mL稀HSO 完全反应的固体粉末的质量为y,
2 4
y=54g<58.5g
固体粉末过量,以硫酸的量进行计算:
V(CO)== (2分)
2
答:(略)