文档内容
2019 年四川省绵阳市中考化学试卷(教师版)
一、选择题(每小题3分,每个小题只有一个选项最符合题目要求)
1.(3分)化学对科技发展具有重要作用,下列说法错误的是( )
A.尖端技术采用液氮获得低温,利用了氮气的化学性质
B.用作新型电池电极材料的石墨烯与金刚石组成元素相同
C.中国具有自主知识产权的大飞机C919机身主体材料是铝合金
D.通过改变钢铁组成,表面覆盖保护层,可以确保港珠澳大桥使用寿命
【微点】常见气体的用途;合金与合金的性质;金属锈蚀的条件及其防护;碳元素组成
的单质.
【思路】A、根据液氮的温度低,进行分析判断。
B、根据石墨烯是碳元素形成的单质,进行分析判断。
C、根据合金的性质和用途,进行分析判断。
D、根据防止金属锈蚀的方法,进行分析判断。
【解析】解:A、液氮的温度低,尖端技术采用液氮获得低温,利用了氮气的物理性质,
故选项说法错误。
B、石墨烯是碳元素形成的单质,石墨烯与金刚石组成元素相同,故选项说法正确。
C、铝合金硬度大、强度高、密度小等,中国具有自主知识产权的大飞机C919机身主体
材料是铝合金,故选项说法正确。
D、通过改变钢铁组成,表面覆盖保护层,能防止钢铁生锈,可以确保港珠澳大桥使用
寿命,故选项说法正确。
故选:A。
【点拨】本题难度不大,掌握防止金属锈蚀的方法、合金的性质和用途等是正确解答本
题的关键。
2.(3分)冰毒是一种毒品。吸食初期有多语,对种种刺激过敏、焦躁、抑郁循环性病态。
继之,在幻听、幻视的错乱状态下,呈现被杀、被跟踪、嫉妒等多种妄想症,我们应该
远离毒品。某种冰毒的化学式为 C H NO Cl,下列关于该冰毒的说法正确的是
10 14 2
( )
A.是一种有机高分子化合物
B.相对分子质量为215.5 g
第 1 页 / 共 16 页C.N、H两种元素的质量分数相同
D.在空气中燃烧只生成CO 和H O
2 2
【微点】有机物的特征、分类及聚合物的特性;化学式的书写及意义;相对分子质量的
概念及其计算;元素的质量分数计算.
【思路】A.根据物质的相对分子质量来分析;
B.根据相对分子质量的单位来分析;
C.根据化合物中元素的质量比来分析;
D.根据物质的组成以及质量守恒定律来分析。
【解析】解:A.有机高分子化合物的相对分子质量大到几万、甚至几十万,而
C H NO Cl的相对分子质量为:12×10+1×14+14+16×2+35.5=215.5,所以不属于有机
10 14 2
高分子化合物,故错误;
B.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
C.C H NO Cl中,N、H两种元素的质量比为:14:(1×14)=1:1,所以N、H两
10 14 2
种元素的质量分数相同,故正确;
D.C H NO Cl中含有碳、氢、氮、氯、氧五种元素,所以在空气中燃烧除生成二氧
10 14 2
化碳和水以外,还会生成含氮、含氯的物质,故错误。
故选:C。
【点拨】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进
行分析问题、解决问题的能力。
3.(3分)下列关于资源、能源利用的说法正确的是( )
A.最理想的清洁、高能燃料是H
2
B.地球上水储量非常丰富,淡水资源取之不尽
C.我国稀土资源丰富,可随意开采
D.为快速提高人类生活质量,必须加速开采石油
【微点】水资源状况;金属元素的存在及常见的金属矿物;化石燃料及其综合利用;资
源综合利用和新能源开发.
【思路】A.根据氢气的特点来分析;
B.根据地球上的水资源储量来分析;
C.根据稀土资源来分析;
D.根据能源的利用来分析。
【解析】解:A.氢气的热值高、原料来源广、燃烧产物只有水,不会对环境造成任何
第 2 页 / 共 16 页污染,故正确;
B.地球上的水储量是丰富的,但人类能直接利用的淡水资源仅占全球水量的 0.3%,是
有限的,故产物;
C.我国稀土资源丰富,但是也不可随意开采,故错误;
D.大量使用石油会增加大气中二氧化碳的含量,造成温室效应,故错误。
故选:A。
【点拨】在能源和资源匮乏的今天,它既是社会热点,也是化学考查的热点,对于能源
主要侧重能源的分类、能源使用对环境的影响、新能源开发的技术和前景等;对于资源
主要考查贮存、开采状况,以及资源的保护。
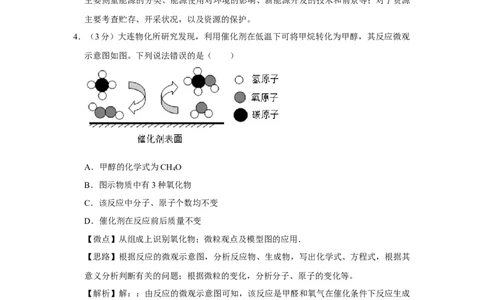
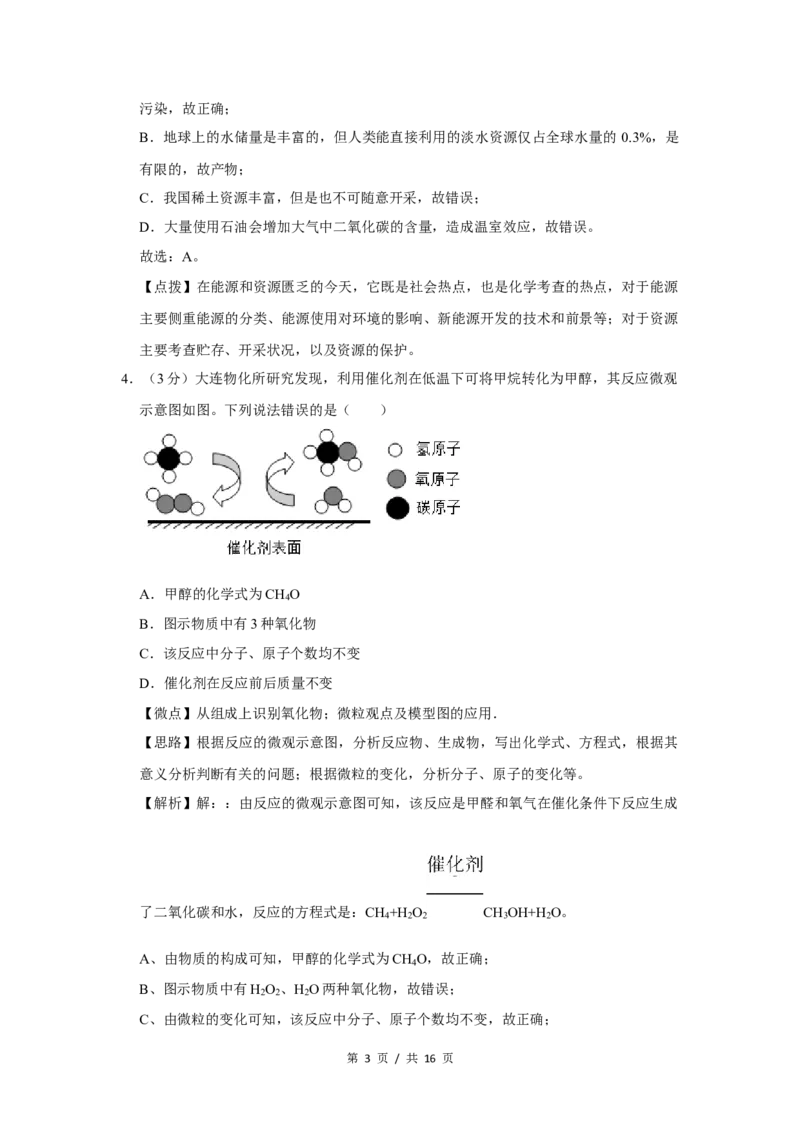
4.(3分)大连物化所研究发现,利用催化剂在低温下可将甲烷转化为甲醇,其反应微观
示意图如图。下列说法错误的是( )
A.甲醇的化学式为CH O
4
B.图示物质中有3种氧化物
C.该反应中分子、原子个数均不变
D.催化剂在反应前后质量不变
【微点】从组成上识别氧化物;微粒观点及模型图的应用.
【思路】根据反应的微观示意图,分析反应物、生成物,写出化学式、方程式,根据其
意义分析判断有关的问题;根据微粒的变化,分析分子、原子的变化等。
【解析】解::由反应的微观示意图可知,该反应是甲醛和氧气在催化条件下反应生成
了二氧化碳和水,反应的方程式是:CH +H O CH OH+H O。
4 2 2 3 2
A、由物质的构成可知,甲醇的化学式为CH O,故正确;
4
B、图示物质中有H O 、H O两种氧化物,故错误;
2 2 2
C、由微粒的变化可知,该反应中分子、原子个数均不变,故正确;
第 3 页 / 共 16 页D、催化剂在反应前后质量不变,故正确;
故选:B。
【点拨】本题为化学反应的微观模型表示,完成此题,关键是根据图示得出有关反应的
化学方程式,然后根据已有的知识进行。
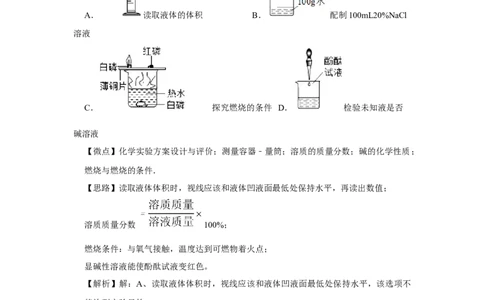
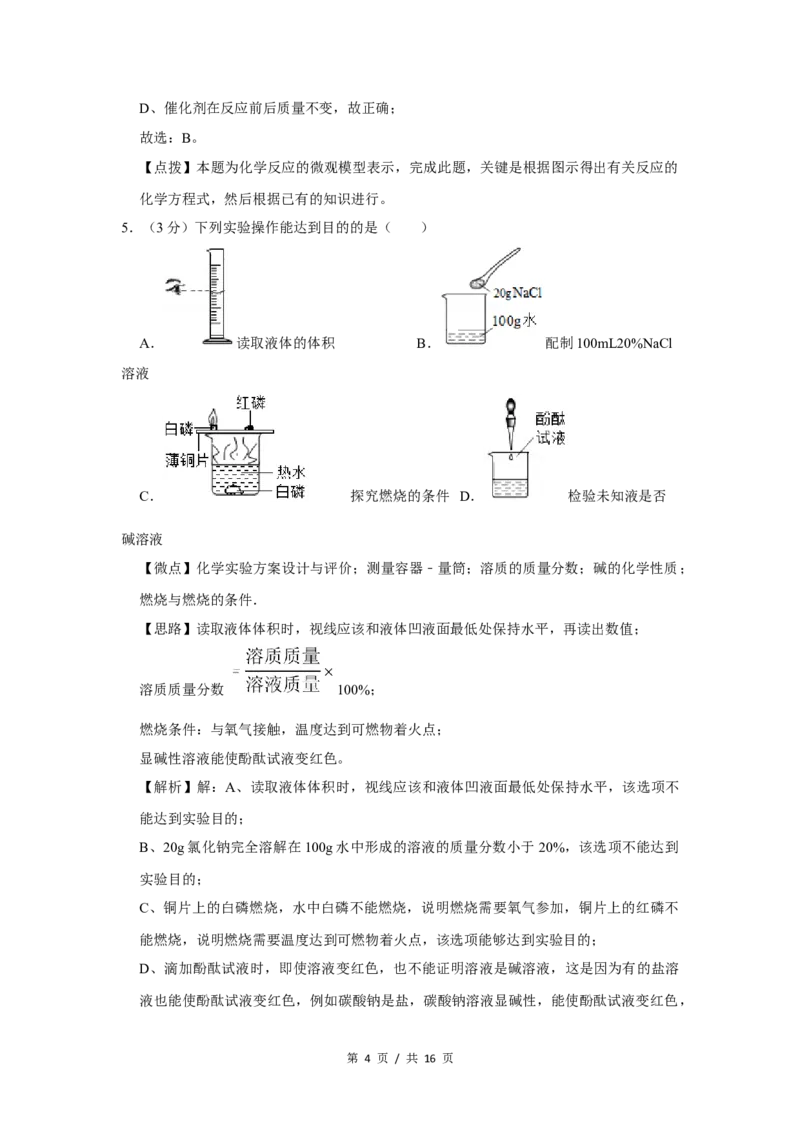
5.(3分)下列实验操作能达到目的的是( )
A. 读取液体的体积 B. 配制100mL20%NaCl
溶液
C. 探究燃烧的条件 D. 检验未知液是否
碱溶液
【微点】化学实验方案设计与评价;测量容器﹣量筒;溶质的质量分数;碱的化学性质;
燃烧与燃烧的条件.
【思路】读取液体体积时,视线应该和液体凹液面最低处保持水平,再读出数值;
溶质质量分数 100%;
燃烧条件:与氧气接触,温度达到可燃物着火点;
显碱性溶液能使酚酞试液变红色。
【解析】解:A、读取液体体积时,视线应该和液体凹液面最低处保持水平,该选项不
能达到实验目的;
B、20g氯化钠完全溶解在100g水中形成的溶液的质量分数小于20%,该选项不能达到
实验目的;
C、铜片上的白磷燃烧,水中白磷不能燃烧,说明燃烧需要氧气参加,铜片上的红磷不
能燃烧,说明燃烧需要温度达到可燃物着火点,该选项能够达到实验目的;
D、滴加酚酞试液时,即使溶液变红色,也不能证明溶液是碱溶液,这是因为有的盐溶
液也能使酚酞试液变红色,例如碳酸钠是盐,碳酸钠溶液显碱性,能使酚酞试液变红色,
第 4 页 / 共 16 页该选项不能达到实验目的。
故选:C。
【点拨】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
6.(3分)高铁酸钾(K FeO )可用于净水,也可用作电池的电极材料,可通过下列反应
2 4
制备:
MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2
①
3Cl +2Fe(OH) +xKOH═2K FeO +6KCl+yH O
2 3 2 4 2
②下列说法正确的是( )
A.在反应 中,氯的化合价全部发生了改变
B.反应 ①中x=10,y=6
C.反应② 中共涉及了5种类型的化合物
D.上述①反应②不属于四种基本反应类型中的任何一种
【微点】单质和化合物的判别;物质的相互转化和制备.
【思路】A、根据化合价原则分析;
B、根据质量守恒定律分析判断;
C、根据物质的组成分析;
D、根据反应的特点分析。
【解析】解:A、在反应 中,在HCl、MnCl 、Cl 中氯的化合价分别为﹣1、﹣1、
2 2
0,没有全部发生了改变,①故A错误;
B、由质量守恒定律可知,反应 中x=10,y=8,故B错误;
C、反应 中共涉及了酸、碱②、盐、氧化物4种类型的化合物,故C错误;
D、由反①应的②特点可知,上述反应不属于四种基本反应类型中的任何一种,故D正确。
故选:D。
【点拨】本题通过两个方程式考查了化合价原则、质量守恒定律、物质的分类和反应的
基本类型,涉及的知识点较多,理解化学方程式的意义是解答的基础。
7.(3分)根据如图所示溶解度曲线判断,下列说法正确的是( )
第 5 页 / 共 16 页A.28℃时,将40 g KNO 溶于100 g水得到饱和溶液
3
B.将43℃的Na CO 饱和溶液升高10℃,有晶体析出
2 3
C.三种物质的饱和溶液由40℃降温至23℃,所得溶液中溶质质量:m(NaCl)=m
(KNO )>m(Na CO )
3 2 3
D.除去KNO 中混有的Na CO ,可在40℃配成饱和溶液,再降温结晶、过滤
3 2 3
【微点】固体溶解度曲线及其作用;晶体和结晶的概念与现象.
【思路】根据固体的溶解度曲线可以: 查出某物质在一定温度下的溶解度,从而确定
物质的溶解性, 比较不同物质在同一①温度下的溶解度大小,从而判断饱和溶液中溶质
的质量分数的大小②, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结
晶还是蒸发结晶的方法③达到提纯物质的目的。
【解析】解:A、28℃时,硝酸钾的溶解度大于40g,所以将40 g KNO 溶于100 g水
3
得到不饱和溶液,故A错误;
B、将43℃的Na CO 饱和溶液升高10℃,溶解度减小,所以有晶体析出,故B正确;
2 3
C、三种物质的饱和溶液的质量不能确定,所以由40℃降温至23℃,所得溶液中溶质质
量也不能确定,故C错误;
D、低于40℃时,碳酸钠、硝酸钾的溶解度受温度的变化影响都比较大,所以除去
KNO 中混有的Na CO ,可在40℃配成饱和溶液,再降温结晶、过滤的方法不能除杂,
3 2 3
故D错误。
故选:B。
【点拨】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体
的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
8.(3分)向一定质量的AgNO 、Fe(NO ) 混合溶液中加入a g Zn粉,充分反应后过
3 3 2
滤,将滤渣洗涤、干燥、称量,所得质量仍为a g.下列说法正确的是( )
A.滤液一定呈无色
B.滤液中一定含Fe(NO ) 和Zn(NO )
3 2 3 2
C.滤渣中一定含Fe
第 6 页 / 共 16 页D.滤渣滴加稀盐酸一定无气泡产生
【微点】金属的化学性质.
【思路】金属活动性顺序中,排在氢前面的金属,能和稀盐酸或稀硫酸反应生成盐和氢
气,排在前面的金属,能把排在后面的金属从它的盐溶液中置换出来。
【解析】解:锌和硝酸银反应生成硝酸锌和银,反应后固体质量增大,和硝酸亚铁反应
生成硝酸锌和铁,反应后固体质量减小,将滤渣洗涤、干燥、称量,所得质量仍为 ag,
说明硝酸银完全反应,硝酸亚铁部分或全部反应;
A、硝酸亚铁不一定完全反应,如果硝酸亚铁部分反应,则滤液是浅绿色的,该选项说
法不正确;
B、滤液中一定含有硝酸锌,不一定含有硝酸亚铁,该选项说法不正确;
C、硝酸亚铁参加了反应,因此滤渣中一定含有铁,该选项说法正确;
D、滤渣中含有铁,滴加稀盐酸时,反应生成氢气,产生气泡,该选项说法不正确。
故选:C。
【点拨】要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但
氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换
出来。
9.(3分)我国古代将赤铜(Cu O)、炉甘石(ZnCO )和木炭混合加热到800℃得到黄
2 3
铜(铜锌合金)。若冶炼时所用Cu O与ZnCO 的质量比为26:25,则所得黄铜的含铜
2 3
量为( )
A.67.5% B.51% C.65% D.64%
【微点】根据化学反应方程式的计算.
【思路】根据Cu O与ZnCO 的质量比计算分子个数比,进一步计算黄铜的含铜量。
2 3
【解析】解:设Cu O与ZnCO 的个数比为x:y
2 3
则(64×2+16)x:(65+12+16×3)y=26:25
x:y=65:72
由质量守恒定律可知,Cu O转化为铜,ZnCO 转化为锌,
2 3
所得黄铜的含铜量为 100%=64%
故选:D。
【点拨】本题考查了根据质量守恒定律的计算,完成此题,可以依据已有的知识结合物
质的性质进行。
第 7 页 / 共 16 页二、(本题包括2小题,共15分)
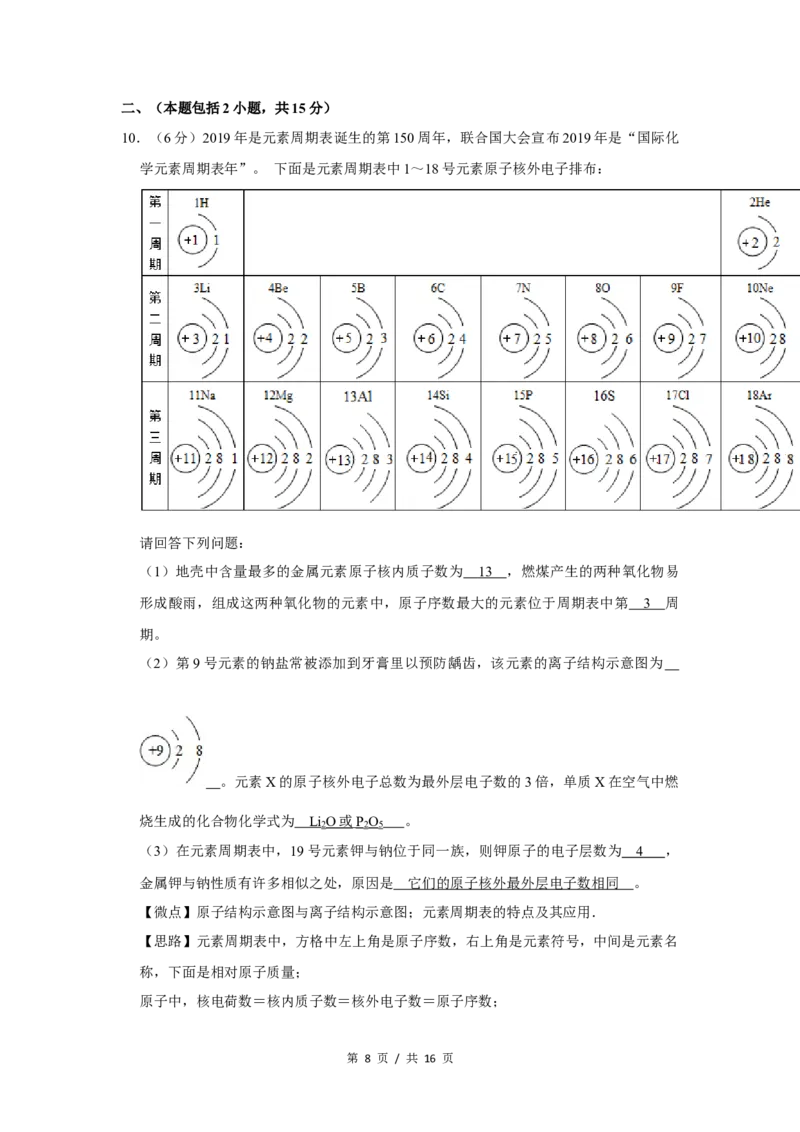
10.(6分)2019年是元素周期表诞生的第150周年,联合国大会宣布2019年是“国际化
学元素周期表年”。 下面是元素周期表中1~18号元素原子核外电子排布:
请回答下列问题:
(1)地壳中含量最多的金属元素原子核内质子数为 13 ,燃煤产生的两种氧化物易
形成酸雨,组成这两种氧化物的元素中,原子序数最大的元素位于周期表中第 3 周
期。
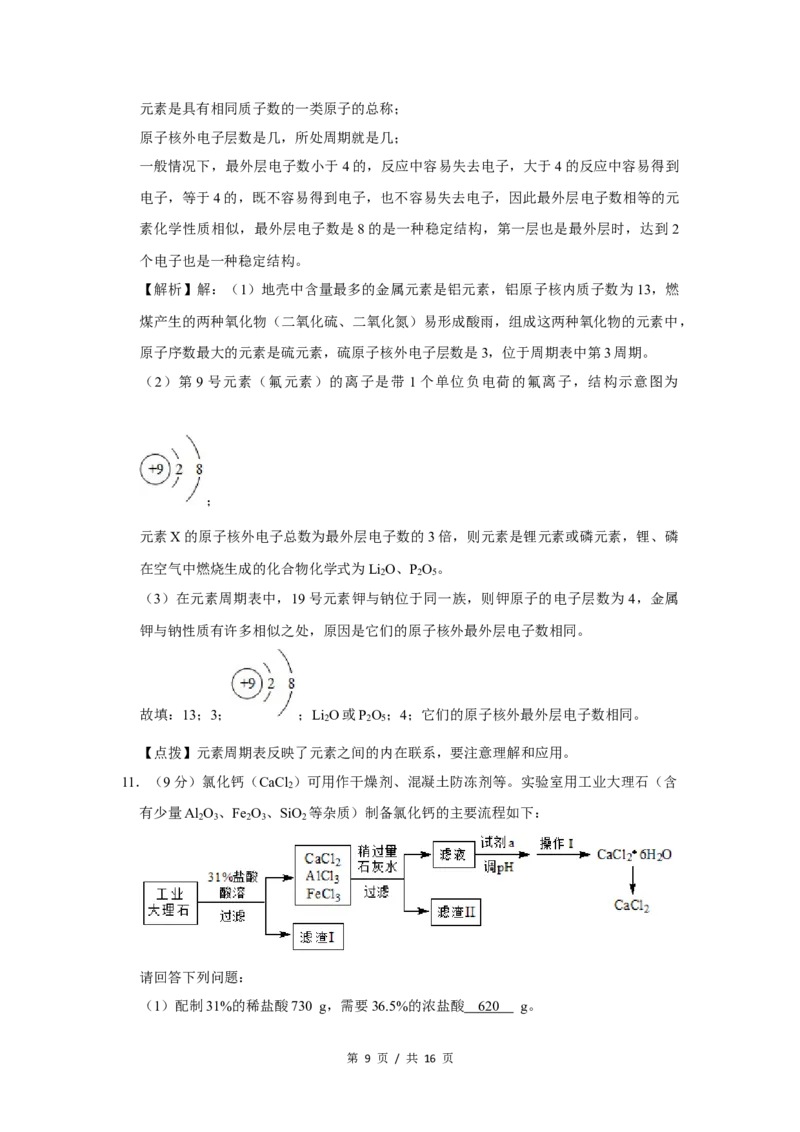
(2)第9号元素的钠盐常被添加到牙膏里以预防龋齿,该元素的离子结构示意图为
。元素X的原子核外电子总数为最外层电子数的3倍,单质X在空气中燃
烧生成的化合物化学式为 L i O 或 P O 。
2 2 5
(3)在元素周期表中,19号元素钾与钠位于同一族,则钾原子的电子层数为 4 ,
金属钾与钠性质有许多相似之处,原因是 它们的原子核外最外层电子数相同 。
【微点】原子结构示意图与离子结构示意图;元素周期表的特点及其应用.
【思路】元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名
称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
第 8 页 / 共 16 页元素是具有相同质子数的一类原子的总称;
原子核外电子层数是几,所处周期就是几;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到
电子,等于4的,既不容易得到电子,也不容易失去电子,因此最外层电子数相等的元
素化学性质相似,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到 2
个电子也是一种稳定结构。
【解析】解:(1)地壳中含量最多的金属元素是铝元素,铝原子核内质子数为13,燃
煤产生的两种氧化物(二氧化硫、二氧化氮)易形成酸雨,组成这两种氧化物的元素中,
原子序数最大的元素是硫元素,硫原子核外电子层数是3,位于周期表中第3周期。
(2)第9号元素(氟元素)的离子是带 1个单位负电荷的氟离子,结构示意图为
;
元素X的原子核外电子总数为最外层电子数的3倍,则元素是锂元素或磷元素,锂、磷
在空气中燃烧生成的化合物化学式为Li O、P O 。
2 2 5
(3)在元素周期表中,19号元素钾与钠位于同一族,则钾原子的电子层数为 4,金属
钾与钠性质有许多相似之处,原因是它们的原子核外最外层电子数相同。
故填:13;3; ;Li O或P O ;4;它们的原子核外最外层电子数相同。
2 2 5
【点拨】元素周期表反映了元素之间的内在联系,要注意理解和应用。
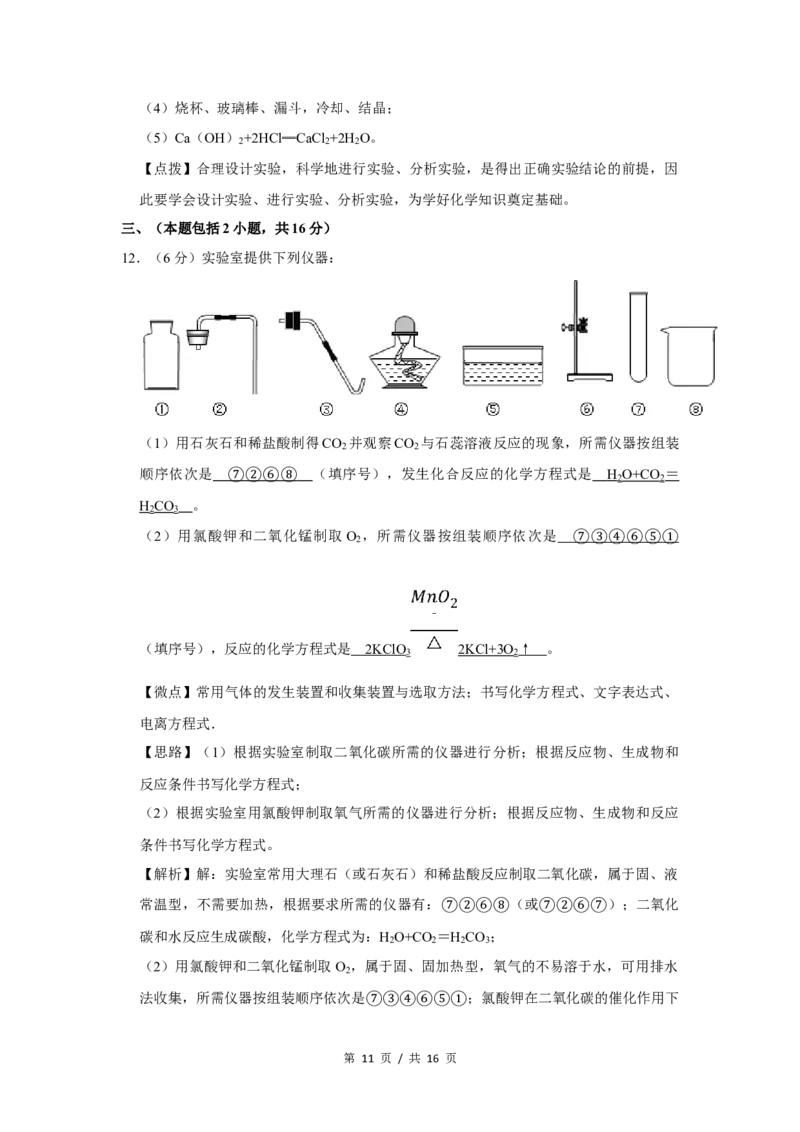
11.(9分)氯化钙(CaCl )可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含
2
有少量Al O 、Fe O 、SiO 等杂质)制备氯化钙的主要流程如下:
2 3 2 3 2
请回答下列问题:
(1)配制31%的稀盐酸730 g,需要36.5%的浓盐酸 62 0 g。
第 9 页 / 共 16 页(2)酸溶时碳酸钙参与反应的化学方程式为 CaCO +2HCl ═ CaCl +CO ↑ +H O 。
3 2 2 2
(3)滤渣I的成分为 SiO ,滤渣II中含有Al(OH) 和 F e ( OH ) 。
2 3 3
(4)过滤使用到的玻璃仪器有 烧杯、玻璃棒、漏斗 。操作I采用的方法是:蒸发浓
缩、 冷却 、 结晶 、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为 C a ( OH )
+2HCl ═ CaCl +2H O 。
2 2 2
【微点】用水稀释改变浓度的方法;物质的相互转化和制备;书写化学方程式、文字表
达式、电离方程式.
【思路】(1)根据溶液稀释前后,溶质质量不变进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据金属氧化物会与酸反应生成盐和水,二氧化硅不会与酸反应,氯化铝和氢氧
化钙反应生成氢氧化铝,氯化铁和氢氧化钙反应生成氢氧化铁沉淀进行分析;
(4)根据过滤使用到的玻璃仪器有:烧杯、漏斗、玻璃棒,操作I采用的方法是:蒸发
浓缩、冷却结晶、过滤进行分析;
(5)根据氢氧化钙和盐酸反应生成氯化钙和水进行分析。
【解析】解:(1)溶液稀释前后,溶质质量不变,所以需要 36.5%的浓盐酸
620g;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:
CaCO +2HCl═CaCl +CO ↑+H O;
3 2 2 2
(3)金属氧化物会与酸反应生成盐和水,二氧化硅不会与酸反应,氯化铝和氢氧化钙
反应生成氢氧化铝,氯化铁和氢氧化钙反应生成氢氧化铁沉淀,所以滤渣 I的成分为
SiO ,滤渣II中含有Al(OH) 和Fe(OH) ;
2 3 3
(4)过滤使用到的玻璃仪器有:烧杯、漏斗、玻璃棒,操作I采用的方法是:蒸发浓缩、
冷却、结晶、过滤;
(5)氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为: Ca(OH)
+2HCl═CaCl +2H O。
2 2 2
故答案为:(1)620;
(2)CaCO +2HCl═CaCl +CO ↑+H O;
3 2 2 2
(3)SiO ,Fe(OH) ;
2 3
第 10 页 / 共 16 页(4)烧杯、玻璃棒、漏斗,冷却、结晶;
(5)Ca(OH) +2HCl═CaCl +2H O。
2 2 2
【点拨】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因
此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。
三、(本题包括2小题,共16分)
12.(6分)实验室提供下列仪器:
(1)用石灰石和稀盐酸制得CO 并观察CO 与石蕊溶液反应的现象,所需仪器按组装
2 2
顺序依次是 (填序号),发生化合反应的化学方程式是 H O+CO =
2 2
H CO 。 ⑦②⑥⑧
2 3
(2)用氯酸钾和二氧化锰制取O ,所需仪器按组装顺序依次是
2
⑦③④⑥⑤①
(填序号),反应的化学方程式是 2KClO 2KCl+3O ↑ 。
3 2
【微点】常用气体的发生装置和收集装置与选取方法;书写化学方程式、文字表达式、
电离方程式.
【思路】(1)根据实验室制取二氧化碳所需的仪器进行分析;根据反应物、生成物和
反应条件书写化学方程式;
(2)根据实验室用氯酸钾制取氧气所需的仪器进行分析;根据反应物、生成物和反应
条件书写化学方程式。
【解析】解:实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,属于固、液
常温型,不需要加热,根据要求所需的仪器有: (或 );二氧化
碳和水反应生成碳酸,化学方程式为:H O+CO =⑦H②CO⑥;⑧ ⑦②⑥⑦
2 2 2 3
(2)用氯酸钾和二氧化锰制取O ,属于固、固加热型,氧气的不易溶于水,可用排水
2
法收集,所需仪器按组装顺序依次是 ;氯酸钾在二氧化碳的催化作用下
⑦③④⑥⑤①
第 11 页 / 共 16 页加热生成氯化钾和氧气,化学方程式为:2KClO 2KCl+3O ↑。
3 2
故答案为:
(1) (或 ); H O+CO =H CO ;
2 2 2 3
⑦②⑥⑧ ⑦②⑥⑦
(2) ;2KClO 2KCl+3O ↑。
3 2
⑦③④⑥⑤①
【点拨】本题主要考查了实验室气体的制取,熟练掌握气体的制取原理,了解确定发生
装置、收集装置的因素和注意事项等知识是解答本题的关键。
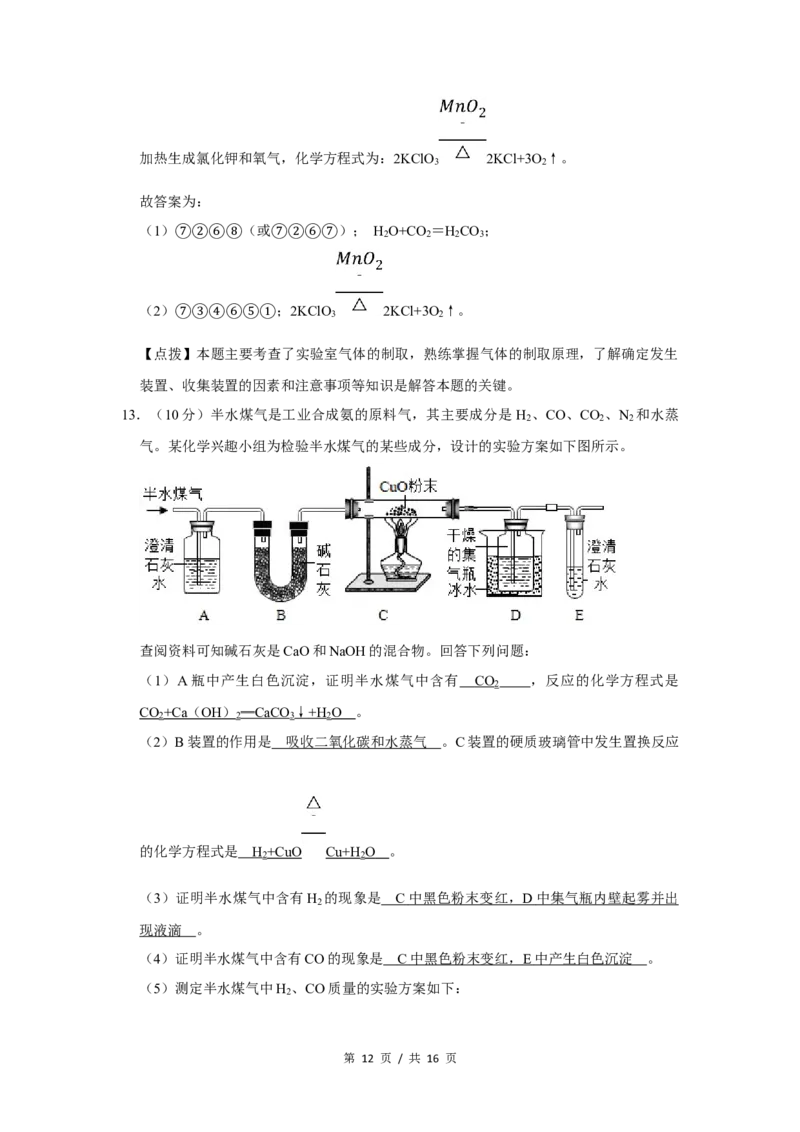
13.(10分)半水煤气是工业合成氨的原料气,其主要成分是 H 、CO、CO 、N 和水蒸
2 2 2
气。某化学兴趣小组为检验半水煤气的某些成分,设计的实验方案如下图所示。
查阅资料可知碱石灰是CaO和NaOH的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,证明半水煤气中含有 CO ,反应的化学方程式是
2
CO +Ca ( OH ) ═ CaCO ↓ +H O 。
2 2 3 2
(2)B装置的作用是 吸收二氧化碳和水蒸气 。C装置的硬质玻璃管中发生置换反应
的化学方程式是 H +CuO Cu+H O 。
2 2
(3)证明半水煤气中含有H 的现象是 C 中黑色粉末变红, D 中集气瓶内壁起雾并出
2
现液滴 。
(4)证明半水煤气中含有CO的现象是 C 中黑色粉末变红, E 中产生白色沉淀 。
(5)测定半水煤气中H 、CO质量的实验方案如下:
2
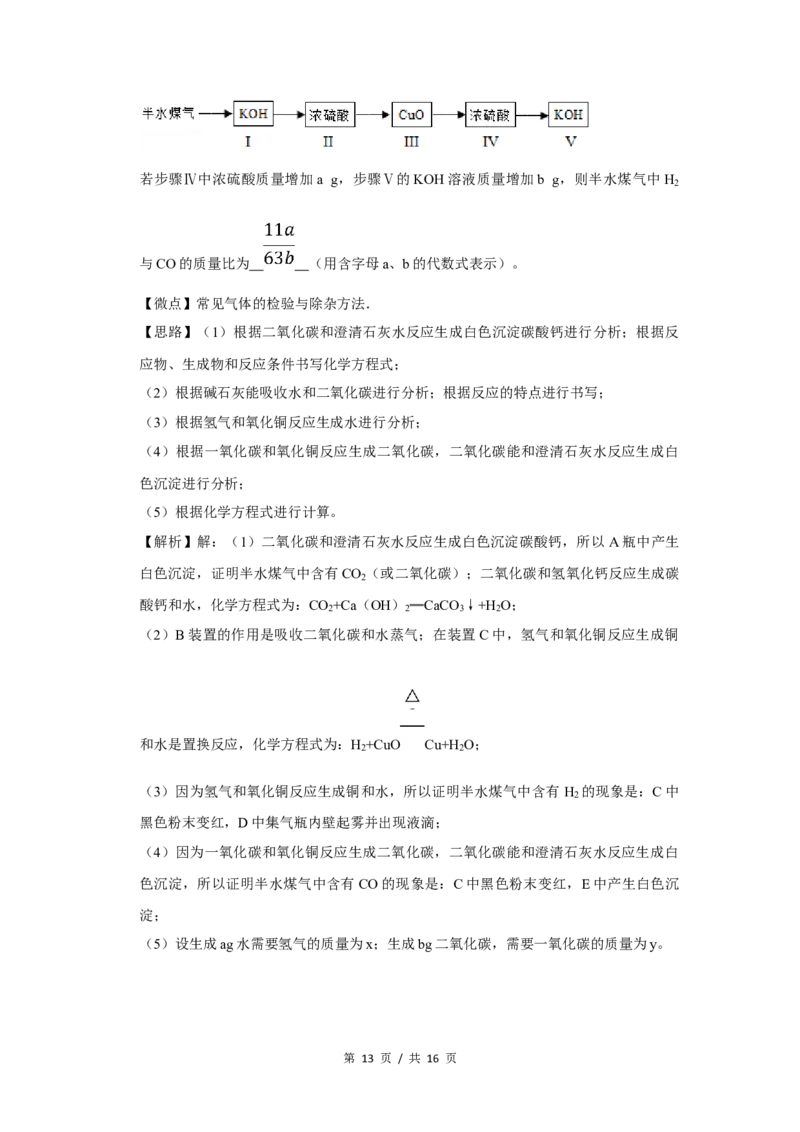
第 12 页 / 共 16 页若步骤Ⅳ中浓硫酸质量增加a g,步骤Ⅴ的KOH溶液质量增加b g,则半水煤气中H
2
与CO的质量比为 (用含字母a、b的代数式表示)。
【微点】常见气体的检验与除杂方法.
【思路】(1)根据二氧化碳和澄清石灰水反应生成白色沉淀碳酸钙进行分析;根据反
应物、生成物和反应条件书写化学方程式;
(2)根据碱石灰能吸收水和二氧化碳进行分析;根据反应的特点进行书写;
(3)根据氢气和氧化铜反应生成水进行分析;
(4)根据一氧化碳和氧化铜反应生成二氧化碳,二氧化碳能和澄清石灰水反应生成白
色沉淀进行分析;
(5)根据化学方程式进行计算。
【解析】解:(1)二氧化碳和澄清石灰水反应生成白色沉淀碳酸钙,所以A瓶中产生
白色沉淀,证明半水煤气中含有CO (或二氧化碳);二氧化碳和氢氧化钙反应生成碳
2
酸钙和水,化学方程式为:CO +Ca(OH) ═CaCO ↓+H O;
2 2 3 2
(2)B装置的作用是吸收二氧化碳和水蒸气;在装置C中,氢气和氧化铜反应生成铜
和水是置换反应,化学方程式为:H +CuO Cu+H O;
2 2
(3)因为氢气和氧化铜反应生成铜和水,所以证明半水煤气中含有 H 的现象是:C中
2
黑色粉末变红,D中集气瓶内壁起雾并出现液滴;
(4)因为一氧化碳和氧化铜反应生成二氧化碳,二氧化碳能和澄清石灰水反应生成白
色沉淀,所以证明半水煤气中含有CO的现象是:C中黑色粉末变红,E中产生白色沉
淀;
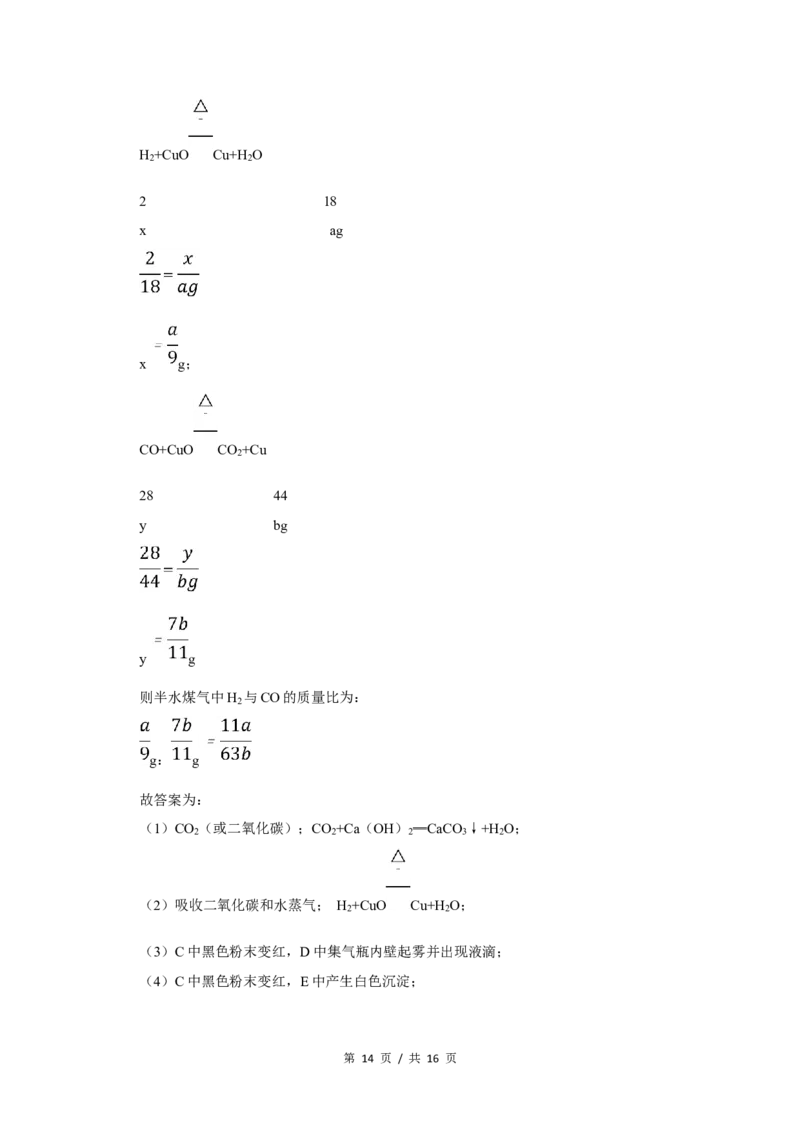
(5)设生成ag水需要氢气的质量为x;生成bg二氧化碳,需要一氧化碳的质量为y。
第 13 页 / 共 16 页H +CuO Cu+H O
2 2
2 18
x ag
x g;
CO+CuO CO +Cu
2
28 44
y bg
y g
则半水煤气中H 与CO的质量比为:
2
g: g
故答案为:
(1)CO (或二氧化碳);CO +Ca(OH) ═CaCO ↓+H O;
2 2 2 3 2
(2)吸收二氧化碳和水蒸气; H +CuO Cu+H O;
2 2
(3)C中黑色粉末变红,D中集气瓶内壁起雾并出现液滴;
(4)C中黑色粉末变红,E中产生白色沉淀;
第 14 页 / 共 16 页(5) 。
【点拨】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
四、(本题包括1小题,共7分)
14.(7分)酸奶作为世界公认的长寿食品之一正愈来愈受到人们的重视和喜爱。酸奶中
的酸味来自乳酸(化学式为C H O )。
3 6 3
(1)酸奶主要提供人类营养物质中的哪一类? 蛋白质 。乳酸在人体内可被完全氧
化为CO 和H O,1.8 g乳酸完全氧化消耗O 的质量为 0.04 5 g。
2 2 2
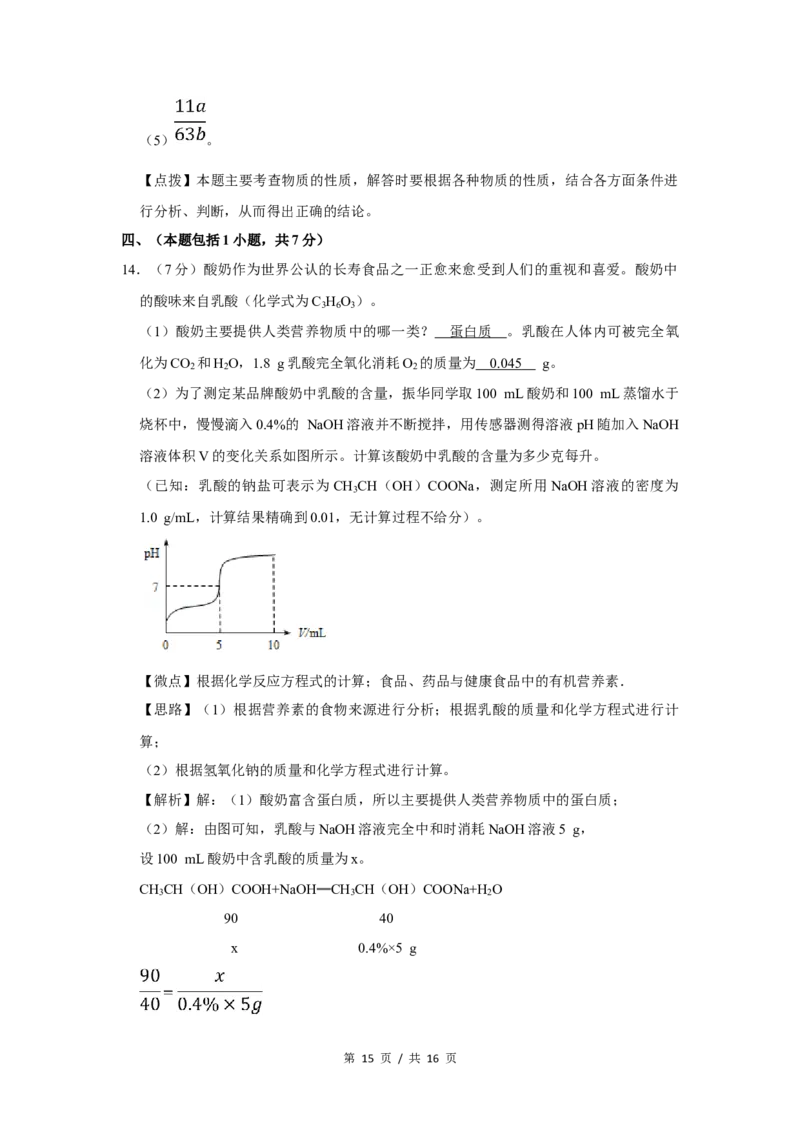
(2)为了测定某品牌酸奶中乳酸的含量,振华同学取100 mL酸奶和100 mL蒸馏水于
烧杯中,慢慢滴入0.4%的 NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH
溶液体积V的变化关系如图所示。计算该酸奶中乳酸的含量为多少克每升。
(已知:乳酸的钠盐可表示为 CH CH(OH)COONa,测定所用NaOH溶液的密度为
3
1.0 g/mL,计算结果精确到0.01,无计算过程不给分)。
【微点】根据化学反应方程式的计算;食品、药品与健康食品中的有机营养素.
【思路】(1)根据营养素的食物来源进行分析;根据乳酸的质量和化学方程式进行计
算;
(2)根据氢氧化钠的质量和化学方程式进行计算。
【解析】解:(1)酸奶富含蛋白质,所以主要提供人类营养物质中的蛋白质;
(2)解:由图可知,乳酸与NaOH溶液完全中和时消耗NaOH溶液5 g,
设100 mL酸奶中含乳酸的质量为x。
CH CH(OH)COOH+NaOH═CH CH(OH)COONa+H O
3 3 2
90 40
x 0.4%×5 g
第 15 页 / 共 16 页x 0.045g
酸奶中乳酸的含量 0.45 g/L
答:该酸奶中乳酸的含量为0.45 g/L。
故答案为:
(1)蛋白质;0.045;
(2)0.45 g/L。
【点拨】(1)根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确
的数据,第三计算过程要完整。
第 16 页 / 共 16 页