文档内容
绝密★启用前
四川省 2026届高三第一次教学质量联合测评
化 学 试 卷
试卷共8页,19小题,满分100分。考试用时75分钟。
注意事项:
1.考查范围:必修第一册;必修第二册;选择性必修1第一章和第二章;选择性必修2;选择性必修3。
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷
上无效。
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
可能用到的相对原子质量:N—14 O—16 Al—27 S—32 Cl—35.5 Cu—64 Zn—65
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目
要求。
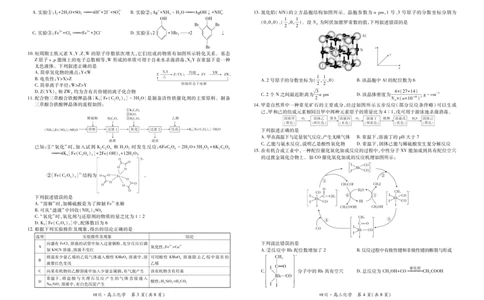
1.文物留存文明印记,延续根脉。下列文物的主要成分属于无机非金属材料的是
A.成都金沙遗址出土的“太阳神鸟金箔” B.广汉三星堆遗址出土的青铜神树
C.眉山三苏祠内保存的苏轼手书碑刻 D.自贡遷海井遗存的清代木制井架
2.下列与物质性质相关的说法正确的是
A.用纯碱溶液清洗厨房油污,是因为其水溶液呈碱性
B.硝酸保存于棕色试剂瓶中,是因为其具有强氧化性
C.蔗糖加入浓硫酸后变黑,说明浓硫酸具有吸水性
D.白酒在陈化过程中产生香味,是因为其发生了氧化反应
3.PA3和 PA-MDA6(结构如图)均属于聚酰胺(尼龙)类高分子材料。下列关于这两种高分子材料
的叙述错误的是
! ! !
# # # #
#! + + " +# " # " " , #! #
! ! !
$%* $%&’(%)
A.均为线型结构的有机高分子材料 B.都能自然降解成小分子
C.单体都含有亲水基团 D.合成二者的芳香族单体互为同系物
4.我国某科研团队设计了一种新型共轭聚合分子反应器,实现 CO 和硝酸盐的高效 C—N偶联。原
2
催化剂
理为 CO+3HO+2NO-CO(NH)+4O+2OH-。下列叙述正确的是
2 2 3 通电 2 2 2
A.CO 的电子式为!!!"!!!
2
四川·高三化学 第1页(共8页) 四川·高三化学 第2页(共8页)
书书书
!
!
!
!
5.化合物 M是从中草药中分离出来的活性成分,具有抗菌、抗炎、抗癌等功效,结构如图所示。下列
关于 M分子的说法正确的是
!
!
!
!
"! !
"!
"
A.遇 FeCl溶液能发生显色反应 B.含有手性碳原子
3
C.含有7个采用 sp2杂化的碳原子 D.1molM最多能消耗3molNaOH
6.科学家成功合成了一种新型全碳分子———环[48]碳(C ),让由 48个碳原子组成的环像穿项链
48
般穿过3个小型“保护套”分子,从而形成稳定的“套环”结构———C ·M,其结构如图所示。下
48 3
列说法错误的是
!!
" "
"
" "
" "
" "
! !
! !
A.C ·M 属于超分子 B.C 只存在非极性键
48 3 48
C.C 与 C 互为同位素 D.C 与 M分子之间存在范德华力
48 60 48
7.下列实验装置正确或操作规范的是
干燥的!" # -. !"# %&!"!’(!
/01 )*+,-./
!"# !" 012"345#
+, #$
$%!
$%
&’(
湿润的 干燥的 $%&’ &’( )* 678
红纸条 红纸条 溶液 9:
A.证明HClO具有漂白性 B.中和反应反应热的测定 C.制备乙烯 D.制备[Cu(NH)]SO·HO晶体
3 4 4 2
8.钠及其化合物在一定条件下的转化关系如图所示。设 N 为阿伏加德罗常数 !"
A #$ # $
的值。下列叙述正确的是 $ !
A.1molNa 2 18O中含有的质子数为32N A !"&’ !" $ %
B.反应②中,若有22.4LO
2
反应,则生成2molNa
2
O
2 # " %
C.反应③中,NaO 既是氧化剂又是还原剂 !" $
2 2 !" $ % $
D.反应④中,若生成71gCl,则转移的电子数为 N
2 A
9.下列根据实验操作及现象书写的离子方程式正确的是
实验 操作及现象
B.NO-的 VSEPR模型为平面三角形
3 ① 向碘水中通入SO,棕黄色褪去
2
C.CO(NH)分子中含有6个 σ键
2 2 ② 向AgNO 溶液中加入过量氨水,得到无色溶液
3
!!"" #" $%
③ 向FeCl溶液中通入氯气,溶液由浅绿色变为黄色
D.基态 N原子的电子排布式为 2
④ 向盛有少量苯酚稀溶液的试管中滴加饱和溴水,产生白色沉淀,溶液变为无色
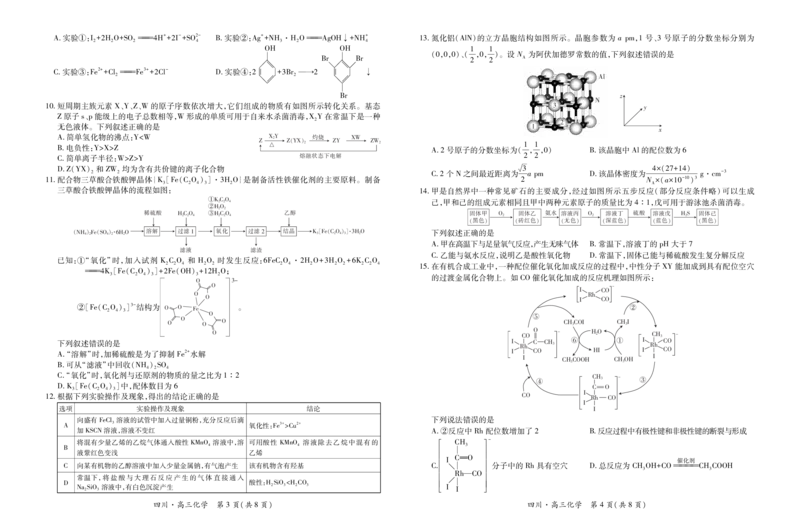
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}A.实验①:I+2HO+SO 4H++2I-+SO2- B.实验②:Ag++NH·HOAgOH↓+NH+ 13.氮化铝(AlN)的立方晶胞结构如图所示。晶胞参数为 apm,1号、3号原子的分数坐标分别为
2 2 2 4 3 2 4
OH OH 1 1
(0,0,0)、( ,0, )。设 N 为阿伏加德罗常数的值,下列叙述错误的是
師師 Br 師師 Br 2 2 A
C.实验③:Fe2++ClFe3++2Cl- D.实验④:2帨帨 +3Br→2 帨帨 ↓
2 師師 2 師師 !"
Br "
#
10.短周期主族元素 X、Y、Z、W的原子序数依次增大,它们组成的物质有如图所示转化关系。基态 $ #
Z原子 s、p能级上的电子总数相等,W形成的单质可用于自来水杀菌消毒,XY在常温下是一种
2
&
无色液体。下列叙述正确的是 %
!
A.简单氢化物的沸点:Y<W ! # $ " !!"#" () !" #% !%
! $ $ 1 1
B.电负性:Y>X>Z
A.2号原子的分数坐标为( , ,0) B.该晶胞中 Al的配位数为6
C.简单离子半径:W>Z>Y !"#$%&’ 2 2
D.Z(YX)和 ZW 均为含有共价键的离子化合物 槡3 4×(27+14)
2 2 C.2个 N之间最近距离为 apm D.该晶体密度为 g·cm-3
11.配合物三草酸合铁酸钾晶体{K[Fe(CO)]·3HO}是制备活性铁催化剂的主要原料。制备 2 N×(a×10-10)3
3 2 4 3 2 A
三草酸合铁酸钾晶体的流程如图: 14.甲是自然界中一种常见矿石的主要成分,经过如图所示五步反应(部分反应条件略)可以生成
!,+(
$ $ # 己,甲和己的组成元素相同且甲中两种元素原子的质量比为41,戊可用于游泳池杀菌消毒。
""(
$ $
)*+ "+( #"+( ,- &’( ! &’* 23 !"# ! !"- 45 !"0 #$ &’1
$ $ # $ $ # " " "
!)%" !+,%" !$%" !./%" !/%" !)%"
!!" # " $ %&!’( # " $ #)" $ ( !" #$* %& #$$ ’( , - $%&!+ $ ( # " - %#-" $ ( 下列叙述正确的是
A.甲在高温下与足量氧气反应,产生无味气体 B.常温下,溶液丁的 pH大于7
$. $/
C.乙能与氨水反应,说明乙是酸性氧化物 D.常温下,固体己能与稀硫酸发生复分解反应
已知:①“氧化”时,加入试剂 KCO 和 HO 时发生反应:6FeCO·2HO+3HO+6KCO
2 2 4 2 2 2 4 2 2 2 2 2 4 15.在有机合成工业中,一种配位催化氧化加成反应的过程中,中性分子 XY能加成到具有配位空穴
4K[Fe(CO)]+2Fe(OH)+12HO;
3 2 4 3 3 2
的过渡金属化合物上。如 CO催化氧化加成的反应机理如图所示:
! "#
! )
& !’
! $%
! & !’
②[Fe(CO)]3-结构为 ! ! $% 。 $
2 4 3
!
!
!
! ! ! !" # !’& !" # &
! !’ ’ ) " ( ’ !" # )
下列叙述错误的是 & ! !" " # & !’
$% # $%
A.“溶解”时,加稀硫酸是为了抑制 Fe2+水解 & !’ "& & !’
& !"!’’" !"’" &
B.可从“滤液”中回收(NH)SO # #
4 2 4
C.“氧化”时,氧化剂与还原剂的物质的量之比为12 & !" # ) %
D.K[Fe(CO)]中,配体数目为6 ! ’
3 2 4 3
&
12.根据下列实验操作及现象,得出的结论正确的是 !’ $% !’
&
选项 实验操作及现象 结论 &
向盛有FeCl溶液的试管中加入过量铜粉,充分反应后滴 下列说法错误的是
A 3 氧化性:Fe3+>Cu2+
加KSCN溶液,溶液不变红 A.②反应中 Rh配位数增加了2 B.反应过程中有极性键和非极性键的断裂与形成
将混有少量乙烯的乙烷气体通入酸性 KMnO 溶液中,溶 可用酸性 KMnO 溶液除去乙烷中混有的 CH -
B 4 4 3
液紫红色变浅 乙烯
I
CO
催化剂
C 向某有机物的乙醇溶液中加入少量金属钠,有气泡产生 该有机物含有羟基 C. 分子中的 Rh具有空穴 D.总反应为 CHOH+COCHCOOH
3 3
RhCO
常温下,将盐酸与大理石反应产生的气体直接通入
D
Na 2 SiO 3 溶液中,有白色沉淀产生
酸性:H
2
SiO
3
<H
2
CO
3
I
I
四川·高三化学 第3页(共8页) 四川·高三化学 第4页(共8页)
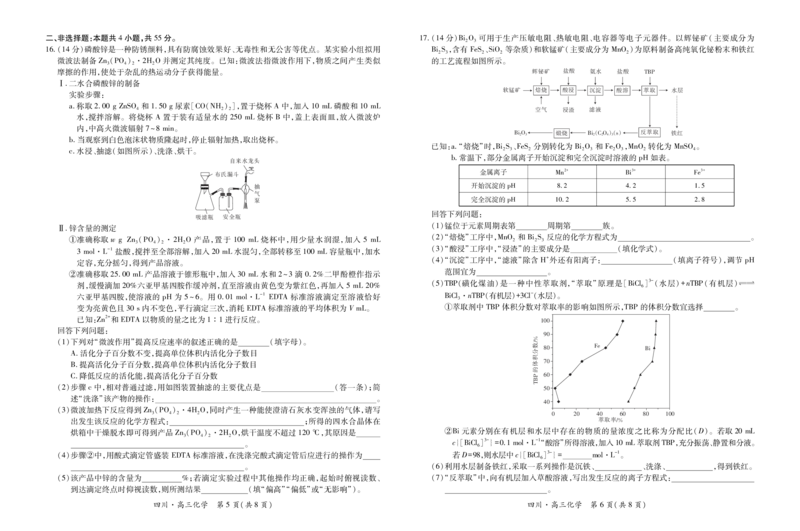
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}二、非选择题:本题共4小题,共55分。 17.(14分)BiO 可用于生产压敏电阻、热敏电阻、电容器等电子元器件。以辉铋矿(主要成分为
2 3
16.(14分)磷酸锌是一种防锈颜料,具有防腐蚀效果好、无毒性和无公害等优点。某实验小组拟用 BiS,含有 FeS、SiO 等杂质)和软锰矿(主要成分为 MnO)为原料制备高纯氧化铋粉末和铁红
2 3 2 2 2
微波法制备 Zn(PO)·2HO并测定其纯度。已知:微波法指微波作用下,物质之间产生类似 的工艺流程如图所示。
3 4 2 2
摩擦的作用,使处于杂乱的热运动分子获得能量。 !"# 3( 67 3( !"#
Ⅰ.二水合磷酸锌的制备
$%# &’ () *+ (, -. 78
实验步骤:
a.称取2.00gZnSO 和1.50g尿素[CO(NH)],置于烧杯 A中,加入 10mL磷酸和 10mL
4 2 2 /0 12 45
水,搅拌溶解。将烧杯 A置于装有适量水的 250mL烧杯 B中,盖上表面皿,放入微波炉
内,中高火微波辐射7~8min。
+$’ <’ "$!&’"!*" ;-. 9:
, ) % % ( )
b.当观察到白色泡沫状物质隆起时,停止辐射加热,取出烧杯。
已知:a.“焙烧”时,BiS、FeS分别转化为 BiO 和 FeO,MnO 转化为 MnSO。
c.水浸、抽滤(如图所示)、洗涤、烘干。 2 3 2 2 3 2 3 2 4
b.常温下,部分金属离子开始沉淀和完全沉淀时溶液的 pH如表。
-./01
金属离子 Mn2+ Bi3+ Fe3+
!"#$
% 开始沉淀的pH 8.2 4.2 1.5
&
’ 完全沉淀的pH 10.2 5.5 2.8
回答下列问题:
()* +,*
(1)锰位于元素周期表第 周期第 族。
Ⅱ.锌含量的测定
(2)“焙烧”工序中,MnO 和 BiS反应的化学方程式为 。
①准确称取 wgZn(PO)·2HO产品,置于 100mL烧杯中,用少量水润湿,加入 5mL 2 2 3
3 4 2 2
3mol·L-1盐酸,搅拌至全部溶解,加入20mL水混匀,全部转移至100mL容量瓶中,加水 (3)“酸浸”工序中,“浸渣”的主要成分是 (填化学式)。
(4)“沉淀”工序中,“滤液”除含 H+外还有阳离子: (填离子符号),调节 pH
定容,充分摇匀,得到产品溶液。
范围宜为 。
②准确移取25.00mL产品溶液于锥形瓶中,加入 30mL水和 2~3滴 0.2%二甲酚橙作指示
剂,缓慢滴加20%六亚甲基四胺作缓冲剂,直至溶液由黄色变为紫红色,再加入 5mL20%
(5)TBP(磺化煤油)是一种中性萃取剂,“萃取”原理是[BiCl
6
]3-(水层)+nTBP(有机层)幑幐
六亚甲基四胺,使溶液的 pH为 5~6。用 0.01mol·L-1EDTA标准溶液滴定至溶液恰好 BiCl·nTBP(有机层)+3Cl-(水层)。
3
变为亮黄色且30s内不变色,平行滴定三次,消耗 EDTA标准溶液的平均体积为 VmL。 ①萃取剂中 TBP体积分数对萃取率的影响如图所示,TBP的体积分数宜选择 。
已知:Zn2+和 EDTA以物质的量之比为11进行反应。
回答下列问题:
(1)下列对“微波作用”提高反应速率的叙述正确的是 (填字母)。
!"
A.活化分子百分数不变,提高单位体积内活化分子数目
B.提高活化分子百分数,提高单位体积内活化分子数目
C.降低反应的活化能,提高活化分子百分数
(2)步骤 c中,相对普通过滤,用如图装置抽滤的主要优点是 (答一条);简
述“洗涤”该产物的操作: 。
(3)微波加热下反应得到 Zn(PO)·4HO,同时产生一种能使澄清石灰水变浑浊的气体,请写
3 4 2 2 # $% &% ’% (% )%%
出发生该反应的化学方程式: ;所得的四水合晶体在 !"#*!
烘箱中干燥脱水即可得到产品 Zn(PO)·2HO,烘干温度不超过120℃,其原因是
3 4 2 2
。
(4)步骤②中,用酸式滴定管盛装 EDTA标准溶液,在洗涤完酸式滴定管后应进行的操作为
。
(5)该产品中锌的含量为 %;若滴定实验过程中其他操作均正确,起始时俯视读数、
到达滴定终点时仰视读数,则所测结果 (填“偏高”“偏低”或“无影响”)。
四川·高三化学 第5页(共8页) 四川·高三化学 第6页(共8页)
!*(’&%$-,+
)/% !
0% !
(% ,. !
1% !
’% !
23 !
&% !
②Bi元素分别在有机层和水层中存在的物质的量浓度之比称为分配比(D)。若取 20mL
c{[BiCl]3-}=0.1mol·L-1“酸溶”所得溶液,加入10mL萃取剂TBP,充分振荡、静置和分液。
6
若D=98,则水层中c{[BiCl]3-}= mol·L-1。
6
(6)利用水层制备铁红,采取一系列操作是沉铁、 、洗涤、 ,得到铁红。
(7)“反萃取”中,向有机层加入草酸溶液,写出发生反应的离子方程式:
。
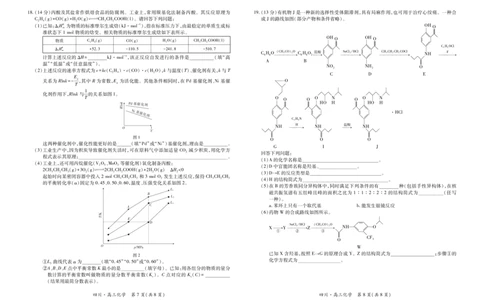
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}18.(14分)丙酸及其盐常作烘焙食品的防腐剂。工业上,常用羰基化法制备丙酸。其反应原理为
CH(g)+CO(g)+HO(g)幑幐CHCHCOOH(l)。请回答下列问题:
2 4 2 3 2
(1)已知:ΔHθ为物质的标准摩尔生成焓(kJ·mol-1),指在标准压力下,由最稳定的单质生成标
f m
准状态下1mol物质的焓变。相关物质的标准摩尔生成焓如下表所示。
物质 CH(g) CO(g) HO(g) CHCHCOOH(l) 2 4 2 3 2
ΔHθ +52.3 -110.5 -241.8 -510.7
f m
计算上述反应的 ΔH= kJ·mol-1,该正反应自发进行的条件是 (填“高
温”“低温”或“任意温度”)。
(2)上述反应的速率方程式为v=kc(CH)·c(CO)·c(HO),k与温度(T)、催化剂有关,k与T
2 4 2
E
a 关系为 Rlnk=- ,其中 R为常数,E 为活化能。其他条件相同时,在 Pd基催化剂、Ni基催
T a
1
化剂作用下,Rlnk与 的关系如图1。
T
!"!"#$
" #
!
四川·高三化学 第7页(共8页) 四川·高三化学 第8页(共8页)
$%$#
&’!%&$
图1
这两种催化剂中,催化性能更好的是 (填“Pd”或“Ni”)基催化剂,理由是 。
(3)工业生产中,因为积炭导致催化剂失活时,可在原料气中添加适量 CO 减少积炭,用化学方
2
程式表示其原理: 。
(4)工业上,还可用丙烷催化(VO、MoO 等催化剂)氧化制备丙酸:
2 5 3
2CHCHCH(g)+3O(g)幑幐2CHCHCOOH(g)+2HO(g) ΔH<0
3 2 3 2 3 2 2 2
起始时向某密闭容器中投入2molCHCHCH 和3molO 发生上述反应,保持 CHCHCH
3 2 3 2 3 2 3
的平衡转化率(α)固定为0.45、0.50、0.60,温度、压强变化关系如图2。
!
# "!"#$
%!$
19.(13分)有机物 J是一种新的选择性受体阻滞剂,具有局麻作用,也可用于治疗心绞痛。一种合
成 J的路线如图(部分产物和条件省略)。
OH
師師
CHO(CH 3 CO) 2 O CHO 混酸帨帨 師師
6 6 → 8 8 2→
A B
NO
2
%
! &
)
! * ’
*
’ (
!
&
(
!
图2
①L曲线代表 α为 (填“0.45”“0.50”或“0.60”)。
3
②A、B、D、E点中平衡常数 K最小的是 (填字母)。已知:用各组分的物质的量分
数计算的平衡常数叫做物质的量分数平衡常数(K)。C点对应的 K(C)=
x x
(结果用最简分数表示)。
OH
O
師師
SnCl/HCl帨帨 2 師師
→
NH
2
C
OH
師師
O 帨帨 師師
CHCHCHCOCl 3 2 2 NH
→
O
D
O
CHOCl
3 5
F
→
E
O
O
師師
帨帨
師師
NH
O
O
師師
帨帨
師師
CHN
3 9
H
NH
→
O
G
O O N
HO H
師師
帨帨
師師
盐酸
NH
→
O
I
O O N
HO H
·HCl
J
回答下列问题:
(1)A的化学名称是 。
(2)D中官能团名称是羟基、 。
(3)D→E的反应类型是 。
(4)H的结构简式为 。
(5)在 B的芳香族同分异构体中,同时满足下列条件的有 种(包括手性异构体),在核
磁共振氢谱有五组峰且峰的面积之比为 11222的结构简式为 (任写
一种)。
a.苯环上只有一个取代基 b.能发生银镜反应
(6)药物 W的合成路线如图所示。
師師
SnCl/HCl (CHCO)O
X→Y 2 →Z 3 2 → NH師師師師O
① ② ③
CF
O 3
W
已知 X含羟基,按照 E→G的原理合成 Y。Z的结构简式为 ;步骤①的
化学方程式为 。
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}四川省 2026届高三第一次教学质量联合测评
化学参考答案及评分细则
1.【答案】C
【解析】金箔、青铜神树的主要成分均属于金属材料,木制井架的主要成分属于有机高分子材料,A、B、D项不符
合题意;碑石的主要成分属于无机非金属材料,C项符合题意。
2.【答案】A
【解析】纯碱溶液呈碱性,能与油脂发生反应,将其分解为可溶于水的甘油和高级脂肪酸盐,从而去除油污,A项
正确;硝酸保存于棕色试剂瓶中,是因为 HNO 在光照条件下易分解,B项错误;蔗糖加入浓硫酸后变黑,说明浓
3
硫酸具有脱水性,蔗糖被脱水碳化,C项错误;白酒在陈化过程中产生香味,与其发生酯化反应生成了乙酸乙酯
有关,D项错误。
3.【答案】D
【解析】由PA3和PA-MDA6的结构可知,它们都是线型结构的有机高分子材料,A项正确;上述两种高分子均含
酰胺基,能在自然界水解生成羧酸、胺类小分子,B项正确;它们的单体含氨基或羧基(亲水基团),都能与水形成
NH
2
師師師師
師師 帩帩
氢键,C项正确;合成二者的芳香族单体均为HN師師師師 ,D项错误。
2
4.【答案】B
【解析】CO 的电子式为!!!!"!!!!
2
四川·高三化学 第 1页(共5页)
书书书
! ! ,每个原子最外层均满足8电子结构,A项错误;NO-的中心原子 N的价层电子
3
H C
5+1-3×2
对数为 +3=3,VSEPR模型是平面三角形,B项正确; N
2
H
O
H
N 分子含7个σ键,C项错误;基态 N
H
原子的电子排布式为1s22s22p3,D项错误。
5.【答案】B
【解析】M不含酚羟基,遇 FeCl溶液不能发生显色反应,A项错误;分子中含有 8个手性碳原子(用标记):
3
!
! # # #
# ! ,B项正确;碳碳双键和碳氧双键上的碳原子均为sp2杂化,共6个,C项错误;
#
!
"!
# !
# #
"!
"
醇羟基不能与碱反应,M分子只含1个酯基,1molM最多能消耗1molNaOH,D项错误。
6.【答案】C
【解析】C ·M 是由C 与三个有机物分子以分子间作用力结合形成的稳定聚集体,属于超分子,A项正确;C
48 3 48 48
只存在C—C非极性键,B项正确;C 和C 是由碳元素构成的结构不同的单质,两者互为同素异形体,C项错
48 60
误;C 与M均属于分子晶体,两者之间存在范德华力,D项正确。
48
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}7.【答案】D
【解析】氯气通过湿润的红纸条时带有水,且NaOH溶液中的水蒸气会进入装有干燥的红纸条的试剂瓶中,所以
湿润的红纸条和干燥的红纸条都会褪色,不能证明HClO具有漂白性,A项不符合题意;铁制搅拌器会与酸反应,
且会散失热量,B项不符合题意;制备乙烯时,温度计的水银球应在液面下,C项不符合题意;将足量氨水滴入硫
酸铜溶液中至形成的氢氧化铜溶解,得到深蓝色透明溶液,加入 95%乙醇后析出[Cu(NH)]SO·HO晶体,
3 4 4 2
玻璃棒摩擦试管壁是为了加快晶体析出速率,D项符合题意。
8.【答案】C
【解析】Na原子含有11个质子,18O原子含有8个质子,1molNa18O中含有的质子数为(11×2+8)mol=30mol,
2
A项错误;未说明温度、压强,无法确定 22.4LO 的物质的量,B项错误;反应③为 2NaO+4H+4Na++
2 2 2
电解
O↑+2HO,NaO 既是氧化剂又是还原剂,C项正确;反应④为 2NaCl(熔融)2Na+Cl↑,若生成 71g即
2 2 2 2 2
1molCl,则转移的电子数为2N,D项错误。
2 A
9.【答案】A
【解析】HI是强酸,在水中完全电离,写离子方程式时要拆开,A项正确;向硝酸银溶液中加入氨水,得到无色溶
液的离子反应为 Ag++2NH·HO[Ag(NH)]++2HO,B项错误;电荷不守恒,正确的离子方程式为
3 2 3 2 2
2Fe2++Cl2Fe3++2Cl-,C项错误;溴水与苯酚发生取代反应,有溴化氢生成,D项错误。
2
10.【答案】B
【解析】XY在常温下是一种无色液体,则 XY为 HO;基态 Z原子的电子排布式为1s22s22p4或1s22s22p63s2,
2 2 2
根据转化关系图可知,Z为Mg,X为H,Y为O,W为 Cl。HO分子间存在氢键,水的沸点高于 HCl,A项错误;
2
O、H、Mg的电负性依次减小,B项正确;一般情况下,电子层数越多,离子半径越大,电子层数相同时,核电荷数
越小的离子半径越大,因此简单离子半径:Cl->O2->Mg2+,C项错误;MgCl只含离子键,Mg(OH)含离子键和
2 2
共价键,D项错误。
11.【答案】D
【解析】Fe2+在水溶液中会发生水解,加稀硫酸可以抑制 Fe2+水解,A项正确;草酸与 Fe2+反应生成草酸亚铁,
“滤液”的溶质主要为(NH)SO,B项正确;“氧化”时,发生反应为 6FeCO·2HO+3HO+6KCO
4 2 4 2 4 2 2 2 2 2 4
4K[Fe(CO)]+2Fe(OH)+12HO,氧化剂(HO)与还原剂(FeCO·2HO)的物质的量之比为12,C项
3 2 4 3 3 2 2 2 2 4 2
正确;K[Fe(CO)]中,配体数目为3,D项错误。
3 2 4 3
12.【答案】A
【解析】FeCl与Cu的反应为2Fe3++Cu2Fe2++Cu2+,Fe3+作氧化剂,Cu2+是氧化产物,根据“氧化剂的氧化性
3
强于氧化产物的氧化性”,反应后的溶液中滴加 KSCN溶液,溶液不变红,说明 Fe3+反应完,即氧化性:Fe3+>
Cu2+,A项符合题意;酸性 KMnO 溶液会把乙烯氧化为 CO,引入新杂质 CO,因此不能用酸性 KMnO 溶液除
4 2 2 4
去乙烷中混有的乙烯,应选溴水(乙烯与溴发生加成反应,乙烷不反应),B项不符合题意;乙醇中含有羟基,有
气泡产生不能说明该有机物含有羟基,C项不符合题意;CO 气体中混有 HCl,HCl也会与 NaSiO 反应产生
2 2 3
HSiO 沉淀,D项不符合题意。
2 3
13.【答案】C
1 1
【解析】由1、3号原子的分数坐标可知,2号原子的分数坐标为( , ,0),A项正确;1个晶胞中,N(Al)=8×
2 2
1 1 1
+6× =4,N(N)=12× +1=4,1个 Al原子上、下、前、后、左、右共6个 N相邻且最近,B项正确;晶胞中,2
8 2 4
四川·高三化学 第 2页(共5页)
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}槡2
个N原子之间最近距离等于面对角线的一半,等于 apm,C项错误;根据均摊法可知晶胞中含有4个 N原子
2
4×(27+14)
和4个Al原子,该晶体密度为 g·cm-3,D项正确。
N×(a×10-10)3
A
14.【答案】B
【解析】依题意可知,甲为CuS(元素原子的质量比为41),乙为 CuO,丙为含[Cu(NH)]+的溶液,丁为含
2 2 3 2
[Cu(NH)]2+的溶液,戊为含Cu2+的溶液,己为CuS。高温条件下,硫化亚铜在足量氧气中反应生成具有刺激
3 4
性气味的SO 气体,A项错误;溶液丁的溶质主要是[Cu(NH)](OH),溶液呈碱性,B项正确;CuO溶于氨
2 3 4 2 2
水生成[Cu(NH)]+,氨水提供的NH 作为配体与Cu+形成配合物,不能说明 CuO是碱性氧化物,C项错误;
3 2 3 2
因为能发生反应:CuSO+HSCuS↓+HSO,说明CuS和HSO 不反应,D项错误。
4 2 2 4 2 4
15.【答案】B
【解析】②反应中 Rh配位数由4增加到6,A项正确;反应过程中没有非极性键断裂,B项错误;由题干信息可
CH -
3
I CO
知反应④的反应物 中的Rh具有空穴,C项正确;由反应历程可知反应物为一氧化碳和甲醇,生
RhCO
I
I
催化剂
成物为乙酸,总反应为CHOH+COCHCOOH,D项正确。
3 3
16.【答案】(1)B(2分)
(2)过滤速度快、所得固体较干燥等合理答案(2分) (关闭抽气泵,)用玻璃棒引流向布氏漏斗中加入蒸馏水
至浸没固体(1分),待水自然流出(或打开抽气泵抽滤)后重复2~3次(1分)
(3)3ZnSO+2HPO+3CO(NH)+7HOZn(PO)·4HO↓+3(NH)SO+3CO↑(2分,物质、配平错
4 3 4 2 2 2 3 4 2 2 4 2 4 2
误不给分,未写“↓、↑”不扣分) 避免产品失去剩余的结晶水(或避免产品分解,1分)
(4)用0.01mol·L-1EDTA标准溶液润洗滴定管(1分)
0.26V
(5) (2分) 偏高(2分)
w
【解析】(1)依题意,微波作用使物质产生热运动获取能量,即升高温度,提高活化分子百分数,反应的活化能没
有降低,A、C项错误,B项正确。
(2)抽滤时,抽气使装置内产生负压,过滤速度较快,固体与液体易分离、固体较干燥等。根据布氏漏斗特殊情
况,用玻璃棒引流加入蒸馏水,不能用玻璃棒搅拌,待水自然流出后重复操作2~3次。
(3)依题意,尿素中N显-3价,C显+4价。制备产品时产生 CO 气体,氮元素转化成铵根离子,发生反应的化
2
学方程式为3ZnSO+2HPO+3CO(NH)+7HOZn(PO)·4HO↓+3(NH)SO+3CO↑。温度过
4 3 4 2 2 2 3 4 2 2 4 2 4 2
高,会导致产品失水或分解。
(4)滴定管洗涤后需要用待装溶液润洗。
100
0.01V×10-3× ×65
25 0.26V
(5)根据反应比例关系可知,ω= ×100%= %。起始时俯视读数,测得初始体积(V )
w w 初
偏小,到达滴定终点时仰视读数,测得终点体积(V )偏大,结果测得体积(V =V -V )偏大,因此所测结果
终 测 终 始
偏高。
四川·高三化学 第 3页(共5页)
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}17.【答案】(1)四 ⅦB(两空共1分,有错不给分)
焙烧
(2)6MnO+2BiS+9O 2BiO+6MnSO(2分,物质、配平错误不给分,未写条件扣 1分,条件写成“高温、
2 2 3 2 2 3 4
灼烧、△”不扣分)
(3)SiO(1分)
2
(4)NH+、Mn2+(2分,1个1分) 5.5≤pH<8.2(1分,写5.5~8.2不扣分)
4
(5)①50%(1分) ②2.0×10-3(2分)
(6)过滤(1分) 灼烧(1分)
(7)2(BiCl·nTBP)+3HCO Bi(CO)↓+2nTBP+6H++6Cl-(2分,物质、配平错误不给分,未写“↓”
3 2 2 4 2 2 4 3
不扣分)
【解析】(1)基态Mn原子的价层电子排布式为3d54s2,位于元素周期表第四周期第ⅦB族。
(2)根据提示信息,二氧化锰、硫化铋在氧气作用下生成硫酸锰和氧化铋。
(3)原料中的二氧化硅在盐酸浸取中分离出来。
(4)根据表格信息,锰离子残留在滤液中。根据表格中金属离子沉淀的数据,调节 pH使 Fe3+、Bi3+完全沉淀,使
Mn2+不沉淀。
(5)根据图像信息,TBP体积分数为50%时,Fe、Bi分离效果最好,主要萃取 Bi。设水层中 c{[BiCl]3-}=x,根
6
20
(0.1-x)×
10
据元素守恒有D= =98,解得x=2.0×10-3mol·L-1。
x
(6)加入氨水等碱使铁离子沉淀,过滤、洗涤、灼烧得到铁红。
(7)加入HCO,产物为萃取剂、盐酸和草酸铋固体。
2 2 4
18.【答案】(1)-210.7(2分) 低温(1分)
(2)Pd(1分) 升高相同温度,Pd基催化剂对应的曲线变化值较小,说明活化能较小(2分)
高温
(3)C+CO 2CO(2分,物质、配平错误不给分,未写条件扣1分)
2
4
(4)①0.60(2分) ②B(2分) (2分)
3
【解析】(1)根据反应热和生成焓关系,代入数据计算得:ΔH=(-52.3+110.5+241.8-510.7)kJ·mol-1=
-210.7kJ·mol-1。正反应是气体分子数减小的放热反应,即熵减、焓减,故该反应在低温下能自发进行。
1
(2)从图1看,Pd基催化剂的Rlnk- 曲线平缓,即斜率较小。根据关系式,升高温度,活化能越小,斜率变化值
T
较小,活化能小说明催化剂性能更好。
高温
(3)充入CO 能与C反应生成反应物CO:C+CO 2CO。
2 2
(4)①根据图2分析,正反应是气体分子数减小的放热反应,相同温度下,增大压强,丙烷的平衡转化率增大,故
L曲线代表丙烷的平衡转化率为0.45,L曲线代表丙烷的平衡转化率为0.60。②升高温度,平衡常数减小,图
1 3
2中有K(E)=K(D)>K(A)>K(B)。C点丙烷的平衡转化率为0.50,列出三段式:
2CHCHCH(g)+3O(g)幑幐2CHCHCOOH(g)+2HO(g)
3 2 3 2 3 2 2
起始量/mol: 2 3 0 0
转化量/mol: 1 1.5 1 1
平衡量/mol: 1 1.5 1 1
2 3 2 2
物质的量分数:
9 9 9 9
2 2
( )2×( )2
x2(CHCHCOOH)·x2(HO)
9 9 4
K(C)= 3 2 2 = = 。
x x2(CHCHCH)·x3(O) 2 3 3
3 2 3 2 ( )2×( )3
9 9
四川·高三化学 第 4页(共5页)
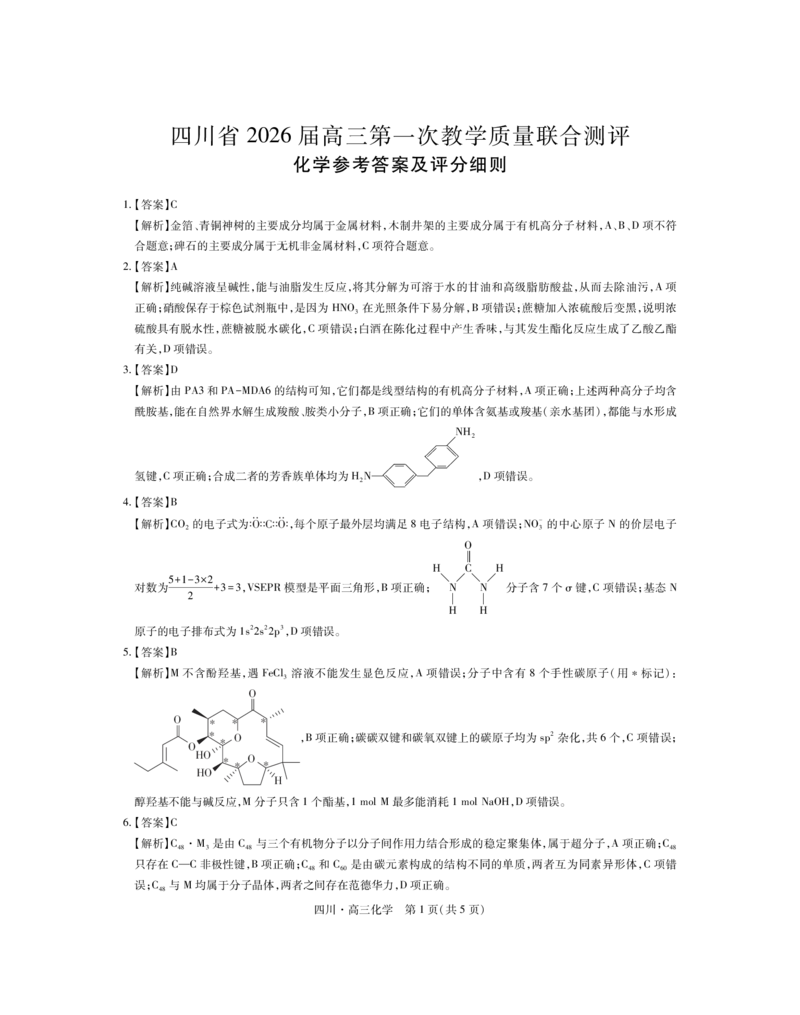
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}19.【答案】(1)苯酚(1分)
(2)酮羰基或羰基、氨基(2分,1个1分)
(3)取代反应(1分)
NH
2
(4) CH (2分)
HC CH
3 3
師師師師 師師師師
(5)4(2分) OCHCHO或 CHOCH
2 2
帩帩 帩帩
四川·高三化学 第 5页(共5页)
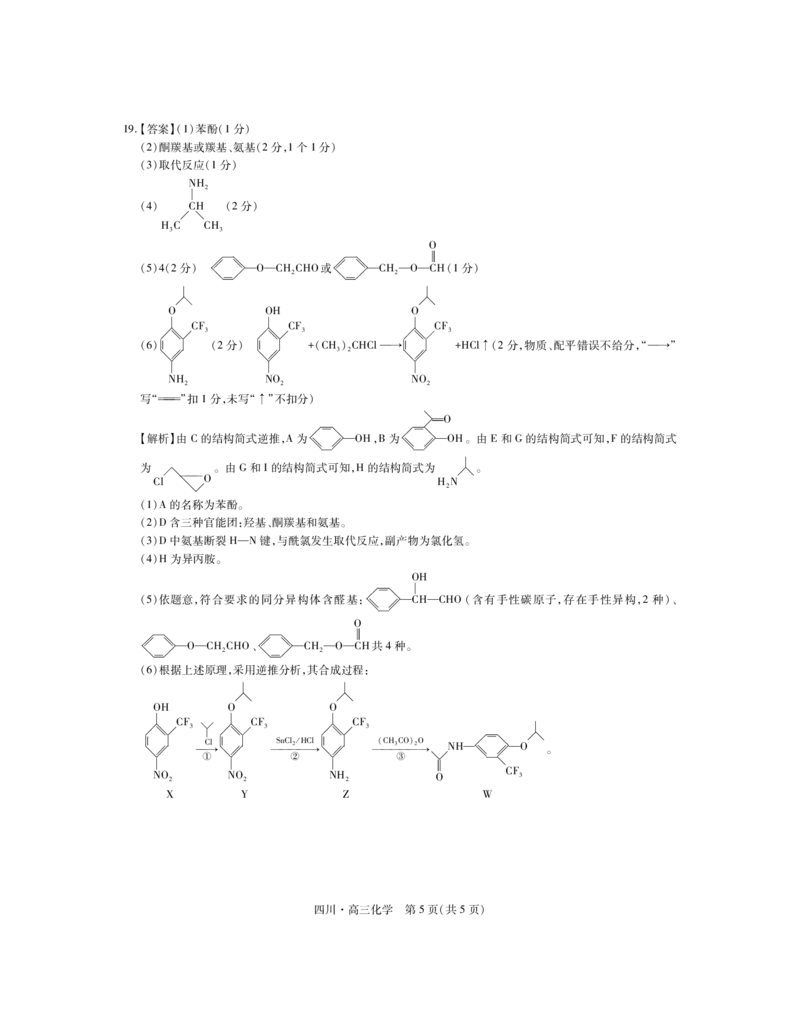
O
(1分)
O OH O
CF CF CF
師師 3 師師 3 師師 3
(6)帨帨 (2分) 帨帨 +(CH)CHCl→帨帨 +HCl↑(2分,物质、配平错误不给分,“→”
師師 師師 3 2 師師
NH NO NO
2 2 2
写“”扣1分,未写“↑”不扣分)
O
師師 師師
【解析】由C的结构简式逆推,A为師師師師OH,B为師師師師OH。由E和G的结构简式可知,F的结构简式
为 。由G和I的结构简式可知,H的结构简式为 。
O
Cl HN
2
(1)A的名称为苯酚。
(2)D含三种官能团:羟基、酮羰基和氨基。
(3)D中氨基断裂H—N键,与酰氯发生取代反应,副产物为氯化氢。
(4)H为异丙胺。
OH
師師
(5)依题意,符合要求的同分异构体含醛基:師師師師CHCHO(含有手性碳原子,存在手性异构,2种)、
師師師師 師師師師
OCHCHO、 CHOCH
2 2
帩帩 帩帩
O
共4种。
(6)根据上述原理,采用逆推分析,其合成过程:
OH O O
CF CF CF
師師 3 師師 3 師師 3
師師
帨帨 師師 C → l帨帨 師師 S nC l 2 /HC → l帨帨 師師 ( CH 3 CO ) 2 O → NH師師師師O 。
① ② ③
CF
NO NO NH O 3
2 2 2
X Y Z W
{#{QQABZQSUggCIAIJAAQgCAQ2CCkAYkBAAAAgGQAAUMAABwAFABAA=}#}