文档内容
机密 启用前
★
2025 年湖北省普通高中学业水平选择性考试(仿真模拟)
化 学
本试卷满分 100分,考试用时 75分钟。
祝考试顺利
★ ★
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
认真核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡
上的非答题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答
题卡上作答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:H1 C12 O16 Sc45
本卷涉及的实验均须在专业人士指导和安全得到充分保障的条件下完成。
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,
只有一项是符合题目要求的。
1.湖北是楚文化的发源地,湖北各地市各具特色。下列有关说法错误的是
A.神农架盛产的草药中常含有苷类、生物碱、有机酸等成分,可用铁锅煎煮中草药
B.宜昌三峡大坝举世闻名,它的修筑离不开钢筋混凝土,钢筋混凝土属于复合材料
C.恩施被称为“世界硒都”,硒是M层电子全充满的p区元素
D.十堰是重要的汽车城,氮化硅用于制备汽车电机轴承利用其电绝缘性和高耐磨性
2.化学与生活或生产密切相关,下面运用化学知识解释正确的是
生活中的化学 化学解释
食品包装袋中常有硅胶、生石灰、还原 硅胶具有吸水性,生石灰、还原铁粉
A
铁粉三类小包 能与水反应,都是用于防止食品受潮
B 糖类是维持生命活动所需能量的主要来源 糖类水解的最终产物均为葡萄糖
石墨烯是新型无机非金属材料,可以
C 问天实验舱使用了石墨烯导热索技术
有效导热
实验室盛碱的试剂瓶用橡皮塞,氢氟酸 SiO 是两性氧化物,与碱和酸都能反
2
D
溶液只能用塑料瓶盛装 应
A.A B.B C.C D.D
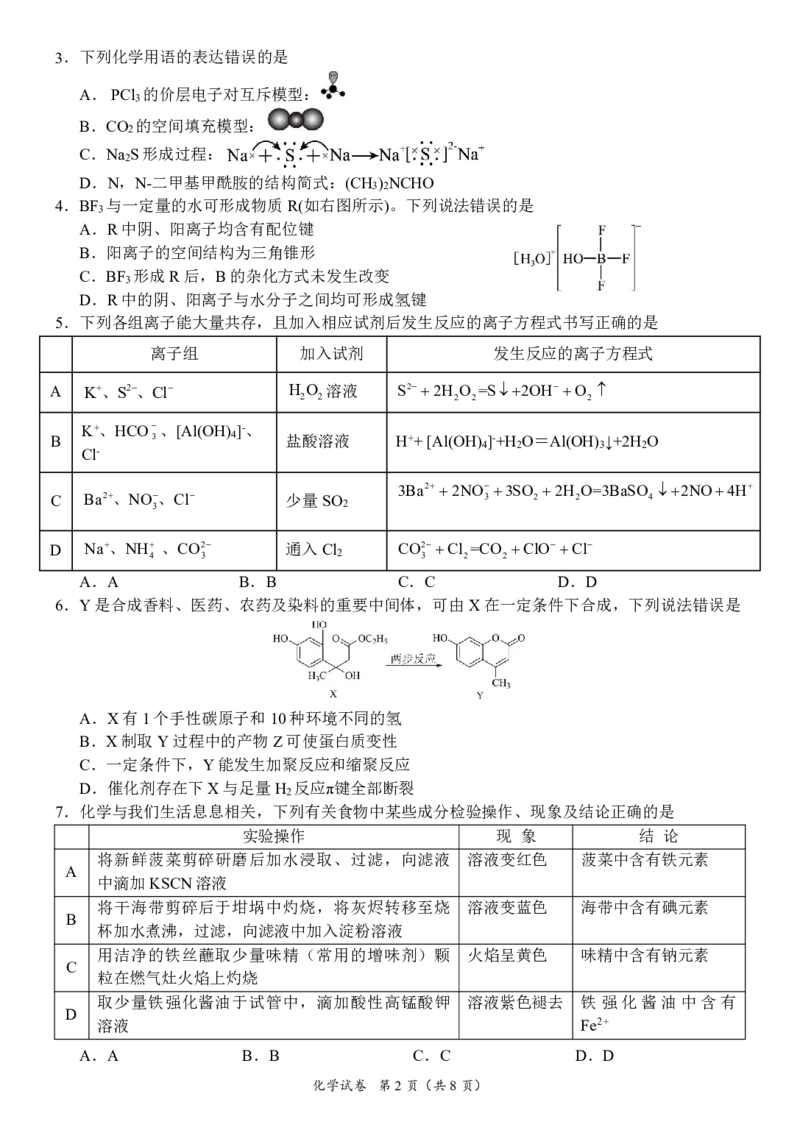
化学试卷 第1页(共8页)3.下列化学用语的表达错误的是
A.PCl 的价层电子对互斥模型:
3
B.CO 的空间填充模型:
2
C.Na S形成过程:
2
D.N,N-二甲基甲酰胺的结构简式:(CH ) NCHO
3 2
4.BF 与一定量的水可形成物质R(如右图所示)。下列说法错误的是
3
A.R中阴、阳离子均含有配位键
B.阳离子的空间结构为三角锥形
C.BF 形成R后,B的杂化方式未发生改变
3
D.R中的阴、阳离子与水分子之间均可形成氢键
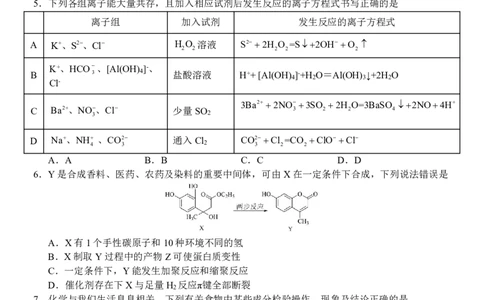
5.下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式书写正确的是
离子组 加入试剂 发生反应的离子方程式
A K、S2、Cl H O 溶液 S22H O =S2OHO
2 2 2 2 2
K+、HCO、[Al(OH) ]-、
B 3 4 盐酸溶液 H++[Al(OH) ]-+H O=Al(OH) ↓+2H O
4 2 3 2
Cl-
3Ba2 2NO3SO 2H O=3BaSO 2NO4H
C Ba2、NO、Cl 少量SO 3 2 2 4
3 2
D Na、NH 、CO2 通入Cl CO2Cl =CO ClOCl
4 3 2 3 2 2
A.A B.B C.C D.D
6.Y是合成香料、医药、农药及染料的重要中间体,可由X在一定条件下合成,下列说法错误是
A.X有1个手性碳原子和10种环境不同的氢
B.X制取Y过程中的产物Z可使蛋白质变性
C.一定条件下,Y能发生加聚反应和缩聚反应
D.催化剂存在下X与足量H 反应π键全部断裂
2
7.化学与我们生活息息相关,下列有关食物中某些成分检验操作、现象及结论正确的是
实验操作 现 象 结 论
将新鲜菠菜剪碎研磨后加水浸取、过滤,向滤液 溶液变红色 菠菜中含有铁元素
A
中滴加KSCN溶液
将干海带剪碎后于坩埚中灼烧,将灰烬转移至烧 溶液变蓝色 海带中含有碘元素
B
杯加水煮沸,过滤,向滤液中加入淀粉溶液
用洁净的铁丝蘸取少量味精(常用的增味剂)颗 火焰呈黄色 味精中含有钠元素
C
粒在燃气灶火焰上灼烧
取少量铁强化酱油于试管中,滴加酸性高锰酸钾 溶液紫色褪去 铁强化酱油中含有
D
溶液 Fe2+
A.A B.B C.C D.D
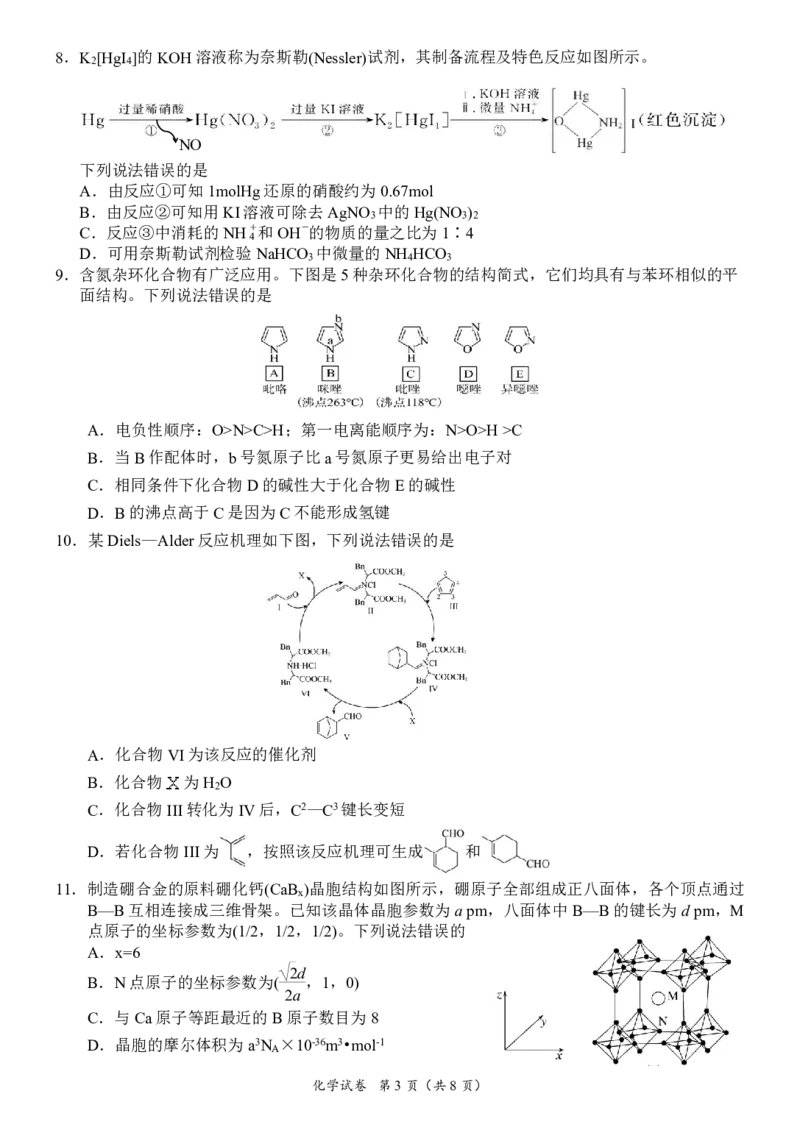
化学试卷 第2页(共8页)8.K [HgI ]的KOH溶液称为奈斯勒(Nessler)试剂,其制备流程及特色反应如图所示。
2 4
NO
下列说法错误的是
A.由反应①可知1molHg还原的硝酸约为0.67mol
B.由反应②可知用KI溶液可除去AgNO 中的Hg(NO )
3 3 2
C.反应③中消耗的NH+和OH-的物质的量之比为1∶4
4
D.可用奈斯勒试剂检验NaHCO 中微量的NH HCO
3 4 3
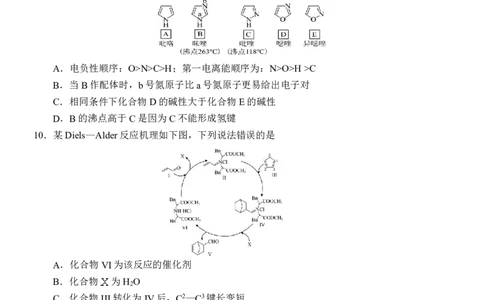
9.含氮杂环化合物有广泛应用。下图是5种杂环化合物的结构简式,它们均具有与苯环相似的平
面结构。下列说法错误的是
A.电负性顺序:O>N>C>H;第一电离能顺序为:N>O>H>C
B.当B作配体时,b号氮原子比a号氮原子更易给出电子对
C.相同条件下化合物D的碱性大于化合物E的碱性
D.B的沸点高于C是因为C不能形成氢键
10.某Diels—Alder反应机理如下图,下列说法错误的是
A.化合物VI为该反应的催化剂
B.化合物 为H O
2
C.化合物III转化为IV后,C2—C3键长变短
D.若化合物III为 ,按照该反应机理可生成 和
11.制造硼合金的原料硼化钙(CaB )晶胞结构如图所示,硼原子全部组成正八面体,各个顶点通过
x
B—B互相连接成三维骨架。已知该晶体晶胞参数为apm,八面体中B—B的键长为dpm,M
点原子的坐标参数为(1/2,1/2,1/2)。下列说法错误的
A.x=6
2d
B.N点原子的坐标参数为( ,1,0)
2a
C.与Ca原子等距最近的B原子数目为8
D.晶胞的摩尔体积为a3N ×10-36m3•mol-1
A
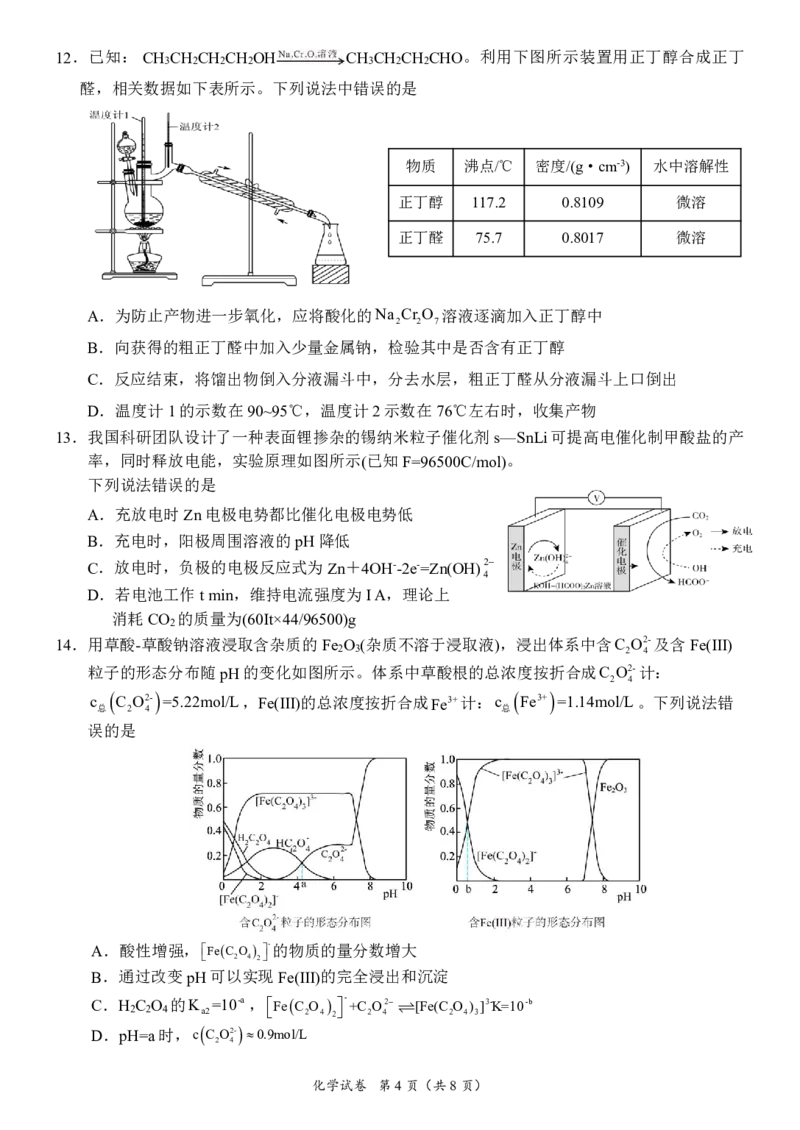
化学试卷 第3页(共8页)12.已知: CH CH CH CH OH CH CH CH CHO。利用下图所示装置用正丁醇合成正丁
3 2 2 2 3 2 2
醛,相关数据如下表所示。下列说法中错误的是
物质 沸点/℃ 密度/(g·cm-3) 水中溶解性
正丁醇 117.2 0.8109 微溶
正丁醛 75.7 0.8017 微溶
A.为防止产物进一步氧化,应将酸化的Na CrO 溶液逐滴加入正丁醇中
2 2 7
B.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.温度计1的示数在90~95℃,温度计2示数在76℃左右时,收集产物
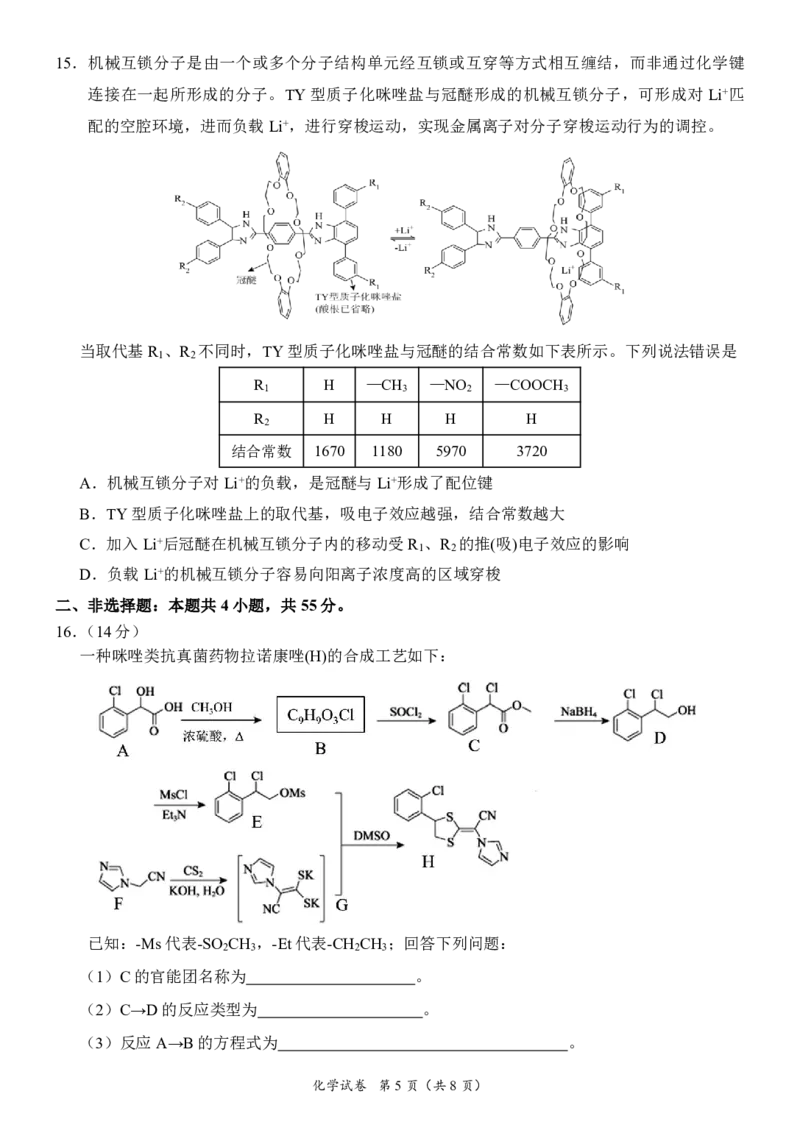
13.我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s—SnLi可提高电催化制甲酸盐的产
率,同时释放电能,实验原理如图所示(已知F=96500C/mol)。
下列说法错误的是
A.充放电时Zn电极电势都比催化电极电势低
B.充电时,阳极周围溶液的pH降低
C.放电时,负极的电极反应式为Zn+4OH--2e-=Zn(OH)2
4
D.若电池工作tmin,维持电流强度为IA,理论上
消耗CO 的质量为(60It×44/96500)g
2
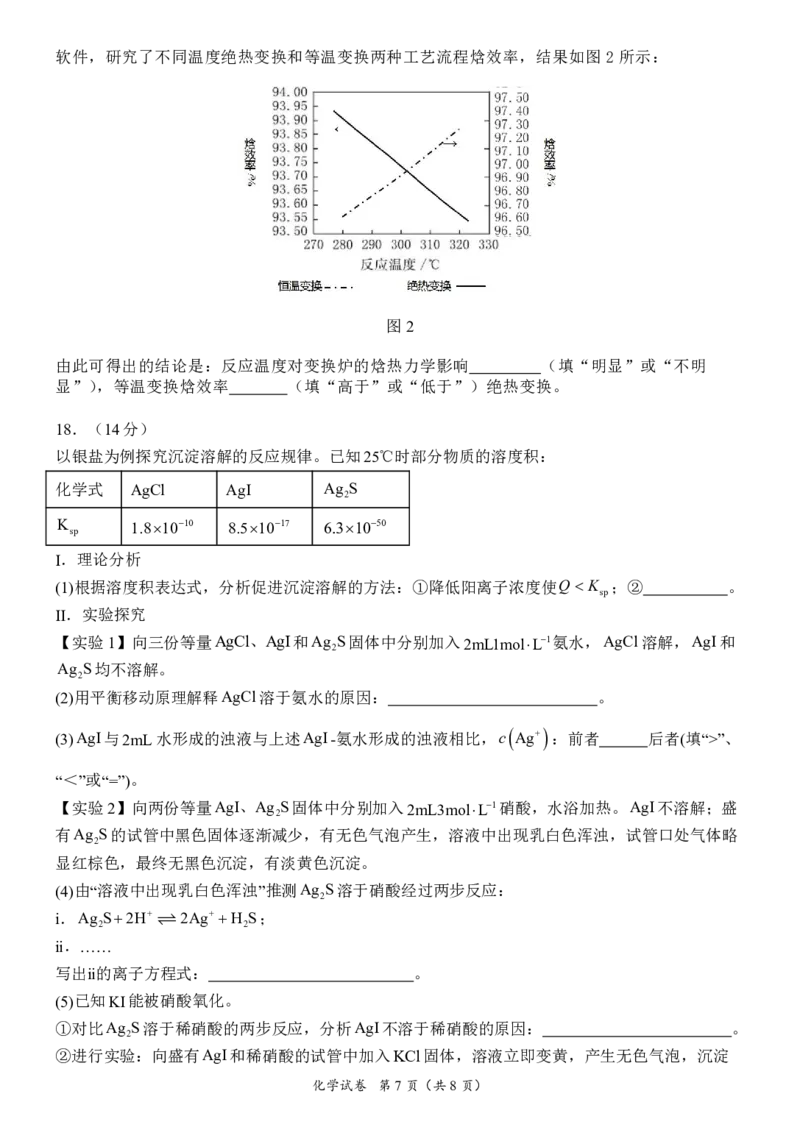
14.用草酸-草酸钠溶液浸取含杂质的Fe O (杂质不溶于浸取液),浸出体系中含C O2-及含Fe(Ⅲ)
2 3 2 4
粒子的形态分布随pH的变化如图所示。体系中草酸根的总浓度按折合成C O2-计:
2 4
c
C
O2-
=5.22mol/L,Fe(Ⅲ)的总浓度按折合成Fe3+计:c
Fe3+
=1.14mol/L。下列说法错
总 2 4 总
误的是
A.酸性增强, FeC 2 O 4 2 -的物质的量分数增大
B.通过改变pH可以实现Fe(Ⅲ)的完全浸出和沉淀
C.H 2 C 2 O 4 的K a2 =10-a, FeC 2 O 4 2 - +C 2 O 4 2 [Fe(C 2 O 4 ) 3 ]3-K=10-b
D.pH=a时,c C O2-0.9mol/L
2 4
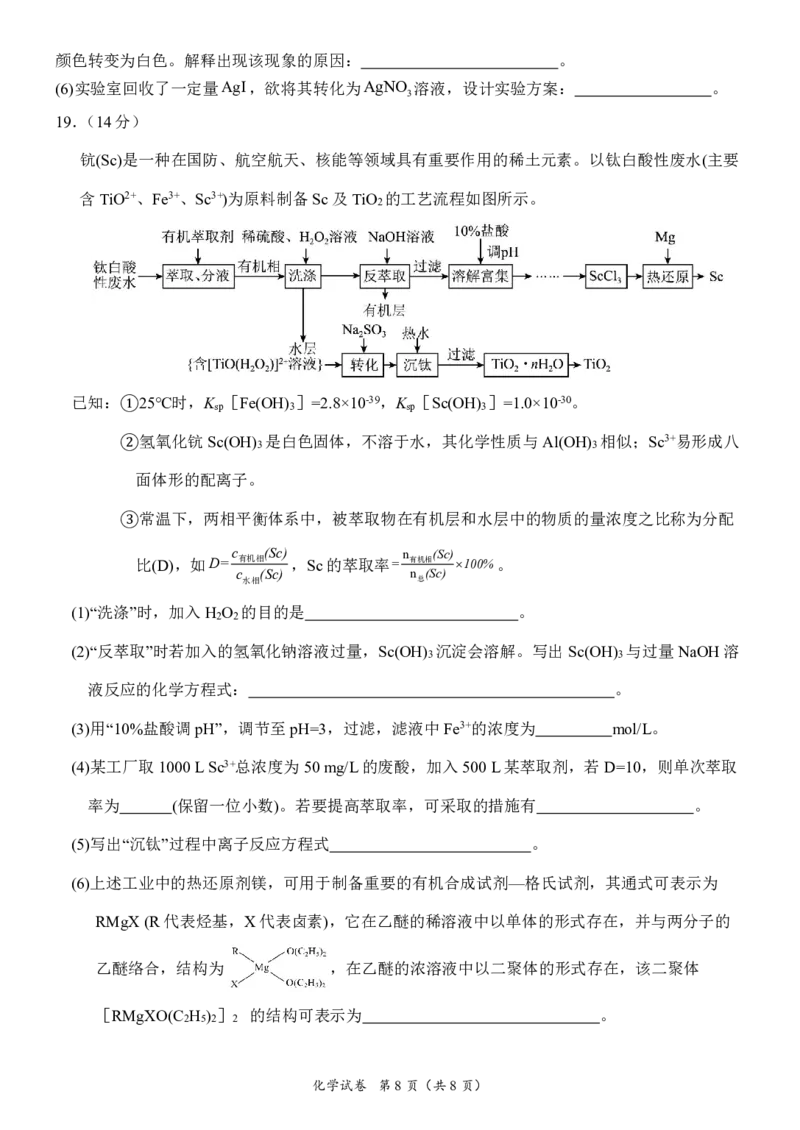
化学试卷 第4页(共8页)15.机械互锁分子是由一个或多个分子结构单元经互锁或互穿等方式相互缠结,而非通过化学键
连接在一起所形成的分子。TY型质子化咪唑盐与冠醚形成的机械互锁分子,可形成对Li+匹
配的空腔环境,进而负载Li+,进行穿梭运动,实现金属离子对分子穿梭运动行为的调控。
当取代基R 、R 不同时,TY型质子化咪唑盐与冠醚的结合常数如下表所示。下列说法错误是
1 2
R1 H —CH3 —NO2 —COOCH3
R H H H H
2
结合常数 1670 1180 5970 3720
A.机械互锁分子对Li+的负载,是冠醚与Li+形成了配位键
B.TY型质子化咪唑盐上的取代基,吸电子效应越强,结合常数越大
C.加入Li+后冠醚在机械互锁分子内的移动受R 、R 的推(吸)电子效应的影响
1 2
D.负载Li+的机械互锁分子容易向阳离子浓度高的区域穿梭
二、非选择题:本题共4小题,共55分。
16.(14分)
一种咪唑类抗真菌药物拉诺康唑(H)的合成工艺如下:
已知:-Ms代表-SO CH ,-Et代表-CH CH ;回答下列问题:
2 3 2 3
(1)C的官能团名称为 。
(2)C→D的反应类型为 。
(3)反应A→B的方程式为 。
化学试卷 第5页(共8页)(4)A的酸性 (填“强于”或“弱于”) ,原因是 。
(5)反应D→E中Et N的作用是 。
3
(6)反应E+G→H的副产物H,(与H互为同分异构体)的结构简式为 。
(7)D的同分异构体中,能与氯化铁溶液显色,核磁共振氢谱有四组峰,且峰面积之比为1:
2:2:3的结构简式为 。(写出一种即可)
17.(13分)
煤的气化是将煤转化为可燃性气体的过程,主要反应:①C(s)+H O(g)⇌CO(g)+H (g) ΔH
2 2 1
煤间接液化是先转化为CO和H ,然后催化剂作用合成甲醇等,主要反应:② CO(g) +2H (g) ⇌
2 2
CH OH(g) ΔH
3 2
回答下列问题:
(1)反应①在 (填“高温”或“低温”)条件下自发进行。
(2)已知部分化学键键能如下:
化学键 H-H C-H C-O O-H
键能/kJ·mol-1 1075 436 413 351 463
C=���O CO
计算反应②的焓变ΔH = 。
2
(3)上述反应体系中还存在水煤气变换反应:CO+H O ⇌ CO +H 。一定条件下,该反应的中间产
2 2 2
物是 HCOOH。
Ⅰ.CO+H O ⇌ HCOOH(快反应)
2
Ⅱ.HCOOH ⇌ CO +H (慢反应) 注:反应Ⅰ速率远大于反应Ⅱ
2 2
为探究该反应过程,将 0.01mol CO 和 0.01mol CO 完全密封在充满水的 10mL石英管中,研究
2
存在的分子反应。假设水足量且反应物和产物均完全溶于水,则含碳物种浓度与 t 的变化关系
如图 1所示(忽略碳元素的其他存在形式)。
图 1 含碳物种浓度与反应时间的变化图
t 时刻测得 CO、CO 的浓度分别为 0.75mol·L-1、1.15mol·L-1。
1 2
①单纯从反应Ⅰ的角度分析,0至 t 时刻生成 HCOOH的平均反应速率为 (用含 t 的代
1 1
数式表示);在该温度下,反应Ⅰ在 t 时刻是否达到平衡? (填“是”或“否”);请简叙理
1
由 。
②反应Ⅱ达平衡时,测得c(H )=amol·L-1,体系达平衡后c(CO ):c(CO)= (用含a的代
2 2
数式表示)。
③焓效率是热力循环中的一个重要参数,用以评估热能转换系统的能量转换效率。焓效率定义
为系统输出的净工作(或输出功)与输入的热能之比。某研究团队基于 Aspen Plus 流程模拟
化学试卷 第6页(共8页)软件,研究了不同温度绝热变换和等温变换两种工艺流程焓效率,结果如图 2 所示:
图 2
由此可得出的结论是:反应温度对变换炉的焓热力学影响 (填“明显”或“不明
显”),等温变换焓效率 (填“高于”或“低于”)绝热变换。
18.(14分)
以银盐为例探究沉淀溶解的反应规律。已知25℃时部分物质的溶度积:
化学式 AgCl AgI Ag S
2
K 1.81010 8.51017 6.31050
sp
Ⅰ.理论分析
(1)根据溶度积表达式,分析促进沉淀溶解的方法:①降低阳离子浓度使QK ;② 。
sp
Ⅱ.实验探究
【实验1】向三份等量AgCl、AgI和Ag S固体中分别加入2mL1molL1氨水,AgCl溶解,AgI和
2
Ag S均不溶解。
2
(2)用平衡移动原理解释AgCl溶于氨水的原因: 。
(3)AgI与2mL水形成的浊液与上述AgI-氨水形成的浊液相比,c
Ag
:前者 后者(填“>”、
“<”或“=”)。
【实验2】向两份等量AgI、Ag S固体中分别加入2mL3molL1硝酸,水浴加热。AgI不溶解;盛
2
有Ag S的试管中黑色固体逐渐减少,有无色气泡产生,溶液中出现乳白色浑浊,试管口处气体略
2
显红棕色,最终无黑色沉淀,有淡黄色沉淀。
(4)由“溶液中出现乳白色浑浊”推测Ag S溶于硝酸经过两步反应:
2
ⅰ.Ag S2H 2AgH S;
2 2
ⅱ.……
写出ⅱ的离子方程式: 。
(5)已知KI能被硝酸氧化。
①对比Ag S溶于稀硝酸的两步反应,分析AgI不溶于稀硝酸的原因: 。
2
②进行实验:向盛有AgI和稀硝酸的试管中加入KCl固体,溶液立即变黄,产生无色气泡,沉淀
化学试卷 第7页(共8页)颜色转变为白色。解释出现该现象的原因: 。
(6)实验室回收了一定量AgI,欲将其转化为AgNO 溶液,设计实验方案: 。
3
19.(14分)
钪(Sc)是一种在国防、航空航天、核能等领域具有重要作用的稀土元素。以钛白酸性废水(主要
含TiO2+、Fe3+、Sc3+)为原料制备Sc及TiO 的工艺流程如图所示。
2
已知: 25℃时,K [Fe(OH) ]=2.8×10-39,K [Sc(OH) ]=1.0×10-30。
sp 3 sp 3
①氢氧化钪Sc(OH) 是白色固体,不溶于水,其化学性质与Al(OH) 相似;Sc3+易形成八
3 3
②面体形的配离子。
常温下,两相平衡体系中,被萃取物在有机层和水层中的物质的量浓度之比称为分配
③ c (Sc) n (Sc)
比(D),如D= 有机相 ,Sc的萃取率= 有机相 100%。
c (Sc) n (Sc)
水相 总
(1)“洗涤”时,加入H O 的目的是 。
2 2
(2)“反萃取”时若加入的氢氧化钠溶液过量,Sc(OH) 沉淀会溶解。写出Sc(OH) 与过量NaOH溶
3 3
液反应的化学方程式: 。
(3)用“10%盐酸调pH”,调节至pH=3,过滤,滤液中Fe3+的浓度为 mol/L。
(4)某工厂取1000LSc3+总浓度为50mg/L的废酸,加入500L某萃取剂,若D=10,则单次萃取
率为 (保留一位小数)。若要提高萃取率,可采取的措施有 。
(5)写出“沉钛”过程中离子反应方程式 。
(6)上述工业中的热还原剂镁,可用于制备重要的有机合成试剂—格氏试剂,其通式可表示为
RMgX(R代表烃基,X代表卤素),它在乙醚的稀溶液中以单体的形式存在,并与两分子的
乙醚络合,结构为 ,在乙醚的浓溶液中以二聚体的形式存在,该二聚体
[RMgXO(C H ) ] 的结构可表示为 。
2 5 2 2
化学试卷 第8页(共8页)