文档内容
常德市一中 2024 届高三第六次月水平检测
CH
2
OH(CHOH)
4
CHO+2Cu(OH)
2
+OH----→ CH
2
OH(CHOH)
4
COO- + Cu
2
O↓+3H
2
O
D.铅酸蓄电池放电时正极反应:PbO +4H++SO+ 2e- === PbSO + 2H O
2 4 2
化 学
5.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结
构如图所示。X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,X原子中电子
时量:75分钟 满分:100分
只有一种自旋方向,Y、Z、Q为同一周期元素,W的原子核外有3个未成对电子。下列说
可能用到的相对原子质量:H 1 法错误的是
一、选择题(本题共14小题,每小题3分,共计42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。)
1.化学与社会、科技、生活密切相关,下列说法错误的是
A.碳化硅、氮化硅陶瓷具有耐高温、耐磨蚀等优良性能,属于新型无机非金属材料
B.“尿不湿”的主要成分是高分子树脂,其分子结构中因含有大量的羧基、羟基等亲水基
A.简单离子半径:W>Z>Q
团而具有强吸水性
B.Z 和 W 的简单氢化物的沸点:Z>W
C.以来自生物质的纤维素、淀粉等为原料的化工生产路线因其低碳排放和可再生性将逐步
C.X 分别与 Y、Z 均能形成既含极性键又含非极性键的化合物
替代以煤、石油和天然气为原料的生产路线
D.Q、Z、W 的最高价氧化物对应的水化物的酸性:Q>Z>W
D.我国研制的某种超级钢中含有其他四种元素:Mn 10%、C 0.47%、Al 2%、V 0.7%,它
6.利用如图所示装置进行下列实验,打开或关闭弹簧夹a,Z 中实验现象完全相同的是
属于合金,该合金中有两种元素属于过渡元素
选项 气体X Y中试剂 Z中试剂
2.制取HO 的反应为NaO +HSO +10HO === NaSO ·10H O+HO ,下列说法不正确的
2 2 2 2 2 4 2 2 4 2 2 2
是 A HCl Na CO 溶液 NaAlO 溶液
2 3 2
A.钠离子的结构示意图: B.HO 的电子式: B NH HO AgNO 溶液
2 2 3 2 3
C Cl 饱和食盐水 淀粉-KI溶液
2
C.SO的空间结构为正四面体形 D.基态O原子的轨道表示式:
D SO 酸性KMnO 溶液 Ba(NO ) 溶液
2 4 3 2
3.布洛芬具有抗炎、镇痛、解热作用,口服该药对胃、肠道有刺激性,可以对该分子进行如
图所示的修饰,以降低毒副作用。下列说法错误的是 7.下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
A.该修饰过程可以通过酯化反应实现
B.1mol布洛芬最多可以与4molH 发生加成反应
2 甲 乙 丙 丁
C.修饰后的产物X能发生加成反应、氧化反应、取代反应
A.用装置甲除去废铜屑表面的油污 B.用装置乙溶解废铜屑
D.两种有机物中碳原子都为sp² 、sp³ 两种杂化方式
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
4.下列有关电极方程式或离子方程式错误的是
A.碳酸银粉末加入到稀盐酸中:Ag CO+2H+=== 2Ag++CO ↑+ H O
2 3 2 2 8.利用电化学方法制备氨可以大大降低目前的热 Haber-Bosch 工艺产生的温室气体排放。下
B.用醋酸滴定氨水:CHCOOH + NH ·H O === CHCOO- + NH + H O
3 3 2 3 2 图所示为一种合成氨的方法,下列说法错误的是
C.葡萄糖与新制氢氧化铜反应:
第1页 共4页
学学科科网网((北北京京))股股份份有有限限公公司司下列说法正确的是
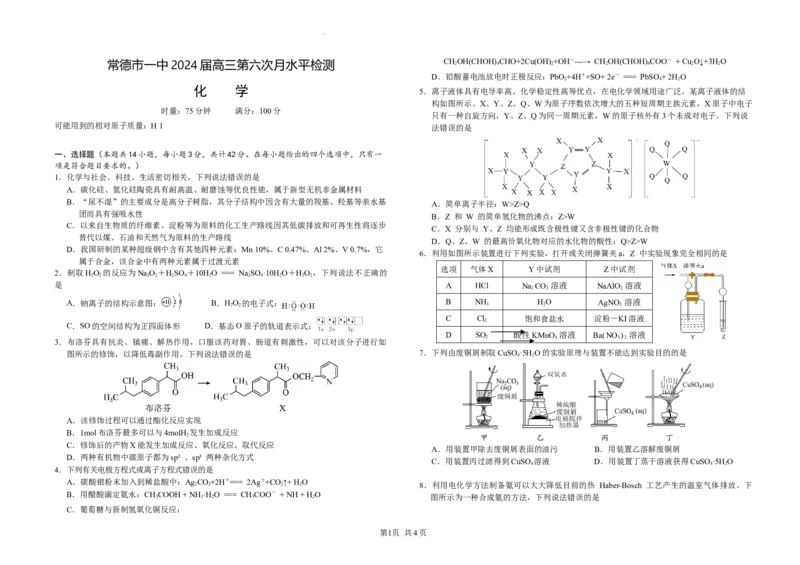
A.“滤渣I”的主要成分为Fe O、CaCO 、SiO
2 3 3 2
B.惰性电极电解Ga(SO ) 溶液时,在阳极有金属镓生成
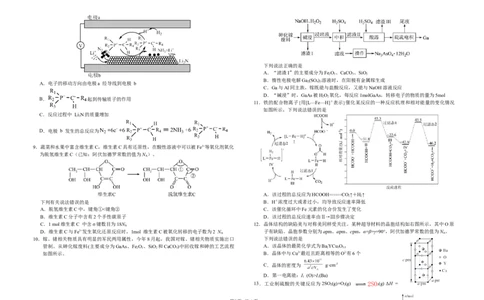
A.电子的移动方向由电极a 经导线到电极 b 2 4 3
C.Ga与Al同主族,镓既能与盐酸反应,又能与NaOH溶液反应
D.“碱浸”时,GaAs被HO 氧化,每反应1molGaAs,转移电子的物质的量为5mol
2 2
B. 起到传输质子的作用
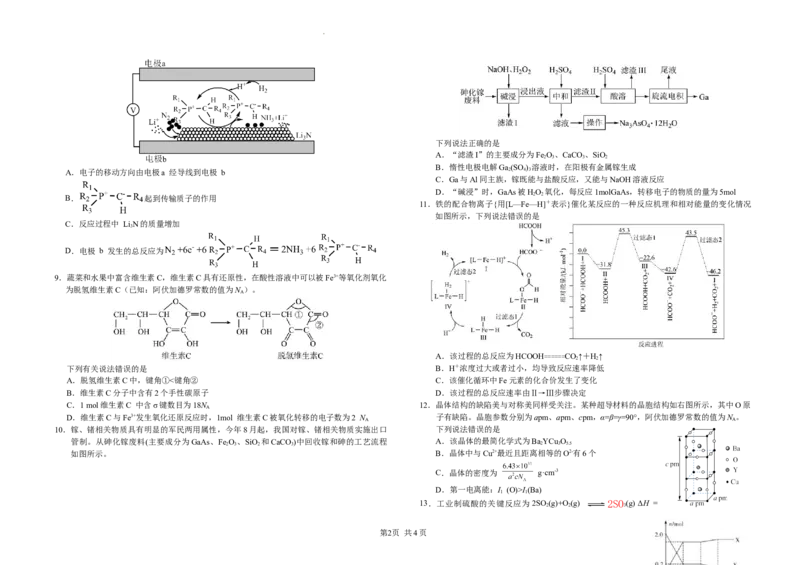
11.铁的配合物离子{用[L—Fe—H]+表示}催化某反应的一种反应机理和相对能量的变化情况
如图所示,下列说法错误的是
C.反应过程中 LiN的质量增加
3
D.电极 b 发生的总反应为
9.蔬菜和水果中富含维生素C,维生素C具有还原性,在酸性溶液中可以被Fe3+等氧化剂氧化
为脱氢维生素C(已知:阿伏加德罗常数的值为N )。
A
A.该过程的总反应为HCOOH======CO↑+H↑
2 2
下列有关说法错误的是 B.H+浓度过大或者过小,均导致反应速率降低
A.脱氢维生素C中,键角①<键角② C.该催化循环中Fe元素的化合价发生了变化
B.维生素C分子中含有2个手性碳原子 D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
C.1 mol维生素C 中含σ键数目为18N 12.晶体结构的缺陷美与对称美同样受关注。某种超导材料的晶胞结构如右图所示,其中O原
A
D.维生素C与Fe3+发生氧化还原反应时,1mol 维生素C被氧化转移的电子数为2 N 子有缺陷。晶胞参数分别为apm、apm、cpm,α=β=γ=90°,阿伏加德罗常数的值为N 。
A A
10.镓、锗相关物质具有明显的军民两用属性,今年8月起,我国对镓、锗相关物质实施出口 下列说法错误的是
管制。从砷化镓废料(主要成分为GaAs、Fe O 、SiO 和CaCO )中回收镓和砷的工艺流程 A.该晶体的最简化学式为Ba YCu O
2 3 2 3 2 3 5.5
如图所示。 B.晶体中与Cu2+最近且距离相等的O2-有6个
C.晶体的密度为 g·cm-3
D.第一电离能:I (O)>I(Ba)
1 1
13.工业制硫酸的关键反应为 2SO (g)+O(g) 2SO(g) ΔH =
2 2 3
第2页 共4页
学学科科网网((北北京京))股股份份有有限限公公司司-196 kJ·mol-1,T K时向10 L恒容密闭容器中按照物质的量之比2:1通入SO 和O ,测 (3)B装置的烧瓶中发生反应的离子方程式为___________________________。
2 2
得容器内某些物质的量随时间变化如图。下列说法正确的是 (4)实验时,要先加入浓盐酸,使B装置中开始生成氯气,待 (填现象)时,
A.用O 表示2min内的平均反应速率为0.45 mol·L·min-1 再加热A装置,目的是 。
2
B.4min时改变的条件可能是降温或增加O 的量 Ⅱ.三氯化六氨合钴(Ⅲ)的制备。
2
C.T K时,正反应的化学平衡常数K为810
D.2min时,若再加入SO 、O 和SO 各0.2mol,平衡逆向移动
2 2 3
14.在催化剂作用下,CO 氧化C H 可获得C H。其主要化学反应为:
2 2 6 2 4
C
反应I. CO(g)+ C H (g) H (g)+CO(g)+ H O(g) ΔH= +177 kJ·mol-1
2 2 6 2 4 2 1
4CO(g) +3H
反应II. 2CO (g)+ C H (g) (g) ΔH= +430 kJ·mol-1
2 2 6 2 2
压强分别为P 、P 时,将2mol C H 和2mol CO 的混合气体置于密闭容器中反应,不同温
1 2 2 6 2
度下体系中乙烷的平衡转化率、乙烯的选择性( )如图所示。
①先向三颈烧瓶中加入活性炭、CoCl 和NH Cl溶液,然后滴加稍过量的浓氨水;
2 4
②冷水浴冷却至10 ℃以下,缓慢滴加HO 溶液并不断搅拌;
下列说法正确的是 2 2
A.P>P
③转移至60 ℃水浴中,恒温加热同时缓慢搅拌;
1 2
B.压强为P,温度为210℃时,反应达平衡时, ④冷却结晶,过滤洗涤可得三氯化六氨合钴(Ⅲ){[Co(NH 3 ) 6 ]Cl 3 }粗产品。
1
n (CO)= n (C H)
(5)D装置中制备三氯化六氨合钴(Ⅲ)的总反应化学方程式为________________________。
生成 生成 2 4
Ⅲ.纯度测定。
C.C H 的选择性下降的原因可能是随着温度的
2 4
(6)称取m g粗产品与氢氧化钠在空气中混合煅烧得氧化钴→将氧化钴用稀硫酸溶解→配成
升高,反应II中生成的CO抑制了反应I的进
250 mL溶液→ (按顺序填序号),纯度为 (写出表达式)。
行
D.研发低温下C H 转化率高和C H 选择性高的催
a.向锥形瓶中加入稍过量的KI溶液(Co3+被还原后的产物为Co2+),充分反应
2 6 2 4
化剂,可以提高平衡时C H 产率 b.平行滴定三次,消耗标准溶液的体积平均值为V mL
2 4
二、非选择题(本题共4小题,共58分。)
c.取25.00 mL待测液于锥形瓶中
15.(14分)钴的化合物种类较多,其中三氯化六氨合钴(Ⅲ){[Co(NH 3 ) 6 ]Cl 3 }(M=267.5 d.用淀粉溶液作指示剂,用c mol·L-1 Na 2 S 2 O 3 标准溶液滴定(产物为S 4 O)
g/mol),在工业上用途广泛。实验室以活性炭作为催化剂,以HO 作氧化剂氧化CoCl 的方
16.(15分)硫酸锌(ZnSO
4
)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应
2 2 2
法制备三氯化六氨合钴。
用。硫酸锌可由菱锌矿制备,菱锌矿的主要成分为ZnCO
3
,杂质为SiO
2
以及Ca、Mg、
已知:①钴单质在300 ℃以上易被氧气氧化,CoCl 易潮解。②Co2+不易被氧化,Co3+具 Fe、Cu等的化合物。其制备流程如下:
2
有强氧化性;[Co(NH )]2+具有较强的还原性,[Co(NH )]3+性质稳定。
3 6 3 6
Ⅰ.CoCl 的制备。
2
本题中所涉及离子的氢氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K 4.0×10-38 6.7×10-17 2.2×10-20 8.0×10-16 1.8×10-11
sp
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为 。
(1)B装置中盛放浓盐酸的仪器名称是 。
(2)为了提高锌的浸取效果,可采取的措施有 、 。
(2)按照气体流向从左到右连接仪器的顺序为 → → 。
第3页 共4页
学学科科网网((北北京京))股股份份有有限限公公司司(3)加入物质X调溶液pH=5,最适宜使用的X是 (填标号)。
A.NH ·H O B.Ca(OH) C.NaOH
3 2 2
滤渣①的主要成分是 、 、 。
(4)向 80~90 ℃的滤液①中分批加入适量 KMnO 溶液充分反应后过滤,滤渣②中有
4
MnO ,该步反应的离子方程式为_______________________________________。
2
(5)滤液②中加入锌粉的目的是_______________________。
(6)滤渣④与浓HSO 反应可以释放HF并循环利用,同时得到的副产物是 、 。
2 4
17.(14分)NaBH 储氢材料、燃料电池等方面具有重要应用。
4
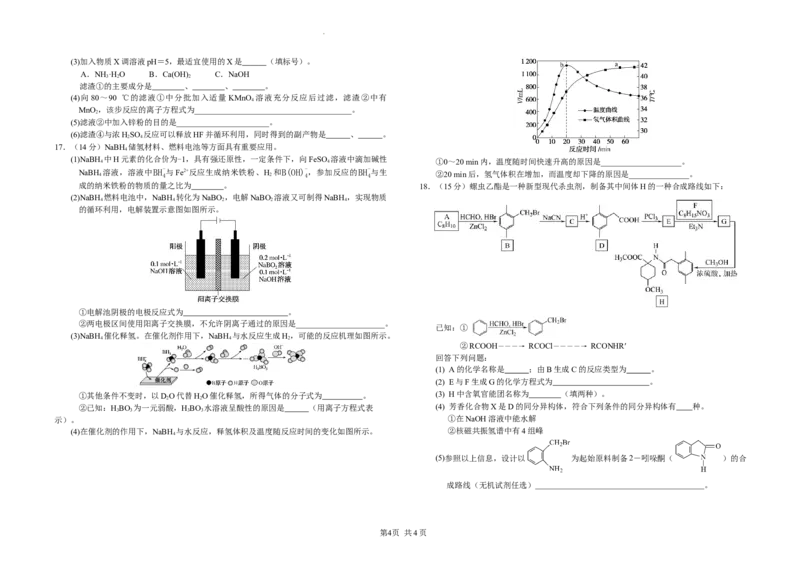
(1)NaBH 4 中H元素的化合价为-1,具有强还原性,一定条件下,向FeSO 4 溶液中滴加碱性 ①0~20 min内,温度随时间快速升高的原因是____________________。
NaBH
4
溶液,溶液中BH
4
-与Fe2+反应生成纳米铁粉、H
2
和B(OH)
4
-,参加反应的BH
4
-与生 ②20 min后,氢气体积在增加,而温度却下降的原因是_______________。
成的纳米铁粉的物质的量之比为 。 18.(15分)螺虫乙酯是一种新型现代杀虫剂,制备其中间体H的一种合成路线如下:
(2)NaBH 燃料电池中,NaBH 转化为NaBO ,电解NaBO 溶液又可制得NaBH ,实现物质
4 4 2 2 4
的循环利用,电解装置示意图如图所示。
①电解池阴极的电极反应式为 。
②两电极区间使用阳离子交换膜,不允许阴离子通过的原因是______________________。
已知:①
(3)NaBH 催化释氢。在催化剂作用下,NaBH 与水反应生成H,可能的反应机理如图所示。
4 4 2
②RCOOH―――→ RCOCl――――→ RCONHR′
回答下列问题:
(1) A的化学名称是 ;由B生成C的反应类型为 。
(2) E与F生成G的化学方程式为 。
①其他条件不变时,以DO代替HO催化释氢,所得气体的分子式为 。 (3) H中含氧官能团名称为 (填两种)。
2 2
②已知:HBO 为一元弱酸,HBO 水溶液呈酸性的原因是 (用离子方程式表 (4) 芳香化合物X是D的同分异构体,符合下列条件的同分异构体有 种。
3 3 3 3
示)。 ①在NaOH溶液中能水解
(4)在催化剂的作用下,NaBH 与水反应,释氢体积及温度随反应时间的变化如图所示。 ②核磁共振氢谱中有4组峰
4
(5)参照以上信息,设计以 为起始原料制备2-吲哚酮( )的合
成路线(无机试剂任选)__________________________________________。
第4页 共4页
学学科科网网((北北京京))股股份份有有限限公公司司