文档内容
澄宜六校联盟高三年级 10 月学情调研试卷
化 学
2025年10月
命题人:
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
1. 本试卷共7页,满分为100分,考试时间为75分钟。考试结束后,请将本试卷和答题卡交回。
2. 答题前,请务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题卡的规定
位置。
3. 请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4. 作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满涂黑;如需改动,请用橡皮擦干净
后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上的指定位置作
答,在其他位置作答一律无效。
5. 如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。
可能用到的相对原子质量:H 1 O 16 N14 Mg 24 Ga 70
一、单项选择题:本题包括13小题,每小题3分,共39分。每小题只有一个选项符合题意。
1.氮气是重要的工业原料。下列宜兴市的相关产业生产中以氮气作反应物的是
A.高性能氮化铝陶瓷制备
B.紫砂陶坯高温烧结
C.竹纤维水解制备羧甲基纤维素
D.污水处理厂尾气脱硝
2.反应11P+60CuSO +96HO=20Cu P+24HPO +60HSO 可用于处理不慎沾到皮肤上的白磷。
4 4 2 3 3 4 2 4
下列说法正确的是
A.HO的空间构型为V形
2
B.S2-的结构示意图为
C.P 分子中的键角为109°28'
4
D.基态Cu2+的价层电子排布式为3d84s1
3.下列与铁有关的实验对应装置或操作设计不能达到实验目的的是
甲 乙 丙 丁
A.用装置甲制备Fe(OH)
2
B.用装置乙在铁件外表镀一层光亮的铜
C.用装置丙蒸干Fe (SO ) 溶液获得硫酸铁晶体
2 4 3
D.用装置丁将铁与水蒸气反应并验证气体产物
4.高岭石的化学组成可表示为Al [Si O ](OH) ,其性质相当稳定,被誉为“万能石”,常作为制
4 4 10 8造瓷器和陶器的主要原料。下列说法正确的是
A.半径:r(Al3+)>r(O2-) B.第一电离能:I(Al)>I(Si)
1 1
C.酸性:HSiO<HCO D.热稳定性:SiH>HO
2 3 2 3 4 2
阅读下列材料,完成5~7题。
铁、钴、镍是第四周期第Ⅷ族元素,物理性质和化学性质比较相似。FeCl 溶液可用于蚀刻铜
3
制品、制备Fe(OH) 胶体,FeS可用于除去废水中的Cu2+。草酸钴(CoC O)可在空气中焙烧制备催
3 2 4
化剂Co O。废镍渣(NiO)与硫酸铵一起煅烧可得NiSO ,在碱性溶液中用NaClO氧化NiSO 可制得
3 4 4 4
电极材料NiO(OH)。铁、钴、镍能形成多种配合物,如(NH )Fe(SO )·6H O、[Co(NH )]Cl 、
4 2 4 2 2 3 6 3
Ni(CO) 等,其中Ni(CO) 常温下为液态,熔点低,易溶于CCl 、苯等有机溶剂。
4 4 4
5.下列说法正确的是
A.铁、钴、镍的基态原子最外层电子数不同
B.Ni(CO) 属于离子晶体
4
C.NH + 的键角比NH 的键角大
4 3
D.1 mol [Co(NH )]3+中有18 mol σ键
3 6
6.下列化学反应表示正确的是
A.向FeCl 溶液中加入NaCO:2Fe3++3CO2 -=Fe (CO)↓
3 2 3 3 2 3 3
B.用 FeCl 溶液制备Fe(OH) 胶体:Fe3++3HO Fe(OH) +3H+
3 3 2 3(胶体)
C.CoC O 在空气中焙烧:3CoC O=====CoO+3CO↑+3CO↑
2 4 2 4 3 4 2
D.NaClO氧化NiSO 制得电极材料:2Ni2++2ClO-+2OH-=2NiO(OH)↓+Cl↑
4 2
7.下列物质的结构与性质或性质与用途具有对应关系的是
A.FeCl 溶液呈酸性,可用于蚀刻铜制品
3
B.FeS有还原性,可用于除去废水中的Cu2+
C.Co O 难溶于水,可用作催化剂
3 4
D.Co3+有空轨道,可与NH 形成[Co(NH )]3+
3 3 6
8.在给定条件下,下列物质间的转化均可实现的是
A.FeS―—_x001F_—→SO ―—_x001F_—→NaSO
2 2 2 4
B.漂白粉―—_x001F_—→HClO―——→Cl
2
C.CuO―—_x001F_—→Cu(OH) ―——→Cu O
2 2
D.SiO―—_x001F_—→CO―———→HSiO
2 2 2 3
9.前四周期主族元素X、Y、Z、W的原子序数依次增大,且位于周期表4个不同的周期。Y的电
负性仅次于氟元素,常温下Z单质是气体,基态W原子的外围电子排布为ns2np5。下列有关说法
正确的是
A.W位于元素周期表中第四周期ⅤA族
B.Z的最高价氧化物的水化物为弱酸
C.X与Y组成的化合物分子间可形成氢键
D.Z和W形成的化合物中W显负价
10.全固态氟离子电池的固态电解质晶胞如图所示。F-电池工作时,发生迁移。晶胞参数越大,可
供离子迁移的空间越大,越有利于离子传输。F位点空缺也可使离子传输更加高效。下列说法不
正确的是
A. 晶体中与Cs距离最近且相等的F有12个
B. 该固态电解质的化学式为CsPbF
3
C. 在Pb位点掺杂K,F位点将出现空缺
D. 随Pb位点掺杂K含量的增大,离子传输效率一定提高11.室温下,下列实验方案能达到探究目的的是
选项 实验方案 探究目的
A 将红热的木炭投入浓HNO 中,有红棕色气体产生 证明木炭具有还原性
3
在N 氛围中高温加热FeSO 固体使其分解,将气体产物
2 4
FeSO 分解的气体产物
4
B 依次通入Ba(NO ) 溶液和品红溶液,Ba(NO ) 溶液产生白
3 2 3 2
中有SO ,没有SO
3 2
色沉淀,品红溶液不褪色
结合H+的能力:
C 向Na[Al(OH)]溶液中滴加NaHSO 溶液,产生白色沉淀
4 3
[Al(OH) ]->SO 2 -
4 3
将生锈的铁钉置于稀盐酸中充分反应后,向所得溶液中滴
D 铁锈中不含有Fe3+
加KSCN溶液,无明显现象
12.室温下,通过下列实验探究Ca(ClO) 溶液的性质。
2
实验1:向0.1 mol·L-1 Ca(ClO) 溶液中滴加酚酞试剂,溶液先变红后褪色。
2
实验2:向0.1 mol·L-1 Ca(ClO) 溶液中通入少量CO 气体,出现白色沉淀。
2 2
实验3:向0.1 mol·L-1 Ca(ClO) 溶液中通入少量SO 气体,出现白色沉淀。
2 2
下列说法不正确的是
A.实验1说明Ca(ClO) 溶液中存在反应ClO-+HO HClO+OH-
2 2
B.Ca(ClO) 溶液中存在:c(OH-)=c(H+)+c(HClO)
2
C.实验2反应静置后的上层清液中有c(Ca2+)·c(CO2 -)=K (CaCO)
3 sp 3
D.实验3中生成的白色沉淀主要成分是CaSO
3
13.废旧CPU中的金(Au)、Ag和Cu回收的部分流程如下:
已知:HAuCl === H++AuCl
4
4
-
。
下列说法正确的是
A.“酸溶”时用浓硝酸产生NO 的量比稀硝酸的少
x
B.“过滤”所得滤液中的Cu2+和Ag+可用过量浓氨水分离
C.用浓盐酸和NaNO 也可以溶解金
3
D.用过量Zn粉将1 mol HAuCl 完全还原为Au,参加反应的Zn为1.5 mol
4
二、非选择题:本题共4小题,共61分。
14.(16分)从锡冶炼烟尘(含SnO 、ZnO、CdO、SnS及少量Fe O、As O)中脱除砷,并分离回收锡、
2 2 3 2 3
锌、镉的部分工艺流程如下图。已知:i.SnO 难溶于水和稀酸;酸浓度越高,SnO 溶解得越多。
2 2
ii.HAsO 、HAsO 均为弱酸,FeAsO 难溶于水。
3 3 3 4 4
(1)酸性条件下,SnS易被O 氧化为SnO 。
2 2
反应分两步:i.SnS+2H+=Sn2++HS;ii. ▲ 。
2
(2)浸出液中含有H+、SO 2 -、Zn2+、Cd2+、HAsO 、Fe2+等微粒。硫酸浓度、浸出时间等
4 3 3
条件不变时,反应温度对烟尘中锡、锌、镉浸出率的影响如题14图-1所示。
① 酸浸过程中铁元素被还原,还原剂是 ▲ 。
② 升高温度有利于减少浸出液中锡元素的残留。反应温度升高,锡浸出率下降的可能原
因有 ▲ 。
(3)向浸出液中加入HO 溶液,随后用CaO调pH至4~6,产生富砷渣(主要含FeAsO )。该
2 2 4
种脱砷方法称为FeAsO 沉淀法。
4
① 加入 HO 溶液的目的是 ▲ 。
2 2
② 若将烟尘中的砷充分转化为FeAsO 沉淀脱除,烟尘成分应满足的条件是 ▲ 。
4
(4)置换时,先加入接近理论投加量的锌粉,充分反应后过滤,再向滤液2中加入少量锌粉。
这样操作的目的有 ▲ (写两点)。
(5)锌黄锡矿(K型)是制备薄膜太阳能电池的重要原料。其晶胞结构如题14图-2所示,该晶
胞化学式为 ▲ 。
15.(15分)利用镁泥(主要成分为MgCO 、FeCO 和SiO 等)为主要原料制取碳酸镁(MgCO ·3HO)的
3 3 2 3 2
工业流程如下:
(1)酸溶。某工厂用1.78吨发烟硫酸(化学式:HSO ·SO )配制质量分数为50% HSO 溶液,
2 4 3 2 4
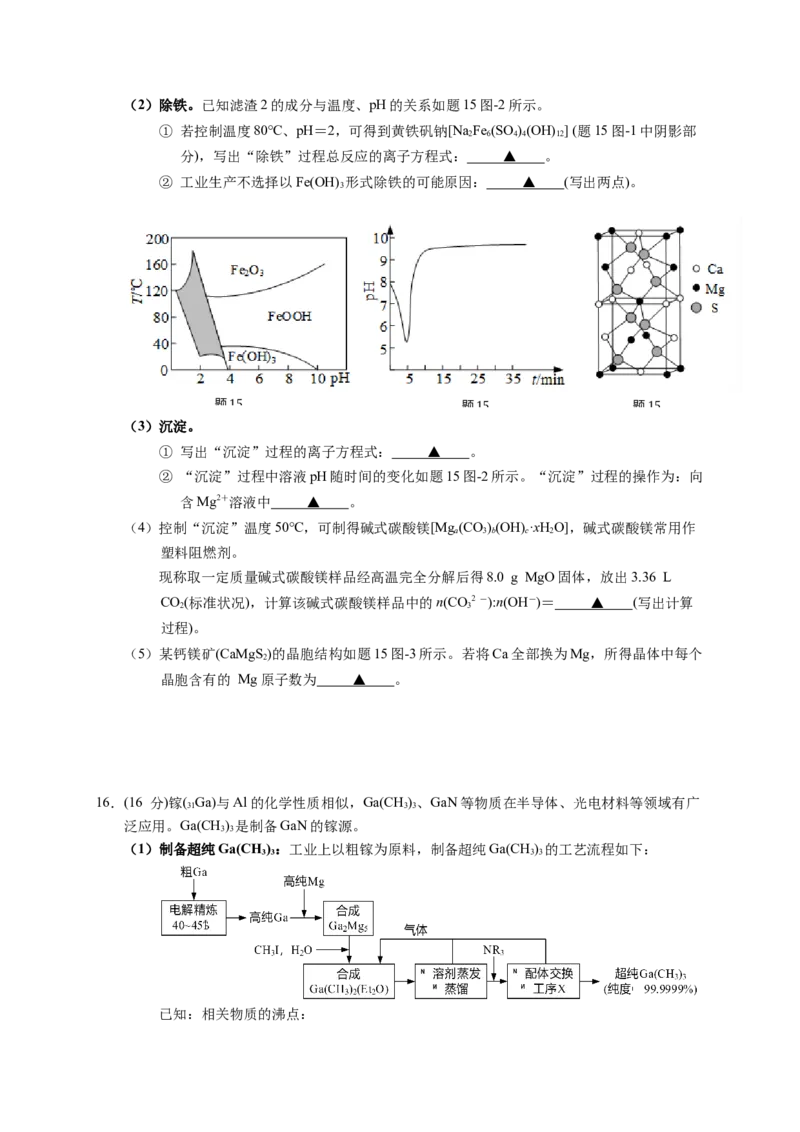
配制时需要水的质量为 ▲ 吨。(2)除铁。已知滤渣2的成分与温度、pH的关系如题15图-2所示。
① 若控制温度80℃、pH=2,可得到黄铁矾钠[Na Fe (SO )(OH) ] (题15图-1中阴影部
2 6 4 4 12
分),写出“除铁”过程总反应的离子方程式: ▲ 。
② 工业生产不选择以Fe(OH) 形式除铁的可能原因: ▲ (写出两点)。
3
题 题 题
(3)沉淀。
15 15 15
① 写出“沉淀”过程的离子方程式: ▲ 。
② “沉淀”过程中溶液pH随时间的变化如题15图-2所示。“沉淀”过程的操作为:向
含Mg2+溶液中 ▲ 。
(4)控制“沉淀”温度50℃,可制得碱式碳酸镁[Mg (CO)(OH)·xHO],碱式碳酸镁常用作
a 3 b c 2
塑料阻燃剂。
现称取一定质量碱式碳酸镁样品经高温完全分解后得8.0 g MgO固体,放出3.36 L
CO(标准状况),计算该碱式碳酸镁样品中的n(CO2 -):n(OH-)= ▲ (写出计算
2 3
过程)。
(5)某钙镁矿(CaMgS )的晶胞结构如题15图-3所示。若将Ca全部换为Mg,所得晶体中每个
2
晶胞含有的 Mg原子数为 ▲ 。
16.(16 分)镓( Ga)与Al的化学性质相似,Ga(CH )、GaN等物质在半导体、光电材料等领域有广
31 3 3
泛应用。Ga(CH ) 是制备GaN的镓源。
3 3
(1)制备超纯Ga(CH ):工业上以粗镓为原料,制备超纯Ga(CH ) 的工艺流程如下:
3 3 3 3
已知:相关物质的沸点:物质 Ga Ga(CH ) EtO(乙醚) CHI NR
3 3 2 3 3
沸点/C 29.8 55.7 34.6 42.4 365.8
① 分子中的C-Ga-C键角大小:Ga(CH ) ▲ Ga(CH )(Et O) (填
3 3 3 3 2
“>”、“=”或“<”)。
②“合成Ga(CH )(Et O)”工序中的产物还包括MgI 和CHMgI,写出该反应的化学方程
3 3 2 2 3
式: ▲ 。
③“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是 ▲ 。
④ 直接分解Ga(CH )(Et O)不能制备超纯Ga(CH ),而本流程采用“配体交换”工艺制
3 3 2 3 3
备超纯Ga(CH ) 的理由是 ▲ 。
3 3
(2)氮化镓(GaN)的制备并测定纯度:
① 测定GaN样品的纯度:准确称取0.2000 g GaN样品,加入NaOH溶液并加热使固体
充分溶解,用足量HBO 溶液吸收产生的NH 。向吸收液中滴加指示剂,用0.1000
3 3 3
mol·L-1 的盐酸滴定至终点,四次平行实验滴定所消耗盐酸的体积分别为:23.01
mL、22.50 mL、23.00 mL、22.99 mL。过程中涉及反应:NH +HBO=
3 3 3
NH ·H BO;NH ·H BO+HCl=NH Cl+HBO,计算GaN样品的纯度 ▲ (写出
3 3 3 3 3 3 4 3 3
计算过程)。
② 工业上常利用炼锌矿渣[主要含铁酸镓Ga(Fe O)、铁酸锌ZnFe O、SiO]为原料来制
2 2 4 3 2 4 2
备高产率的GaN。请补充完整实验方案:取一定量的炼锌矿渣经稀硫酸充分反应后过
滤,取酸浸液分批加入ZnO粉末并不断搅拌至溶液pH为4.0,过滤,洗涤, ▲
,向有机层中加入2 mol·L-1的盐酸充分振荡后, ▲ ,向溶液中滴加1 mol·L-
1 的 NaOH溶液至不再产生沉淀,过滤,洗涤,干燥,将得到的固体热分解得到
GaO,并利用CVD(化学气相沉积)技术将热分解得到的GaO 与NH 在高温下反应
2 3 2 3 3
可制得GaN。
(实验中必须使用的试剂:1 mol·L-1 的 NaSO 溶液,2 mol·L-1 的硫酸,KSCN溶
2 3
液,P204)
已知:① P204对Zn2+、Ga3+和 Fe3+都有萃取作用,对Fe2+无萃取作用。
② Zn2+开始沉淀的pH为6.0,Ga3+完全沉淀的pH为4.0,Fe3+完全沉淀的pH为
3.2。
17.(14分)工业废水中的重金属离子会导致环境污染危害人体健康,可用多种方法去除。
Ⅰ.臭氧法
络合态的金属离子难以直接去除。O 与水反应产生的·OH (羟基自由基)可以氧化分解金属配
3
合物[mRa+·nX]中的有机配体,使金属离子游离到水中,反应原理为:
·OH+[mRa+·nX] → mRa++CO+HO(Ra+表示金属离子,X表示配体)
2 2
·OH同时也能与溶液中的CO
3
-2 、HCO反应。在某废水中加入Ca(OH) ,再通入O 可处理其 2 3
中的络合态镍(II)。
(1)基态Ni2+的核外电子排布式为 ▲ 。
(2)加入的Ca(OH) 的作用是 ▲ 。
2
Ⅱ.纳米零价铝法
纳米铝粉有很强的吸附性和还原性,水中溶解的氧在纳米铝粉表面产生·OH (羟基自由基),可将甘氨酸铬中的有机基团降解,释放出的铬(Ⅵ)被纳米铝粉去除。
(3)向AlCl 溶液中滴加碱性NaBH 溶液,溶液中BH(B元素的化合价为+3)与Al3+反应可生
3 4
成纳米铝粉、H 和B(OH),其离子方程式为 ▲ 。
2
(4)向含有甘氨酸铬的废水中加入纳米铝粉,研究溶液中总氮含量随时间的变化可知甘氨酸
铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如题17-1图所示,
反应初期溶液中的总氮含量[ 先迅速降低后随即上升的原因是 ▲ 。
]
Ⅲ.金属炭法
其他条件相同,分别取铝炭混合物和铁炭混合物,与含Zn2+的废水反应相同时间,Zn2+去除率
与废水pH的关系如题17图-2所示。
(5)废水pH为3时,铝炭混合物对Zn2+去除率远大于铁炭混合物的主要原因是 ▲ 。
(6)废水pH大于6,随着pH增大,铝炭混合物对Zn2+去除率增大的原因是 ▲ 。