文档内容
湖北省仙桃中学 2025-2026 学年度上学期高三期中考试
高三化学试卷
试卷满分:100分
可能用到的相对原子质量:H 1 B 10.8 C 12 O 16 Mg 24 S 32
一、选择题:本题共15小题,每小题3分,共45分,在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与社会生活密切相关,下列表述错误的是
A. 新型手机以石墨烯为材料利用其电阻率低、热导率高
B. 聚乳酸、淀粉等混合制成的一次性餐具会造成白色污染
C. 我国研制的超级钢性能居于世界领先水平,属于合金
D. 蚂蚁打架喷射的有机胺、甲酸可反应生成离子液体
2. 下列说法正确的是
A. 第二周期元素中,第一电离能介于B和O之间的元素有3种
B. O 分子的球棍模型:
3
C. 电负性越大,元素的非金属性越强,第一电离能也越大
D. 二甲基硅二醇经脱水缩聚生成聚硅氧烷:
3. 已知反应: ,设 为阿伏加德罗常数
的值,下列有关说法正确的是
A. 标准状况下, 乙酸含有的 键数目为
B. 向足量乙醇中加入 金属钠,转移电子数为
C. 乙醇与等量乙酸充分发生上述反应,生成乙酸乙酯分子的数目为
D. 醋酸钠溶于稀醋酸中使溶液呈中性,混合溶液中 数目小于
4. 下列过程中发生反应的离子方程式书写错误的是
A. 铅酸蓄电池总反应:B. 用绿矾处理酸性重铬酸根离子:
C. 碱性条件下用次氯酸钠与 制备绿色消毒剂高铁酸钠:
D. 等物质的量浓度的NH Al(SO ) 与Ba(OH) 溶液按体积比为1:2反应:
4 4 2 2
5. 下列对物质性质比较结果的原因解释错误的是
选
性质比较 原因
项
氧化性:
配位键的电子占据 的空轨道,导致 得电
A
子能力减弱
B 在水中的溶解度: O 相对分子质量小
2
C 沸点:乙醇>一氯乙烷 乙醇分子之间可以形成氢键
与金属钠反应剧烈程度:水> 乙基是推电子基,使乙醇羟基中的O-H键的极性
D
乙醇 减弱
A. A B. B C. C D. D
6. X、Y、Z和R为原子序数依次增大的短周期主族元素,其中Y、Z和R处于同一周期,R是非金属性最
强的元素。一定条件下,上述元素形成的物质M可发生如下转化。下列说法正确的是
A. YR 是含有极性键的极性分子
3
B. M、N中原子均达到八电子稳定结构
C. M中含有的化学键为离子键、氢键和共价键
D. 简单氢化物的沸点:Z>R
7. “证据推理与模型认知”是高中化学学科核心素养之一,也是学习化学的重要方法,相关说法正确的是
A. CuS固体难溶于稀硫酸,推测FeS固体也难溶于稀硫酸
B. HCl气体常温下易溶于水,推测HI气体常温下也易溶于水
C. 常温下CaCO 的溶解度小于Ca(HCO ),推测水溶液中溶解度NaCO 小于NaHCO
3 3 2 2 3 3D. CH 的正四面体结构中键角为 ,推测P 的正四面体结构中键角也是
4 4
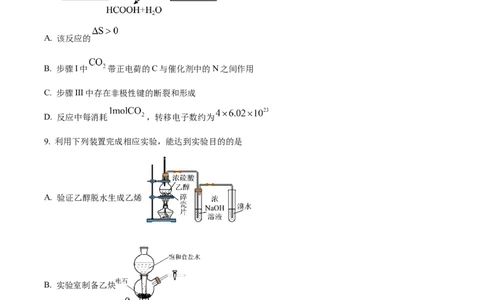
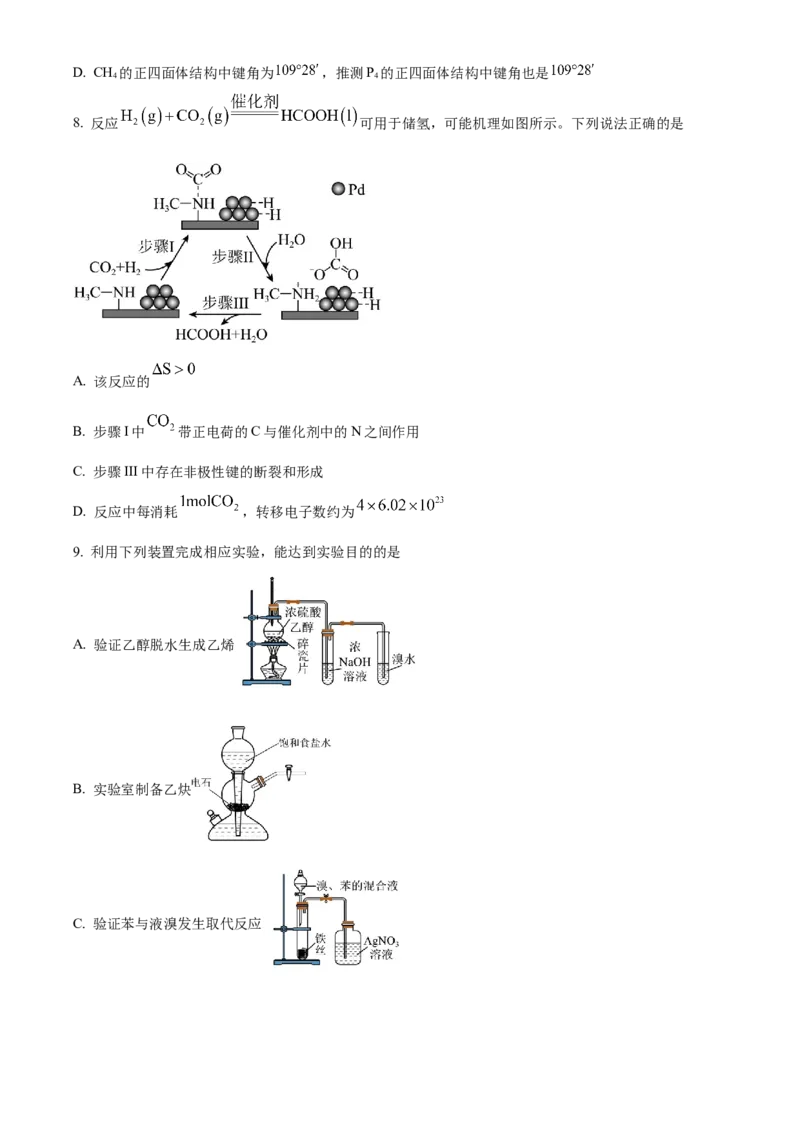
8. 反应 可用于储氢,可能机理如图所示。下列说法正确的是
A. 该反应的
B. 步骤I中 带正电荷的C与催化剂中的N之间作用
C. 步骤III中存在非极性键的断裂和形成
D. 反应中每消耗 ,转移电子数约为
9. 利用下列装置完成相应实验,能达到实验目的的是
A. 验证乙醇脱水生成乙烯
B. 实验室制备乙炔
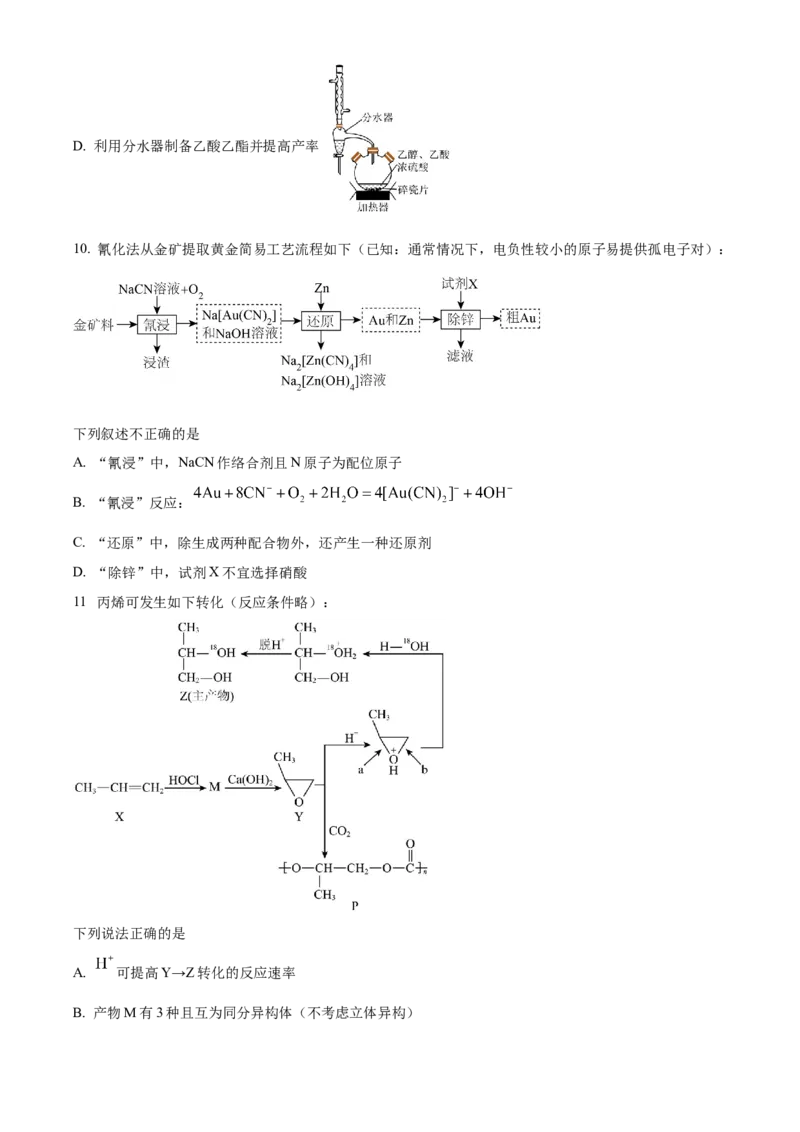
C. 验证苯与液溴发生取代反应D. 利用分水器制备乙酸乙酯并提高产率
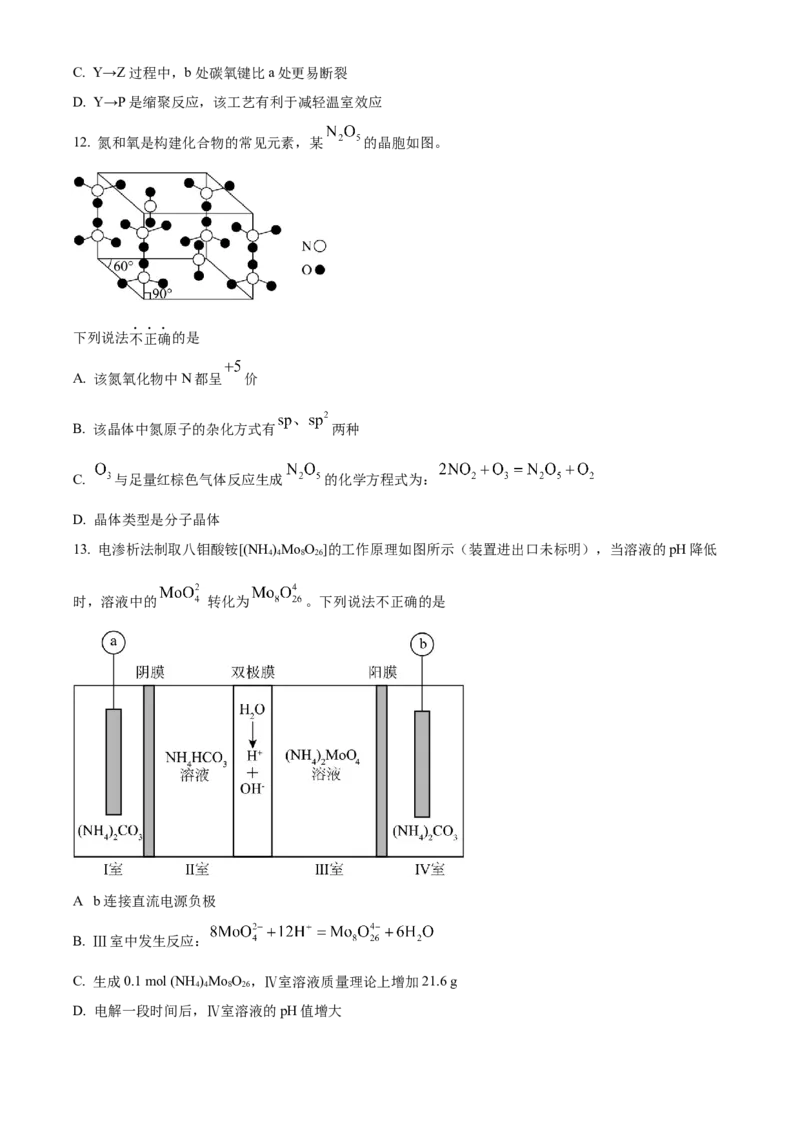
10. 氰化法从金矿提取黄金简易工艺流程如下(已知:通常情况下,电负性较小的原子易提供孤电子对):
下列叙述不正确的是
A. “氰浸”中,NaCN作络合剂且N原子为配位原子
B. “氰浸”反应:
C. “还原”中,除生成两种配合物外,还产生一种还原剂
D. “除锌”中,试剂X不宜选择硝酸
.
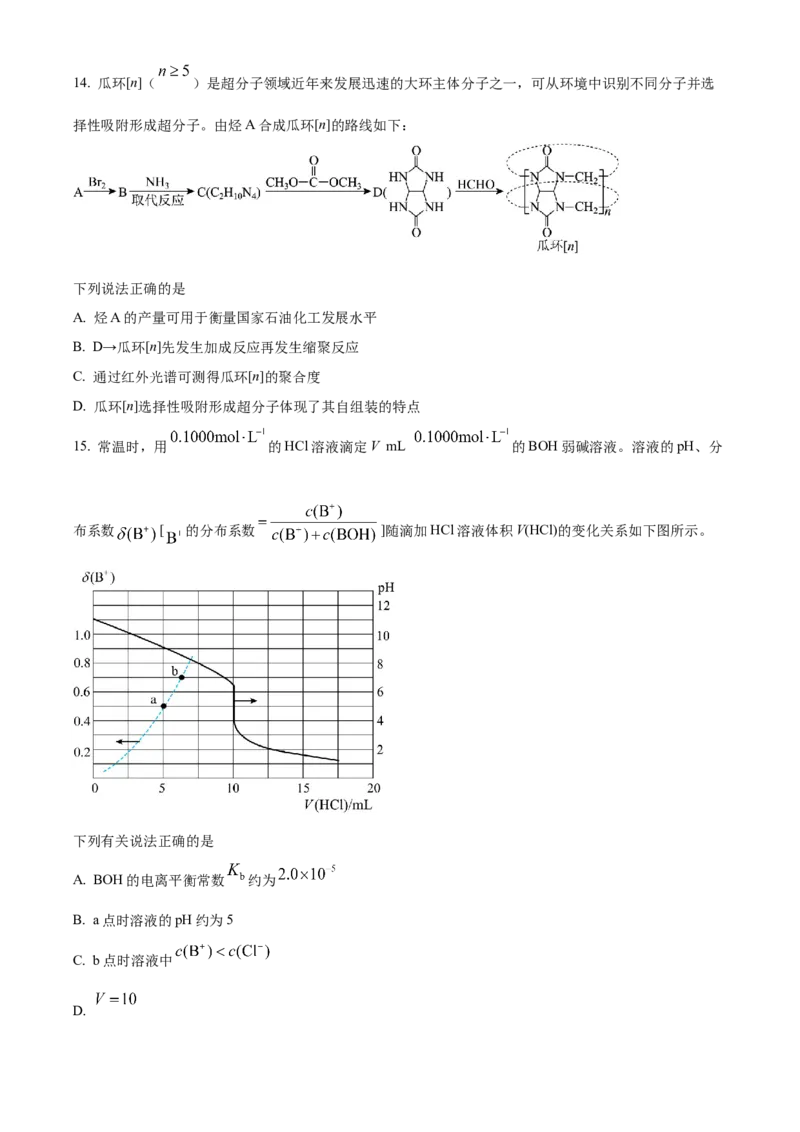
11 丙烯可发生如下转化(反应条件略):
下列说法正确的是
A. 可提高Y→Z转化的反应速率
B. 产物M有3种且互为同分异构体(不考虑立体异构)C. Y→Z过程中,b处碳氧键比a处更易断裂
D. Y→P是缩聚反应,该工艺有利于减轻温室效应
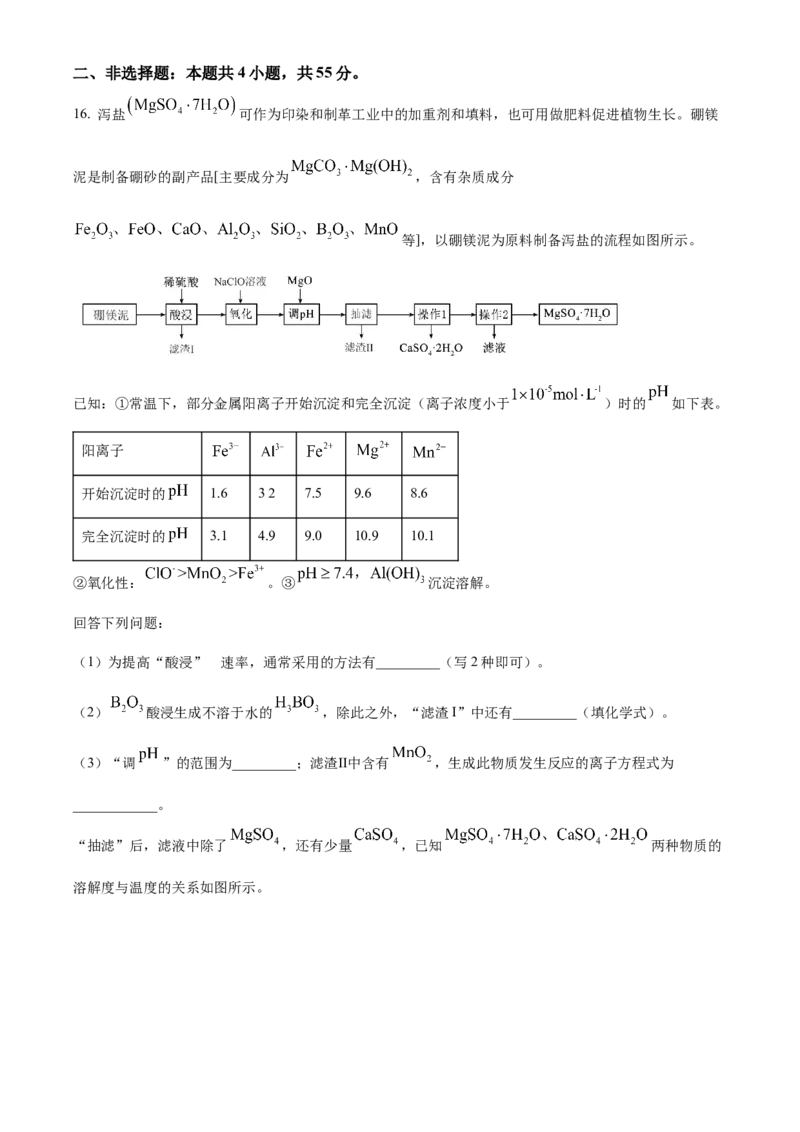
12. 氮和氧是构建化合物的常见元素,某 的晶胞如图。
下列说法不正确的是
A. 该氮氧化物中N都呈 价
B. 该晶体中氮原子的杂化方式有 两种
C. 与足量红棕色气体反应生成 的化学方程式为:
D. 晶体类型是分子晶体
13. 电渗析法制取八钼酸铵[(NH )MoO ]的工作原理如图所示(装置进出口未标明),当溶液的pH降低
4 4 8 26
时,溶液中的 转化为 。下列说法不正确的是
.
A b连接直流电源负极
B. Ⅲ室中发生反应:
C. 生成0.1 mol (NH )MoO ,Ⅳ室溶液质量理论上增加21.6 g
4 4 8 26
D. 电解一段时间后,Ⅳ室溶液的pH值增大14. 瓜环[n]( )是超分子领域近年来发展迅速的大环主体分子之一,可从环境中识别不同分子并选
择性吸附形成超分子。由烃A合成瓜环[n]的路线如下:
下列说法正确的是
A. 烃A的产量可用于衡量国家石油化工发展水平
B. D→瓜环[n]先发生加成反应再发生缩聚反应
C. 通过红外光谱可测得瓜环[n]的聚合度
D. 瓜环[n]选择性吸附形成超分子体现了其自组装的特点
15. 常温时,用 的HCl溶液滴定V mL 的BOH弱碱溶液。溶液的pH、分
布系数 [ 的分布系数 ]随滴加HCl溶液体积V(HCl)的变化关系如下图所示。
下列有关说法正确的是
A. BOH的电离平衡常数 约为
B. a点时溶液的pH约为5
C. b点时溶液中
D.二、非选择题:本题共4小题,共55分。
16. 泻盐 可作为印染和制革工业中的加重剂和填料,也可用做肥料促进植物生长。硼镁
泥是制备硼砂的副产品[主要成分为 ,含有杂质成分
等],以硼镁泥为原料制备泻盐的流程如图所示。
已知:①常温下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于 )时的 如下表。
阳离子
.
开始沉淀时的 1.6 32 7.5 9.6 8.6
完全沉淀时的 3.1 4.9 9.0 10.9 10.1
②氧化性: 。③ 沉淀溶解。
回答下列问题:
的
(1)为提高“酸浸” 速率,通常采用的方法有_________(写2种即可)。
(2) 酸浸生成不溶于水的 ,除此之外,“滤渣I”中还有_________(填化学式)。
(3)“调 ”的范围为_________;滤渣Ⅱ中含有 ,生成此物质发生反应的离子方程式为
____________。
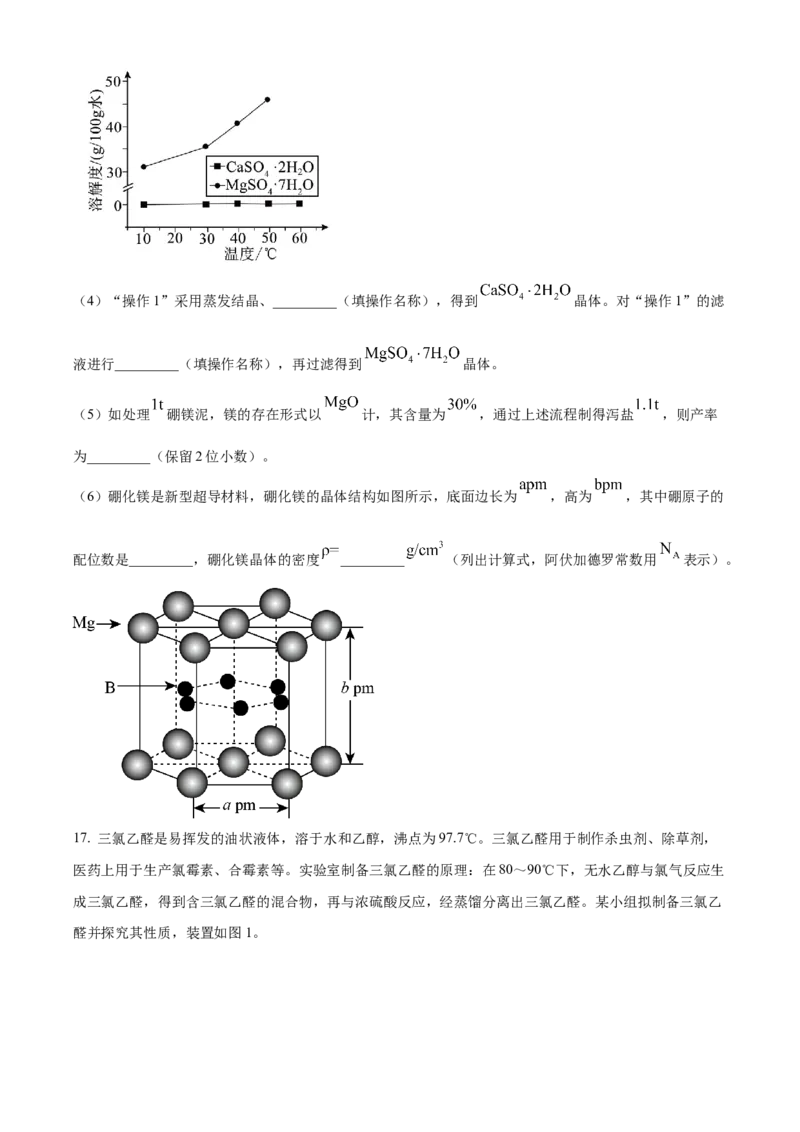
“抽滤”后,滤液中除了 ,还有少量 ,已知 两种物质的
溶解度与温度的关系如图所示。(4)“操作1”采用蒸发结晶、_________(填操作名称),得到 晶体。对“操作1”的滤
液进行_________(填操作名称),再过滤得到 晶体。
(5)如处理 硼镁泥,镁的存在形式以 计,其含量为 ,通过上述流程制得泻盐 ,则产率
为_________(保留2位小数)。
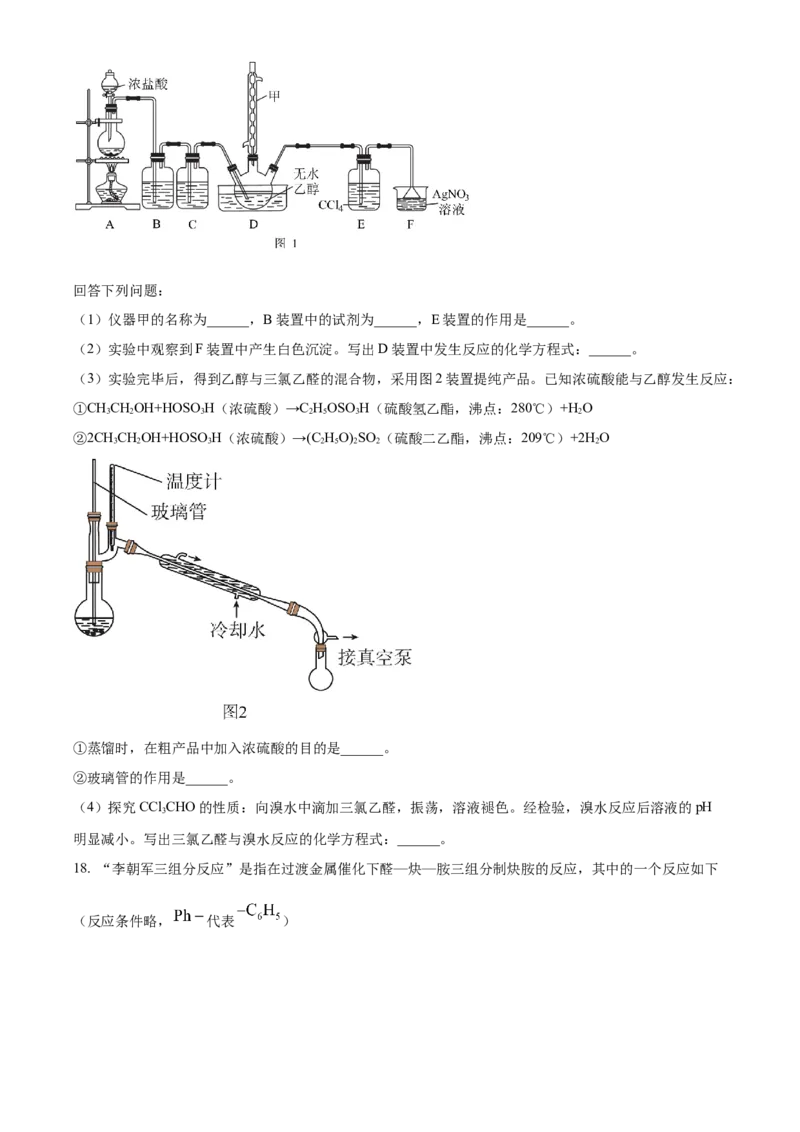
(6)硼化镁是新型超导材料,硼化镁的晶体结构如图所示,底面边长为 ,高为 ,其中硼原子的
配位数是_________,硼化镁晶体的密度 _________ (列出计算式,阿伏加德罗常数用 表示)。
17. 三氯乙醛是易挥发的油状液体,溶于水和乙醇,沸点为97.7℃。三氯乙醛用于制作杀虫剂、除草剂,
医药上用于生产氯霉素、合霉素等。实验室制备三氯乙醛的原理:在80~90℃下,无水乙醇与氯气反应生
成三氯乙醛,得到含三氯乙醛的混合物,再与浓硫酸反应,经蒸馏分离出三氯乙醛。某小组拟制备三氯乙
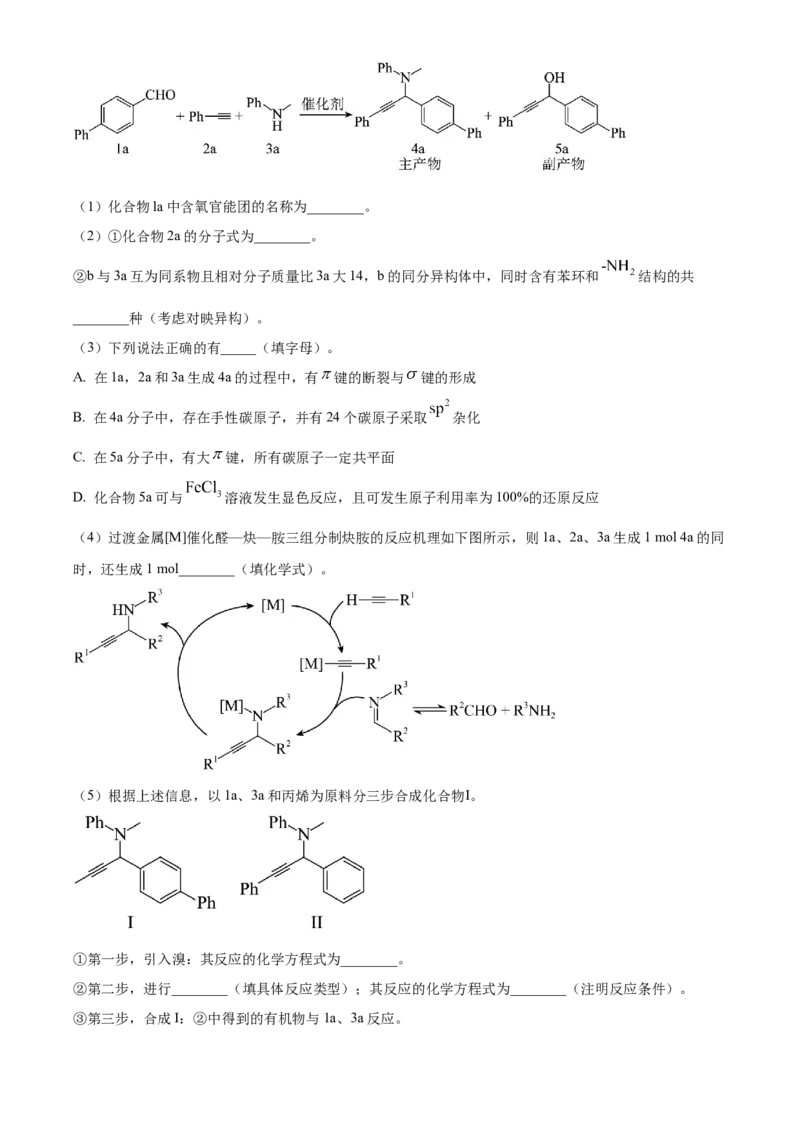
醛并探究其性质,装置如图1。回答下列问题:
(1)仪器甲的名称为______,B装置中的试剂为______,E装置的作用是______。
(2)实验中观察到F装置中产生白色沉淀。写出D装置中发生反应的化学方程式:______。
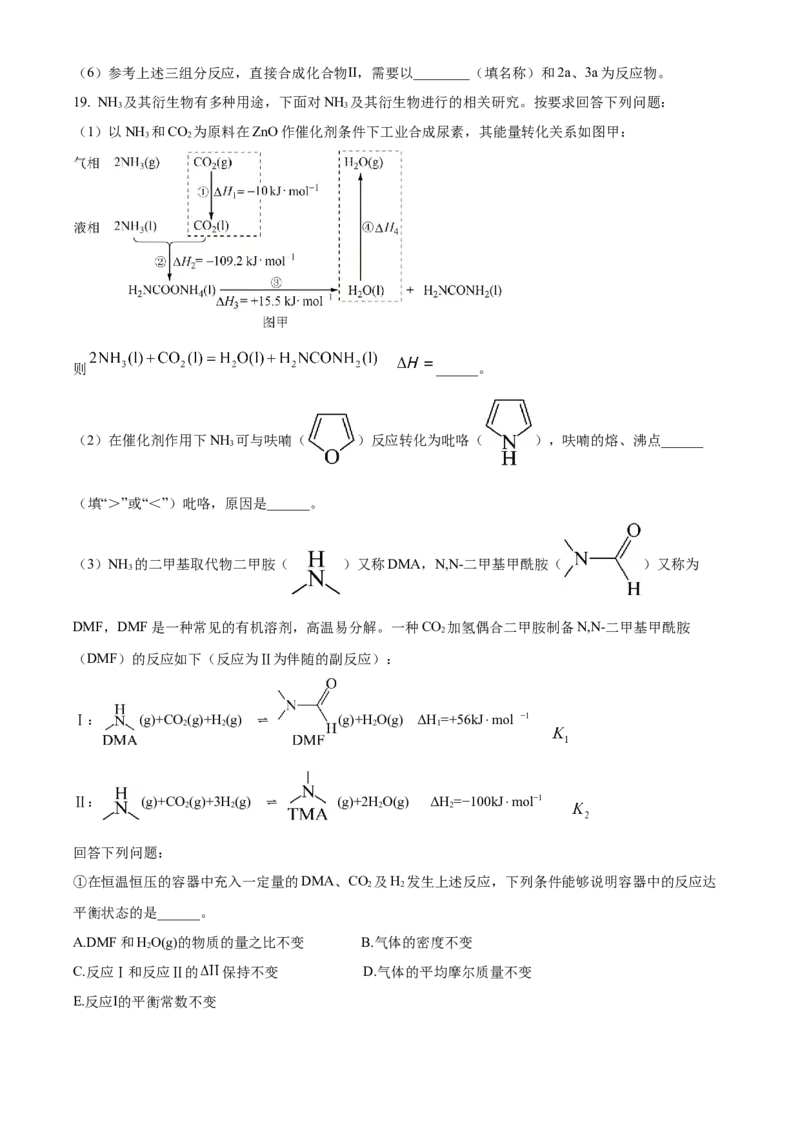
(3)实验完毕后,得到乙醇与三氯乙醛的混合物,采用图2装置提纯产品。已知浓硫酸能与乙醇发生反应:
①CHCHOH+HOSO H(浓硫酸)→C HOSO H(硫酸氢乙酯,沸点:280℃)+H O
3 2 3 2 5 3 2
②2CHCHOH+HOSO H(浓硫酸)→(C HO) SO (硫酸二乙酯,沸点:209℃)+2H O
3 2 3 2 5 2 2 2
①蒸馏时,在粗产品中加入浓硫酸的目的是______。
②玻璃管的作用是______。
(4)探究CCl CHO的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,溴水反应后溶液的pH
3
明显减小。写出三氯乙醛与溴水反应的化学方程式:______。
18. “李朝军三组分反应”是指在过渡金属催化下醛—炔—胺三组分制炔胺的反应,其中的一个反应如下
(反应条件略, 代表 )(1)化合物la中含氧官能团的名称为________。
(2)①化合物2a的分子式为________。
②b与3a互为同系物且相对分子质量比3a大14,b的同分异构体中,同时含有苯环和 结构的共
________种(考虑对映异构)。
(3)下列说法正确的有_____(填字母)。
A. 在1a,2a和3a生成4a的过程中,有 键的断裂与 键的形成
B. 在4a分子中,存在手性碳原子,并有24个碳原子采取 杂化
C. 在5a分子中,有大 键,所有碳原子一定共平面
D. 化合物5a可与 溶液发生显色反应,且可发生原子利用率为100%的还原反应
(4)过渡金属[M]催化醛—炔—胺三组分制炔胺的反应机理如下图所示,则1a、2a、3a生成1 mol 4a的同
时,还生成1 mol________(填化学式)。
(5)根据上述信息,以1a、3a和丙烯为原料分三步合成化合物Ⅰ。
①第一步,引入溴:其反应的化学方程式为________。
②第二步,进行________(填具体反应类型);其反应的化学方程式为________(注明反应条件)。
③第三步,合成I:②中得到的有机物与1a、3a反应。(6)参考上述三组分反应,直接合成化合物Ⅱ,需要以________(填名称)和2a、3a为反应物。
19. NH 及其衍生物有多种用途,下面对NH 及其衍生物进行的相关研究。按要求回答下列问题:
3 3
(1)以NH 和CO 为原料在ZnO作催化剂条件下工业合成尿素,其能量转化关系如图甲:
3 2
则 ______。
(2)在催化剂作用下NH 可与呋喃( )反应转化为吡咯( ),呋喃的熔、沸点______
3
(填“>”或“<”)吡咯,原因是______。
(3)NH 的二甲基取代物二甲胺( )又称DMA,N,N-二甲基甲酰胺( )又称为
3
DMF,DMF是一种常见的有机溶剂,高温易分解。一种CO 加氢偶合二甲胺制备N,N-二甲基甲酰胺
2
(DMF)的反应如下(反应为Ⅱ为伴随的副反应):
Ⅰ: (g)+CO 2 (g)+H 2 (g) ⇌ (g)+H 2 O(g) ΔH 1 =+56kJ⋅mol −1
Ⅱ: (g)+CO 2 (g)+3H 2 (g) ⇌ (g)+2H 2 O(g) ΔH 2 =−100kJ⋅mol−1
回答下列问题:
①在恒温恒压的容器中充入一定量的DMA、CO 及H 发生上述反应,下列条件能够说明容器中的反应达
2 2
平衡状态的是______。
A.DMF和HO(g)的物质的量之比不变 B.气体的密度不变
2
C.反应Ⅰ和反应Ⅱ的 保持不变 D.气体的平均摩尔质量不变
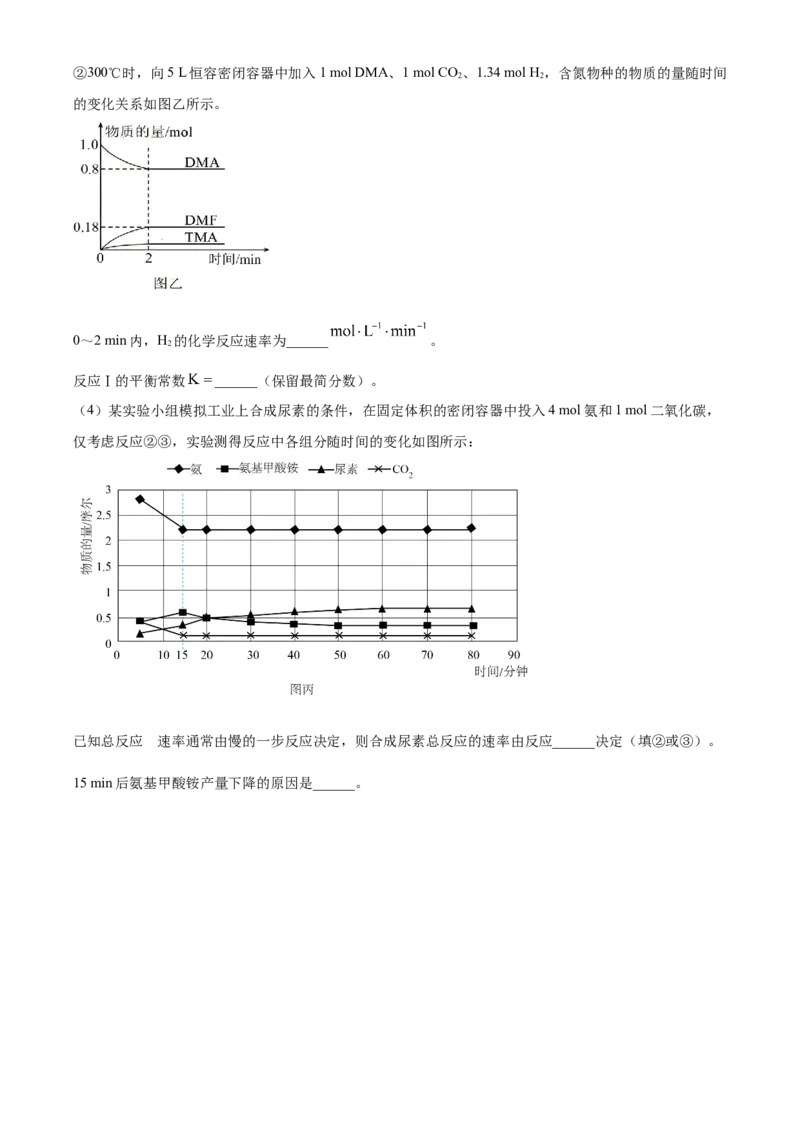
E.反应Ⅰ的平衡常数不变②300℃时,向5 L恒容密闭容器中加入1 mol DMA、1 mol CO 、1.34 mol H,含氮物种的物质的量随时间
2 2
的变化关系如图乙所示。
0~2 min内,H 的化学反应速率为______ 。
2
反应Ⅰ的平衡常数 ______(保留最简分数)。
(4)某实验小组模拟工业上合成尿素的条件,在固定体积的密闭容器中投入4 mol氨和1 mol二氧化碳,
仅考虑反应②③,实验测得反应中各组分随时间的变化如图所示:
的
已知总反应 速率通常由慢的一步反应决定,则合成尿素总反应的速率由反应______决定(填②或③)。
15 min后氨基甲酸铵产量下降的原因是______。