文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
眉山市 2023 年初中学业水平暨高中阶段学校招生考试理科
综合能力测试化学试卷
注意事项:
1.本试卷分第Ⅰ卷(选择题:1-14小题为化学;15-26小题为物理)和第Ⅱ卷(非选择题:第一部
分物理,27-38小题;第二部分化学,39-44小题)。全卷共14页,满分150分,考试时间120
分钟。
2.在答题前,考生务必将自己的姓名、座位号、准考证号准确填写在答题卡相应的位置。
3.答选择题时,必须使用2B铅笔将答题卡上对应题号的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其它答案标号;答非选择题时,必须使用0.5毫米黑色签字笔将答案书写在
答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上答题无效;考试结束后,将试卷和答题卡一并
交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Fe-56
第Ⅰ卷(选择题1-26小题,共64分)
一、选择题(本大题共26个小题,1-14每小题2分,15-26每小题3分,共计64分;在每小题
列出的四个选项中,只有一项符合题目要求)
1. 从中草药中分离出青蒿素,应用于疟疾的治疗,从而获得了诺贝尔医学奖的科学家是
A. 侯德榜 B. 屠呦呦 C. 门捷列夫 D. 道尔顿
【答案】B
【解析】
【详解】A、侯德榜发明了制碱法,不符合题意;
B、屠呦呦从中草药中分离出青蒿素,从而获得了诺贝尔医学奖,符合题意;
C、门捷列夫编写了元素周期表,不符合题意;
D、道尔顿提出了原子论,不符合题意。
故选B。
2. 空气中体积分数约占78%的气体是
A. 二氧化碳 B. 氮气 C. 氧气 D. 稀有气体
【答案】B
【解析】
【详解】空气的成分按体积分数计算:氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳0.03%,
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
其他气体和杂质0.03%。
3. 化学与我们的生活息息相关,下列说法错误的是
A. 氮气可用于食品充氮防腐
B. 活性炭可用于冰箱除味剂
C. 氢氧燃料电池用作汽车的驱动电源可以减少空气污染
D. 商场里标有“补钙”“补铁”的保健品,这里的“钙铁”指的是单质
【答案】D
【解析】
【详解】A、氮气在常温化学性质很稳定,可用于食品充氮防腐,A选项正确;
B、活性炭具有吸附性,可用于冰箱除味剂,B选项正确;
C、氢气燃烧只生成水,对环境无污染,所以氢氧燃料电池用作汽车的驱动电源可以减少空气污染,C选
项正确;
D、商场里标有“补钙”“补铁”的保健品,这里的“钙铁”指的是元素,D选项错误。
故选:D。
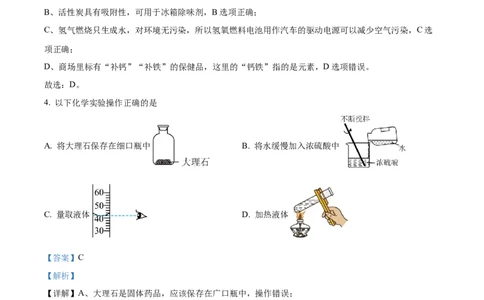
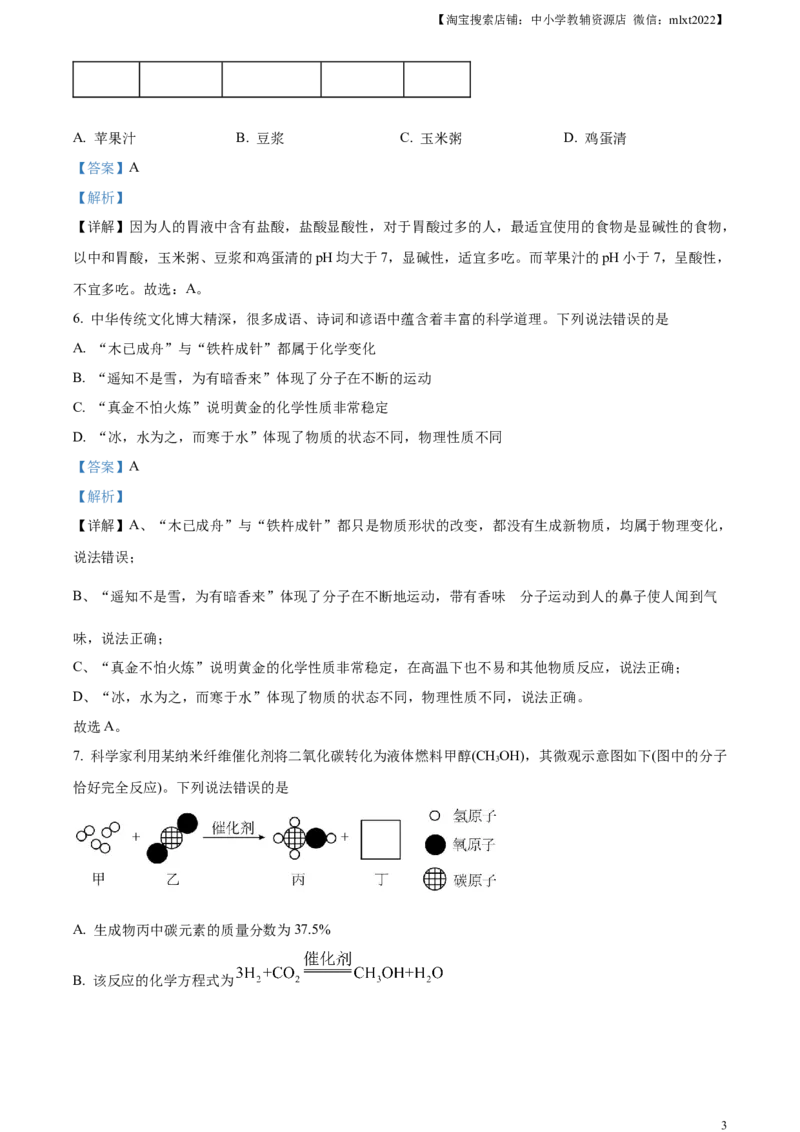
4. 以下化学实验操作正确的是
A. 将大理石保存在细口瓶中 B. 将水缓慢加入浓硫酸中
C. 量取液体 D. 加热液体
【答案】C
【解析】
【详解】A、大理石是固体药品,应该保存在广口瓶中,操作错误;
B、稀释浓硫酸,应该将酸注入水中,防止液体暴沸,操作错误;
C、量取液体时,视线应与液面的凹液面保持水平,操作正确;
D、加热液体时,液体不能超过试管的三分之一,且拇指应放在长柄处,操作错误。
故选C。
5. 下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )
食物 苹果汁 豆浆 玉米粥 鸡蛋清
pH 2.9-3.3 7.4-7.9 6.8-8.0 7.6-8.0
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 苹果汁 B. 豆浆 C. 玉米粥 D. 鸡蛋清
【答案】A
【解析】
【详解】因为人的胃液中含有盐酸,盐酸显酸性,对于胃酸过多的人,最适宜使用的食物是显碱性的食物,
以中和胃酸,玉米粥、豆浆和鸡蛋清的pH均大于7,显碱性,适宜多吃。而苹果汁的pH小于7,呈酸性,
不宜多吃。故选:A。
6. 中华传统文化博大精深,很多成语、诗词和谚语中蕴含着丰富的科学道理。下列说法错误的是
A. “木已成舟”与“铁杵成针”都属于化学变化
B. “遥知不是雪,为有暗香来”体现了分子在不断的运动
C. “真金不怕火炼”说明黄金的化学性质非常稳定
D. “冰,水为之,而寒于水”体现了物质的状态不同,物理性质不同
【答案】A
【解析】
【详解】A、“木已成舟”与“铁杵成针”都只是物质形状的改变,都没有生成新物质,均属于物理变化,
说法错误;
的
B、“遥知不是雪,为有暗香来”体现了分子在不断地运动,带有香味 分子运动到人的鼻子使人闻到气
味,说法正确;
C、“真金不怕火炼”说明黄金的化学性质非常稳定,在高温下也不易和其他物质反应,说法正确;
D、“冰,水为之,而寒于水”体现了物质的状态不同,物理性质不同,说法正确。
故选A。
7. 科学家利用某纳米纤维催化剂将二氧化碳转化为液体燃料甲醇(CHOH),其微观示意图如下(图中的分子
3
恰好完全反应)。下列说法错误的是
A. 生成物丙中碳元素的质量分数为37.5%
B. 该反应的化学方程式为
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C. 生成物丙和丁的质量比为1:1
D. 该反应有助于实现“碳中和”
【答案】C
【解析】
【详解】A、生成物丙是甲醇,甲醇中碳元素的质量分数= ,说法正确;
B、由微观示意图可知,该反应是氢气和二氧化碳在催化剂的催化下生成甲醇和物质丁,根据质量守恒定
律可知,化学反应前有6个氢原子、1个碳原子和2个氧原子,反应后有1个碳原子、4个氢原子和一个氧
原子,所以物质丁是水,化学方程式为: ,说法正确;
C、生成物丙和丁的质量比=(12+16+1×4):(16+1×2)=16:9,说法错误;
D、该反应可以吸收二氧化碳,有助于实现“碳中和”,说法正确。
故选C。
8. 下列有关纯碱的认识错误的是
A. 组成:由碳、氧和钠三种元素组成
B. 性质:能与BaCl 、NaCl等盐溶液反应
2
C. 用途:用于玻璃、造纸、纺织等的生产
D. 生产:侯氏制碱法
【答案】B
【解析】
【详解】A、纯碱是碳酸钠的俗称,所以纯碱由碳、氧和钠三种元素组成,说法正确;
B、碳酸钠可以和氯化钡反应生成碳酸钡沉淀,但是碳酸钠无法和氯化钠生成气体或沉淀或水,所以碳酸
钠无法和氯化钠发生反应,说法错误;
C、碳酸钠可以用于玻璃、造纸、纺织等的生产,说法正确;
D、碳酸钠的生产,可以使用侯氏制碱法,说法正确。
故选B 。
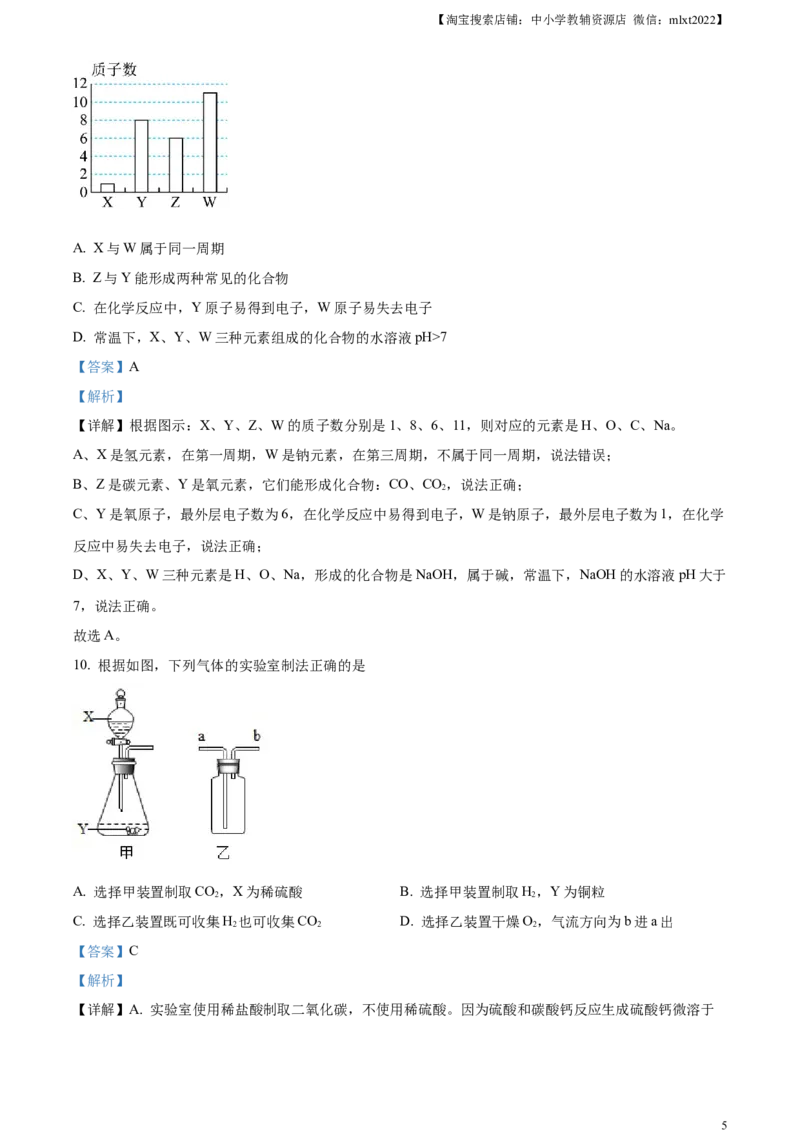
9. X、Y、Z、W四种元素的质子数如图所示。下列说法错误的是
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. X与W属于同一周期
B. Z与Y能形成两种常见的化合物
C. 在化学反应中,Y原子易得到电子,W原子易失去电子
D. 常温下,X、Y、W三种元素组成的化合物的水溶液pH>7
【答案】A
【解析】
【详解】根据图示:X、Y、Z、W的质子数分别是1、8、6、11,则对应的元素是H、O、C、Na。
A、X是氢元素,在第一周期,W是钠元素,在第三周期,不属于同一周期,说法错误;
B、Z是碳元素、Y是氧元素,它们能形成化合物:CO、CO,说法正确;
2
C、Y是氧原子,最外层电子数为6,在化学反应中易得到电子,W是钠原子,最外层电子数为1,在化学
反应中易失去电子,说法正确;
D、X、Y、W三种元素是H、O、Na,形成的化合物是NaOH,属于碱,常温下,NaOH的水溶液pH大于
7,说法正确。
故选A。
10. 根据如图,下列气体的实验室制法正确的是
A. 选择甲装置制取CO,X为稀硫酸 B. 选择甲装置制取H,Y为铜粒
2 2
C. 选择乙装置既可收集H 也可收集CO D. 选择乙装置干燥O,气流方向为b进a出
2 2 2
【答案】C
【解析】
【详解】A. 实验室使用稀盐酸制取二氧化碳,不使用稀硫酸。因为硫酸和碳酸钙反应生成硫酸钙微溶于
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
水,会附着在固体药品表面阻碍反应进行。错误。
B. 铜活动性比氢弱,不能和酸反应放出氢气。所以Y不能为铜。错误。
C. 二氧化碳密度比空气大,从乙a端通入,空气从b排出。氢气密度比空气小,从乙b端通入,空气从a
端排出。选择乙装置既可收集H 也可收集CO,正确。
2 2
D. 乙作洗气装置,需要药品和气体充分接触,则气体通入药品中,所以氧气从a进入。错误。
故选:C。
11. 实验设计是实验探究的基本环节。下列实验设计能达到对应实验目的的是
选
实验目的 实验设计
项
A 鉴别白酒和白糖水 观察颜色
B 除去KCl溶液中的少量KSO 加适量BaCl 溶液,过滤
2 4 2
C 除去氨气中的水蒸气 将气体通过浓硫酸
D 探究铜、银的金属活动性顺序 将铜丝、银丝分别浸入稀盐酸溶液中
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、白酒和白糖水均为无色液体,用观察颜色的方法不能鉴别,故选项实验设计不能达到对应实
验目的;
B、KSO 能与适量BaCl 溶液反应生成硫酸钡沉淀和氯化钾,能除去杂质且没有引入新的杂质,符合除杂
2 4 2
原则,故选项实验设计能达到对应实验目的;
C、浓硫酸具有吸水性,但能与氨气反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故
选项实验设计不能达到对应实验目的;
D、将铜丝、银丝分别浸入稀盐酸溶液中,均不反应,不能探究铜、银的金属活动性顺序,故选项实验设
计不能达到对应实验目的;
故选:B。
12. 下列描述涉及反应的化学方程式正确的是
A. 服用含氢氧化铝的药物治疗胃酸过多:
B. 用过氧化氢溶液制氧气:
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C. 将铁丝浸入稀盐酸中:
D. 用食醋清洗水壶中的水垢:
【答案】D
【解析】
【详解】A、胃酸主要成分是HCl,所以服用含氢氧化铝的药物治疗胃酸过多是氢氧化铝和盐酸反应,化
学方程式为: ,书写错误;
B、过氧化氢在二氧化锰 催化下生成水和氧气,化学方程式为: ,书写错误;
的
C、铁丝和稀盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl +H ↑,书写错误;
2 2
D、水垢的主要成分是碳酸钙,食醋和碳酸钙反应,生成醋酸钙、二氧化碳和水,化学方程式为:
,书写正确。
故选D。
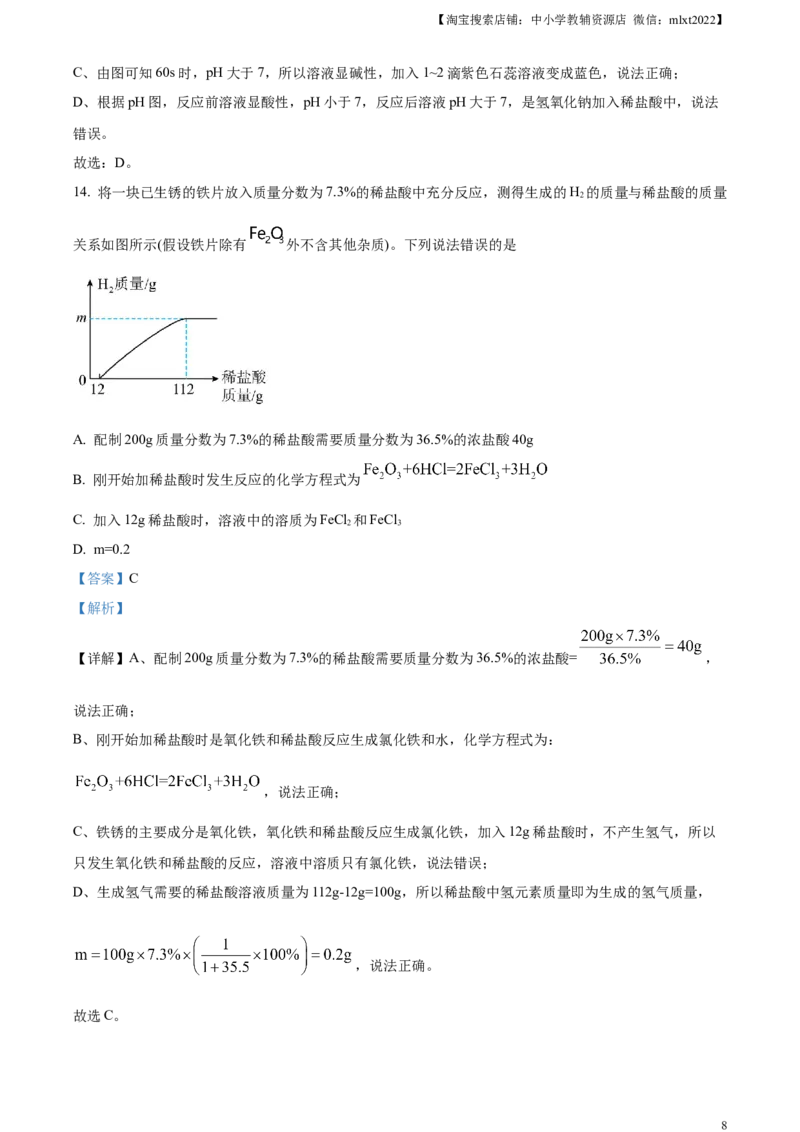
13. 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示。下列
说法错误的是
A. 反应过程中有热量放出
B. 30s时,溶液中溶质为HCl和NaCl
C. 60s时,加入1~2滴紫色石蕊溶液变成蓝色
D. 该实验是将稀盐酸加入稀NaOH溶液
【答案】D
【解析】
【详解】A、氢氧化钠和盐酸反应生成氯化钠和水,由图可知反应过程中温度升高,有热量放出,说法正
确;
B、由图可知30s时溶液pH小于7,溶液显酸性,说明盐酸未完全反应,故溶液中溶质为HCl和NaCl,说
法正确;
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C、由图可知60s时,pH大于7,所以溶液显碱性,加入1~2滴紫色石蕊溶液变成蓝色,说法正确;
D、根据pH图,反应前溶液显酸性,pH小于7,反应后溶液pH大于7,是氢氧化钠加入稀盐酸中,说法
错误。
故选:D。
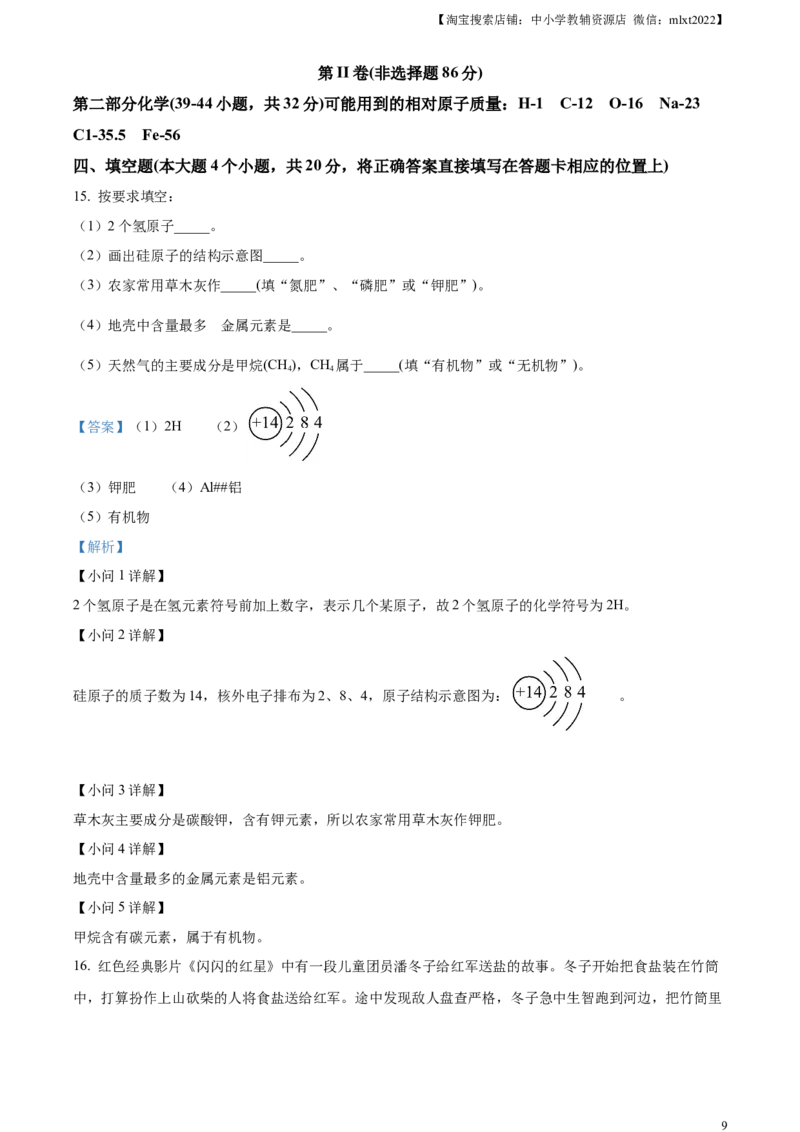
14. 将一块已生锈的铁片放入质量分数为7.3%的稀盐酸中充分反应,测得生成的H 的质量与稀盐酸的质量
2
关系如图所示(假设铁片除有 外不含其他杂质)。下列说法错误的是
A. 配制200g质量分数为7.3%的稀盐酸需要质量分数为36.5%的浓盐酸40g
B. 刚开始加稀盐酸时发生反应的化学方程式为
C. 加入12g稀盐酸时,溶液中的溶质为FeCl 和FeCl
2 3
D. m=0.2
【答案】C
【解析】
【详解】A、配制200g质量分数为7.3%的稀盐酸需要质量分数为36.5%的浓盐酸= ,
说法正确;
B、刚开始加稀盐酸时是氧化铁和稀盐酸反应生成氯化铁和水,化学方程式为:
,说法正确;
C、铁锈的主要成分是氧化铁,氧化铁和稀盐酸反应生成氯化铁,加入12g稀盐酸时,不产生氢气,所以
只发生氧化铁和稀盐酸的反应,溶液中溶质只有氯化铁,说法错误;
D、生成氢气需要的稀盐酸溶液质量为112g-12g=100g,所以稀盐酸中氢元素质量即为生成的氢气质量,
,说法正确。
故选C。
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
第II卷(非选择题86分)
第二部分化学(39-44小题,共32分)可能用到的相对原子质量:H-1 C-12 O-16 Na-23
C1-35.5 Fe-56
四、填空题(本大题4个小题,共20分,将正确答案直接填写在答题卡相应的位置上)
15. 按要求填空:
(1)2个氢原子_____。
(2)画出硅原子的结构示意图_____。
(3)农家常用草木灰作_____(填“氮肥”、“磷肥”或“钾肥”)。
的
(4)地壳中含量最多 金属元素是_____。
(5)天然气的主要成分是甲烷(CH),CH 属于_____(填“有机物”或“无机物”)。
4 4
【答案】(1)2H (2)
(3)钾肥 (4)Al##铝
(5)有机物
【解析】
【小问1详解】
2个氢原子是在氢元素符号前加上数字,表示几个某原子,故2个氢原子的化学符号为2H。
【小问2详解】
硅原子的质子数为14,核外电子排布为2、8、4,原子结构示意图为: 。
【小问3详解】
草木灰主要成分是碳酸钾,含有钾元素,所以农家常用草木灰作钾肥。
【小问4详解】
地壳中含量最多的金属元素是铝元素。
【小问5详解】
甲烷含有碳元素,属于有机物。
16. 红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒
中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:
(1)从物质分类的角度分析,盐水属于_____(填“纯净物”或“混合物”);从物质变化的角度分析,食
盐溶成盐水属于_____(填“物理变化”或“化学变化”)。
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和_____。
(3)氯化钠的溶解度如下表。假设冬子的竹筒中有179g氯化钠,10°C时完全溶解所需水的质量至少为
_____g。
温度/°C 0 10 20 30 40 50 60
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
(4)氯化钠在生活中的用途:_____(任写一点即可)。
【答案】(1) ①. 混合物 ②. 物理变化
(2)漏斗 (3)500
(4)调味品(合理即可)
【解析】
【小问1详解】
从物质分类的角度分析,盐水中含有氯化钠、水,是由不同种物质组成,属于混合物;从物质变化的角度
分析,食盐溶成盐水,只是微粒运动的结果,没有新物质生成,属于物理变化;
【小问2详解】
过滤是把不溶于液体的固体与液体分离的一种方法,过滤操作的装置由铁架台、烧杯、玻璃棒、漏斗四种
仪器组成;蒸发操作的装置由铁架台、玻璃棒、酒精灯、蒸发皿四种仪器组成;其中用到的玻璃仪器有烧
杯、玻璃棒、酒精灯和漏斗;
【小问3详解】
10℃时氯化钠的溶解度为35.8g,冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为
;
【小问4详解】
氯化钠在生活中可用作调味品,用于腌制咸菜,用于制造生理盐水,农业生产中用于选种,用于融雪等。
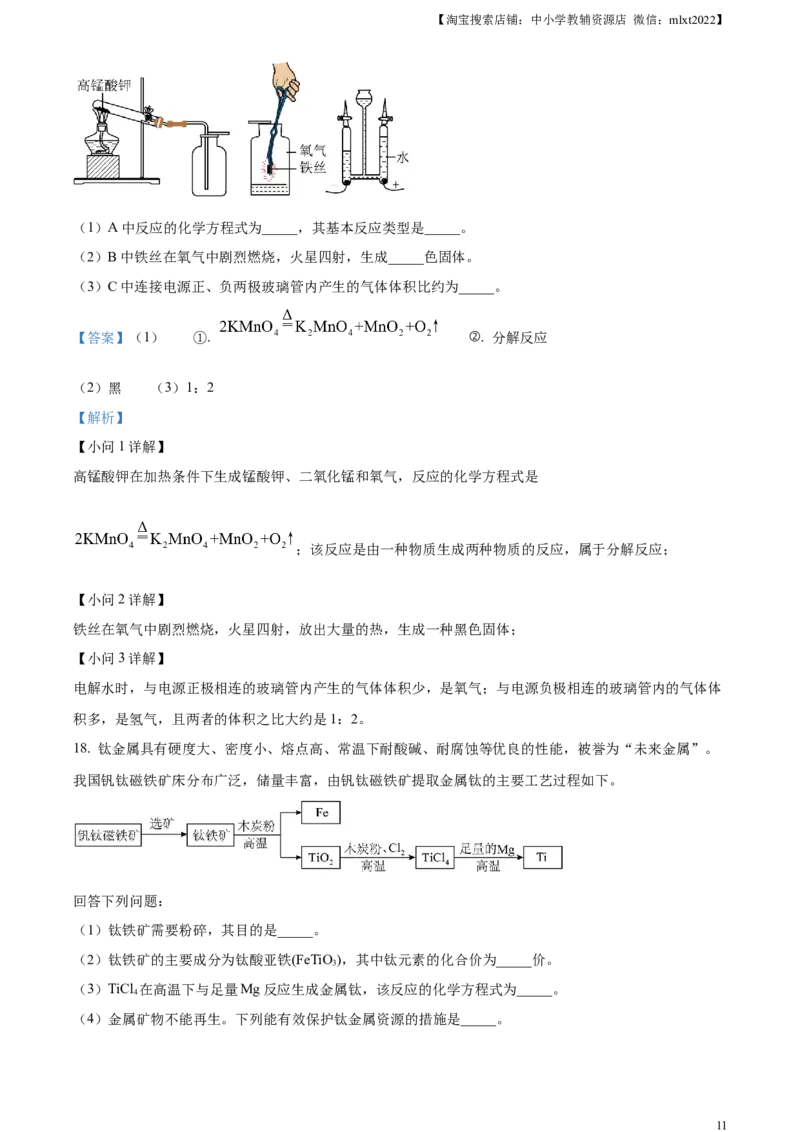
17. 根据下图所示实验回答问题。
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(1)A中反应的化学方程式为_____,其基本反应类型是_____。
(2)B中铁丝在氧气中剧烈燃烧,火星四射,生成_____色固体。
(3)C中连接电源正、负两极玻璃管内产生的气体体积比约为_____。
【答案】(1) ①. ②. 分解反应
(2)黑 (3)1:2
【解析】
【小问1详解】
高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是
;该反应是由一种物质生成两种物质的反应,属于分解反应;
【小问2详解】
铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;
【小问3详解】
电解水时,与电源正极相连的玻璃管内产生的气体体积少,是氧气;与电源负极相连的玻璃管内的气体体
积多,是氢气,且两者的体积之比大约是1:2。
18. 钛金属具有硬度大、密度小、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。
我国钒钛磁铁矿床分布广泛,储量丰富,由钒钛磁铁矿提取金属钛的主要工艺过程如下。
回答下列问题:
(1)钛铁矿需要粉碎,其目的是_____。
(2)钛铁矿的主要成分为钛酸亚铁(FeTiO),其中钛元素的化合价为_____价。
3
(3)TiCl 在高温下与足量Mg反应生成金属钛,该反应的化学方程式为_____。
4
(4)金属矿物不能再生。下列能有效保护钛金属资源的措施是_____。
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 回收利用废旧钛金属制品 B. 任意开采钛金属矿石
C. 钛金属抗腐蚀性能好,可随意堆放储存 D. 寻找、开发钛金属的代替品
【答案】(1)增大接触面积,加快反应速率
(2)+4 (3) (4)AD
【解析】
【小问1详解】
钛铁矿需粉碎,其目的是增大反应物接触面积,使反应更快、更充分。
【小问2详解】
设其中钛元素的化合价为x,根据化合价代数和为0,x+2+(-2)×3=0,x=+4。
【小问3详解】
TiCl4在高温下与足量Mg反应生成金属钛,化学方程式为: 。
【小问4详解】
A、回收利用废旧金属制品能有效保护钛金属资源,正确;
B、任意开采钛金属矿石,不利于保护钛金属资源,会造成钛金属资源浪费,错误;
C、钛金属虽然抗腐蚀性能好,但也不能随意堆放储存,错误;
D、寻找、开发金属的代用品,能有效保护钛金属资源,正确。
故选AD。
五、实验探究题(本大题1个小题,共7分,将正确答案直接填写在答题卡相应的位置上)
19. 某化学兴趣小组发现上次做实验用的澄清石灰水忘记了盖瓶盖,试剂瓶内壁附着一层白色固体、底部
也有白色固体。
【提出问题】白色固体是什么?怎样产生的?
【猜想与假设】
猜想一:碳酸钙;空气中的二氧化碳与澄清石灰水反应生成碳酸钙。猜想二:氢氧化钙;水分蒸发,析出
氢氧化钙固体。猜想三:氢氧化钙和碳酸钙的混合物。
【实验探究】
(1)甲同学取少量白色固体于试管中,加入过量稀盐酸,振荡,固体全部溶解并有气泡产生。产生气泡
的化学方程式为_____。
甲同学得出结论:猜想一正确。
(2)乙同学提出质疑,认为甲同学实验结论不够严谨,其理由是_____(用化学方程式表示),并补充实验
如下:
12【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
实验步骤 实验现象 实验结论
_____ _____ 白色固体既含有碳酸钙又含有氢氧化钙
【实验结论】
综上所述,猜想三正确。
【实验反思】
(3)澄清石灰水必须要_____保存。
【答案】(1)
(2) ①. ②. 取少量白色固体于试管中,加入适量的水充分振
荡后加入1~2滴无色酚酞溶液(或取少量白色固体于试管中,加入适量的水充分振荡后加入 1~2滴紫色石
蕊溶液) ③. 浊液变红(或浊液变蓝)
(3)密封
【解析】
【小问1详解】
甲同学取少量白色固体于试管中,加入过量稀盐酸,振荡,固体全部溶解并有气泡产生,说明白色固体为
碳酸钠,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为
,故填: ;
【小问2详解】
①白色固体也可能是氢氧化钙和碳酸钙的混合物,氢氧化钙与稀盐酸反应生成氯化钙和水,化学方程式为
,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学反应方程式为
,取少量白色固体于试管中,加入过量稀盐酸,振荡,固体也会全
部溶解并有气泡产生,故填: ;
②可增加实验检验是否存在氢氧化钙,氢氧化钙显碱性,可用无色酚酞溶液检验,无色酚酞溶液遇碱变蓝,
也可用紫色石蕊溶液鉴别,紫色石蕊溶液遇碱变红,故填:取少量白色固体于试管中,加入适量的水充分
振荡后加入1~2滴无色酚酞溶液(或取少量白色固体于试管中,加入适量的水充分振荡后加入1~2滴紫色
石蕊溶液);
13【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
③实验结论为白色固体既含有碳酸钙又含有氢氧化钙,碳酸钙不溶于水,加入适量的水充分振荡后加入
1~2滴无色酚酞溶液,浊液变红(或取少量白色固体于试管中,加入适量的水充分振荡后加入1~2滴紫色
石蕊溶液,浊液变蓝),故填:浊液变红(或浊液变蓝);
【小问3详解】
空气中的二氧化碳会与澄清石灰水反应生成碳酸钙,因此澄清石灰水必须要密封保存,故填:密封。
六、计算题(本大题1个小题,共5分,将正确答案填写在答题卡相应的位置上)
20. 磁铁矿石(主要成分为 )是常用的炼铁原料,工业上可通过如下反应:
将其中的Fe O 转化为Fe.
3 4
(1)Fe O 中铁、氧的微观粒子数目之比为_____。
3 4
(2)假设炼铁过程中铁没有损耗,用含348吨Fe O 的磁铁矿石理论上可以炼出含铁96%的生铁的质量是
3 4
多少(写出计算过程)?
【答案】(1)3:4 (2)解:含348吨Fe O 的磁铁矿石理论上可以炼出铁的质量为
3 4
=252t
折合为含铁96%的生铁的质量为:
答:含348吨Fe O 的磁铁矿石理论上可以炼出含铁96%的生铁的质量是262.5吨。
3 4
【解析】
【小问1详解】
由四氧化三铁的分子式可知,Fe O 中铁、氧的微观粒子数目之比为3:4。
3 4
【小问2详解】
见答案 。
14