文档内容
化学考后巩固卷
高二 2025 年 10 月版
姓名: 班级:
强化记忆
举一反三 步步为赢 点石成金
点石联考出题中心点石联考
巩固卷采集了所有学生的考试数据,运用人工智能技术诊断出
每道题的知识点,通过“算法推荐+专家干预”精准推送习题,
提供与试卷同结构的巩固卷供您追踪效果,巩固卷每道原题衍
生1道基础题、3到巩固题、1道提升题,助力您精准高效提升!
1.及时分析,明确薄弱点
错题复盘:逐题分析错误原因(审题不清、知识点遗忘、计算失误等),用不同颜色标注错题类型。
统计归类:按知识点或题型分类整理错题(如函数、几何、语法、实验设计),统计高频失分模块,
明确需优先突破的薄弱环节。
2. 针对性突破 , 夯实基础
知识补漏:针对错题涉及的课本概念、公式、定理,重新梳理核心内容,结合例题理解应用场景。
专项训练:根据错题类型,精选同类题目进行限时练习(如每天10道同类题),强化解题思维和熟练
度。
3. 构建思维框架 , 提炼方法
思路对比:对比参考答案与自己的解题步骤,标注关键思路差异(如是否遗漏隐含条件、逻辑跳步)。
总结模板:针对高频题型(如阅读理解主旨题、数学压轴题),归纳通用解题步骤或答题模板。
4. 模拟应用 , 检验效果
变式训练:将原题条件或设问方式稍作改动,自主改编1-2道同类题,测试是否真正掌握核心逻辑。
限时重测:1-2周后重做巩固卷,对比正确率变化,重点关注反复出错的题目。
5. 长期规划 , 动态调整
建立档案:将错题整理成电子文档或活页本,标注错误日期和重做结果,形成个人学习轨迹。
定期回顾:每周抽取10分钟复习错题本,考前集中筛查易错点,避免重复错误。点石联考
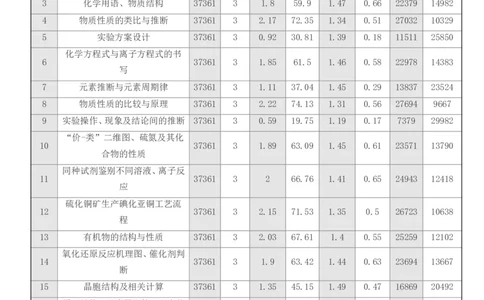
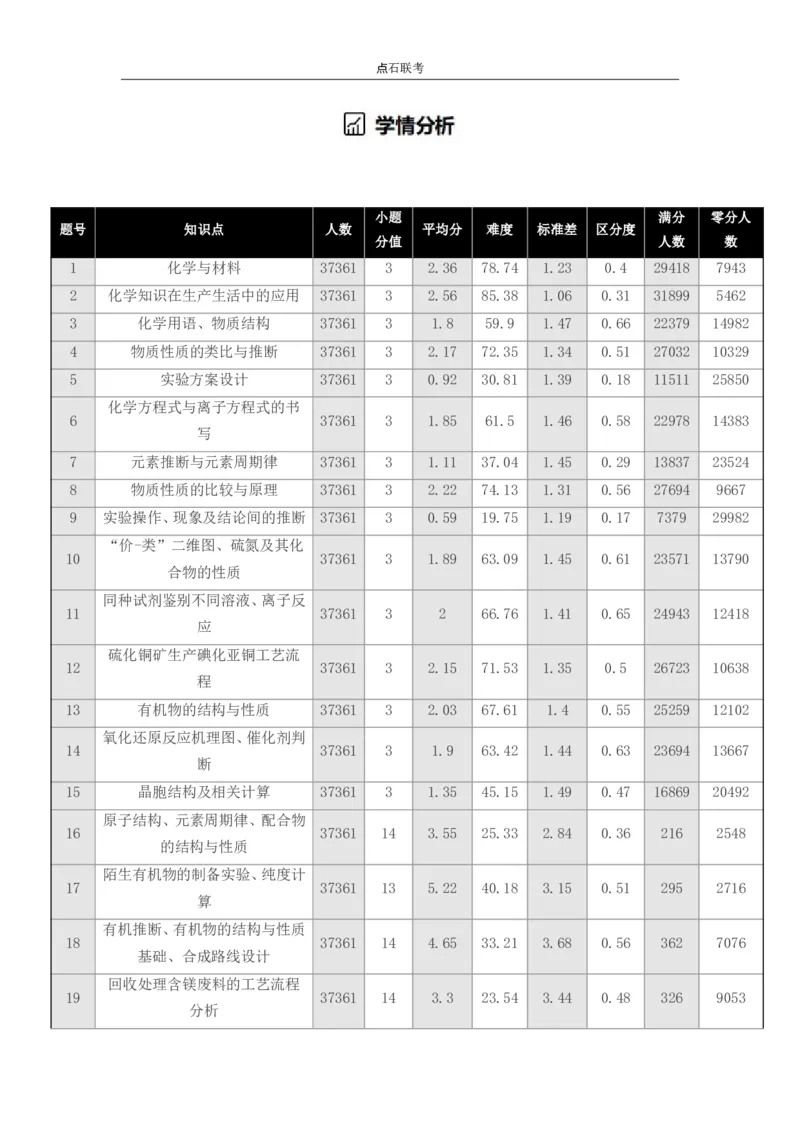
小题 满分 零分人
题号 知识点 人数 平均分 难度 标准差 区分度
分值 人数 数
1 化学与材料 37361 3 2.36 78.74 1.23 0.4 29418 7943
2 化学知识在生产生活中的应用 37361 3 2.56 85.38 1.06 0.31 31899 5462
3 化学用语、物质结构 37361 3 1.8 59.9 1.47 0.66 22379 14982
4 物质性质的类比与推断 37361 3 2.17 72.35 1.34 0.51 27032 10329
5 实验方案设计 37361 3 0.92 30.81 1.39 0.18 11511 25850
化学方程式与离子方程式的书
6 37361 3 1.85 61.5 1.46 0.58 22978 14383
写
7 元素推断与元素周期律 37361 3 1.11 37.04 1.45 0.29 13837 23524
8 物质性质的比较与原理 37361 3 2.22 74.13 1.31 0.56 27694 9667
9 实验操作、现象及结论间的推断 37361 3 0.59 19.75 1.19 0.17 7379 29982
“价-类”二维图、硫氮及其化
10 37361 3 1.89 63.09 1.45 0.61 23571 13790
合物的性质
同种试剂鉴别不同溶液、离子反
11 37361 3 2 66.76 1.41 0.65 24943 12418
应
硫化铜矿生产碘化亚铜工艺流
12 37361 3 2.15 71.53 1.35 0.5 26723 10638
程
13 有机物的结构与性质 37361 3 2.03 67.61 1.4 0.55 25259 12102
氧化还原反应机理图、催化剂判
14 37361 3 1.9 63.42 1.44 0.63 23694 13667
断
15 晶胞结构及相关计算 37361 3 1.35 45.15 1.49 0.47 16869 20492
原子结构、元素周期律、配合物
16 37361 14 3.55 25.33 2.84 0.36 216 2548
的结构与性质
陌生有机物的制备实验、纯度计
17 37361 13 5.22 40.18 3.15 0.51 295 2716
算
有机推断、有机物的结构与性质
18 37361 14 4.65 33.21 3.68 0.56 362 7076
基础、合成路线设计
回收处理含镁废料的工艺流程
19 37361 14 3.3 23.54 3.44 0.48 326 9053
分析点石联考点石联考 2025 年 10 月高二化学巩固卷
【原卷 1 题】 知识点 影响化学反应速率的因素
1-1(基础)[20423203] 化学在生活中的应用随处可见,下列措施不是为了改变化学反应速率的是
A.冰箱保存食物 B.在糕点包装内放置小包除氧剂
C.做馒头时添加膨松剂 D.给学校消防栓刷漆
1-2(巩固)[24493343] 日常生活中的下列做法,其目的是加快反应速率的是
A.用冰箱冷藏食物 B.包装食品时抽真空
C.用温水和面发酵 D.在铁器表面刷油漆
1-3(提升)[24495584] 在生产、生活中,下列措施不是用来调控化学反应速率的是
A.洗衣粉中添加酶 B.口香糖中添加木糖醇
C.将鲜肉存放冰箱中 D.制硫酸时将黄铁矿石粉碎
【原卷 2 题】 知识点 吸热反应和放热反应,反应热 ,化学反应中能量变化的原因
2-1(基础)[27539281] 下列关于化学反应与能量的说法中,不正确的是
A.Al与盐酸的反应属于放热反应
B.化学反应总是伴随着能量的变化
C.当反应物的总能量高于生成物的总能量时,反应向环境放出能量
D.CO 与C的反应属于放热反应
2
2-2(巩固)[27285292] 在化学反应中常伴随能量的释放或吸收。下列说法错误的是
A.化学反应中的能量变化都是以热能形式表现出来的
B.等压条件下进行的化学反应的反应热等于反应的焓变
C.化学反应中的能量变化主要是由化学键变化引起的
D.放热反应的△H<0,吸热反应的△H>0
1/582-3(提升)[28845895] 下列说法不正确的是
A.浓H SO 稀释是放热过程
2 4
B.石墨转变为金刚石是吸热反应,则金刚石比石墨更稳定
C.热化学方程式中的ΔH 与反应是否可逆无关
D.吸热反应中,反应物化学键断裂吸收的总能量高于产物形成化学键放出的总能量
【原卷 3 题】 知识点 一元强酸与一元弱酸的比较,弱电解质的电离平衡,弱电解质在水溶液中的电离平衡
3-1(基础)[28939792] 常温下,下列事实能证明浓度为0.1mol/L的HA是弱酸的是
A.用电导仪测得其导电能力比的1mol/L盐酸弱
B.将该酸加水稀释10倍后,测得溶液的pH=5
C.加入等体积0.1mol/L NaOH溶液恰好完全中和
D.向该溶液中滴加甲基橙,溶液显红色
3-2(巩固)[28931530] 下列实验事实不能证明醋酸是弱电解质的是
A.常温下,测得0.1 mol×L-1醋酸溶液的pH=4
B.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH <4
C.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H 的起始速率相等
2
D.在相同条件下,0.1 mol/L的醋酸溶液的导电性比0.1 mol/L的盐酸的导电性弱
3-3(提升)[28786016] 下列事实一定能证明HNO 是弱电解质的是
2
①用HNO 溶液做导电实验,灯泡很暗;
2
②HNO 和NaCl不能发生反应;
2
③0.1mol/LHNO 溶液的pH=2.1;
2
④NaNO 和H PO 反应,生成HNO ;
2 3 4 2
⑤pH=1的HNO 溶液稀释至100倍,pH约为2.3
2
A.①②③ B.③④⑤ C.②③⑤ D.①②③④⑤
【原卷 4 题】 知识点 反应焓变与热化学方程式的关系,阿伏加德罗常数的应用
2/584-1(基础)[25895561] 设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.等浓度的醋酸和氢氧化钠混合,溶液显碱性
B.1L0.1mol×L-1K CO 溶液中,阴离子总数小于0.1N
2 3 A
C.1L0.1mol×L-1AlCl 的溶液中氯离子的总数为0.3N
3 A
D.稀氨水和稀盐酸完全反应生成N 个H O时放出热量57.3kJ
A 2
4-2(巩固)[24153903] 用N 表示阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol羟基(-OH)含有的电子数目为9N
A
B.0.1mol/L的氨水溶液中,含有NH 、NH+、NH ×H O的数目为0.1N
3 4 3 2 A
C.0.1molN 与足量H 充分反应,转移电子数 0.6N
2 2 A
D.已知:N
2
g+3H
2
g
ƒ
2NH
3
gΔH=-92.4kJ×mol-1,则相同条件下,在密闭容器中,1mol N
2
和
3mol H 混合充分反应后,放出92.4kJ的热量
2
4-3(提升)[27729797] 常温下,在密闭容器中发生反应2NO
2
g
ƒ
N
2
O
4
g △H=-56.9kJ/mol。设N
A
为阿
伏加德罗常数的值,下列说法正确的是
A.恒温恒压充入NO 气体,NO 气体的转化率增大
2 2
B.压缩容器体积,单位体积内活化分子数目增加
C.46g由NO 和N O 组成的混合气体中,氮原子总数小于N
2 2 4 A
D.其他条件不变,往密闭容器内通入92gNO 气体,充分反应后,放出56.9KJ热量
2
【原卷 5 题】 知识点 物质水溶液的导电性,弱电解质的电离平衡,化学反应中能量变化的原因
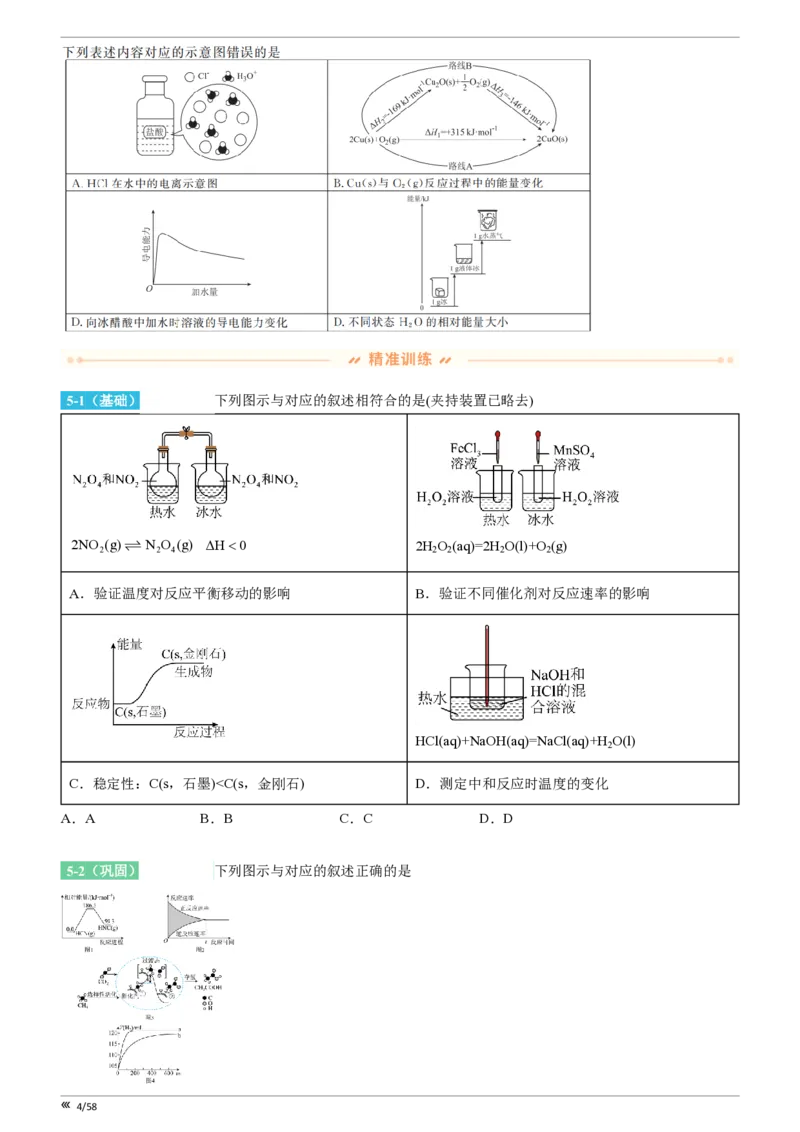
3/585-1(基础)[25197582] 下列图示与对应的叙述相符合的是(夹持装置已略去)
2NO 2 (g) ƒ N 2 O 4 (g) DH<0 2H 2 O 2 (aq)=2H 2 O(l)+O 2 (g)
A.验证温度对反应平衡移动的影响 B.验证不同催化剂对反应速率的影响
HCl(aq)+NaOH(aq)=NaCl(aq)+H O(l)
2
C.稳定性:C(s,石墨)c
HCO-
2 3 2 3
5/58D.向Na S溶液中通入少量CO ,发生反应CO +S2- +H O=CO2- +H S
2 2 2 2 3 2
6-2(巩固)[26147547] 已知K CaCO =2.8´10-9及表中有关信息:
sp 3
弱酸 CH COOH H CO
3 2 3
电离平衡常数(常温) K =1.8´10-5 K =4.3´10-7;K =5.6´10-11
a a1 a2
下列判断正确的是
A.向Na CO 溶液中滴入酚酞,溶液变红,主要原因是CO2-+2H O H CO +2OH-
2 3 3 2 ƒ 2 3
cCH COOH
B.常温时,CH
3
COOH与CH
3
COONa混合溶液的pH=6,则
c CH
3
COO-
=18
3
C.NaHCO 溶液中:c OH- -c H+ =cH CO -c CO2-
3 2 3 3
D.2´10-4mol×L-1的Na CO 溶液与CaCl 溶液等体积混合出现沉淀,则CaCl 溶液的浓度一定是
2 3 2 2
5.6´10-5mol×L-1
6-3(提升)[28815864] 25℃时,有关物质的电离平衡常数如表所示。结合表中数据,完成下列小题。
化学式 电离常数(25℃)
H CO K =4.5´10-7;K =4.7´10-11
2 3 a1 a2
HF K =6.3´10-4
a
H S K =1.1´10-7;K =1.3´10-13
2 a1 a2
H SO K =1.4´10-2;K =6.0´10-8
2 3 a1 a2
CH COOH K =1.8´10-5
3 a
下列说法正确的是
A.若①CH COOH、②HCl、③H SO 、④NaHSO 四种溶液的物质的量浓度相同,其c
H+
的大小顺序为:
3 2 3 3
②>③>④>①
B.中和等物质的量的H S、H CO 、H SO ,消耗NaOH的量相同
2 2 3 2 3
C.等浓度、体积的NaHCO 与NaHSO 混合:HSO-+HCO-=CO +H O+SO2-
3 3 3 3 2 2 3
D.少量SO 通入Na CO 溶液中:SO +H O+CO2-=HSO-+HCO-
2 2 3 2 2 3 3 3
6/58【原卷 7 题】 知识点 吸热反应和放热反应,盖斯定律与热化学方程式
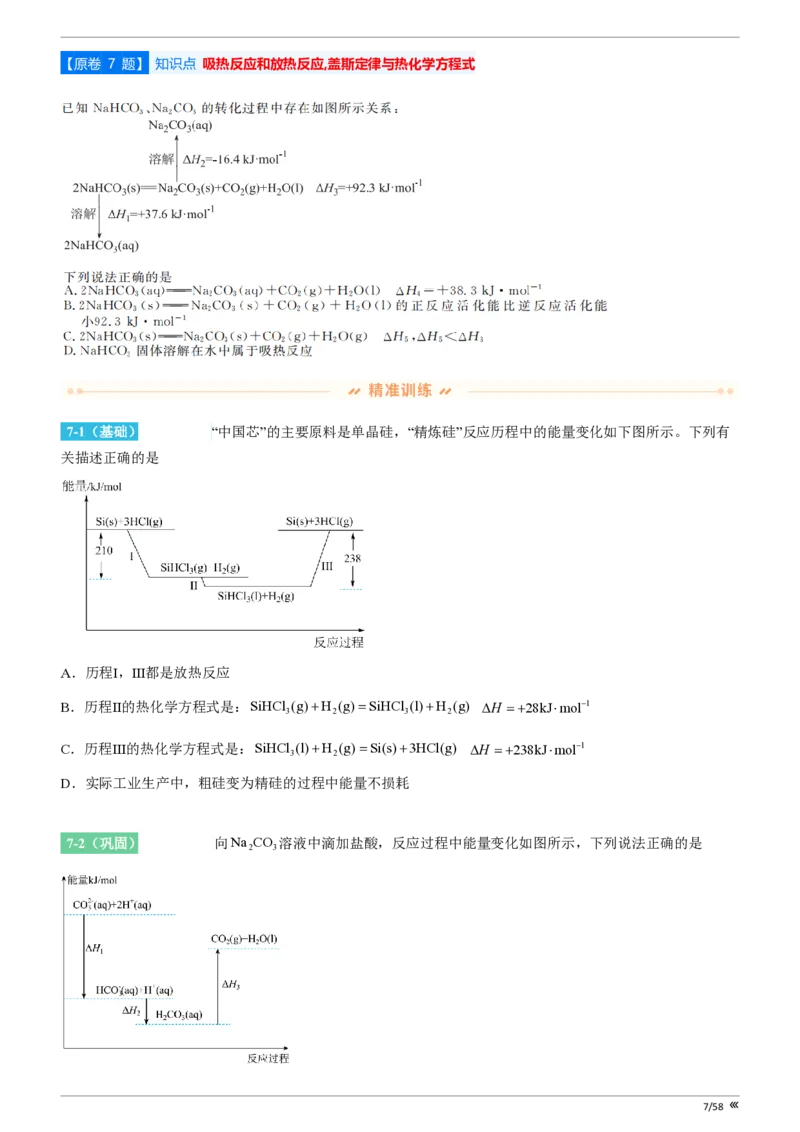
7-1(基础)[25800204] “中国芯”的主要原料是单晶硅,“精炼硅”反应历程中的能量变化如下图所示。下列有
关描述正确的是
A.历程Ⅰ,Ⅲ都是放热反应
B.历程Ⅱ的热化学方程式是:SiHCl (g)+H (g)=SiHCl (l)+H (g) DH =+28kJ×mol-1
3 2 3 2
C.历程Ⅲ的热化学方程式是:SiHCl (l)+H (g)=Si(s)+3HCl(g) DH =+238kJ×mol-1
3 2
D.实际工业生产中,粗硅变为精硅的过程中能量不损耗
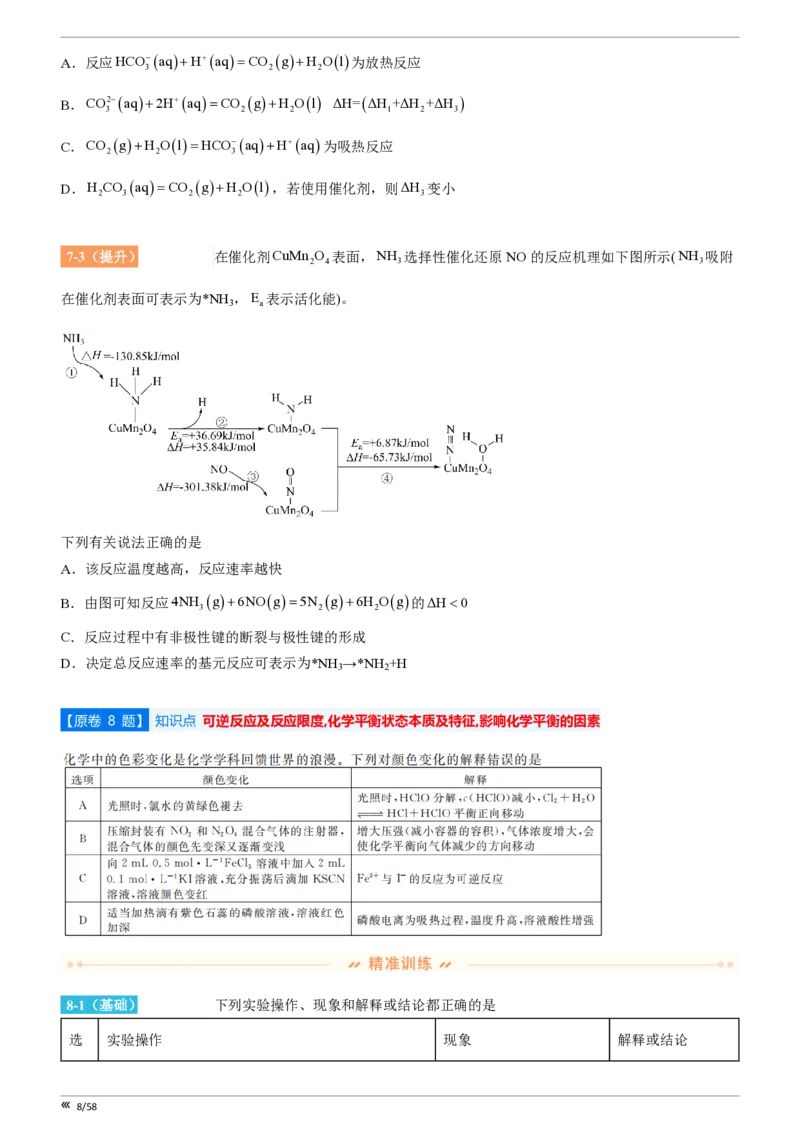
7-2(巩固)[19192192] 向Na CO 溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法正确的是
2 3
7/58A.反应HCO-aq+H+aq=CO g+H Ol为放热反应
3 2 2
B.CO2-aq+2H+aq=CO g+H Ol ΔH=ΔH +ΔH +ΔH
3 2 2 1 2 3
C.CO g+H Ol=HCO-aq+H+aq为吸热反应
2 2 3
D.H CO aq=CO g+H Ol,若使用催化剂,则ΔH 变小
2 3 2 2 3
7-3(提升)[28758360] 在催化剂CuMn O 表面,NH 选择性催化还原NO的反应机理如下图所示(NH 吸附
2 4 3 3
在催化剂表面可表示为*NH ,E 表示活化能)。
3 a
下列有关说法正确的是
A.该反应温度越高,反应速率越快
B.由图可知反应4NH g+6NOg=5N g+6H Og的ΔH<0
3 2 2
C.反应过程中有非极性键的断裂与极性键的形成
D.决定总反应速率的基元反应可表示为*NH →*NH +H
3 2
【原卷 8 题】 知识点 可逆反应及反应限度,化学平衡状态本质及特征,影响化学平衡的因素
8-1(基础)[28669800] 下列实验操作、现象和解释或结论都正确的是
选 实验操作 现象 解释或结论
8/58项
密闭容器中氢气和碘蒸气等物质的量反应,压缩容
A 颜色加深 平衡右移
器容积
向两支盛有等浓度、等体积H O 的试管中分别加入
2 2 Fe3+的催化效果比
B 前者产生气泡的速率快
等浓度、等体积的FeCl 溶液和CuSO 溶液
Cu2+好
3 4
等体积、等物质的量浓度的Na S O 与H SO 溶液 温度高的溶液中先出现浑 温度升高,该反应
2 2 3 2 4
C
浊 速率加快
在不同温度下反应
向两份5mL0.1mol×L-1草酸溶液中,分别滴加0.1 加入0.2mol×L-1的酸性高 反应物浓度越大,
D
mol×L-1和0.2mol×L-1的酸性高锰酸钾溶液2mL 锰酸钾溶液褪色快 反应速率越快
A.A B.B C.C D.D
8-2(巩固)[25588282] 下列有关实验操作、现象和解释或结论都正确的组合是
选
实验操作 现象 解释或结论
项
浓度大的NaHSO 溶 其他条件不变时,反
向2支盛有5mL、不同浓度NaHSO 溶液的试管中同 3
3
① 应物浓度越大,反应
液中气泡产生的速率
时加入2mL5%H O 溶液,观察现象
2 2 速率越快
快
其他条件不变时,增
② 向FeCl 和KSCN的混合溶液中,加入KCl固体 溶液颜色不变 大Cl-的浓度,平衡
3
不移动
根据反应前后的温度
将50mL0.55mol/L氢氧化钠溶液,分批次加入盛有
③ 差和比热容等数值可
50mL0.50mol/L盐酸的量热器内筒中
计算反应热
两支试管分别盛有4mL 0.01mol/L酸性高锰酸钾溶 其他条件相同,反应
草酸溶液浓度大的试
④ 液,同时各加入5mL 0.1mol/L的草酸溶液和5mL 物浓度越大,反应速
管紫色消失更快
0.2mol/L的草酸溶液 率越快
A.②④ B.①③ C.①② D.③④
8-3(提升)[26789621] 下列表格中依据实验操作和实验现象所得结论或解释错误的是选项
9/58选
实验操作 实验现象 结论或解释
项
压缩后,混合气体
将装有NO 和N O 混合气体的
2 2 4
A 的颜色先变深后逐 平衡2NO 2 g ƒ N 2 O 4 g向左移动
注射器由20mL压缩至10 mL
渐变浅
向含有FeSCN 的红色溶液中
B 3 溶液的红色变浅 平衡Fe3+ +3SCN- ƒ FeSCN 向左移动
3
加入少量铁粉,振荡、静置
éCuH O ù 2+ +4Cl- CuCl 2-+4H O的
ë 2 4 û ƒ 4 2
C 加热2mL 0.5mol/L CuCl 溶液 溶液变为黄绿色
2
ΔH>0
向2mL 0.1mol/L K CrO 溶液
2 2 7
D 溶液变为黄色 平衡CrO2-+H O 2CrO2-+2H+向右移动
中滴加5~10滴6mol/L NaOH 2 7 2 ƒ 4
溶液
A.A B.B C.C D.D
【原卷 9 题】 知识点 化学能与物质稳定性之间的关系,吸热反应和放热反应,活化能对反应速率的影响
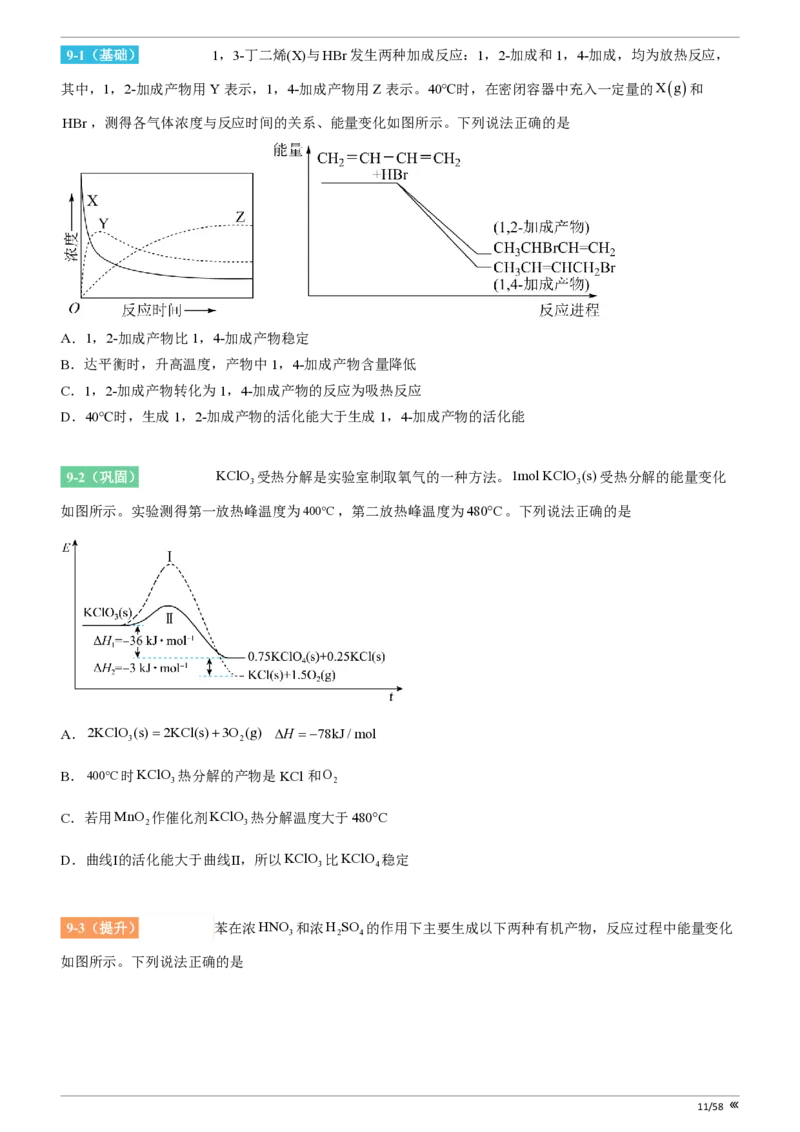
10/589-1(基础)[25219924] 1,3-丁二烯(X)与HBr发生两种加成反应:1,2-加成和1,4-加成,均为放热反应,
其中,1,2-加成产物用Y表示,1,4-加成产物用Z表示。40℃时,在密闭容器中充入一定量的Xg和
HBr,测得各气体浓度与反应时间的关系、能量变化如图所示。下列说法正确的是
A.1,2-加成产物比1,4-加成产物稳定
B.达平衡时,升高温度,产物中1,4-加成产物含量降低
C.1,2-加成产物转化为1,4-加成产物的反应为吸热反应
D.40℃时,生成1,2-加成产物的活化能大于生成1,4-加成产物的活化能
9-2(巩固)[25800206] KClO 受热分解是实验室制取氧气的一种方法。1mol KClO (s)受热分解的能量变化
3 3
如图所示。实验测得第一放热峰温度为400°C,第二放热峰温度为480°C。下列说法正确的是
A.2KClO (s)=2KCl(s)+3O (g) DH =-78kJ/mol
3 2
B.400°C时KClO 热分解的产物是KCl和O
3 2
C.若用MnO 作催化剂KClO 热分解温度大于480°C
2 3
D.曲线Ⅰ的活化能大于曲线Ⅱ,所以KClO 比KClO 稳定
3 4
9-3(提升)[28575142] 苯在浓HNO 和浓H SO 的作用下主要生成以下两种有机产物,反应过程中能量变化
3 2 4
如图所示。下列说法正确的是
11/58A.上述两种进程中,浓H SO 均只作催化剂B.X为苯的取代产物,Y为苯的加成产物
2 4
C.由苯得到M时,苯中的化学键发生了变化 D.产物X的能量更高,更有利于生成产物X
【原卷 10 题】 知识点 化学反应速率计算,催化剂对化学反应速率的影响,化学平衡状态的判断方法
10-1(基础)[27674118] 目前,丙烷脱氢生产丙烯是一项富有前景的技术。丙烷(CH CH CH )脱氢反应原
3 2 3
理为C
3
H
8
g
ƒ
C
3
H
6
g+H
2
g(正反应为吸热反应)。一定条件下,在2L密闭容器中加入5molC
3
H
8
发生
上述反应。反应30min时,测得nC H =0.6mol,下列说法错误的是
3 6
A.上述反应中,反应物断键吸收的总能量大于生成物成键放出的总能量
B.0~30min内平均反应速率vC H =0.01mol·L-1·min-1
3 8
C.向容器内通入氦气能加快该反应的反应速率
D.当v C H =v C H 达到化学平衡状态
正 3 8 逆 3 6
10-2(巩固)[27745285] 向体积为2L的恒温恒容密闭容器中充入1molX(g)和3molY(g),发生反应
X(g)+3Y(g)
ƒ
2M(g)+Q(g),经检测可知从第3min开始,密闭容器中M的物质的量浓度不再发生变化,
且0~3min内,M的平均反应速率为0.1mol×L-1×min-1。下列说法正确的是
A.3v(Y)=2v(Q)
B.保持恒温恒容状态向容器中再充入1molHe(不参与反应),可以使该反应的化学反应速率增大
C.当密闭容器中混合气体的密度不变时,可认为该反应一定达到化学平衡状态
D.该反应达到平衡状态时,X的转化率为30%
12/5810-3(提升)[28316573] 在2L恒温密闭容器中通入气体X并发生反应:2Xg
ƒ
YgΔH<0,X的物质的
量n(X)随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述正确的是
A.反应进行到a点时放出的热量多于反应进行到b点时放出的热量
B.实线表示有催化剂的情形
C.b、c两点表明反应在相应的条件下达到了平衡状态
D.反应从开始到a点的平均反应速率可表示为vY=0.01mol×L-1×min-1
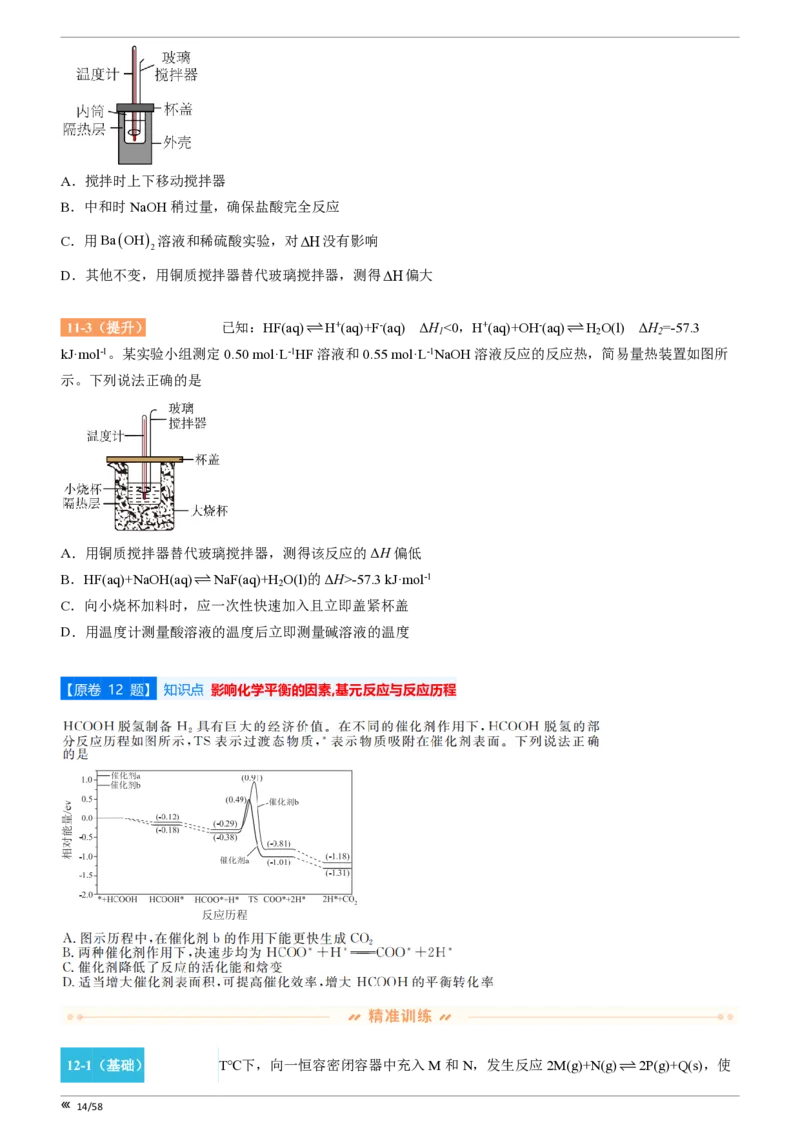
【原卷 11 题】 知识点 中和热的测定与误差分析
11-1(基础)[28971258] 某同学按教材实验要求,用50 mL 0.50mol×L-1的盐酸与50 mL 0.55mol×L-1的
NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热,下列说法错误
的是
A.若将盐酸体积改为60 mL,反应放出的热量更多
B.若将盐酸体积改为60 mL,理论上所求中和热的数值增大
C.实验时不可用温度计代替玻璃搅拌器搅拌溶液
D.烧杯间填满碎泡沫塑料的主要作用是保温,防止热量散失
11-2(巩固)[28941058] 某小组利用如图简易量热计测定0.5 mol×L-1盐酸和0.55 mol×L-1 NaOH溶液反应
的反应热。下列叙述错误的是
13/58A.搅拌时上下移动搅拌器
B.中和时NaOH稍过量,确保盐酸完全反应
C.用BaOH 溶液和稀硫酸实验,对DH没有影响
2
D.其他不变,用铜质搅拌器替代玻璃搅拌器,测得DH偏大
11-3(提升)[28933807] 已知:HF(aq)ƒH+(aq)+F-(aq) ΔH
1
<0,H+(aq)+OH-(aq)ƒH
2
O(l) ΔH
2
=-57.3
kJ·mol-1。某实验小组测定0.50 mol·L-1HF溶液和0.55 mol·L-1NaOH溶液反应的反应热,简易量热装置如图所
示。下列说法正确的是
A.用铜质搅拌器替代玻璃搅拌器,测得该反应的ΔH偏低
B.HF(aq)+NaOH(aq)ƒNaF(aq)+H
2
O(l)的ΔH>-57.3 kJ·mol-1
C.向小烧杯加料时,应一次性快速加入且立即盖紧杯盖
D.用温度计测量酸溶液的温度后立即测量碱溶液的温度
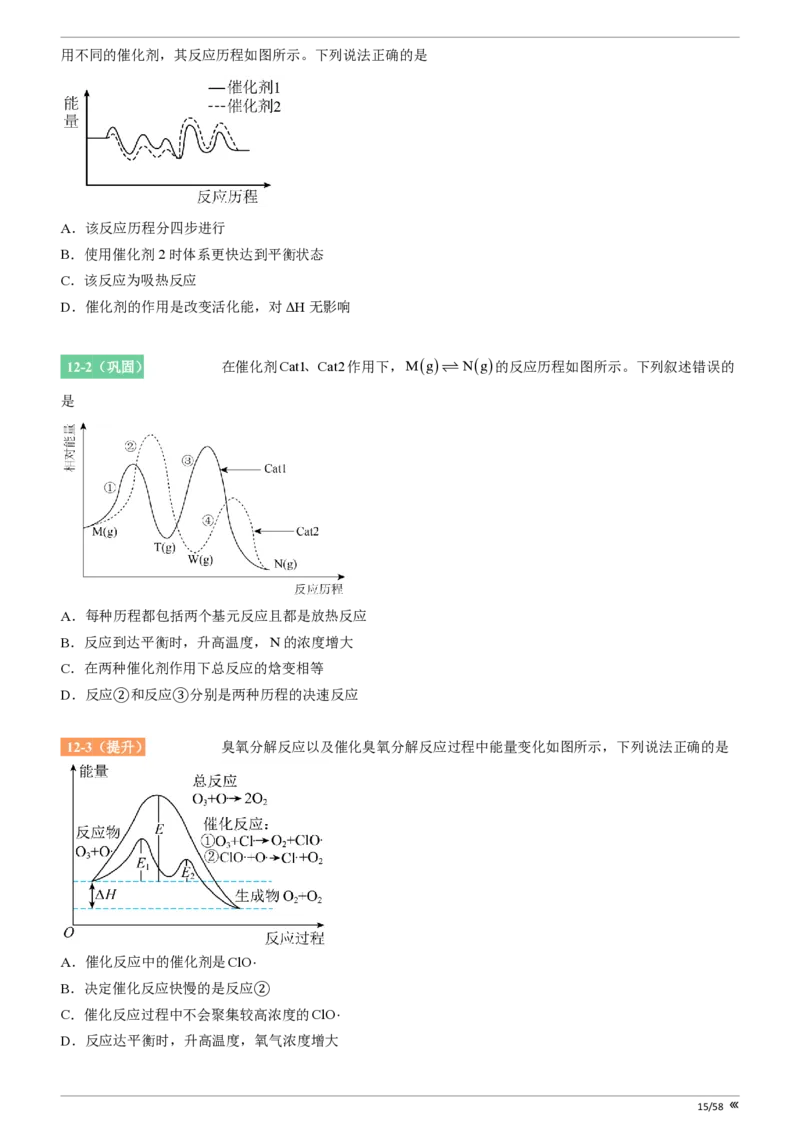
【原卷 12 题】 知识点 影响化学平衡的因素,基元反应与反应历程
12-1(基础)[26055726] T℃下,向一恒容密闭容器中充入M和N,发生反应2M(g)+N(g) 2P(g)+Q(s),使
ƒ
14/58用不同的催化剂,其反应历程如图所示。下列说法正确的是
A.该反应历程分四步进行
B.使用催化剂2时体系更快达到平衡状态
C.该反应为吸热反应
D.催化剂的作用是改变活化能,对ΔH无影响
12-2(巩固)[25457623] 在催化剂Cat1、Cat2作用下,Mg
ƒ
Ng的反应历程如图所示。下列叙述错误的
是
A.每种历程都包括两个基元反应且都是放热反应
B.反应到达平衡时,升高温度,N的浓度增大
C.在两种催化剂作用下总反应的焓变相等
D.反应②和反应③分别是两种历程的决速反应
12-3(提升)[25182334] 臭氧分解反应以及催化臭氧分解反应过程中能量变化如图所示,下列说法正确的是
A.催化反应中的催化剂是ClO×
B.决定催化反应快慢的是反应②
C.催化反应过程中不会聚集较高浓度的ClO×
D.反应达平衡时,升高温度,氧气浓度增大
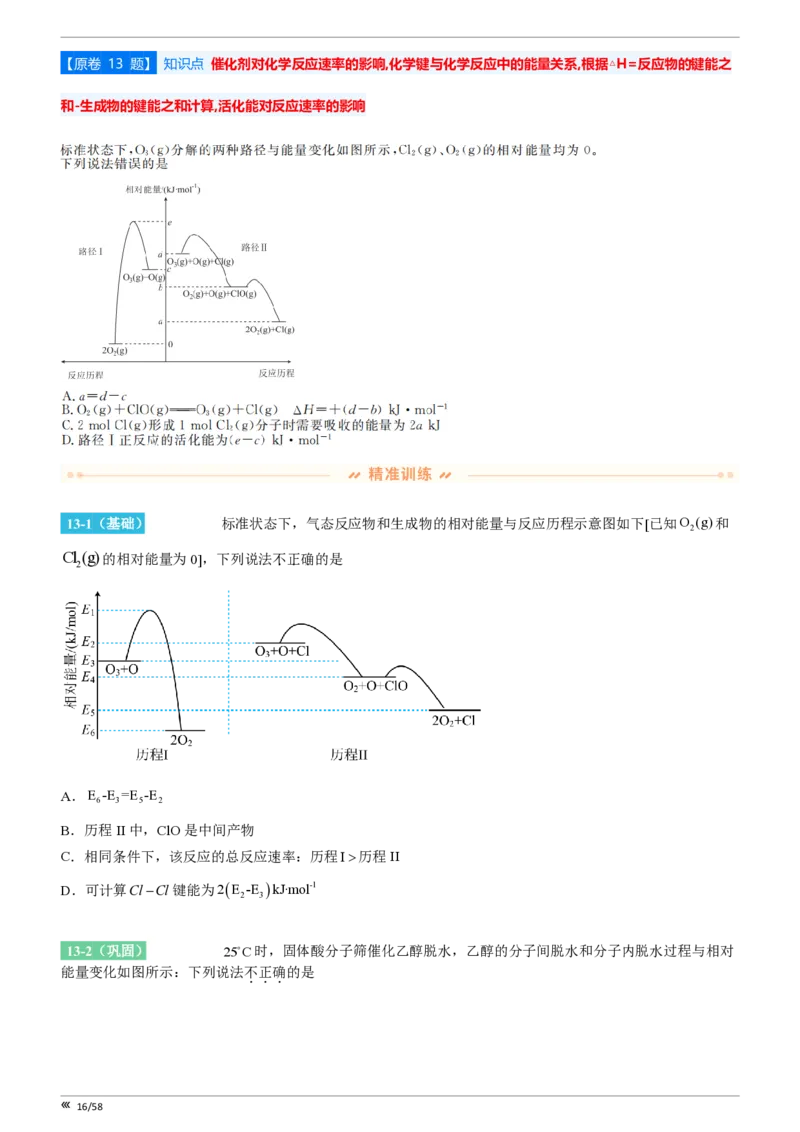
15/58【原卷 13 题】 知识点 催化剂对化学反应速率的影响,化学键与化学反应中的能量关系,根据△H=反应物的键能之
和-生成物的键能之和计算,活化能对反应速率的影响
13-1(基础)[28672679] 标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O (g)和
2
Cl (g)的相对能量为0],下列说法不.正.确.的是
2
A.E -E =E -E
6 3 5 2
B.历程II中,ClO是中间产物
C.相同条件下,该反应的总反应速率:历程I>历程II
D.可计算Cl-Cl键能为2E -E kJ·mol-1
2 3
13-2(巩固)[23270628] 25oC时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对
能量变化如图所示:下列说法不正确的是
...
16/58A.乙醇通过氢键吸附于固体酸分子筛表面并放出热量
B.生成产物2的决速步活化能为60.1kcal×mol-1
C.降低温度有利于提高产物1在反应初始阶段的选择性
D.升高温度可以提高产物2的平衡产率
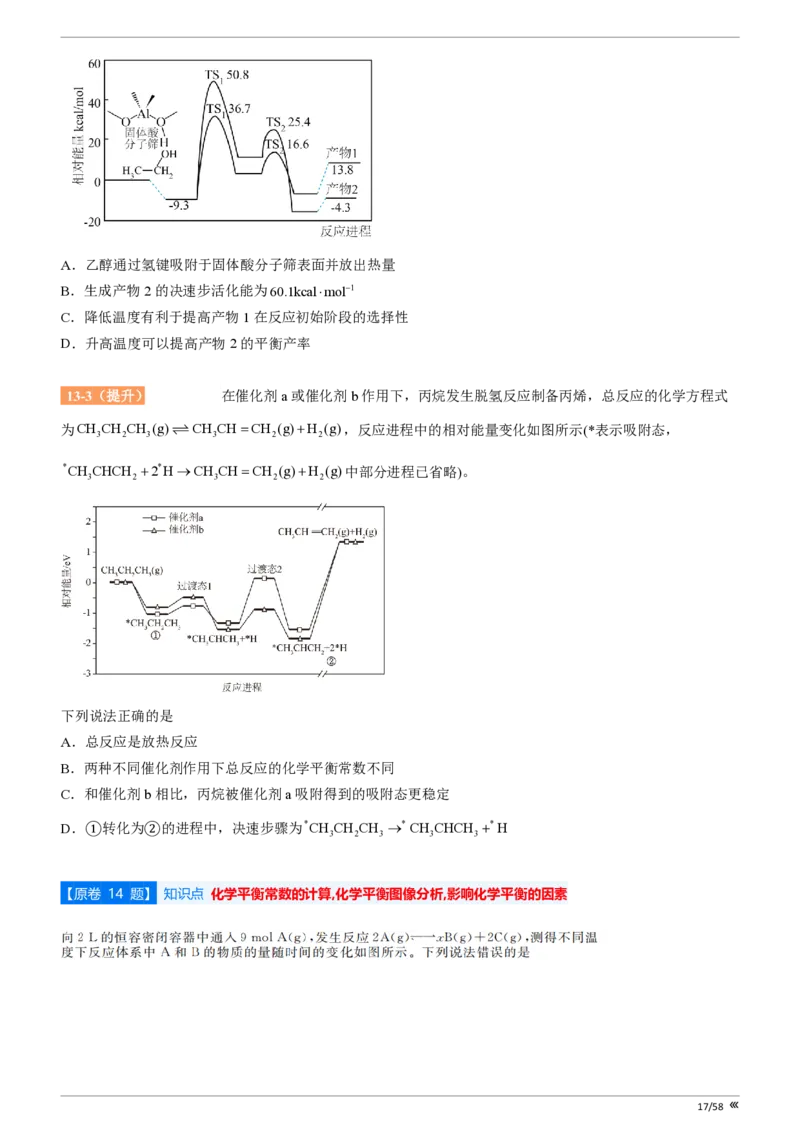
13-3(提升)[27518350] 在催化剂a或催化剂b作用下,丙烷发生脱氢反应制备丙烯,总反应的化学方程式
为CH
3
CH
2
CH
3
(g)
ƒ
CH
3
CH=CH
2
(g)+H
2
(g),反应进程中的相对能量变化如图所示(*表示吸附态,
*CH CHCH +2*H®CH CH=CH (g)+H (g)中部分进程已省略)。
3 2 3 2 2
下列说法正确的是
A.总反应是放热反应
B.两种不同催化剂作用下总反应的化学平衡常数不同
C.和催化剂b相比,丙烷被催化剂a吸附得到的吸附态更稳定
D.①转化为②的进程中,决速步骤为*CH CH CH ®* CH CHCH +*H
3 2 3 3 3
【原卷 14 题】 知识点 化学平衡常数的计算,化学平衡图像分析,影响化学平衡的因素
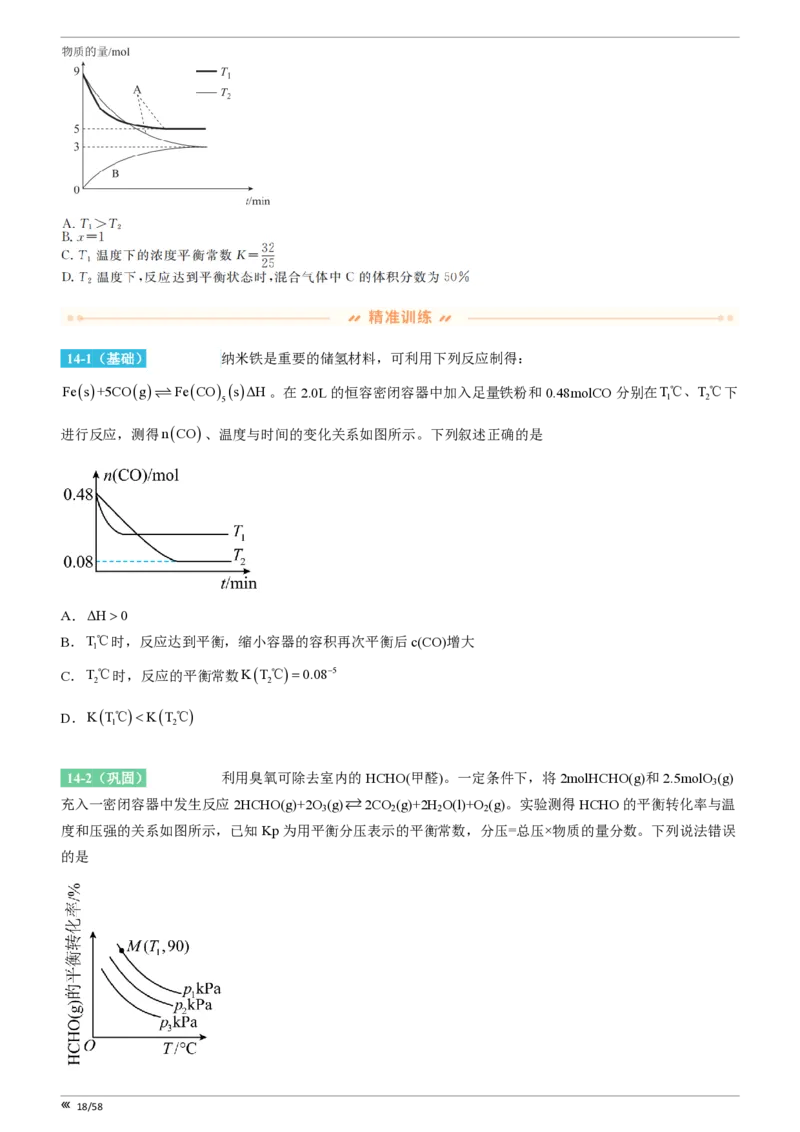
17/5814-1(基础)[25883745] 纳米铁是重要的储氢材料,可利用下列反应制得:
Fes+5COg
ƒ
FeCO
5
sΔH。在2.0L的恒容密闭容器中加入足量铁粉和0.48molCO分别在T
1
℃、T
2
℃下
进行反应,测得nCO、温度与时间的变化关系如图所示。下列叙述正确的是
A.ΔH>0
B.T℃时,反应达到平衡,缩小容器的容积再次平衡后c(CO)增大
1
C.T℃时,反应的平衡常数KT℃=0.08-5
2 2
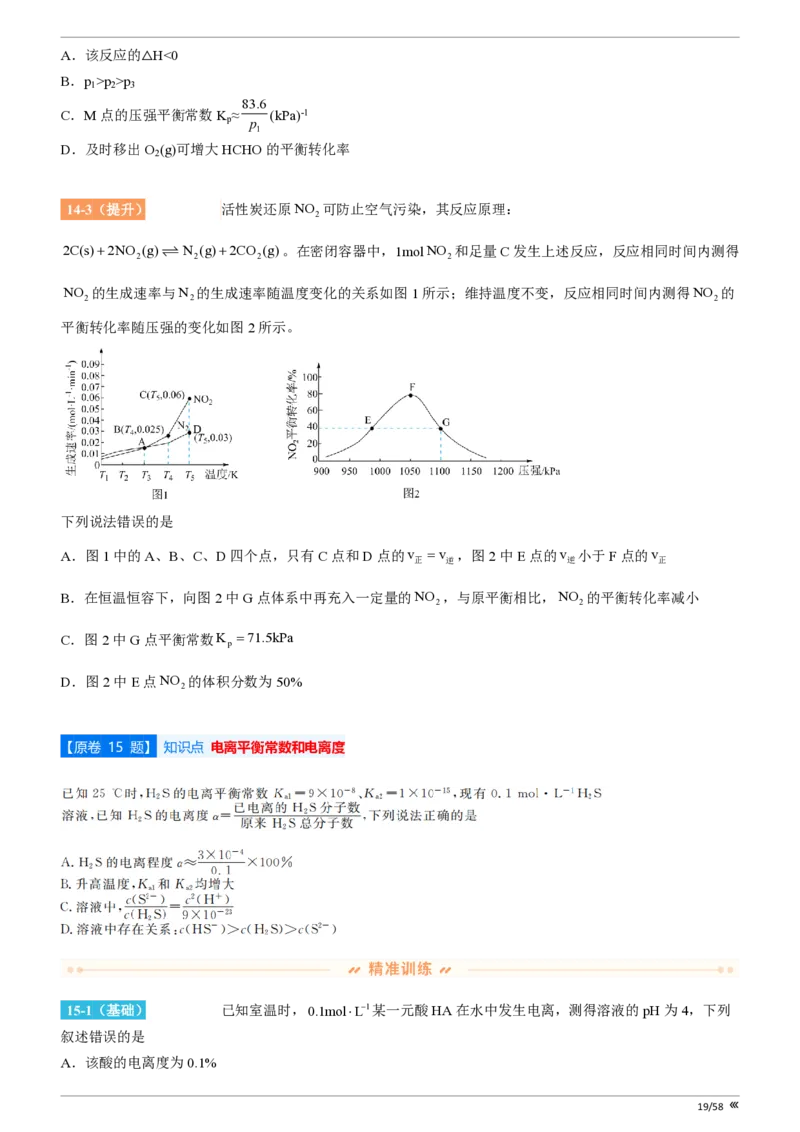
D.KT℃p >p
1 2 3
83.6
C.M点的压强平衡常数K ≈ (kPa)-1
p p
1
D.及时移出O (g)可增大HCHO的平衡转化率
2
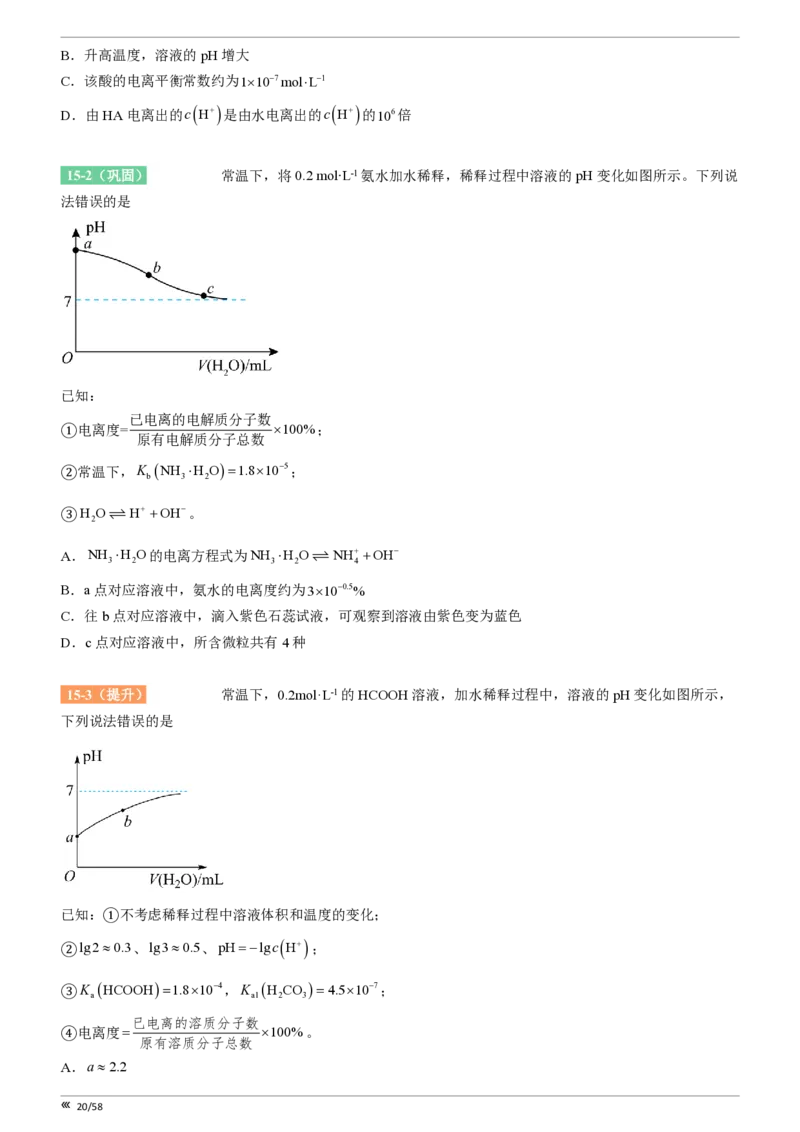
14-3(提升)[25713077] 活性炭还原NO 可防止空气污染,其反应原理:
2
2C(s)+2NO
2
(g)
ƒ
N
2
(g)+2CO
2
(g)。在密闭容器中,1molNO
2
和足量C发生上述反应,反应相同时间内测得
NO 的生成速率与N 的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO 的
2 2 2
平衡转化率随压强的变化如图2所示。
下列说法错误的是
A.图1中的A、B、C、D四个点,只有C点和D点的v =v ,图2中E点的v 小于F点的v
正 逆 逆 正
B.在恒温恒容下,向图2中G点体系中再充入一定量的NO ,与原平衡相比,NO 的平衡转化率减小
2 2
C.图2中G点平衡常数K =71.5kPa
p
D.图2中E点NO 的体积分数为50%
2
【原卷 15 题】 知识点 电离平衡常数和电离度
15-1(基础)[21042602] 已知室温时,0.1mol×L-1某一元酸HA在水中发生电离,测得溶液的pH为4,下列
叙述错误的是
A.该酸的电离度为0.1%
19/58B.升高温度,溶液的pH增大
C.该酸的电离平衡常数约为1´10-7mol×L-1
D.由HA电离出的c
H+
是由水电离出的c
H+
的106倍
15-2(巩固)[24455809] 常温下,将0.2 mol∙L-1氨水加水稀释,稀释过程中溶液的pH变化如图所示。下列说
法错误的是
已知:
已电离的电解质分子数
①电离度= ´100%;
原有电解质分子总数
②常温下,K NH ×H O=1.8´10-5;
b 3 2
③H
2
O
ƒ
H+ +OH-。
A.NH ×H O的电离方程式为NH ×H O NH+ +OH-
3 2 3 2 ƒ 4
B.a点对应溶液中,氨水的电离度约为3´10-0.5%
C.往b点对应溶液中,滴入紫色石蕊试液,可观察到溶液由紫色变为蓝色
D.c点对应溶液中,所含微粒共有4种
15-3(提升)[25195989] 常温下,0.2mol·L-1的HCOOH溶液,加水稀释过程中,溶液的pH变化如图所示,
下列说法错误的是
已知:①不考虑稀释过程中溶液体积和温度的变化;
②lg2»0.3、lg3»0.5、pH=-lgc
H+
;
③K HCOOH=1.8´10-4,K H CO =4.5´10-7;
a a1 2 3
已电离的溶质分子数
④电离度= ´100%。
原有溶质分子总数
A.a»2.2
20/58B.HCOOH的电离度:a>b
C.HCOOH的电离方程式为HCOOH HCOO-+H+
ƒ
D.往b点溶液中滴入NaHCO 溶液,可观察到有气泡产生
3
【原卷 16 题】 知识点 化学反应热的计算,化学反应速率计算,化学平衡状态的判断方法,化学平衡图像分析
16-1(基础)[26819816] 我国力争在2060年前实现“碳中和”,综合利用CO 具有重要的意义。30MPa、
2
200℃条件下,CO 与H 反应可制得气态甲醇(CH OH),其反应方程式为:CO +3H ⇌CH OH+H O(g)。
2 2 3 2 2 3 2
(1)已知生成32 g CH OH放出热量49 kJ,该反应的热化学方程式为 。
3
(2)在该反应中,表示该反应速率最快的是:_______。
A.v(CO )=30 mol∙L-1∙min-1 B.v(CH OH)=0.3 mol∙L-1∙s-1
2 3
C.v(H )=0.8 mol∙L-1∙s-1 D.v(H O)=0.6 mol∙L-1∙s-1
2 2
21/58(3)往一容积为2L的恒容密闭容器中通入1molCO 和3molH ,一定温度下发生上述反应,下列能判断达到化
2 2
学平衡状态时的是_______。
A.容器内气体压强不再发生改变 B.正、逆反应速率相等且均为零
C.气体密度不再发生改变 D.V (CO )=3v (H )
正 2 逆 2
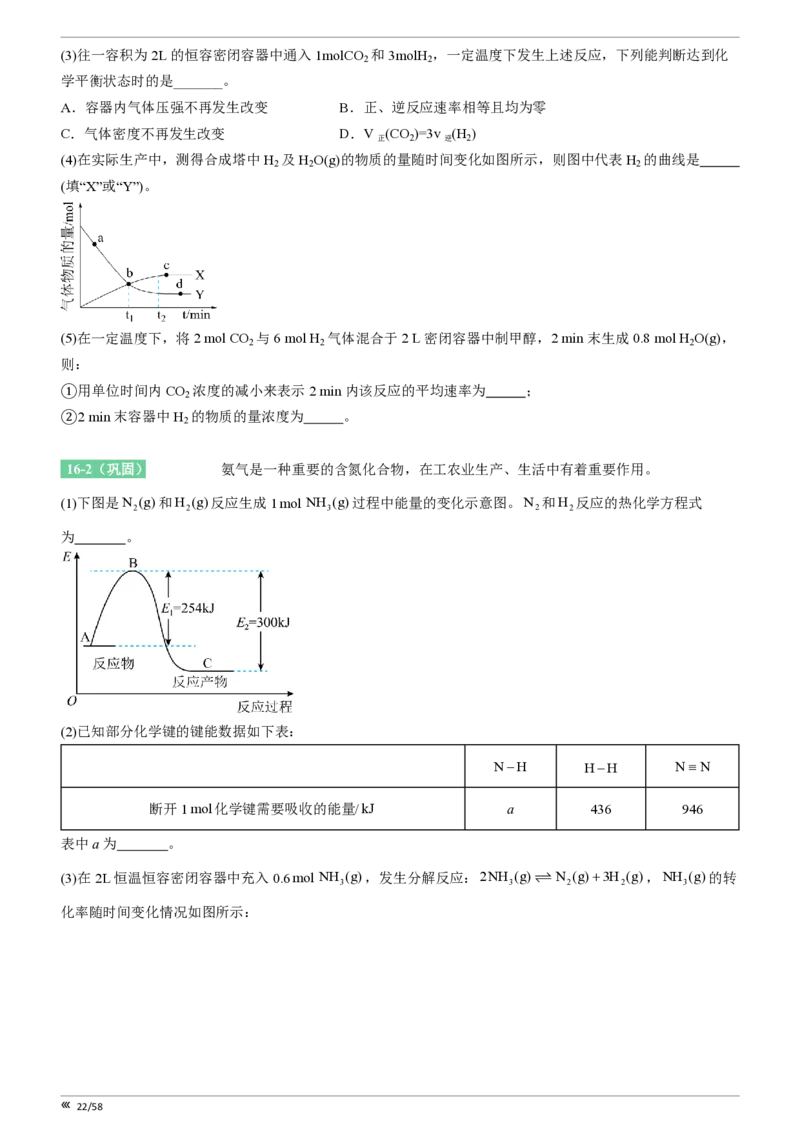
(4)在实际生产中,测得合成塔中H 及H O(g)的物质的量随时间变化如图所示,则图中代表H 的曲线是
2 2 2
(填“X”或“Y”)。
(5)在一定温度下,将2 mol CO 与6 mol H 气体混合于2 L密闭容器中制甲醇,2 min末生成0.8 mol H O(g),
2 2 2
则:
①用单位时间内CO 浓度的减小来表示2 min内该反应的平均速率为 ;
2
②2 min末容器中H 的物质的量浓度为 。
2
16-2(巩固)[26227035] 氨气是一种重要的含氮化合物,在工农业生产、生活中有着重要作用。
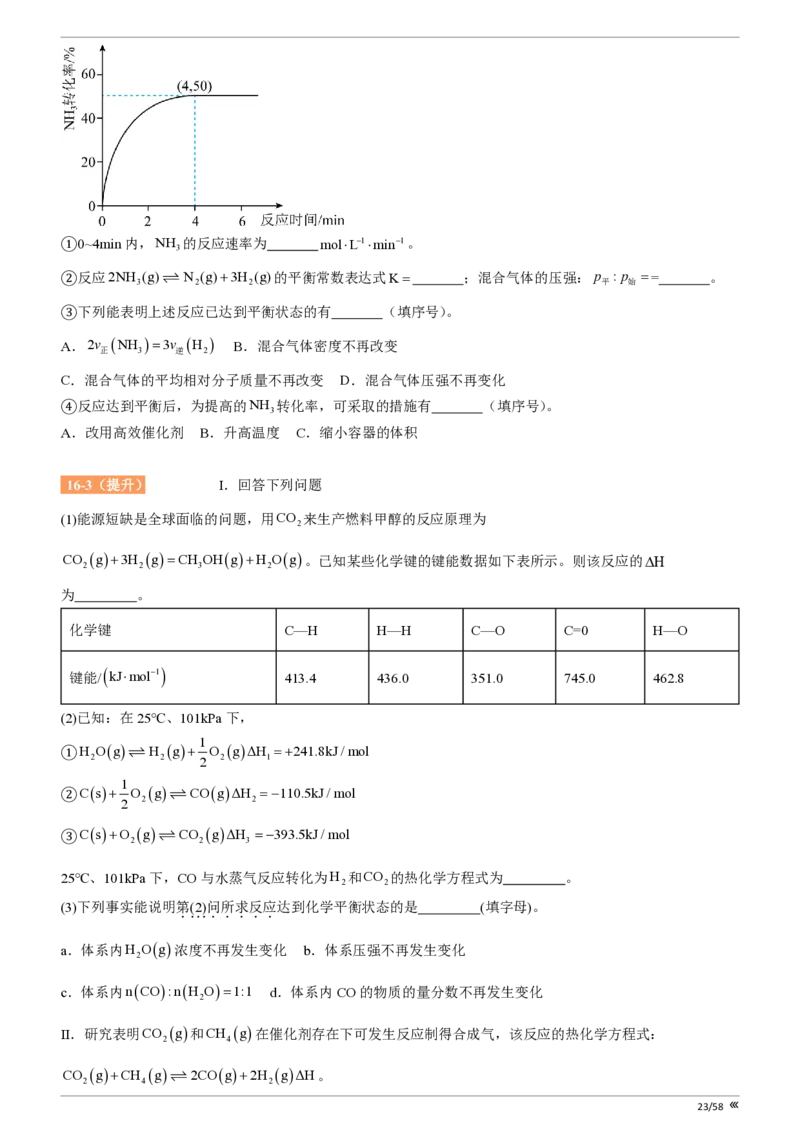
(1)下图是N (g)和H (g)反应生成1mol NH (g)过程中能量的变化示意图。N 和H 反应的热化学方程式
2 2 3 2 2
为 。
(2)已知部分化学键的键能数据如下表:
N-H H-H NºN
断开1mol化学键需要吸收的能量/kJ a 436 946
表中a为 。
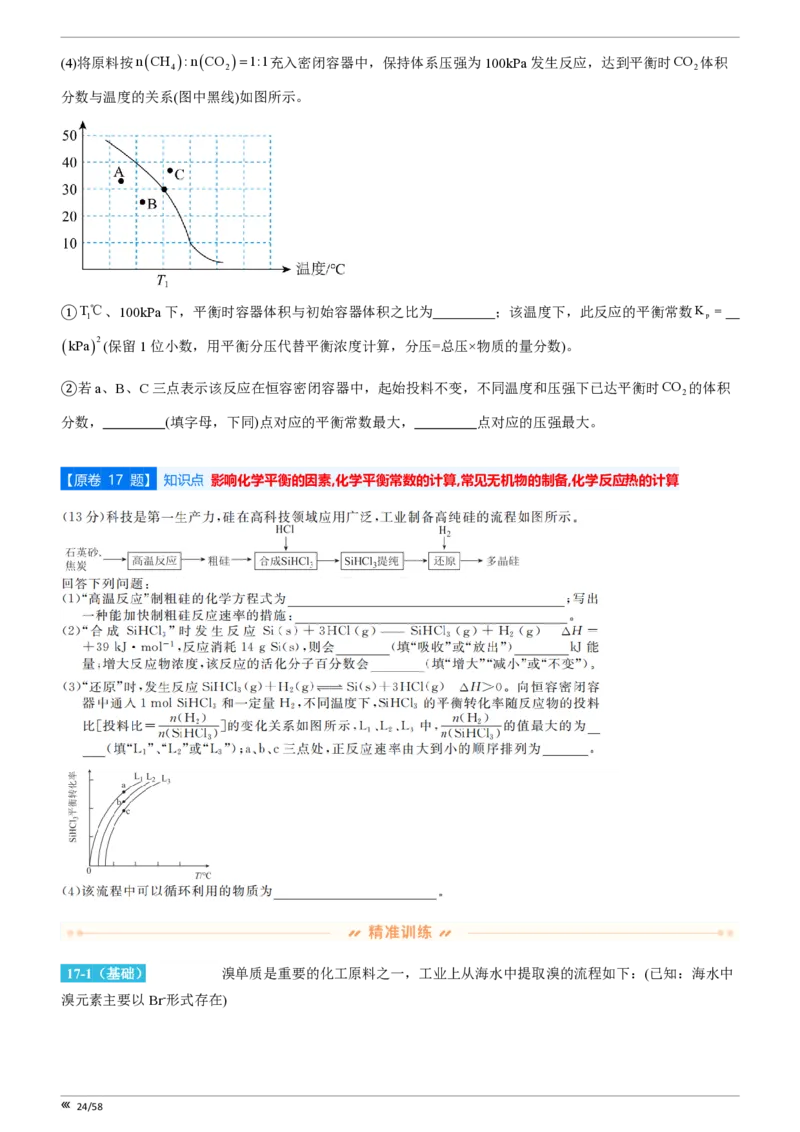
(3)在2L恒温恒容密闭容器中充入0.6mol NH
3
(g),发生分解反应:2NH
3
(g)
ƒ
N
2
(g)+3H
2
(g),NH
3
(g)的转
化率随时间变化情况如图所示:
22/58①0~4min内,NH 的反应速率为 mol×L-1×min-1。
3
②反应2NH
3
(g)
ƒ
N
2
(g)+3H
2
(g)的平衡常数表达式K= ;混合气体的压强:p
平
: p
始
== 。
③下列能表明上述反应已达到平衡状态的有 (填序号)。
A.2v NH =3v H B.混合气体密度不再改变
正 3 逆 2
C.混合气体的平均相对分子质量不再改变 D.混合气体压强不再变化
④反应达到平衡后,为提高的NH 转化率,可采取的措施有 (填序号)。
3
A.改用高效催化剂 B.升高温度 C.缩小容器的体积
16-3(提升)[25337769] I.回答下列问题
(1)能源短缺是全球面临的问题,用CO 来生产燃料甲醇的反应原理为
2
CO g+3H g=CH OHg+H Og。已知某些化学键的键能数据如下表所示。则该反应的DH
2 2 3 2
为 。
化学键 C—H H—H C—O C=0 H—O
键能/
kJ×mol-1
413.4 436.0 351.0 745.0 462.8
(2)已知:在25℃、101kPa下,
1
①H
2
Og
ƒ
H
2
g+
2
O
2
gΔH
1
=+241.8kJ/mol
1
②Cs+
2
O
2
g
ƒ
COgΔH
2
=-110.5kJ/mol
③Cs+O
2
g
ƒ
CO
2
gΔH
3
=-393.5kJ/mol
25℃、101kPa下,CO与水蒸气反应转化为H 和CO 的热化学方程式为 。
2 2
(3)下列事实能说明第(2)问所求反应达到化学平衡状态的是 (填字母)。
.........
a.体系内H Og浓度不再发生变化 b.体系压强不再发生变化
2
c.体系内nCO:nH O=1:1 d.体系内CO的物质的量分数不再发生变化
2
Ⅱ.研究表明CO g和CH g在催化剂存在下可发生反应制得合成气,该反应的热化学方程式:
2 4
CO g+CH g 2COg+2H gΔH。
2 4 ƒ 2
23/58(4)将原料按nCH :nCO =1:1充入密闭容器中,保持体系压强为100kPa发生反应,达到平衡时CO 体积
4 2 2
分数与温度的关系(图中黑线)如图所示。
①T℃、100kPa下,平衡时容器体积与初始容器体积之比为 ;该温度下,此反应的平衡常数K =
1 p
kPa2 (保留1位小数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②若a、B、C三点表示该反应在恒容密闭容器中,起始投料不变,不同温度和压强下已达平衡时CO 的体积
2
分数, (填字母,下同)点对应的平衡常数最大, 点对应的压强最大。
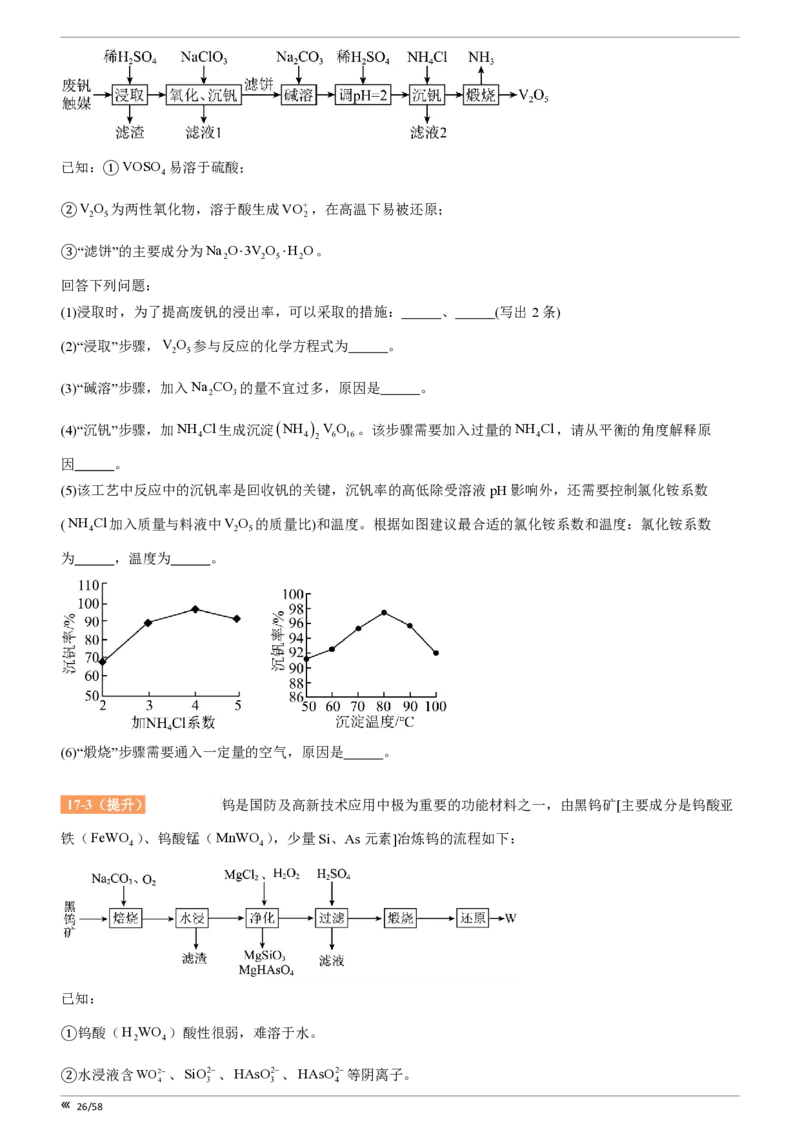
【原卷 17 题】 知识点 影响化学平衡的因素,化学平衡常数的计算,常见无机物的制备,化学反应热的计算
17-1(基础)[25958280] 溴单质是重要的化工原料之一,工业上从海水中提取溴的流程如下:(已知:海水中
溴元素主要以Br-形式存在)
24/58(1)将吹出后的含Br 的空气按一定速率通入吸收塔,用SO 和水进行吸收,写出吸收反应的化学方程
2 2
式: 。
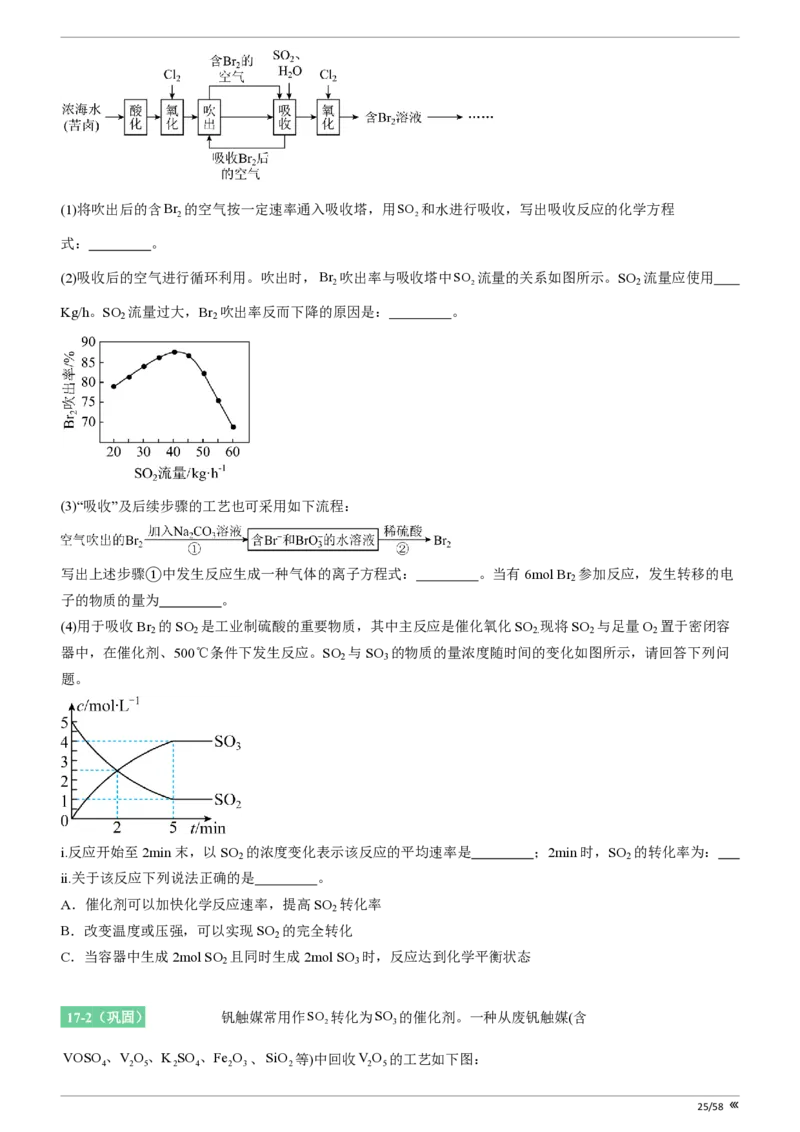
(2)吸收后的空气进行循环利用。吹出时,Br 吹出率与吸收塔中SO 流量的关系如图所示。SO 流量应使用
2 2 2
Kg/h。SO 流量过大,Br 吹出率反而下降的原因是: 。
2 2
(3)“吸收”及后续步骤的工艺也可采用如下流程:
写出上述步骤①中发生反应生成一种气体的离子方程式: 。当有6mol Br 参加反应,发生转移的电
2
子的物质的量为 。
(4)用于吸收Br 的SO 是工业制硫酸的重要物质,其中主反应是催化氧化SO 现将SO 与足量O 置于密闭容
2 2 2. 2 2
器中,在催化剂、500℃条件下发生反应。SO 与SO 的物质的量浓度随时间的变化如图所示,请回答下列问
2 3
题。
ⅰ.反应开始至2min末,以SO 的浓度变化表示该反应的平均速率是 ;2min时,SO 的转化率为:
2 2
ⅱ.关于该反应下列说法正确的是 。
A.催化剂可以加快化学反应速率,提高SO 转化率
2
B.改变温度或压强,可以实现SO 的完全转化
2
C.当容器中生成2mol SO 且同时生成2mol SO 时,反应达到化学平衡状态
2 3
17-2(巩固)[27986669] 钒触媒常用作SO 转化为SO 的催化剂。一种从废钒触媒(含
2 3
VOSO、VO、K SO、Fe O 、SiO 等)中回收VO 的工艺如下图:
4 2 5 2 4 2 3 2 2 5
25/58已知:①VOSO 易溶于硫酸;
4
②VO 为两性氧化物,溶于酸生成VO+,在高温下易被还原;
2 5 2
③“滤饼”的主要成分为Na O×3VO ×H O。
2 2 5 2
回答下列问题:
(1)浸取时,为了提高废钒的浸出率,可以采取的措施: 、 (写出2条)
(2)“浸取”步骤,VO 参与反应的化学方程式为 。
2 5
(3)“碱溶”步骤,加入Na CO 的量不宜过多,原因是 。
2 3
(4)“沉钒”步骤,加NH Cl生成沉淀NH VO 。该步骤需要加入过量的NH Cl,请从平衡的角度解释原
4 4 2 6 16 4
因 。
(5)该工艺中反应中的沉钒率是回收钒的关键,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数
(NH Cl加入质量与料液中VO 的质量比)和温度。根据如图建议最合适的氯化铵系数和温度:氯化铵系数
4 2 5
为 ,温度为 。
(6)“煅烧”步骤需要通入一定量的空气,原因是 。
17-3(提升)[28918148] 钨是国防及高新技术应用中极为重要的功能材料之一,由黑钨矿[主要成分是钨酸亚
铁(FeWO )、钨酸锰(MnWO ),少量Si、As元素]冶炼钨的流程如下:
4 4
已知:
①钨酸(H WO )酸性很弱,难溶于水。
2 4
②水浸液含WO2-、SiO2-、HAsO2-、HAsO2-等阴离子。
4 3 3 4
26/58(1)“焙烧”前,粉碎黑钨矿的目的是 。
(2)滤渣的主要成分为两种金属氧化物,是MnO 、 。
2
(3)“净化”过程中,H O 的作用是 。
2 2
(4)“还原”的总反应为3H
2
g+WO
3
s
ƒ
Ws+3H
2
Og DH实验测得一定条件下,平衡时的体积分数随温度
的变化曲线如图所示。
①该反应DH 0(填“>”或“<”)。
②由图可知,a点处v v (填“>”或“<”或“=”)。
正 逆
③900℃时该反应的压强平衡常数 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(5)工业上可以采用铝热法还原黄钨(WO )生产钨。已知:
3
①3Fe O s+4Ws=9Fes+4WO s DH =akJ×mol-1
3 4 3 1
②3Fe O s+8Als=9Fes+4Al O sDH =bkJ×mol-1
3 4 2 3 2
则WO s+2Als=Ws+Al O s的DH = 。
3 2 3
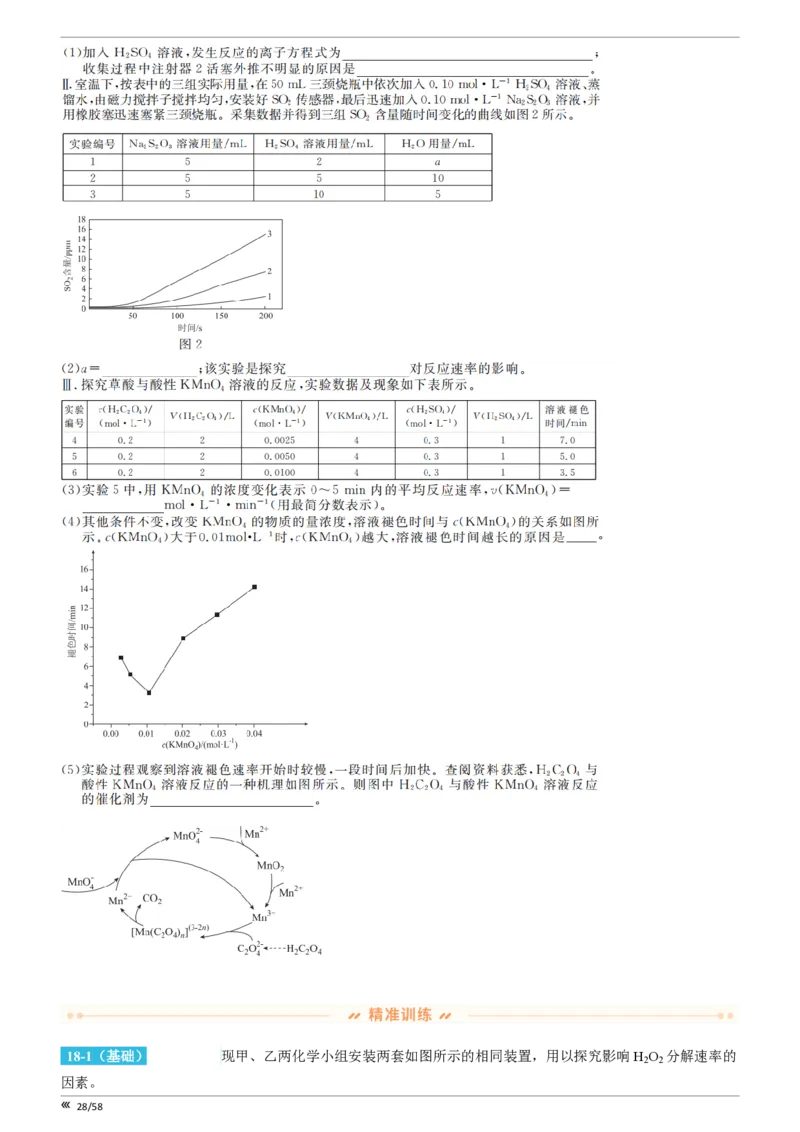
【原卷 18 题】 知识点 外因对化学反应速率影响的综合分析,温度对化学平衡移动的影响,反应速率的测定
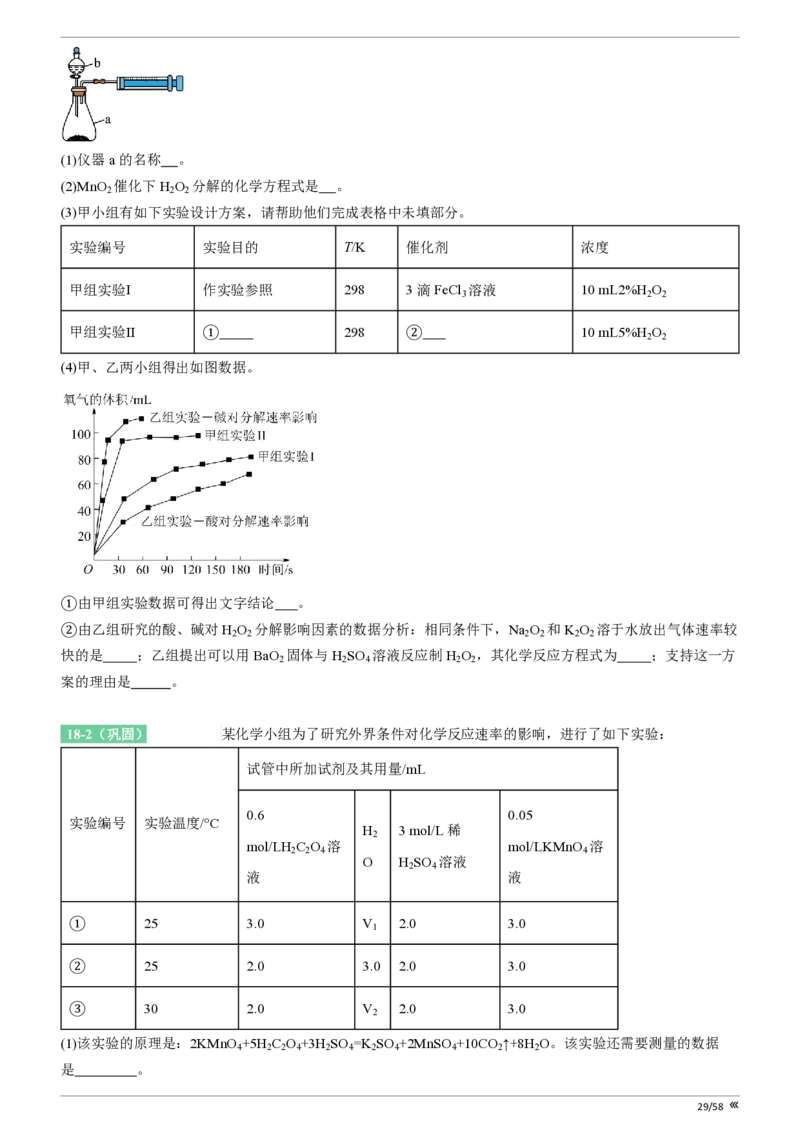
27/5818-1(基础)[28951205] 现甲、乙两化学小组安装两套如图所示的相同装置,用以探究影响H O 分解速率的
2 2
因素。
28/58(1)仪器a的名称 。
(2)MnO 催化下H O 分解的化学方程式是 。
2 2 2
(3)甲小组有如下实验设计方案,请帮助他们完成表格中未填部分。
实验编号 实验目的 T/K 催化剂 浓度
甲组实验Ⅰ 作实验参照 298 3滴FeCl 溶液 10 mL2%H O
3 2 2
甲组实验Ⅱ ① 298 ② 10 mL5%H O
2 2
(4)甲、乙两小组得出如图数据。
①由甲组实验数据可得出文字结论 。
②由乙组研究的酸、碱对H O 分解影响因素的数据分析:相同条件下,Na O 和K O 溶于水放出气体速率较
2 2 2 2 2 2
快的是 ;乙组提出可以用BaO 固体与H SO 溶液反应制H O ,其化学反应方程式为 ;支持这一方
2 2 4 2 2
案的理由是 。
18-2(巩固)[28873977] 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
试管中所加试剂及其用量/mL
0.6 0.05
实验编号 实验温度/°C
H 3 mol/L稀
2
mol/LH C O 溶 mol/LKMnO 溶
2 2 4 4
O H SO 溶液
2 4
液 液
① 25 3.0 V 2.0 3.0
1
② 25 2.0 3.0 2.0 3.0
③ 30 2.0 V 2.0 3.0
2
(1)该实验的原理是:2KMnO +5H C O +3H SO =K SO +2MnSO +10CO ↑+8H O。该实验还需要测量的数据
4 2 2 4 2 4 2 4 4 2 2
是 。
29/58(2)V = ,V = 。
1 2
(3)探究温度对化学反应速率的影响,应选择实验 (填实验编号)。
(4)若实验①用时1.5 min则第一组实验的化学反应速率(用草酸表示)为 。
(5)某同学绘制了瞬时速率v和时间t的图像
①该同学提出猜想
猜想a:温度上升导致速率快速上升
猜想b:反应产生了催化剂
该同学发现该反应前后体系温度上升了0.5℃,因此 不成立(猜想a或猜想b)。
②该同学推测可能的催化剂是 (填物质化学式)。
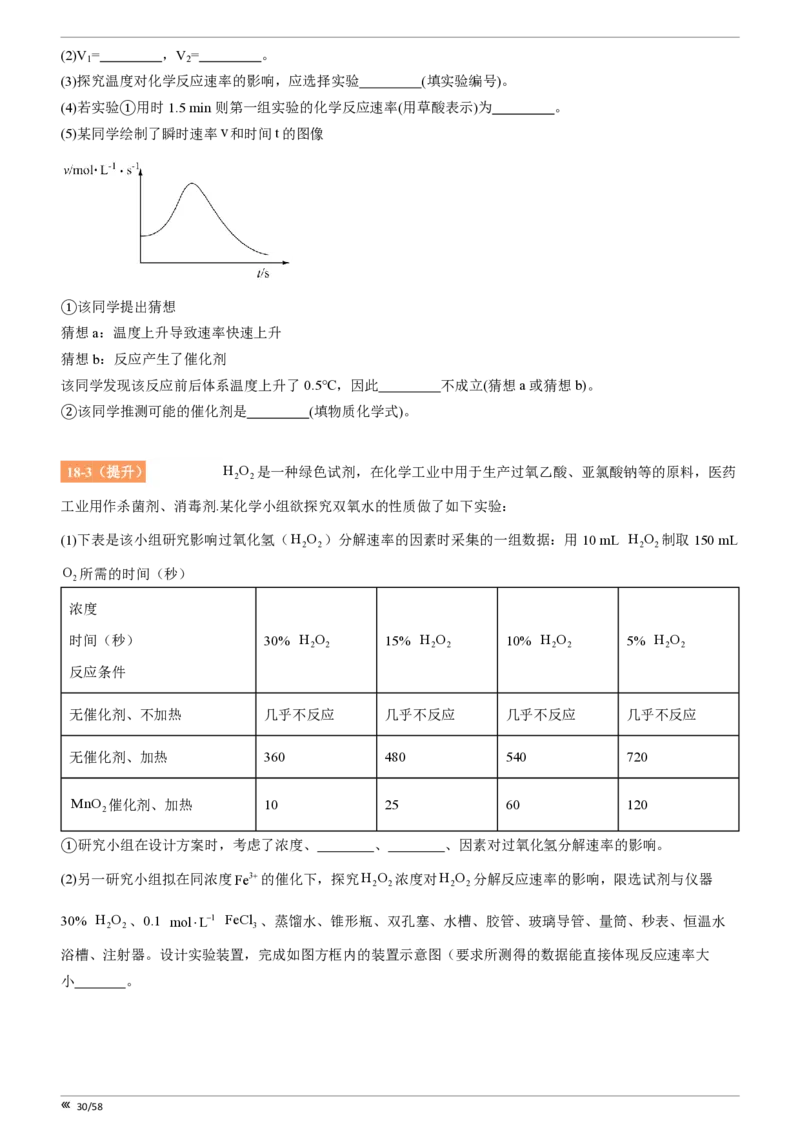
18-3(提升)[28918146] H O 是一种绿色试剂,在化学工业中用于生产过氧乙酸、亚氯酸钠等的原料,医药
2 2
工业用作杀菌剂、消毒剂.某化学小组欲探究双氧水的性质做了如下实验:
(1)下表是该小组研究影响过氧化氢(H O )分解速率的因素时采集的一组数据:用10 mL H O 制取150 mL
2 2 2 2
O 所需的时间(秒)
2
浓度
时间(秒) 30% H O 15% H O 10% H O 5% H O
2 2 2 2 2 2 2 2
反应条件
无催化剂、不加热 几乎不反应 几乎不反应 几乎不反应 几乎不反应
无催化剂、加热 360 480 540 720
MnO 催化剂、加热 10 25 60 120
2
①研究小组在设计方案时,考虑了浓度、 、 、因素对过氧化氢分解速率的影响。
(2)另一研究小组拟在同浓度Fe3+的催化下,探究H O 浓度对H O 分解反应速率的影响,限选试剂与仪器
2 2 2 2
30% H O 、0.1 mol×L-1 FeCl 、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水
2 2 3
浴槽、注射器。设计实验装置,完成如图方框内的装置示意图(要求所测得的数据能直接体现反应速率大
小 。
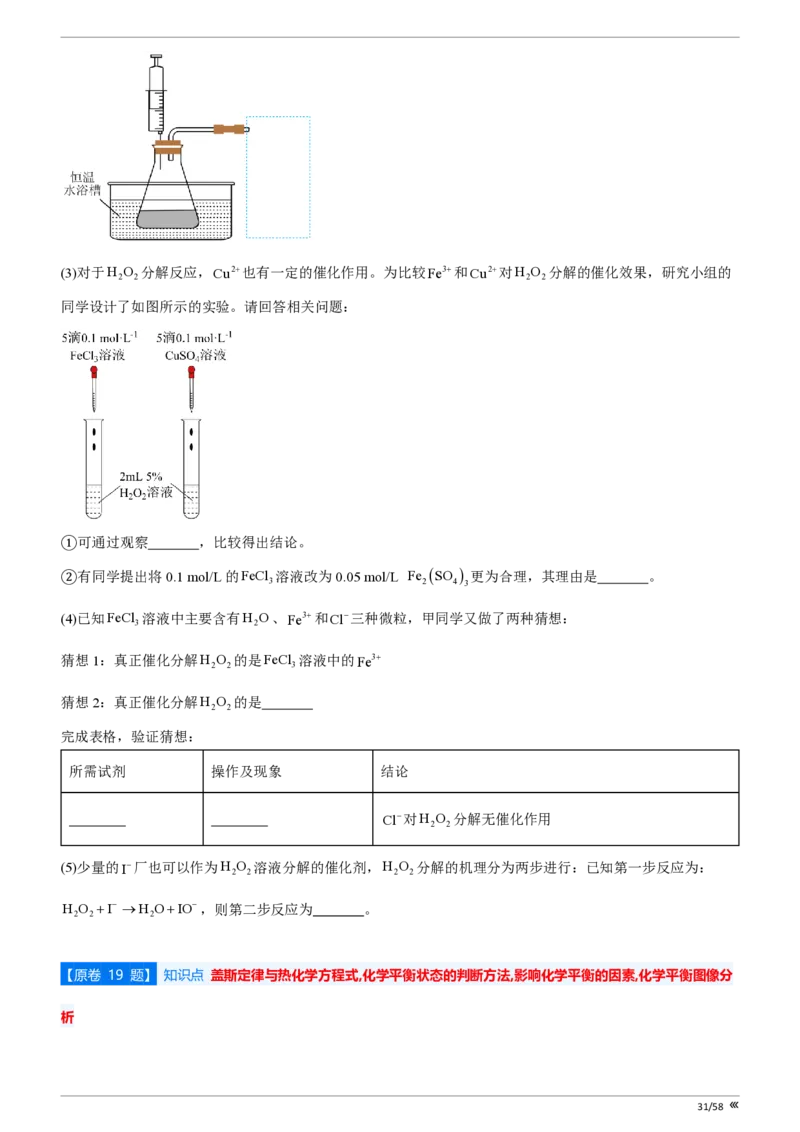
30/58(3)对于H O 分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H O 分解的催化效果,研究小组的
2 2 2 2
同学设计了如图所示的实验。请回答相关问题:
①可通过观察 ,比较得出结论。
②有同学提出将0.1 mol/L的FeCl 溶液改为0.05 mol/L Fe SO 更为合理,其理由是 。
3 2 4 3
(4)已知FeCl 溶液中主要含有H O、Fe3+和Cl-三种微粒,甲同学又做了两种猜想:
3 2
猜想1:真正催化分解H O 的是FeCl 溶液中的Fe3+
2 2 3
猜想2:真正催化分解H O 的是
2 2
完成表格,验证猜想:
所需试剂 操作及现象 结论
Cl-对H O 分解无催化作用
2 2
(5)少量的I-厂也可以作为H O 溶液分解的催化剂,H O 分解的机理分为两步进行:已知第一步反应为:
2 2 2 2
H O +I- ®H O+IO-,则第二步反应为 。
2 2 2
【原卷 19 题】 知识点 盖斯定律与热化学方程式,化学平衡状态的判断方法,影响化学平衡的因素,化学平衡图像分
析
31/5819-1(基础)[28815902] 油气开采、石油化工、煤化工等行业的废气中均含有硫化氢,将其变废为宝的三种
方法如下。按要求回答下列问题。
(1)克劳斯法:利用如下两个反应生成S (g)和H O(g)。
2 2
①2H
2
Sg+3O
2
g
ƒ
2SO
2
g+2H
2
Og ΔH
1
=akJ/mol K
1
32/58②4H 2 Sg+2SO 2 g ƒ 3S 2 g+4H 2 Og ΔH 2 =bkJ/mol K 2
反应①、②的化学平衡常数分别为K 、K 。写出克劳斯法回收处理H S的热化学方程式: ,该反
1 2 2
应的化学平衡常数K= (用K 、K 表示)。
1 2
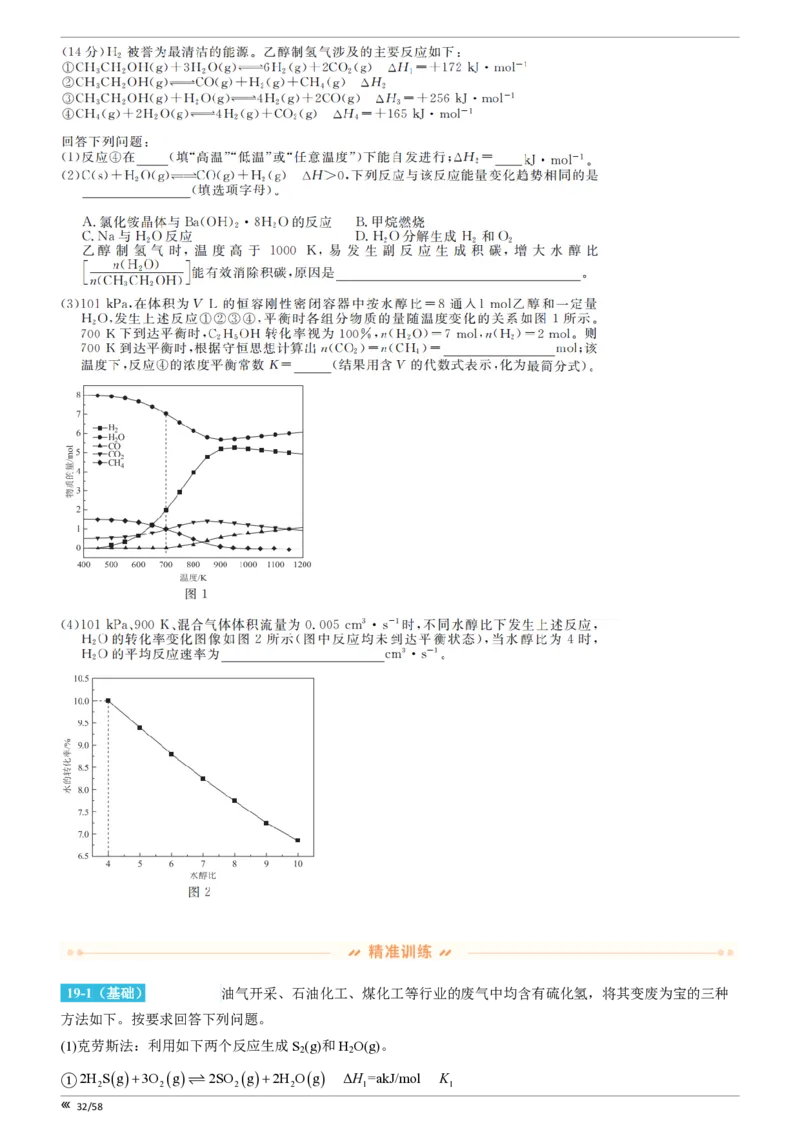
(2)合成用于粮食熏蒸的羰基硫(COS)法:COg+H Sg=COSg+H g。若在2L密闭恒温容器中,反应
2 2
前n(CO)=12mol。在不同温度下该反应达到化学平衡时,H S的平衡转化率如下图所示。
2
①该反应DH (填“>”“ <”或“=”)0。
②150℃下,经5s达到平衡,该反应的平衡常数为0.2,则反应前n(H S)= ;5s内CO平均反应速率
2
为 。
③能极大幅度增大反应速率的措施是 。
(3)高温热分解法:2H 2 Sg ƒ S 2 g+2H 2 g DH=+170kJ/mol
①该反应的化学平衡常数表达式为 。
②其他条件不变增大体系压强,该反应化学平衡常数 (填“变大”“变小”或“不变”)。
19-2(巩固)[28956928] 油气(开采、石油化工、煤化工等行业产生的废气普遍含有硫化氢,需要回收处理并
利用。
回答下列问题:
已知下列反应的热化学方程式:
①2H
2
Sg
ƒ
S
2
g+2H
2
g ΔH
1
=+180kJ×mol-1 K
1
(平衡常数)
②CH
4
g+2H
2
Sg
ƒ
CS
2
g+4H
2
g ΔH
2
K
2
(平衡常数)
③CS
2
g+2H
2
g
ƒ
CH
4
g+S
2
g ΔH
3
=-81kJ×mol-1 K
3
(平衡常数)
(1)K = (用含K 和K 的代数式表示)。
2 1 3
(2)下列叙述一定能说明反应②达到平衡状态的是___________(填标号)。
A.断裂4mol C-H的同时生成4mol H-H
B.在恒温恒容下,CS 和H 浓度之比不再变化
2 2
C.在恒温恒压下,混合气体的密度不再变化
cCS ×c4H
D.在恒容绝热下, 2 2 不再变化
cCH ×c2H S
4 2
33/58(3)列举一种可提高反应②中CH 转化率的措施 。
4
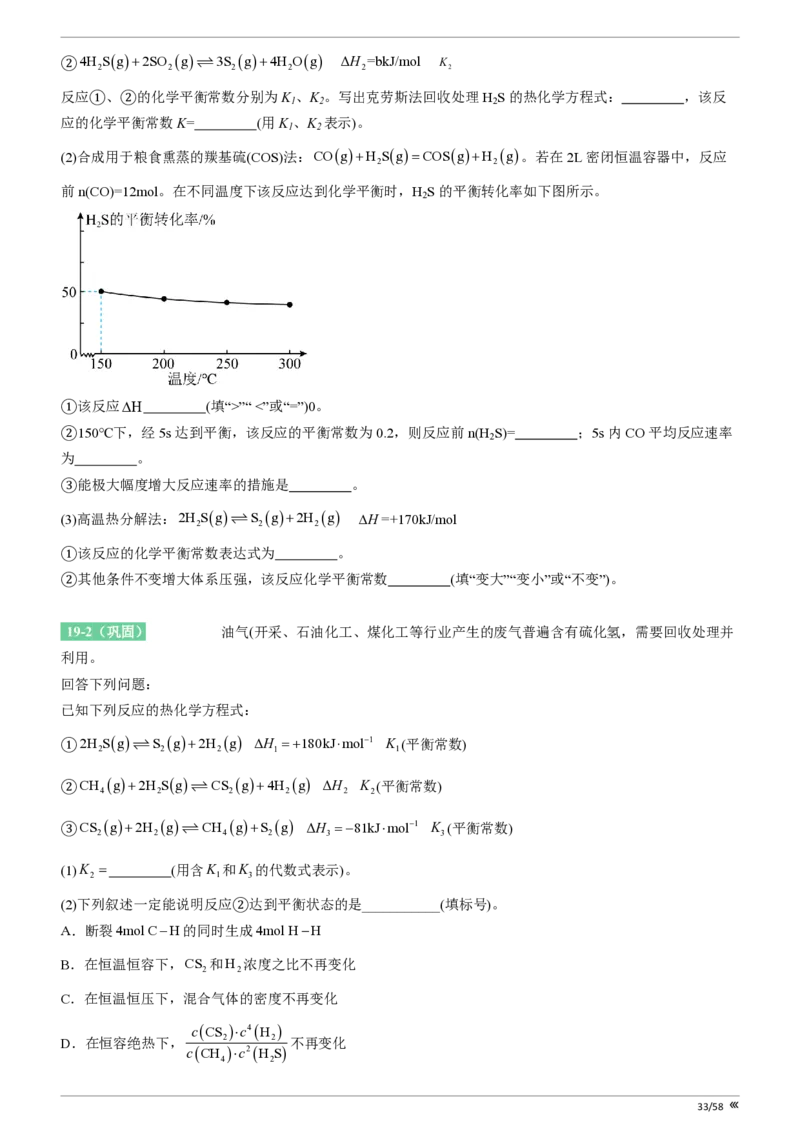
(4)在恒压密闭容器内,充入0.2 mol CS g与0.4 mol H g只发生反应③。CS g的平衡转化率与温度、压
2 2 2
强的关系如图所示。
①请回答:比较压强:p p (填“>”“<”或“=”),维持温度不变,向A点状态的容器中充入氩气,
2 1
CS 的转化率 (填“升高”“降低”或“不变”)。
2
②B点处,容器体积为2 L,则T℃时该反应的平衡常数K= L/mol。
1
(5)若其他条件相同的情况下,反应③在不同温度下反应相同时间后,测得CS 的转化率a随温度的变化曲线
2
如图,其原因是 。
19-3(提升)[28974507] 碳、氮、硫的氧化物是造成污染的重要物质,研究它们的反应机理,对于消除环境
污染有重要的意义。回答下列问题:
Ⅰ.已知反应:
2NO(g)+O (g) 2NO (g) DH =-113.0kJ×mol-1
2 ƒ 2 1
2SO (g) 2SO (g)+O (g) DH =+198kJ×mol-1
3 ƒ 2 2 2
(1)NO (g)与SO (g)反应生成SO (g)和NO(g)的热化学方程式为 。
2 2 3
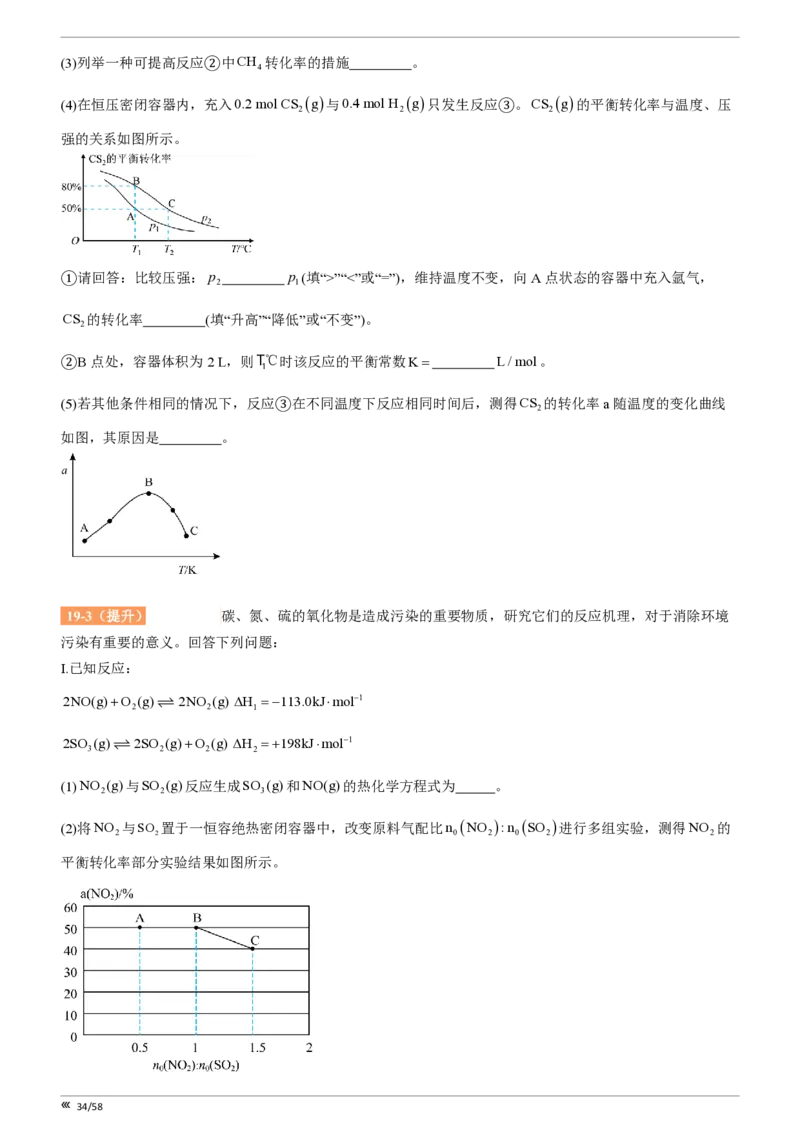
(2)将NO 与SO 置于一恒容绝热密闭容器中,改变原料气配比n NO :n SO 进行多组实验,测得NO 的
2 2 0 2 0 2 2
平衡转化率部分实验结果如图所示。
34/58①下列说法能表示化学反应达到平衡状态的是 (填字母)。
a.气体的平均摩尔质量不变
b.vSO =v(NO)
2
c.气体的压强保持不变
cSO c(NO)
d. 3 保持不变
cNO cSO
2 2
②B点时的化学平衡常数K= 。
Ⅱ.二氧化碳催化加氢制甲醇有利于减少温室气体排放。涉及的主要反应如下:
①CO (g)+3H (g)=CH OH(g)+H O(g) DH =-49.5kJ×mol-1
2 2 3 2 1
②CO (g)+H (g)=CO(g)+H O(g) DH =+40.9kJ×mol-1
2 2 2 2
③CO(g)+2H (g)=CH OH(g) DH =-90.4kJ×mol-1
2 3 3
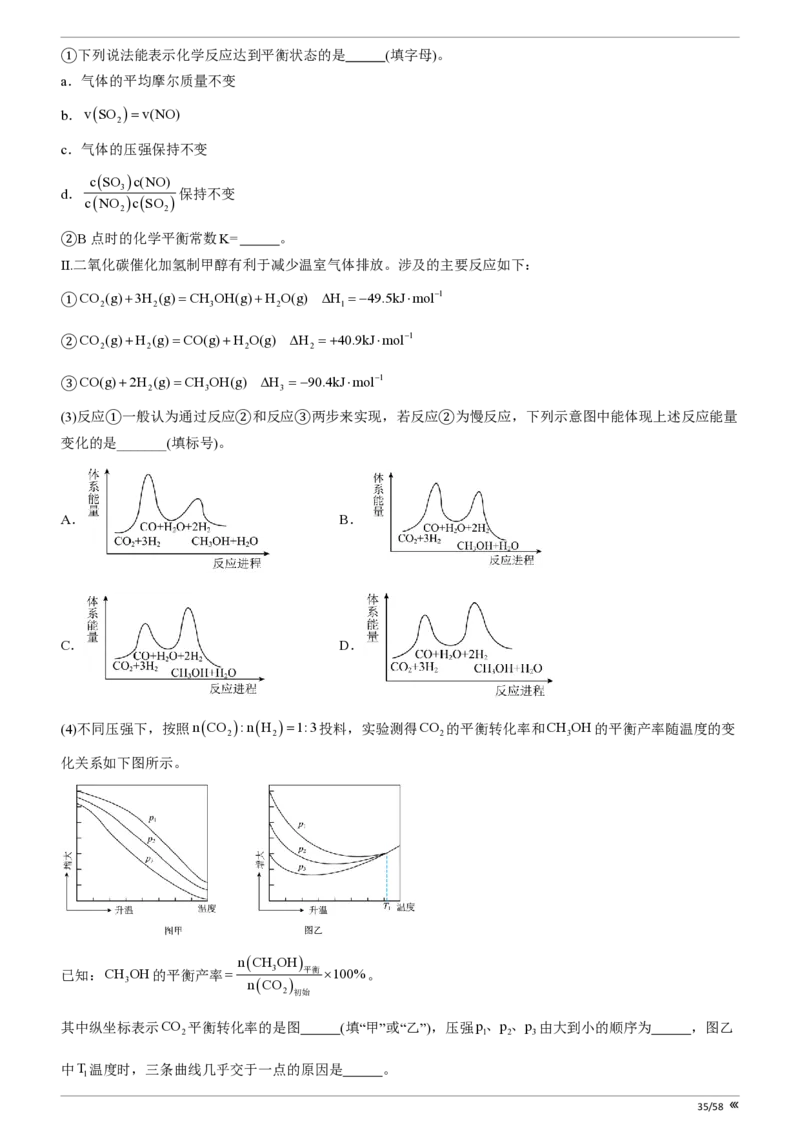
(3)反应①一般认为通过反应②和反应③两步来实现,若反应②为慢反应,下列示意图中能体现上述反应能量
变化的是_______(填标号)。
A. B.
C. D.
(4)不同压强下,按照nCO :nH =1:3投料,实验测得CO 的平衡转化率和CH OH的平衡产率随温度的变
2 2 2 3
化关系如下图所示。
nCH OH
已知:CH OH的平衡产率= 3 平衡 ´100%。
3 nCO
2 初始
其中纵坐标表示CO 平衡转化率的是图 (填“甲”或“乙”),压强p、p、p 由大到小的顺序为 ,图乙
2 1 2 3
中T温度时,三条曲线几乎交于一点的原因是 。
1
35/5836/58