文档内容
化学试卷
注意事项:
1.答卷前,考⽣务必将⾃⼰的姓名、准考证号填写在答题卡上,并将⾃⼰的姓名、准考证号、
座位号填写在本试卷上。
2.回答选择题时,选出每⼩题答案后,⽤2B铅笔把答题卡上对应题⽬的答案标号涂⿊;如需
改动,⽤橡⽪擦⼲净后,再选涂其他答案标号。涂写在本试卷上⽆效。
3.作答⾮选择题时,将答案书写在答题卡上,书写在本试卷上⽆效。
4.考试结束后:将本试卷和答题卡⼀并交回。
可能⽤到的相对原⼦质量:
⼀、选择题:本题共14⼩题,每⼩题3分,共42分。在每⼩题给出的四个选项中,只有⼀
项是符合题⽬要求的。
1.“ 国之重器” 是我国科技综合实⼒的结晶。下述材料属于⾦属材料的是
A.“ C919” ⼤⻜机⽤的氮化硅涂层 B.“ 梦想” 号钻探船钻头⽤的合⾦
C.“ 望宇” 登⽉服⽤的聚酰亚胺隔热层 D.“ 雪⻰2” 号破冰船制淡⽔⽤的反渗透膜
【答案】B
【解析】
【详解】A.氮化硅涂层属于新型陶瓷材料,属于⽆机⾮⾦属材料,A不符合题意;
B.合⾦是⾦属与其他元素熔合⽽成的材料,属于⾦属材料,B符合题意;
C.聚酰亚胺是⾼分⼦有机材料,不属于⾦属材料,C不符合题意;
D.反渗透膜通常由⾼分⼦聚合物制成,属于有机材料,D不符合题意;
故选B。
2. 下列化学⽤语或图示表达正确的是
A. 的电⼦式为 B. 基态 原⼦的价电⼦排布式为
C. 的球棍模型为 D. 反-2-丁烯的结构简式为
【答案】A
【解析】
【详解】A. 与 结构类似,电⼦式为 ,A正确;
第1⻚/共23⻚
学科⽹(北京)股份有限公司B.Be是4号元素,基态 原⼦的价电⼦排布式为 ,B错误;
C.⼄炔的球棍模型为 ,图中表示⼄炔的空间填充模型,C错误;
D.反-2-丁烯的分⼦中,两个甲基位于双键的不同侧,结构简式是 ,D错误;
故选A。
3. 下列有关物质性质与⽤途对应关系错误的是
A. 单晶硅熔点⾼,可⽤于制造芯⽚ B. ⾦属铝具有还原性,可⽤于冶炼⾦属
C. 浓硫酸具有吸⽔性,可⽤作⼲燥剂 D. ⼄炔燃烧⽕焰温度⾼,可⽤于切割⾦属
【答案】A
【解析】
【详解】A.单晶硅⽤于制造芯⽚主要因其半导体性质,⽽⾮熔点⾼,熔点⾼与⽤途⽆直接关联,A错误;
B.⾦属铝还原性强,可通过铝热反应冶炼⾦属(如Fe、Mn等),B正确;
C.浓硫酸吸⽔性使其可⼲燥中性/酸性⽓体(如H 、CO ),C正确;
2 2
D.⼄炔燃烧产⽣⾼温氧炔焰(约3000℃),可熔化⾦属进⾏切割,D正确;
故选A。
4. 抗坏⾎酸葡萄糖苷( )具有抗氧化功能。下列关于 的说法正确的是
A. 不能使溴⽔褪⾊ B. 能与⼄酸发⽣酯化反应
C. 不能与 溶液反应 D. 含有3个⼿性碳原⼦
【答案】B
【解析】
【详解】A.由物质的结构可知,该物质含有碳碳双键,能和溴⽔发⽣加成反应⽽褪⾊,A错误;
B.由物质的结构可知,该物质含有羟基,能和⼄酸在浓硫酸催化下,发⽣酯化反应,B正确;
C.该物质中含有⼀个酯基,能与 溶液反应,C错误;
第2⻚/共23⻚
学科⽹(北京)股份有限公司D.⼿性碳原⼦为连接4个不同基团的碳原⼦,该物质中含有7个⼿性碳, ,
D错误;
故选B。
5.“ 机械键” 是两个或多个分⼦在空间上穿插互锁的⼀种结合形式。我国科研⼈员合成了由两个全苯基⼤
环分⼦组成的具有“ 机械键” 的索烃,结构如图,下列说法错误的是
A. 该索烃属于芳⾹烃 B. 该索烃的相对分⼦质量可⽤质谱仪测定
C. 该索烃的两个⼤环之间不存在范德华⼒ D. 破坏该索烃中的“ 机械键” 需要断裂共价键
【答案】C
【解析】
【详解】A.该物质是由两个全苯基⼤环分⼦组成的具有“机械键”的索烃,含有苯环,属于芳⾹烃,A正确;
B.质谱仪可测定相对分⼦质量,质谱图上最⼤质荷⽐即为相对分⼦质量,B正确;
C.该物质为分⼦晶体,分⼦间存在范德华⼒,C错误;
D.该物质含有共价键,破坏 “机械键”时需要断裂共价键,D正确;
故选C。
6. 下列对物质性质的解释错误的是
选项 物质性质 解释
A 氯化钠熔点⾼于氯化铯 氯化钠离⼦键强于氯化铯
B 碘易溶于四氯化碳 碘和四氯化碳都是⾮极性分⼦
C 草酸氢钠溶液显酸性 草酸氢根离⼦⽔解程度⼤于电离程度
第3⻚/共23⻚
学科⽹(北京)股份有限公司D 离⼦液体导电性良好 离⼦液体中有可移动的阴、阳离⼦
A.A B.B C.C D.D
【答案】C
【解析】
【详解】A.氯化钠中的钠离⼦半径(Na+)⽐氯化铯中的铯离⼦半径(Cs+)⼩,离⼦键强度更⼤,因此熔
点更⾼,解释正确,A正确;
B.碘和四氯化碳均为⾮极性分⼦,符合“ 相似相溶” 原理,解释正确,B正确;
C.草酸氢钠溶液显酸性是因为草酸氢根(HC O )的电离程度(释放H+)⼤于⽔解程度(⽣成OH⁻),
2
解释错误,C错误;
D.离⼦液体的导电性源于其内部可⾃由移动的阴、阳离⼦,解释正确,D正确;
故选C。
7. 下列有关反应⽅程式错误的是
A. 泡沫灭⽕器反应原理:
B. ⽤⾦属钠除去甲苯中的微量⽔:
C. ⽤ 溶液吸收尾⽓中的
D. 氯⽓通⼊冷的⽯灰乳中制漂⽩粉:
【答案】D
【解析】
【详解】A.泡沫灭⽕器中Al3+与HCO 发⽣双⽔解,⽣成Al(OH) 和CO ,⽅程式配平正确,A正确;
3 2
B.⾦属钠优先与⽔反应⽣成NaOH和H ,甲苯不参与反应,⽅程式正确,B正确;
2
C.NO 与NaOH反应⽣成NO 和NO ,⽅程式配平及产物均正确,C正确;
2
D.⽯灰乳(Ca(OH) 悬浊液)不能拆为OH-,正确反应应为2Cl +2Ca(OH) =CaCl +Ca(ClO) +2H O,D
2 2 2 2 2 2
错误;
故选D。
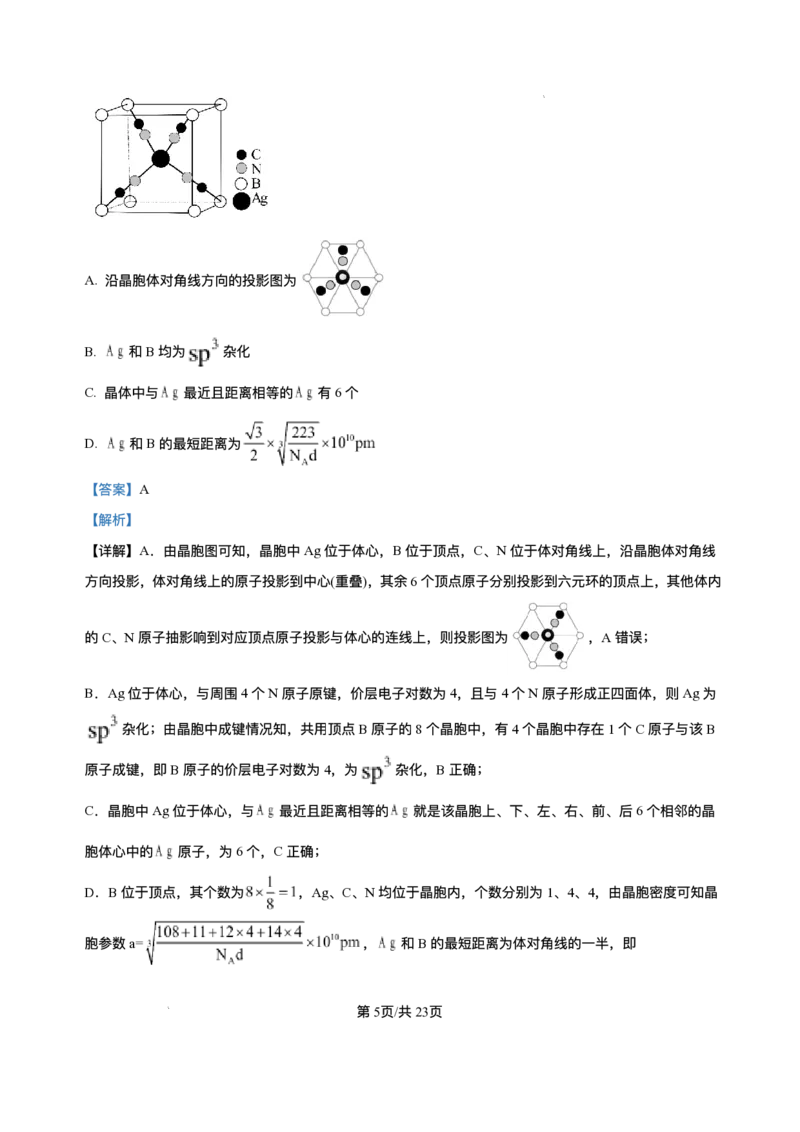
8. ⼀种负热膨胀材料的⽴⽅晶胞结构如图,晶胞密度为 ,阿伏加德罗常数的值为 ,下列说法
错误的是
第4⻚/共23⻚
学科⽹(北京)股份有限公司A. 沿晶胞体对⻆线⽅向的投影图为
B. 和B均为 杂化
C. 晶体中与 最近且距离相等的 有6个
D. 和B的最短距离为
【答案】A
【解析】
【详解】A.由晶胞图可知,晶胞中Ag位于体⼼,B位于顶点,C、N位于体对⻆线上,沿晶胞体对⻆线
⽅向投影,体对⻆线上的原⼦投影到中⼼(重叠),其余6个顶点原⼦分别投影到六元环的顶点上,其他体内
的C、N原⼦抽影响到对应顶点原⼦投影与体⼼的连线上,则投影图为 ,A错误;
B.Ag位于体⼼,与周围4个N原⼦原键,价层电⼦对数为4,且与4个N原⼦形成正四⾯体,则Ag为
杂化;由晶胞中成键情况知,共⽤顶点B原⼦的8个晶胞中,有4个晶胞中存在1个C原⼦与该B
原⼦成键,即B原⼦的价层电⼦对数为4,为 杂化,B正确;
C.晶胞中Ag位于体⼼,与 最近且距离相等的 就是该晶胞上、下、左、右、前、后6个相邻的晶
胞体⼼中的 原⼦,为6个,C正确;
D.B位于顶点,其个数为 ,Ag、C、N均位于晶胞内,个数分别为1、4、4,由晶胞密度可知晶
胞参数a= , 和B的最短距离为体对⻆线的⼀半,即
第5⻚/共23⻚
学科⽹(北京)股份有限公司,D正确;
故选A。
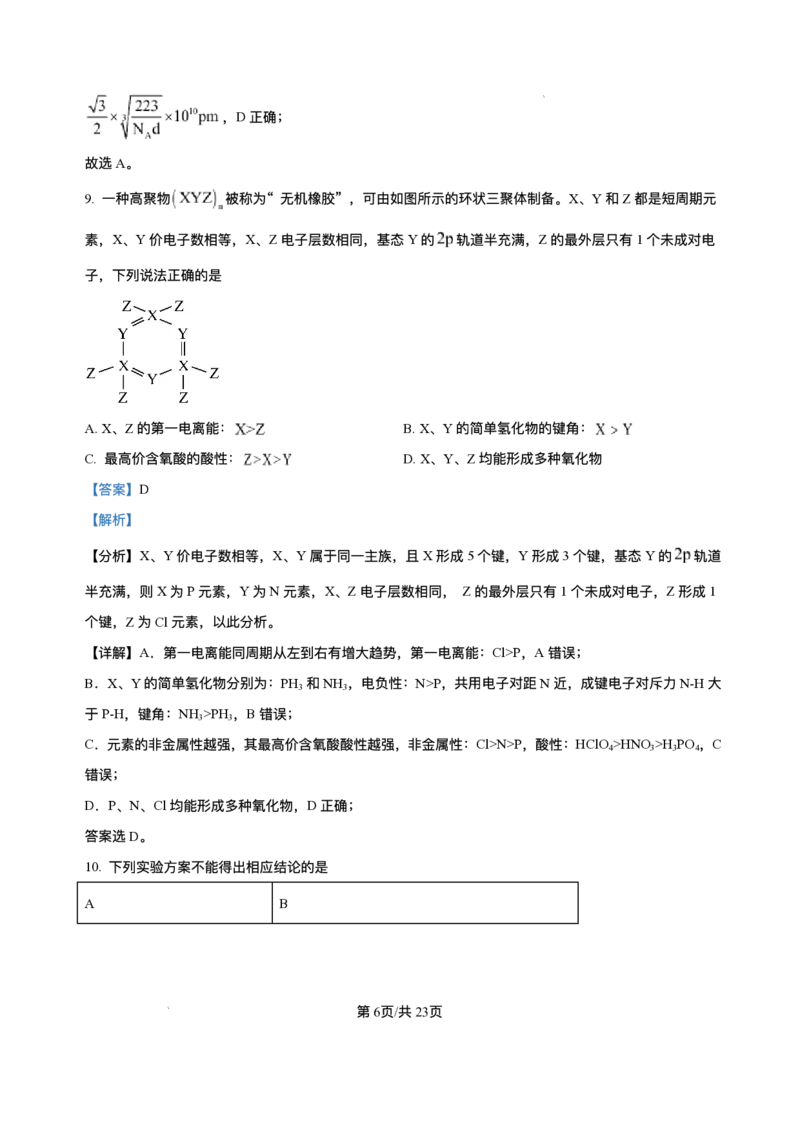
9. ⼀种⾼聚物 被称为“ ⽆机橡胶” ,可由如图所示的环状三聚体制备。X、Y和Z都是短周期元
素,X、Y价电⼦数相等,X、Z电⼦层数相同,基态Y的 轨道半充满,Z的最外层只有1个未成对电
⼦,下列说法正确的是
A.X、Z的第⼀电离能: B.X、Y的简单氢化物的键⻆:
C. 最⾼价含氧酸的酸性: D.X、Y、Z均能形成多种氧化物
【答案】D
【解析】
【分析】X、Y价电⼦数相等,X、Y属于同⼀主族,且X形成5个键,Y形成3个键,基态Y的 轨道
半充满,则X为P元素,Y为N元素,X、Z电⼦层数相同, Z的最外层只有1个未成对电⼦,Z形成1
个键,Z为Cl元素,以此分析。
【详解】A.第⼀电离能同周期从左到右有增⼤趋势,第⼀电离能:Cl>P,A错误;
B.X、Y的简单氢化物分别为:PH 和NH ,电负性:N>P,共⽤电⼦对距N近,成键电⼦对斥⼒N-H⼤
3 3
于P-H,键⻆:NH >PH ,B错误;
3 3
C.元素的⾮⾦属性越强,其最⾼价含氧酸酸性越强,⾮⾦属性:Cl>N>P,酸性:HClO >HNO >H PO ,C
4 3 3 4
错误;
D.P、N、Cl均能形成多种氧化物,D正确;
答案选D。
10. 下列实验⽅案不能得出相应结论的是
A B
第6⻚/共23⻚
学科⽹(北京)股份有限公司结论:⾦属活动性顺序为
结论:氧化性顺序为
C D
结论:甲基使苯环活化 结论:增⼤反应物浓度,该反应速率加快
A.A B.B C.C D.D
【答案】C
【解析】
【详解】A.Fe、Cu、稀硫酸原电池中,电⼦由活泼⾦属Fe流向Cu,Fe、Zn、硫酸原电池中,电⼦有Zn
流向Fe,活泼性:Zn>Fe>Cu,A正确;
B.FeCl 与淀粉KI溶液反应,溶液变蓝⾊,则氧化性:Fe3+>I ,新制氯⽔加⼊含KSCN的FeCl 溶液中,
3 2 2
溶液变红⾊,⽣成了Fe3+,则氧化性:Cl >Fe3+,故氧化性: ,B正确;
2
C.酸性⾼锰酸钾分别滴⼊苯和甲苯中,甲苯能使酸性⾼锰酸钾溶液褪⾊,说明了苯环使甲基活化,C错误;
D.不同浓度的Na S O 与相同浓度的稀硫酸反应,浓度⼤的Na S O 先出现浑浊,说明增⼤反应物浓度,
2 2 3 2 2 3
反应速率加快,D正确;
答案选C
11. 某元素的单质及其化合物的转化关系如图。常温常压下G、J均为⽆⾊⽓体,J具有漂⽩性。阿伏加德
第7⻚/共23⻚
学科⽹(北京)股份有限公司罗常数的值为 。下列说法错误的是
A.G、K均能与 溶液反应 B.H、N既具有氧化性也具有还原性
C.M和N溶液中的离⼦种类相同 D. 与⾜量的J反应,转移电⼦数为
【答案】D
【解析】
【分析】根据转化关系: ,常温常压下G、J均为⽆⾊
⽓体,J具有漂⽩性,J为SO ,K为SO ,G为H S,H为S,M为NaHSO ,N为Na SO ,L为Na SO 。
2 3 2 3 2 3 2 4
【详解】A.H S和SO 均能与NaOH溶液反应,A正确;
2 3
B.S和Na SO 中S的化合价处于S的中间价态,既具有氧化性⼜有还原性,B正确;
2 3
C.M为NaHSO ,N为Na SO ,⼆者的溶液中离⼦种类相同,C正确;
3 2 3
D.1molH S和⾜量的SO 反应⽣成S单质和⽔,2H S+SO =3S↓+2H O,1molH S参加反应,转移2mol
2 2 2 2 2 2
电⼦,转移2N 个电⼦,D错误;
A
答案选D
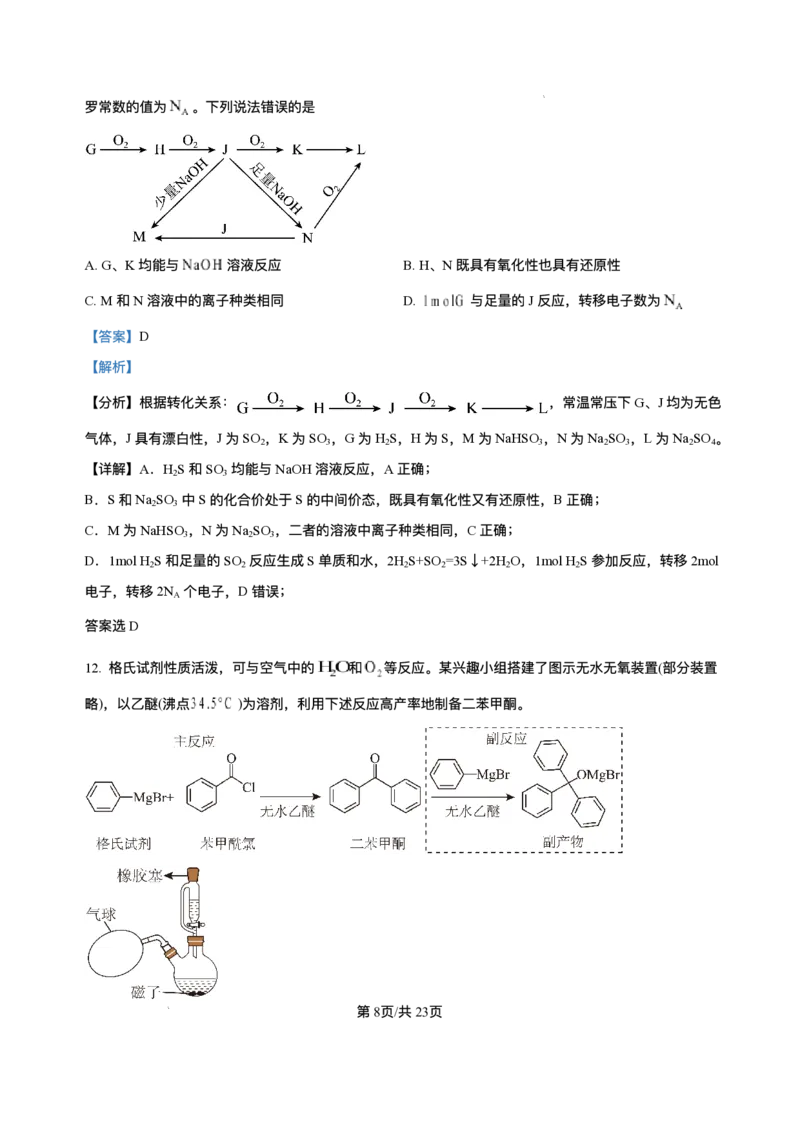
12. 格⽒试剂性质活泼,可与空⽓中的 和 等反应。某兴趣⼩组搭建了图示⽆⽔⽆氧装置(部分装置
略),以⼄醚(沸点 )为溶剂,利⽤下述反应⾼产率地制备⼆苯甲酮。
第8⻚/共23⻚
学科⽹(北京)股份有限公司下列说法错误的是
A. ⽓球中填充保护⽓,并起缓冲压⼒的作⽤
B. 烧瓶中液体是格⽒试剂的⼄醚溶液
C. 图中的漏⽃不能⽤球形分液漏⽃代替
D. 产率⾼表明苯甲酰氯⽐⼆苯甲酮更易与格⽒试剂反应
【答案】B
【解析】
【详解】A.当⽓球被充⼊⽓体时,⽓体在⽓球内产⽣了⼀定的压⼒,这将均匀地作⽤在⽓球内外的表⾯上,
使得外壳可以均匀分担⽓体的压⼒,故A正确;
B.格⽒试剂性质活泼,为避免反应过于剧烈,烧瓶中应加⼊苯甲酰氯,格⽒试剂通过滴液漏⽃缓慢滴加,
故B错误;
C.反应体系为⽆⽔、⽆氧的密封装置,需要⽤图中的漏⽃保持体系能压强不变,保证液体顺利滴下,⽽不
能⽤分液漏⽃,故C正确;
D.苯甲酰氯⽐⼆苯甲酮与格⽒试剂反应速率快,导致苯甲酰氯与与格⽒试剂产率⾼,故D正确;
故答案为C。
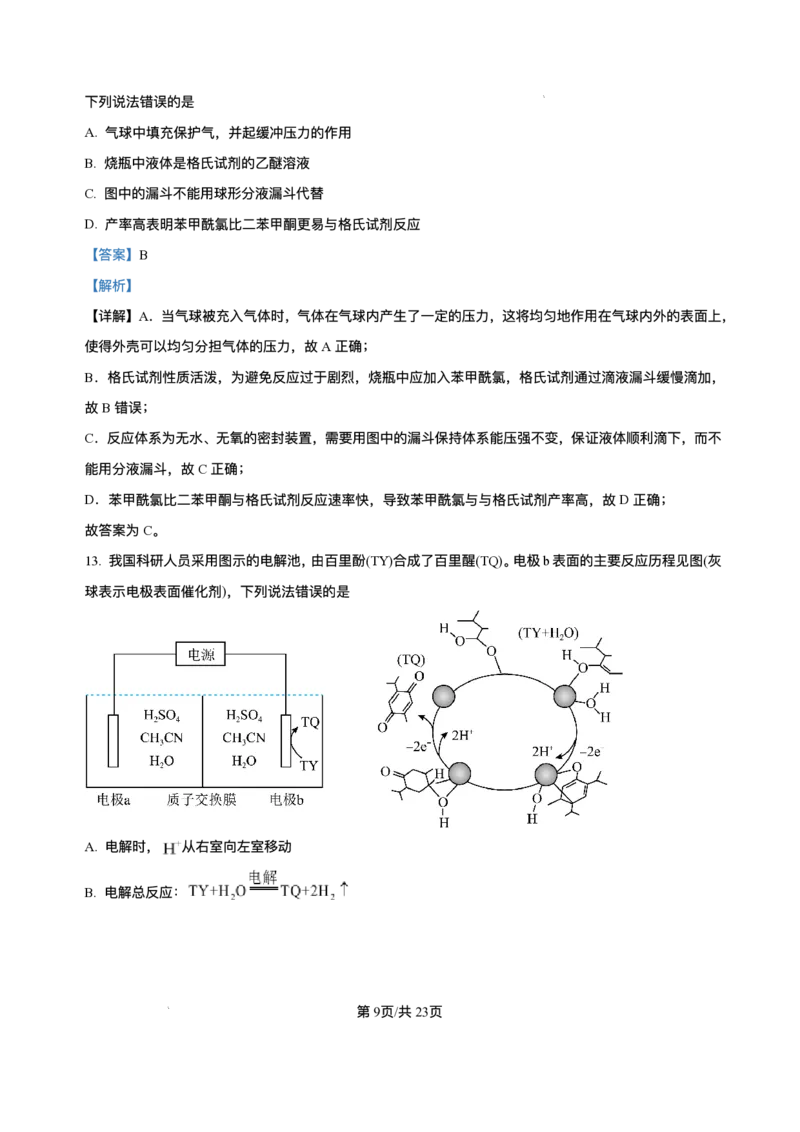
13. 我国科研⼈员采⽤图示的电解池,由百⾥酚(TY)合成了百⾥醒(TQ)。电极b表⾯的主要反应历程⻅图(灰
球表示电极表⾯催化剂),下列说法错误的是
A. 电解时, 从右室向左室移动
B. 电解总反应:
第9⻚/共23⻚
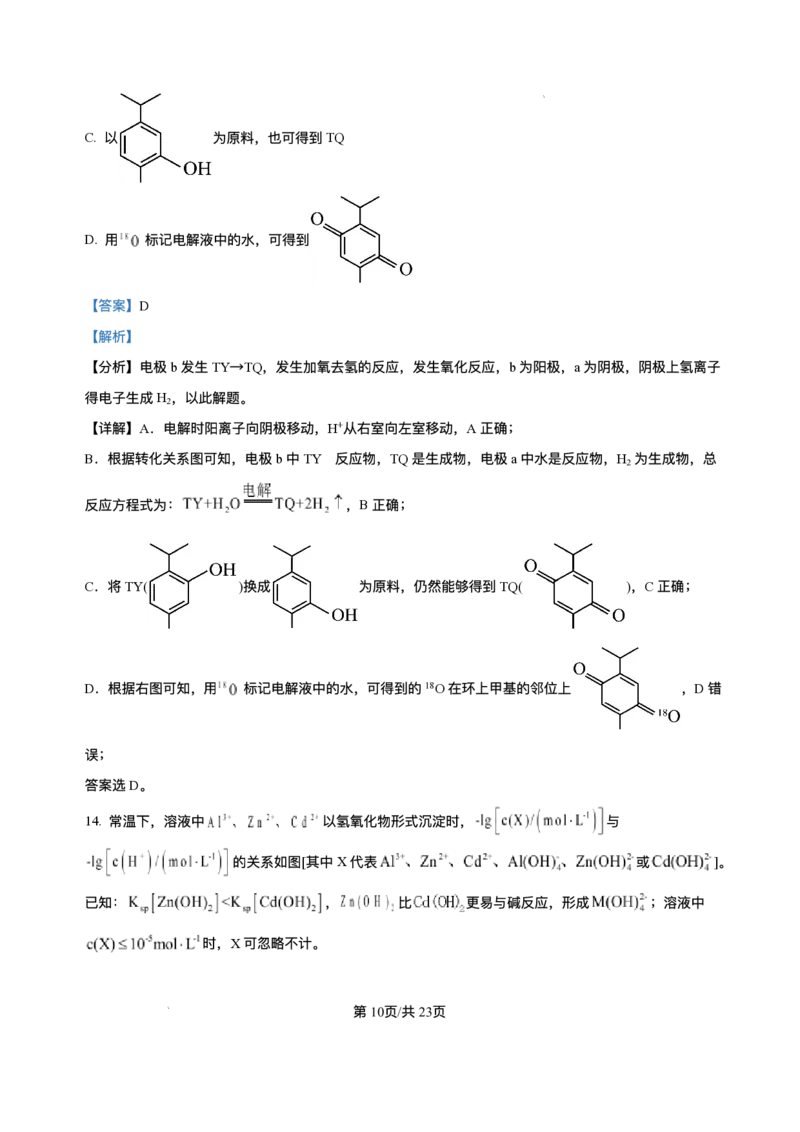
学科⽹(北京)股份有限公司C. 以 为原料,也可得到TQ
D. ⽤ 标记电解液中的⽔,可得到
【答案】D
【解析】
【分析】电极b发⽣TY→TQ,发⽣加氧去氢的反应,发⽣氧化反应,b为阳极,a为阴极,阴极上氢离⼦
得电⼦⽣成H ,以此解题。
2
【详解】A.电解时阳离⼦向阴极移动,H+从右室向左室移动,A正确;
B.根据转化关系图可知,电极b中TY 反应物,TQ是⽣成物,电极a中⽔是反应物,H 为⽣成物,总
2
反应⽅程式为: ,B正确;
C.将TY( )换成 为原料,仍然能够得到TQ( ),C正确;
D.根据右图可知,⽤ 标记电解液中的⽔,可得到的18O在环上甲基的邻位上 ,D错
误;
答案选D。
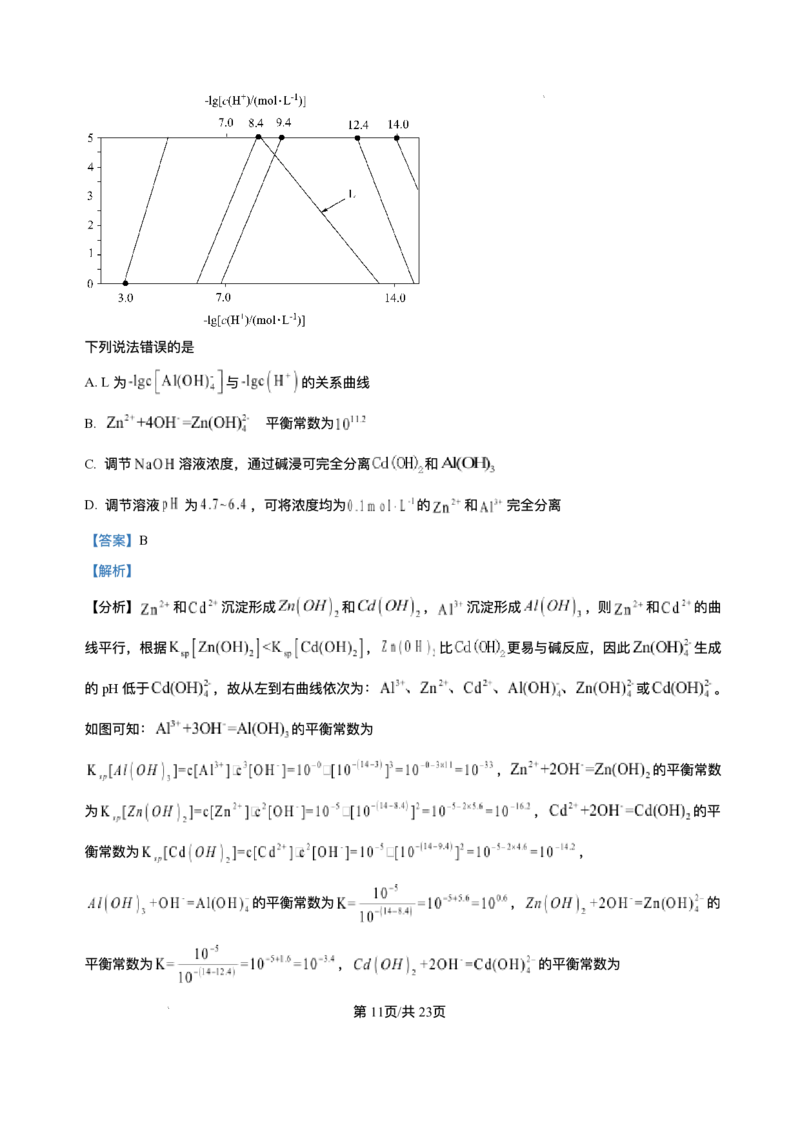
14. 常温下,溶液中 以氢氧化物形式沉淀时, 与
的关系如图[其中X代表 或 ]。
已知: , ⽐ 更易与碱反应,形成 ;溶液中
时,X可忽略不计。
第10⻚/共23⻚
学科⽹(北京)股份有限公司下列说法错误的是
A.L为 与 的关系曲线
B. 平衡常数为
C. 调节 溶液浓度,通过碱浸可完全分离 和
D. 调节溶液 为 ,可将浓度均为 的 和 完全分离
【答案】B
【解析】
【分析】 和 沉淀形成 和 , 沉淀形成 ,则 和 的曲
线平⾏,根据 , ⽐ 更易与碱反应,因此 ⽣成
的pH低于 ,故从左到右曲线依次为: 或 。
如图可知: 的平衡常数为
, 的平衡常数
为 , 的平
衡常数为 ,
的平衡常数为 , 的
平衡常数为 , 的平衡常数为
第11⻚/共23⻚
学科⽹(北京)股份有限公司。据此分析:
【详解】A.据分析,L为 与 的关系曲线,故A正确;
B.如图可知, 的平衡常数为
,则 的平
衡常数为 ,
故B错误;
C.如图可知,pH=14时 开始溶解,pH=8.4时 开始溶解,且pH=14时
,即可认为 完全溶解,并转化为 ,因此调节 溶液浓度,
通过碱浸可完全分离 和 ,故C正确;
D. 的 开始沉淀pH为 , 的 完全沉淀pH为
,因此调节溶液 为 ,可将浓度均为 的 和 完全分离,
故D正确;
故答案为B。
⼆、⾮选择题:本题共4⼩题,共58分。
15. 某实验室制备糖精钴 ,并测定其结晶⽔含量。
已知: 表示糖精根离⼦,其摩尔质量为 ,糖精钴的溶解度在热⽔中较⼤,在冷⽔中较⼩;
丙酮沸点为 ,与⽔互溶。
(⼀)制备
I.称取 ,加⼊ 蒸馏⽔,搅拌溶解,得溶液1。
Ⅱ.称取 (稍过量)糖精钠( ),加⼊ 蒸馏⽔,加热搅拌,得溶液2。
第12⻚/共23⻚
学科⽹(北京)股份有限公司Ⅲ.将溶液2加⼊到接近沸腾的溶液1中,反应3分钟后停⽌加热,静置,冷却结晶。
Ⅳ.过滤,依次⽤三种不同试剂洗涤晶体,晾⼲得产品。
回答下列问题:
(1)I和Ⅱ中除烧杯外,还需⽤到的玻璃仪器有_______、_______(写出两种)
(2)Ⅲ中静置过程有少量晶体出现时,可将烧杯置于_______中,以使⼤量晶体析出。
(3)Ⅳ中⽤①丙酮、②冷⽔、③冷的 溶液洗涤晶体,正确顺序为_______。
A.①③② B.③②① C.②①③
(4)Ⅳ中为了确认氯离⼦⼰经洗净,取⽔洗时的最后⼀次滤液于试管中,_______(将实验操作、现象和结
论补充完整)。
(5)与本实验安全注意事项有关的图标有_______。
(⼆)结晶⽔含量测定
和 形成 配合物。准确称取 糖精钴产品于锥形瓶中,加蒸馏⽔,加热溶解,再加⼊缓冲
溶液和指示剂,在50~60℃下,⽤ 的 标准溶液滴定。
(6)下列操作的正确顺序为_______(⽤字⺟排序)。
a.⽤标准溶液润洗滴定管 b.加⼊标准溶液⾄“ 0” 刻度以上 处
c.检查滴定管是否漏⽔并清洗 d.赶出⽓泡,调节液⾯,准确记录读数
(7)滴定终点时消耗标准溶液 ,则产品 中x的测定值为_______(⽤含m、
c、V的代数式表示);若滴定前滴定管尖嘴处⽆⽓泡,滴定后有⽓泡,会导致x的测定值_______(填“ 偏⾼”
“ 偏低” 或“ ⽆影响” )。
【答案】(1) ①. 玻璃棒 ②. 量筒(或胶头滴管等,合理即可) (2)冰⽔浴 (3)B
(4)加稀硝酸酸化,再滴加AgNO 溶液,⽆⽩⾊沉淀⽣成,说明Cl-已洗净 (5)ABC (6)cabd
3
(7) ①. (或: ) ②. 偏⾼
第13⻚/共23⻚
学科⽹(北京)股份有限公司【解析】
【分析】按照反应 制备糖
精钴,然后在冰⽔浴中结晶,再按照“冷的1%NaSac溶液、冷⽔、丙酮”顺序进⾏洗涤,得到糖精钴晶体,
最后将糖精钴晶体溶解后⽤EDTA标准溶液滴定测定含有结晶⽔的数量。
【⼩问1详解】
步骤I、Ⅱ中需要使⽤量筒、胶头滴管量取蒸馏⽔,并⽤玻璃棒搅拌以加快固体溶解速率。
【⼩问2详解】
因为糖精钴在冷⽔中溶解度较⼩,所以为了尽快让⼤量晶体析出,应降低溶液温度,可将烧杯置于冰⽔浴
中。
【⼩问3详解】
先⽤冷的1%NaSac溶液洗涤,可降低糖精钴溶解度,减少晶体损失,还能将晶体表⾯吸附的Co2+转化为晶
体析出,且不引⼈新的杂质,再⽤冷⽔洗涤,可降低晶体溶解度并洗去溶液中存在的可溶性离⼦,丙酮可
以与⽔互溶且沸点⽐关键⽔的低,故最后⽤丙酮洗涤以除去残留的⽔且能使晶体快速⼲燥,故答案为B。
【⼩问4详解】
Ⅳ中为了确认氯离⼦⼰经洗净的步骤为:取⽔洗时的最后⼀次滤液于试管中,加稀硝酸酸化,再滴加AgNO
3
溶液,⽆⽩⾊沉淀⽣成,说明Cl-已洗净。
【⼩问5详解】
进⾏化学实验需要佩戴护⽬镜,以保护眼睛,同时化学实验结束后,离开实验室前需⽤肥皂等清洗双⼿,
该实验涉及加热操作,因此需要防⽌热烫,要选择合适的⼯具进⾏操作,避免直接触碰,故A、B、C符合
题意;该实验中未涉及锐器的操作,D不符合题意,故答案为ABC。
【⼩问6详解】
使⽤滴定管前⾸先要检漏,确定不漏液之后⽤蒸馏⽔清洗(c),再⽤待装的标准溶液进⾏润洗(a),待润洗完
成后 装⼊标准溶液⾄“0”刻度以上2~3mL处(b),放液赶出⽓泡后调节液⾯⾄“0”刻度或“0”刻度下,准确记
录标准溶液体积的初始读数(d),故答案为cabd。
【⼩问7详解】
滴定消耗的 ,EDTA与Co2+形成1:1配合物,则样品溶解后的
,即样品中的 ,⽽
,所以 ,解
第14⻚/共23⻚
学科⽹(北京)股份有限公司得 ;若滴定前滴定管尖嘴
处⽆⽓泡,滴定后有⽓泡,测得消耗EDTA溶液体积偏⼩,即V偏⼩,根据 ,则x偏⾼。
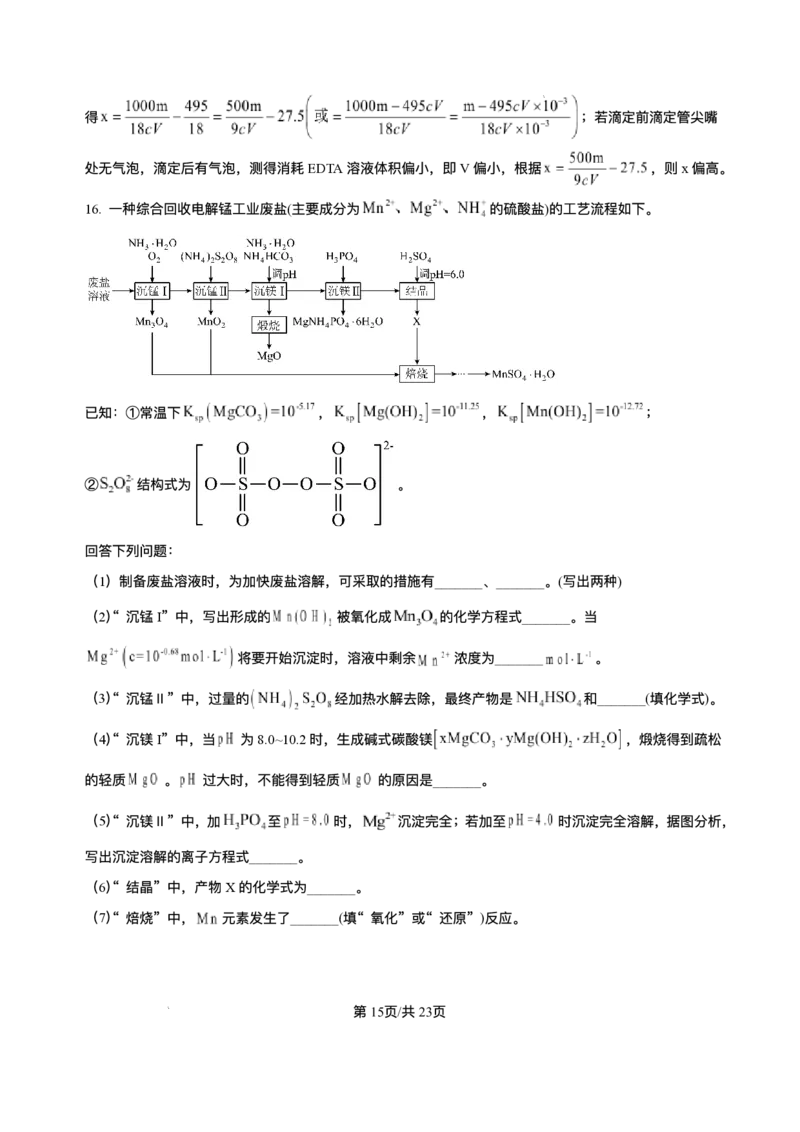
16. ⼀种综合回收电解锰⼯业废盐(主要成分为 的硫酸盐)的⼯艺流程如下。
已知:①常温下 , , ;
② 结构式为 。
回答下列问题:
(1)制备废盐溶液时,为加快废盐溶解,可采取的措施有_______、_______。(写出两种)
(2)“ 沉锰I” 中,写出形成的 被氧化成 的化学⽅程式_______。当
将要开始沉淀时,溶液中剩余 浓度为_______ 。
(3)“ 沉锰Ⅱ” 中,过量的 经加热⽔解去除,最终产物是 和_______(填化学式)。
(4)“ 沉镁I” 中,当 为8.0~10.2时,⽣成碱式碳酸镁 ,煅烧得到疏松
的轻质 。 过⼤时,不能得到轻质 的原因是_______。
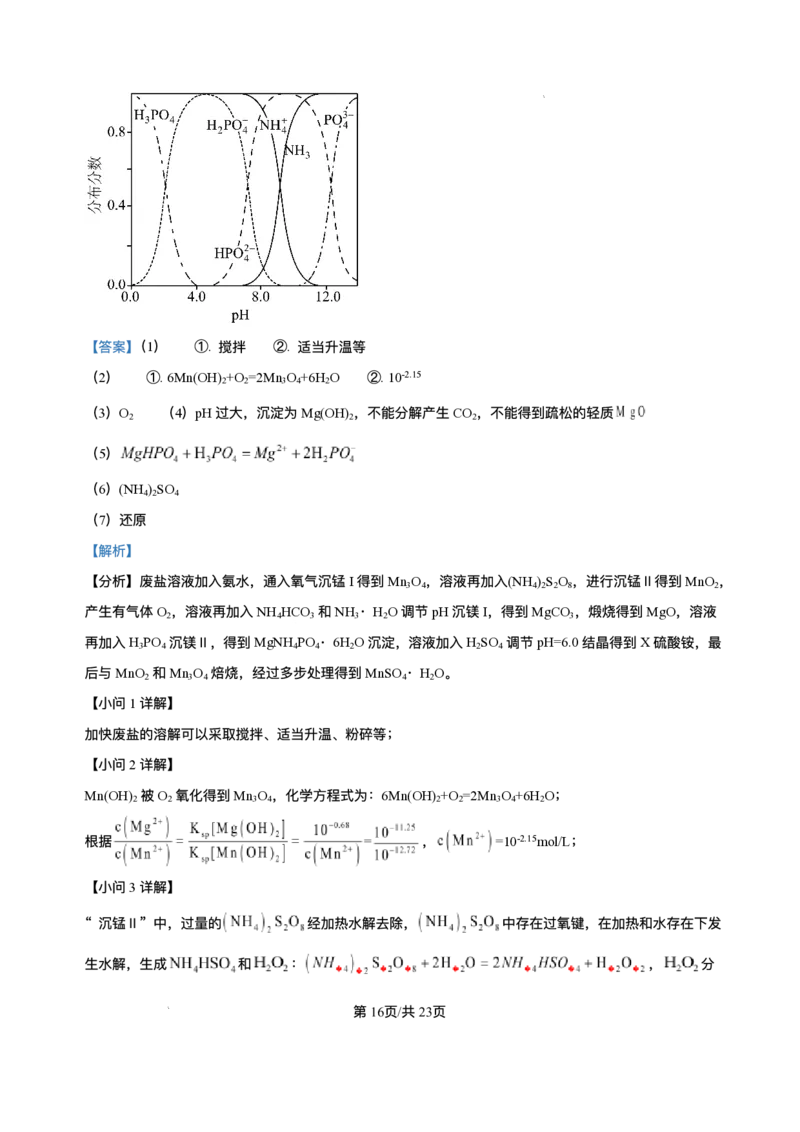
(5)“ 沉镁Ⅱ” 中,加 ⾄ 时, 沉淀完全;若加⾄ 时沉淀完全溶解,据图分析,
写出沉淀溶解的离⼦⽅程式_______。
(6)“ 结晶” 中,产物X的化学式为_______。
(7)“ 焙烧” 中, 元素发⽣了_______(填“ 氧化” 或“ 还原” )反应。
第15⻚/共23⻚
学科⽹(北京)股份有限公司【答案】(1) ①. 搅拌 ②. 适当升温等
(2) ①.6Mn(OH) +O =2Mn O +6H O ②.10-2.15
2 2 3 4 2
(3)O (4)pH过⼤,沉淀为Mg(OH) ,不能分解产⽣CO ,不能得到疏松的轻质
2 2 2
(5)
(6)(NH ) SO
4 2 4
(7)还原
【解析】
【分析】废盐溶液加⼊氨⽔,通⼊氧⽓沉锰I得到Mn O ,溶液再加⼊(NH ) S O ,进⾏沉锰Ⅱ得到MnO ,
3 4 4 2 2 8 2
产⽣有⽓体O ,溶液再加⼊NH HCO 和NH · H O调节pH沉镁I,得到MgCO ,煅烧得到MgO,溶液
2 4 3 3 2 3
再加⼊H PO 沉镁Ⅱ,得到MgNH PO · 6H O沉淀,溶液加⼊H SO 调节pH=6.0结晶得到X硫酸铵,最
3 4 4 4 2 2 4
后与MnO 和Mn O 焙烧,经过多步处理得到MnSO · H O。
2 3 4 4 2
【⼩问1详解】
加快废盐的溶解可以采取搅拌、适当升温、粉碎等;
【⼩问2详解】
Mn(OH) 被O 氧化得到Mn O ,化学⽅程式为:6Mn(OH) +O =2Mn O +6H O;
2 2 3 4 2 2 3 4 2
根据 = , =10-2.15mol/L;
【⼩问3详解】
“ 沉锰Ⅱ” 中,过量的 经加热⽔解去除, 中存在过氧键,在加热和⽔存在下发
⽣⽔解,⽣成 和 : , 分
第16⻚/共23⻚
学科⽹(北京)股份有限公司解 ,总反应为 ,最终产物是
和O ;
2
【⼩问4详解】
煅烧有CO ⽣成,可以得到疏松的轻质氧化镁,pH过⼤,沉淀为Mg
2
(OH) ,不能分解产⽣CO ,不能得到疏松的轻质 ;
2 2
【⼩问5详解】
由图可知,pH=8时,阴离⼦为 ,阳离⼦为 ,产⽣的沉淀为 ,调节到pH=4,磷元
素存在形式为 ,磷酸不是强酸,不能拆,离⼦⽅程式为: ;
【⼩问6详解】
溶液中存在铵根离⼦和硫酸根离⼦,结晶后X为(NH ) SO ;
4 2 4
【⼩问7详解】
“ 焙烧” 中,Mn O 和MnO 最终⽣成MnSO · H O, 元素化合价降低,发⽣了还原反应。
3 4 2 4 2
17. / 循环在 捕获及转化等⽅⾯具有重要应⽤。科研⼈员设计了利⽤ 与 反应
⽣成 的路线,主要反应如下:
I.
II.
III.
回答下列问题,
(1)计算 _______ 。
(2)提⾼ 平衡产率的条件是_______。
A. ⾼温⾼压 B. 低温⾼压 C. ⾼温低压 D. 低温低压
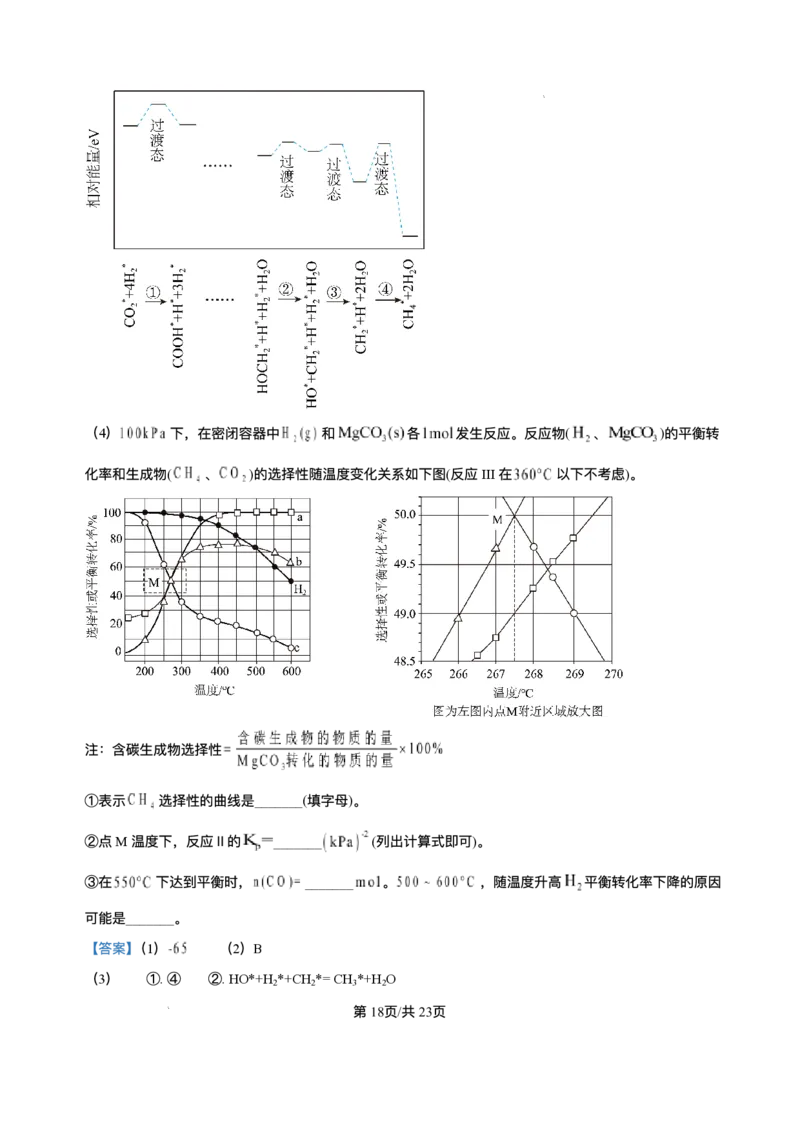
(3)⾼温下 分解产⽣的 催化 与 反应⽣成 ,部分历程如图,其中吸附在催化剂
表⾯的物种⽤*标注,所示步骤中最慢的基元反应是_______(填序号),⽣成⽔的基元反应⽅程式为_______。
第17⻚/共23⻚
学科⽹(北京)股份有限公司(4) 下,在密闭容器中 和 各 发⽣反应。反应物( 、 )的平衡转
化率和⽣成物( 、 )的选择性随温度变化关系如下图(反应III在 以下不考虑)。
注:含碳⽣成物选择性
①表示 选择性的曲线是_______(填字⺟)。
②点M温度下,反应Ⅱ的 _______ (列出计算式即可)。
③在 下达到平衡时, _______ 。 ,随温度升⾼ 平衡转化率下降的原因
可能是_______。
【答案】(1) (2)B
(3) ①.④ ②.HO*+H *+CH *=CH *+H O
2 2 3 2
第18⻚/共23⻚
学科⽹(北京)股份有限公司(4) ①.c ②. ③.0.2 ④. 反应Ⅱ⽣成的氢⽓多于反应Ⅲ消耗的氢⽓
【解析】
【⼩问1详解】
已知:
I.
Ⅱ.
将I+Ⅱ可得 =
,故答案为: ;
【⼩问2详解】
已知反应Ⅱ. 为放热反应,要提⾼ 平衡产
率,要使平衡正向移动。
A.⾼温会使平衡逆向移动,不利于提⾼ 平衡产率,A错误;
B.低温使平衡正向移动,⾼压也使平衡正向移动,可提⾼ 平衡产率,B正确;
C.⾼温会使平衡逆向移动,低压会使平衡逆向移动,不利于提⾼ 平衡产率,C错误;
D.低压会使平衡逆向移动,不利于提⾼ 平衡产率,D错误;
故选B。
【⼩问3详解】
反应活化能越⾼,反应速率越慢,从图中可以看出,第四部活化能最⾼,速率最慢,基元反应为CH
3
*+H*+2H O=CH *+2H O;由图可知,在第三步时⽣成了⽔,基元反应为:HO*+H *+CH *=CH *+H O,
2 4 2 2 2 3 2
故答案为:④;HO*+H *+CH *=CH *+H O;
2 2 3 2
【⼩问4详解】
已知反应I为吸热反应, Ⅱ为放热反应,III为吸热反应,根据图像,温度逐渐升⾼,则碳酸镁的转化率逐
渐升⾼,氢⽓的转化率下降,在 以下不考虑反应Ⅲ,则⼆氧化碳的选择性上升,甲烷的选择性下降,
所以a表示碳酸镁的转化率,b表示⼆氧化碳的选择性,c表示甲烷的选择性。
①表示 选择性的曲线是c,故答案为:c;
第19⻚/共23⻚
学科⽹(北京)股份有限公司②点M温度下,从图中看出碳酸镁的转化率为49%,则剩余的碳酸镁为0.51mol,根据碳原⼦守恒,甲烷和
⼆氧化碳中碳原⼦的物质的量之和为0.49mol,⼜因为此时⼆氧化碳的选择性和甲烷的选择性相等,则⼆氧
化碳和甲烷的物质的量为0.245mol,根据氧原⼦守恒得出⽔的物质的量为0.49mol,根据氢原⼦守恒得出 氢
⽓的物质的量为0.02mol,总的物质的量为0.02+0.245+0.245+0.49=1mol, ,
, ,则反应Ⅱ的
,故答案为: ;
③在 下达到平衡时,碳酸镁完全转化,⼆氧化碳的选择性为70%,甲烷的选择性为10%,则⽣成的⼆
氧化碳为0.7mol,⽣成的甲烷为0.1mol,根据碳原⼦守恒得出 1-0.7-0.1mol=0.2mol;因为反应Ⅱ
是放热的,反应Ⅲ是吸热的。在 ,随温度升⾼,反应Ⅱ逆向移动,反应Ⅲ正向移动,由于反
应Ⅱ⽣成的氢⽓多于反应Ⅲ消耗的氢⽓,导致 平衡转化率下降,故答案为:0.2;反应Ⅱ⽣成的氢⽓多于
反应Ⅲ消耗的氢⽓。
18. 我国某公司研发的治疗消化系统疾病的新药凯普拉⽣(化合物H),合成路线如下(部分试剂、反应条件省
略)。
已知:
回答下列问题:
(1)A中官能团的名称是_______。
(2)B的结构简式为_______。
(3)由C转变为D的反应类型是_______
第20⻚/共23⻚
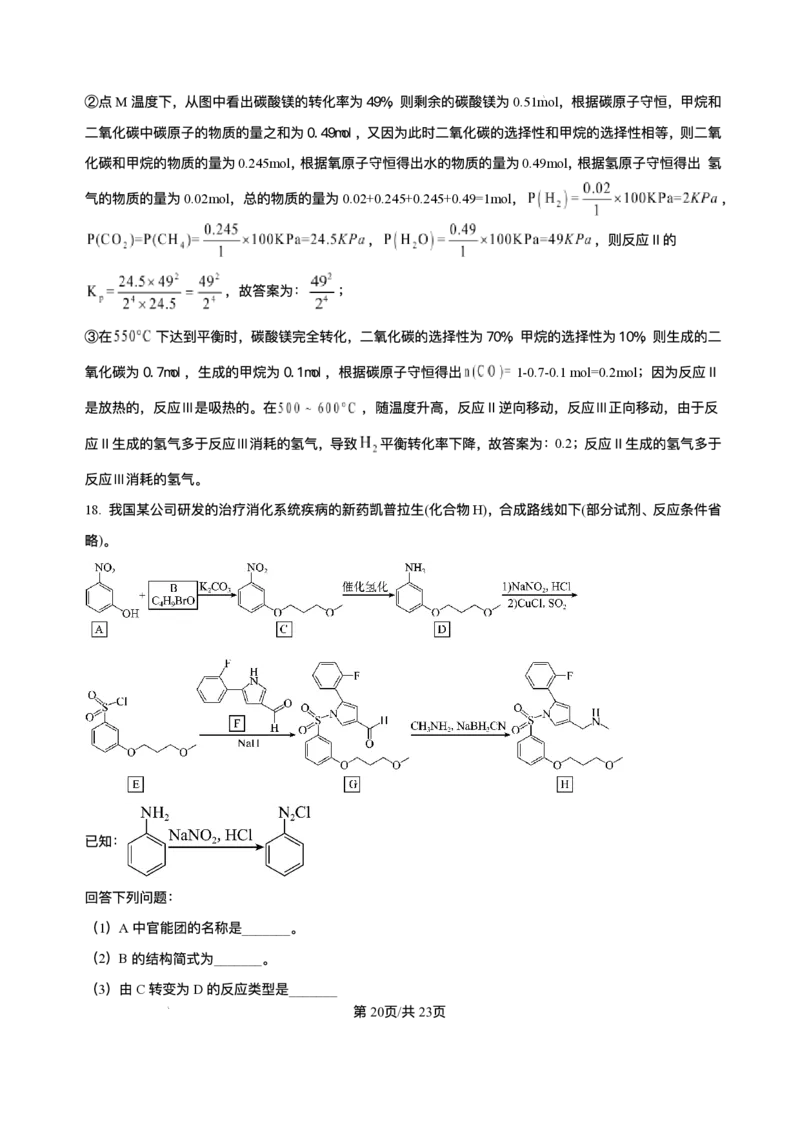
学科⽹(北京)股份有限公司(4)同时满⾜下列条件的B的同分异构体有_______种(不考虑⽴体异构)。
①含有两个甲基;②与钠反应产⽣氢⽓。
(5)由D转变为E的过程中经历了两步反应,第⼀步反应的化学⽅程式是:_______(要求配平)。
(6)下列关于F说法正确的有_______。
A.F能发⽣银镜反应
B.F不可能存在分⼦内氢键
C. 以上路线中E+F→G 的反应产⽣了氢⽓
D. 已知醛基吸引电⼦能⼒较强,与 相⽐F的N-H键极性更⼩
(7)结合合成H的相关信息,以 、 和含⼀个碳原⼦的有机物(⽆机试剂任选)
为原料,设计化合物 的合成路线_______。
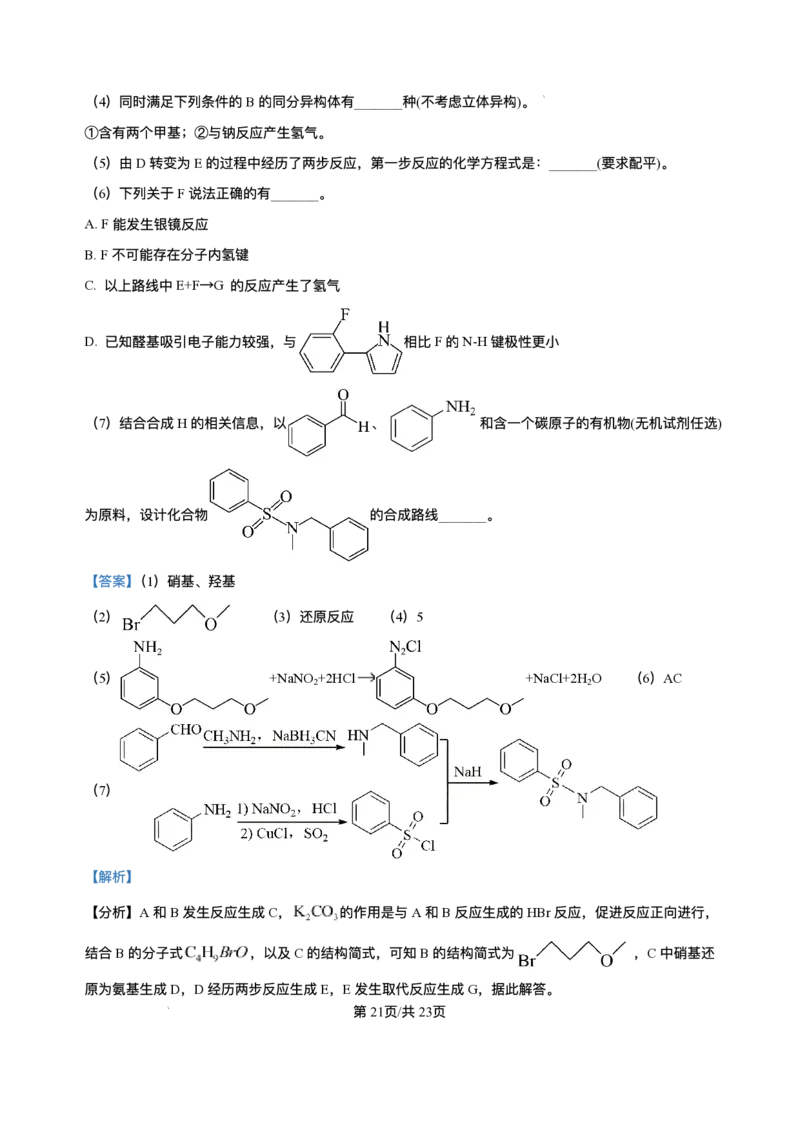
【答案】(1)硝基、羟基
(2) (3)还原反应 (4)5
(5) +NaNO +2HCl +NaCl+2H O (6)AC
2 2
(7)
【解析】
【分析】A和B发⽣反应⽣成C, 的作⽤是与A和B反应⽣成的HBr反应,促进反应正向进⾏,
结合B的分⼦式 ,以及C的结构简式,可知B的结构简式为 ,C中硝基还
原为氨基⽣成D,D经历两步反应⽣成E,E发⽣取代反应⽣成G,据此解答。
第21⻚/共23⻚
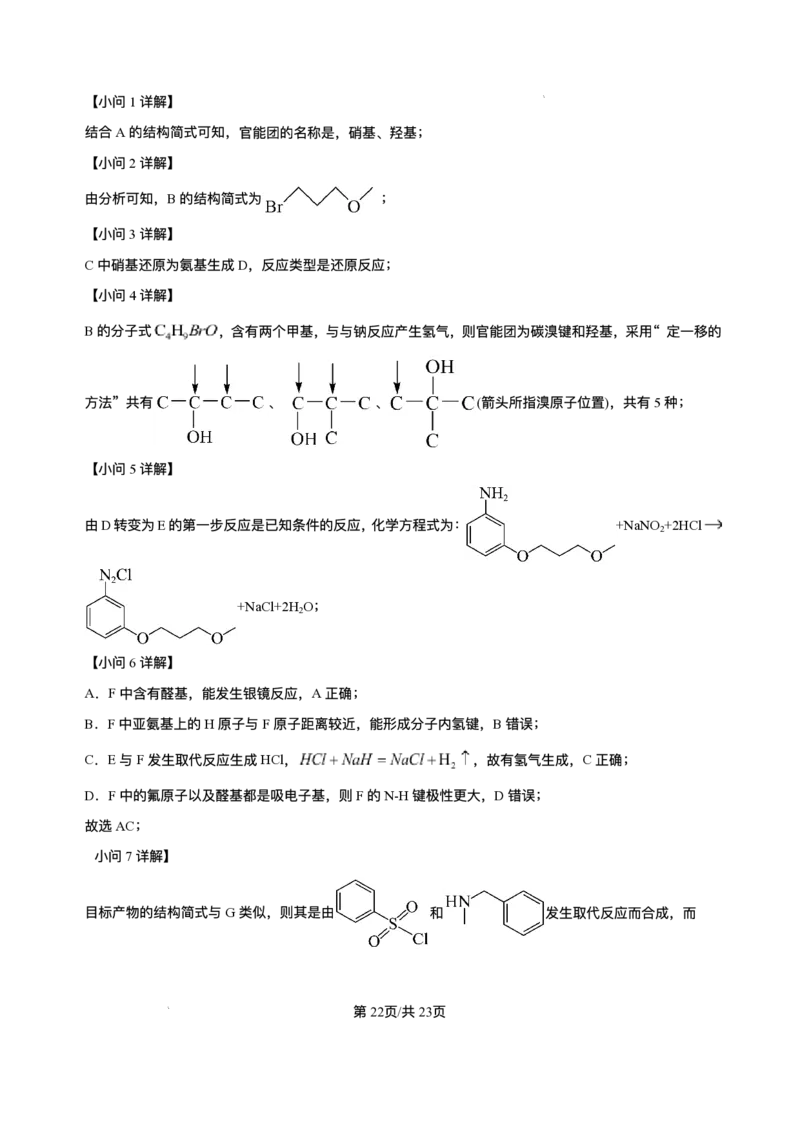
学科⽹(北京)股份有限公司【⼩问1详解】
结合A的结构简式可知,官能团的名称是,硝基、羟基;
【⼩问2详解】
由分析可知,B的结构简式为 ;
【⼩问3详解】
C中硝基还原为氨基⽣成D,反应类型是还原反应;
【⼩问4详解】
B的分⼦式 ,含有两个甲基,与与钠反应产⽣氢⽓,则官能团为碳溴键和羟基,采⽤“ 定⼀移的
⽅法” 共有 、 、 (箭头所指溴原⼦位置),共有5种;
【⼩问5详解】
由D转变为E的第⼀步反应是已知条件的反应,化学⽅程式为: +NaNO +2HCl
2
+NaCl+2H O;
2
【⼩问6详解】
A.F中含有醛基,能发⽣银镜反应,A正确;
B.F中亚氨基上的H原⼦与F原⼦距离较近,能形成分⼦内氢键,B错误;
C.E与F发⽣取代反应⽣成HCl, ,故有氢⽓⽣成,C正确;
D.F中的氟原⼦以及醛基都是吸电⼦基,则F的N-H键极性更⼤,D错误;
故选AC;
⼩问7详解】
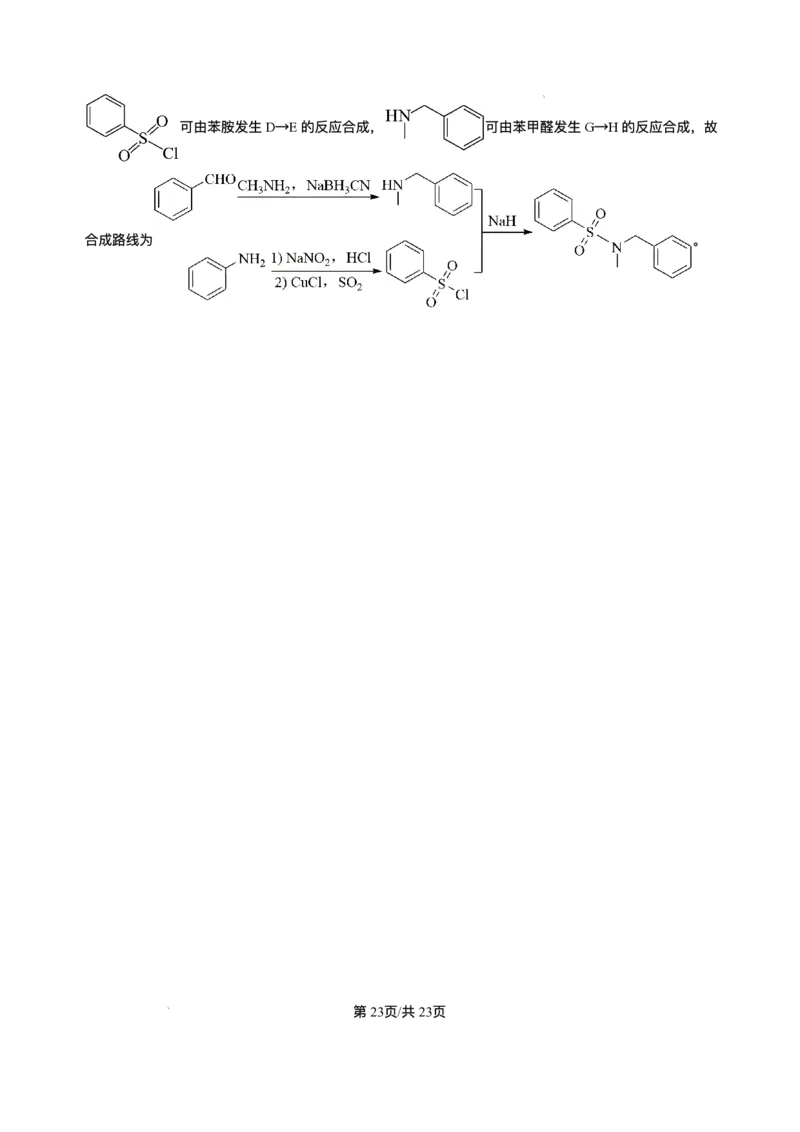
⽬标产物的结构简式与G类似,则其是由 和 发⽣取代反应⽽合成,⽽
第22⻚/共23⻚
学科⽹(北京)股份有限公司可由苯胺发⽣D→E的反应合成, 可由苯甲醛发⽣G→H的反应合成,故
合成路线为 。
第23⻚/共23⻚
学科⽹(北京)股份有限公司