文档内容
2025-2026 学年高二年级化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第一章~第二章第二节(人教版 2019)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39
Ca-40 Ti-48 Cr-52 Fe-56 Ni-59 Cu-64 Ba-137
第Ⅰ卷(选择题 共 45 分)
一、选择题:本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.“嫦娥”揽月,“天和”驻空,“天问”探火,“奋斗者”号探秘深海,我国科技事业取得巨大成就。下列说法
不正
确的是
A.“嫦娥”六号运载火箭的助推器采用液氧-煤油发动机,燃料燃烧时存在化学能到热能的转化
B.“天和”核心舱的太阳能电池板主要成分是二氧化硅
C.“天问”一号火星车使用的保温材料为纳米气凝胶,具有丁达尔效应
D.“奋斗者”号潜水器含钛合金,其强度高于纯钛金属
【答案】B
【详解】A.燃料燃烧时放热,即化学能转化为热能,故 A 正确;
B.太阳能电池板的主要成分是单晶硅,故 B 错误;
C.纳米气凝胶属于胶体,可发生丁达尔效应,故 C 正确;
D.钛合金的强度高于纯钛,故 D 正确;
答案选 B。
2.下列应用涉及的反应属于吸热反应的是
A.NH 和 NO 反应作为火箭推进剂 B.Al 和 Fe O 反应焊接钢轨
2 4 2 2 3
C.煅烧石灰石制取生石灰 D.乙炔与氧气反应用于切割金属
【答案】C
/【详解】A.NH 和 NO 反应作为火箭推进剂,该反应为放热反应,A 项不符合题意;
2 4 2
B.A1 和 Fe O 的反应为铝热反应,反应时放出大量热,可用于焊接钢轨,B 项不符合题意;
2 3
C.煅烧石灰石的反应为吸热反应,C 项符合题意;
D.乙炔燃烧为放热反应,D 项不符合题意。
故选 C。
3.在 反应中,表示该反应速率最快的是
A. B.
C. D.
【答案】B
【详解】A.将 v(A)表示的反应速率转化为用 v(B)表示: ;
B. ;
C.将 v(C)表示的反应速率转化为用 v(B)表示: ;
D.将 v(D)表示的反应速率转化为用 v(B)表示: ;
故选 B。
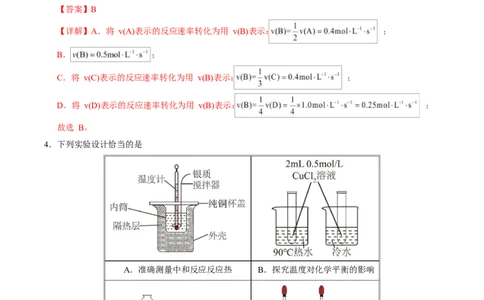
4.下列实验设计恰当的是
A.准确测量中和反应反应热 B.探究温度对化学平衡的影响
D.探究 对 分
C.测生成 的速率
解
速率的影响
A.A B.B C.C D.D
/【答案】B
【详解】A.银质搅拌器、纯铜杯盖都是导热性好的材料,会使体系热量散失,导致测定的反应热的值
不准,A 错误;
B.实验只设置了温度这一个变量,故可以探究温度对化学平衡的影响,B 正确;
C..图示装置中反应产生的气体从长颈漏斗逸出,不能测生成 的速率,C 错误;
D.探究 对 分解速率的影响,需要让 HO 的浓度保持相同,且 对应阴离子种
2 2
类也要相同,B 错误;
5.下列热化学方程式书写正确的是
A.表示硫的燃烧热的热化学方程式:
B.肼( )是一种可燃性液体,燃烧热为 624kJ/mol, 燃烧的热化学方程式:
C.若 ,则稀硫酸与稀 反应的热化学方程式为:
D.密闭容器中,1g 与足量的 混合反应后生成 ,放出 akJ 热量( ):
【答案】B
【详解】A.硫的燃烧热是 1molS 生成 SO (g)的过程所放出的热量,故 A 错误;
2
B.燃烧热指可燃物为 1mol,生成指定的产物所放出的热量,所以 燃烧热的热化学方程式为
,故 B 正确;
C.HSO 与 Ba(OH) 反应会生成 BaSO 沉淀和水,生成 BaSO 沉淀还要放热,所以稀溶液中 1molH SO
2 4 2 4 4 2 4
与 1molBa(OH) 反应放热大于 114.6kJ,故 C 错误;
2
D.密闭容器中,1g 与足量的 混合反应后生成 ,放出 akJ 热量,由于实际是可逆反应,
此时氢气转化率较高,若消耗 1mol ,则放出的热量大于 2akJ,则:
,故 D 错误;
故选 B。
6.下列说法正确的是
A. 与 反应中, 能减小该反应的焓变
B. 制 反应中, 能加快化学反应速率
C.工业合成氨中,使用铁触媒能提高 N 的平衡转化率
2
D.豆科植物固氮过程中,固氮酶能提高该反应的活化能
【答案】B
/【详解】A. 作为反应的催化剂,只能降低反应的活化能,不能改变反应的焓变,A 错误;
B. 作为反应的催化剂,能降低反应的活化能,增加活化分子的数目,加快反应速率,B 正确;
C.铁触媒作为反应的催化剂,能加快反应速率,但不影响平衡,故不能提高 N 的平衡转化率,C 错误;
2
D.固氮酶是豆科植物固氮过程中的催化剂,能降低反应的活化能,加快反应速率,D 错误;
故答案选 B。
7.下列事实不能用平衡移动原理解释的是
A.工业合成氨 ,采用 400℃~500℃的高温条件
B.工业制备 ,加入大量水,同时加热
C.黄色的氯水在光照下颜色变浅
D.25℃~100℃,随温度升高,纯水的 减小
【答案】A
【详解】A.工业合成氨 ,采用 400℃~500℃的高温条件是因为此
温度催化剂活性高,反应速率快,不能用平衡移动原理解释,故选 A;
B.工业制备 ,加入大量水,同时加热,促进 TiCl 水解平
4
衡正向移动,故不选 B;
C.次氯酸见光易分解,黄色的氯水在光照下,次氯酸分解, 正向移动,颜色
变浅,故不选 C;
D.25℃~100℃,随温度升高, 正向移动,氢离子浓度增大,纯水的 减小,故不选 D;
选 A。
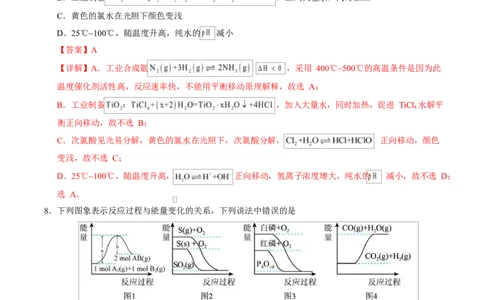
8.下列图象表示反应过程与能量变化的关系,下列说法中错误的是
A.图 1, 和 总键能大于 的总键能
B.图 2, ,则
C.图 3,红磷比白磷稳定
D.图 4,
【答案】B
【详解】A.图 1 表示的反应吸热, 和 总键能大于 的总键能,故 A 正确;
B.等物质的量的气态 S 的能量大于固态 S 的能量,所以同物质的量的气态硫燃烧放出的能量大于固态
/S 燃烧放出的能量,则 ,则 ,故 B 错
误;
C.能量越低越稳定,红磷的能量比白磷低,所以红磷比白磷稳定,故 C 正确;
D.CO、HO 的总能量大于 CO 和 H 的总能量, ,故 D 正确;
2 2 2
选 B。
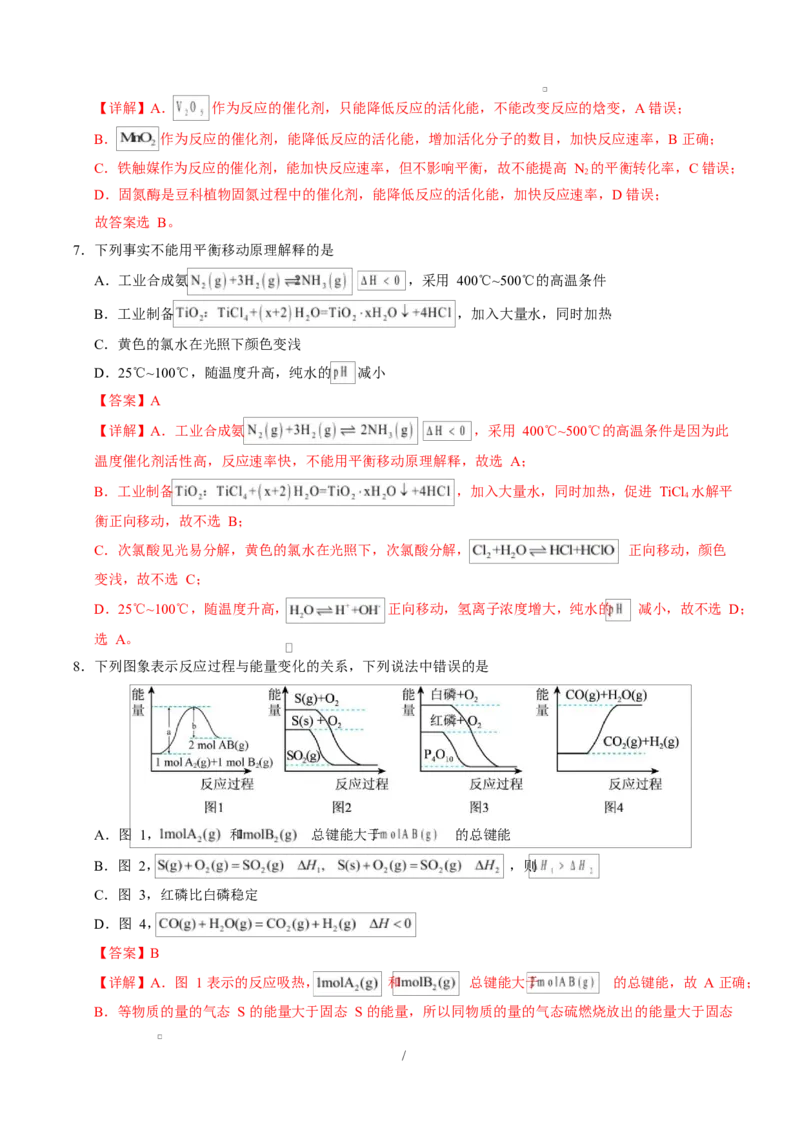
9.我国学者发现 T℃时(各物质均为气态),甲醇( )与水的反应在铜基催化剂作用下分二步进行,其
反应过程和能量图如下:
下列说法错误的是
A.CO 是反应过程中的中间产物
B.反应Ⅱ的热化学方程式为:
C. 和 的总能量小于 和 的总能量
D.改变催化剂可以使反应Ⅰ的活化能<反应Ⅱ的活化能,从而减少过程中的能量消耗和反应焓变
【答案】D
【详解】A.CO(g)在反应中生成又消耗,CO(g)是反应的中间产物,A 不符合题意;
B.结合能量图可知,反应Ⅱ为放热反应,根据反应机理图可知,反应Ⅱ的热化学方程式为:
,B 不符合题意;
C.结合反应机理和能量图可知,E >E ,即 1molCH OH(g)和 1molH O(g)的总能量小于 1molCO
Ⅱ生 Ⅰ反 3 2 2
(g)和 3molH (g)的总能量,C 不符合题意;
2
D.择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,能减少过程中的能耗,但不能减少反应的焓变,D
符合题意;
故选 D;
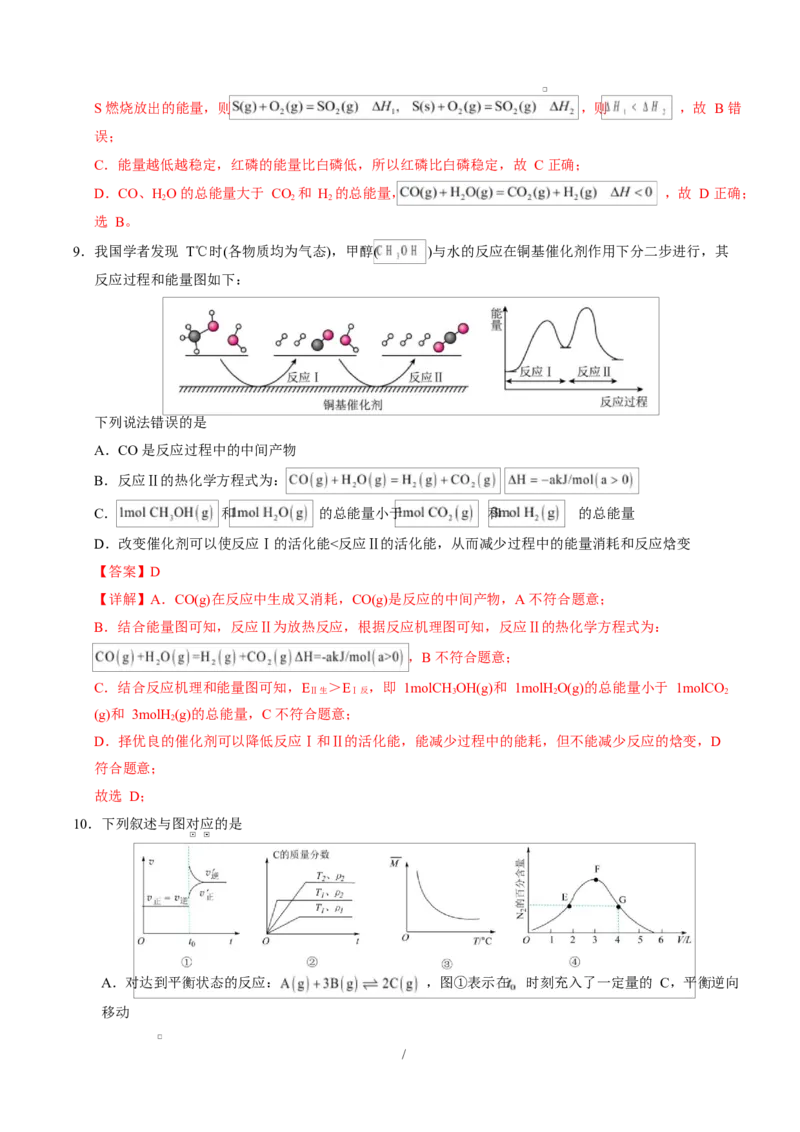
10.下列叙述与图对应的是
A.对达到平衡状态的反应: ,图①表示在 时刻充入了一定量的 C,平衡逆向
移动
/B.由图②可知, 、 ,且满足反应:
C.在恒容密闭容器中进行反应: ,M 为平均摩尔质量,由图③可知该反应
D.在不同的密闭容器中,1mol 和足量 C 发生反应: ,维
持温度不变,反应相同时间后,各容器测得 百分含量的变化如图④所示,则只有 F 点为平衡点
【答案】B
【详解】A.t 时刻充入了一定量的 C, 瞬间不变,A 错误;
0
B.温度越高反应速率越快,达到平衡所需时间短。由图像可知:在压强相同都为 p 时,温度为 T 先
2 1
达到平衡,说明温度:T>T;在温度不变时,增大压强,化学平衡速率加快,达到平衡所需时间缩短;
1 2
根据图像可知:在温度都是 T,压强为 p 时先达到平衡,说明压强:p>p;增大压强,化学平衡向
1 2 2 1
气体体积减小的正反应方向移动,使 C 的平衡平衡含量增大;升高温度,平衡向吸热的逆反应方向移
动,导致 C 的平衡含量降低,因此满足 2A(g)+B(g) 2C(g) ΔH<0,B 正确;
C.依据图像分析,温度升高平均相对分子质量减小,平均相对分子质量减小,总质量不变,说明气体
物质的量变大,所以平衡逆向进行,逆反应是吸热反应,正反应是放热反应, ,C 错误;
D.容器体积越大,压强越小,而该反应为气体分子数增大的反应,减压,平衡正向移动, 的百分
含量变大,则 E、F 点为平衡点,G 点因压强过小,速率过慢,未达到平衡,D 错误;
故选 B。
11.从下列实验事实所引出的相应结论正确的是
选
实验事实 结论
项
其他条件相同, 溶液与稀硫酸反应时, 溶液浓度 当其他条件不变时,增大反应物
A
越大,析出 S 沉淀所需时间越短 浓度,化学反应速率加快
B 在化学反应前后,催化剂的质量和化学性质都没有发生改变 催化剂一定不参与化学反应
取 溶液于试管中,加入 溶
C 液, KI 与 FeCl 的反应是可逆反应
3
滴入 5 滴 KSCN 溶液,溶液变血红色
在容积可变的密闭容器中发生反应 ,把容积 正反应速率加快,逆反应速率不
D
缩小一倍 变
A.A B.B C.C D.D
【答案】A
【详解】A.其他条件相同,增大 溶液浓度导致析出 S 沉淀时间缩短,说明浓度增大使反应速
率加快,A 正确;
B.催化剂参与化学反应,降低反应的活化能,使反应速率加快,但其质量和化学性质在反应前后都没
/有发生改变,不是不参加化学反应,B 错误;
C. 过量导致 KSCN 溶液显红色,不能证明反应可逆,C 错误;
D.缩小容器容积一倍,所有物质的浓度均增大一倍,正逆反应速率均加快,D 错误;
故答案选 A。
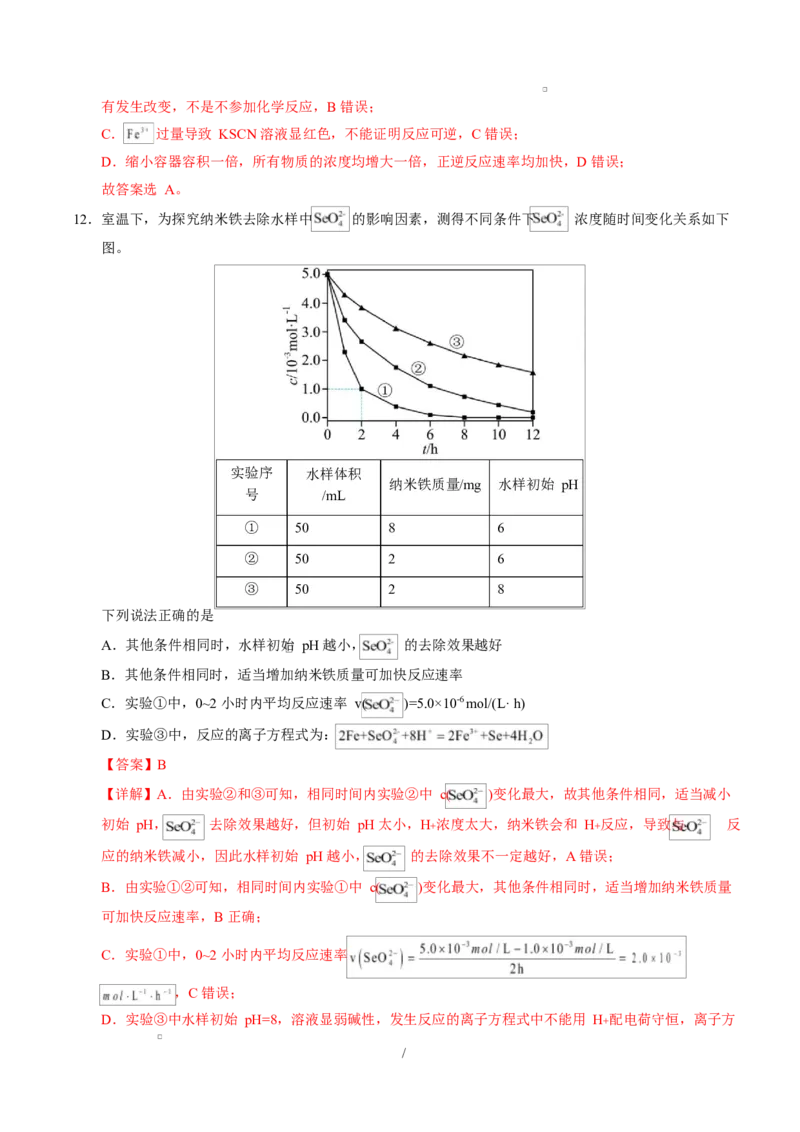
12.室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下 浓度随时间变化关系如下
图。
实验序 水样体积
纳米铁质量/mg 水样初始 pH
号 /mL
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.其他条件相同时,水样初始 pH 越小, 的去除效果越好
B.其他条件相同时,适当增加纳米铁质量可加快反应速率
C.实验①中,0~2 小时内平均反应速率 v( )=5.0×10-6 mol/(L· h)
D.实验③中,反应的离子方程式为:
【答案】B
【详解】A.由实验②和③可知,相同时间内实验②中 c( )变化最大,故其他条件相同,适当减小
初始 pH, 去除效果越好,但初始 pH 太小,H+ 浓度太大,纳米铁会和 H+ 反应,导致与 反
应的纳米铁减小,因此水样初始 pH 越小, 的去除效果不一定越好,A 错误;
B.由实验①②可知,相同时间内实验①中 c( )变化最大,其他条件相同时,适当增加纳米铁质量
可加快反应速率,B 正确;
C.实验①中,0~2 小时内平均反应速率
,C 错误;
D.实验③中水样初始 pH=8,溶液显弱碱性,发生反应的离子方程式中不能用 H+ 配电荷守恒,离子方
/程式: ,D 错误;
故答案选 B。
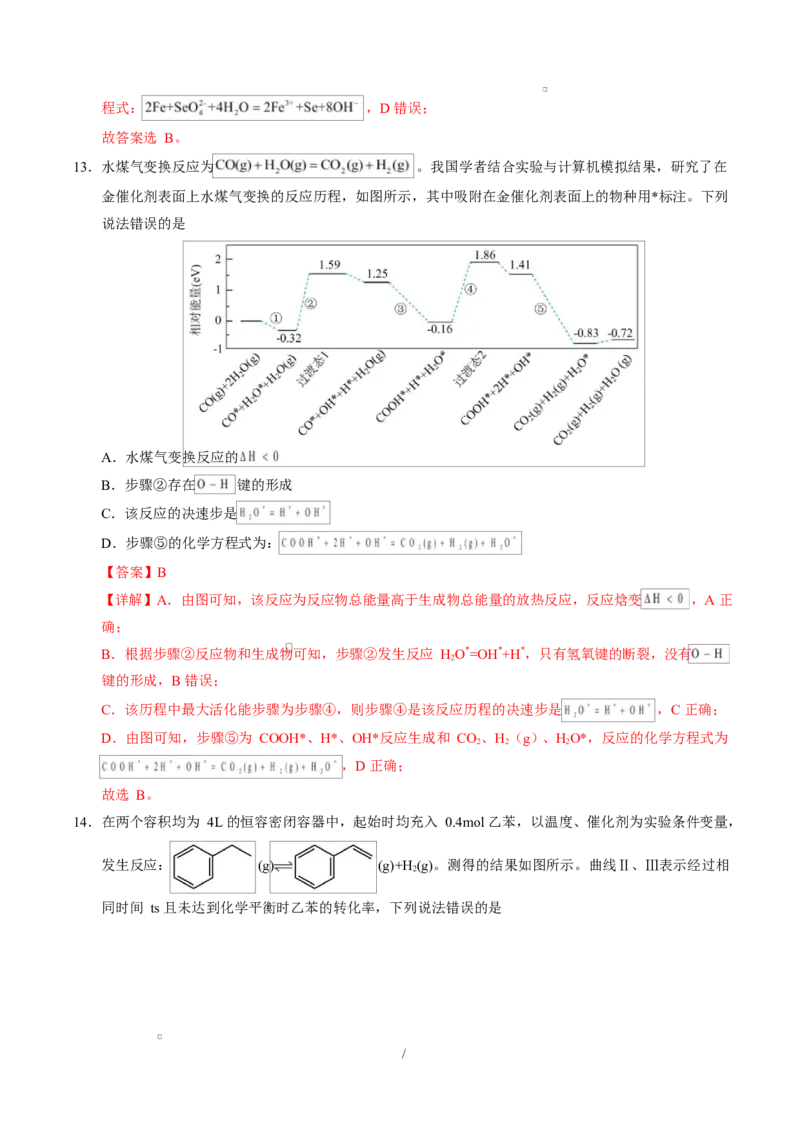
13.水煤气变换反应为 。我国学者结合实验与计算机模拟结果,研究了在
金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。下列
说法错误的是
A.水煤气变换反应的
B.步骤②存在 键的形成
C.该反应的决速步是
D.步骤⑤的化学方程式为:
【答案】B
【详解】A.由图可知,该反应为反应物总能量高于生成物总能量的放热反应,反应焓变 ,A 正
确;
B.根据步骤②反应物和生成物可知,步骤②发生反应 HO*=OH*+H*,只有氢氧键的断裂,没有
2
键的形成,B 错误;
C.该历程中最大活化能步骤为步骤④,则步骤④是该反应历程的决速步是 ,C 正确;
D.由图可知,步骤⑤为 COOH*、H*、OH*反应生成和 CO、H(g)、HO*,反应的化学方程式为
2 2 2
,D 正确;
故选 B。
14.在两个容积均为 4L 的恒容密闭容器中,起始时均充入 0.4mol 乙苯,以温度、催化剂为实验条件变量,
发生反应: (g) (g)+H(g)。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相
2
同时间 ts 且未达到化学平衡时乙苯的转化率,下列说法错误的是
/A.900℃时,无催化剂的容器中,ts 内 的平均反应速率为
B.1100℃时,曲线Ⅱ、Ⅲ几乎重合,可能是因为催化剂失活
C.1000℃时,有催化剂的容器中,延长反应时间乙苯的转化率无法到达 A 点
D.其他条件不变时,降低温度或增大压强均能使平衡向左移动,均能使平衡常数 K 减小
【答案】D
【详解】A.900℃时无催化剂的容器中,ts 时乙苯的转化率为 30%,则生成的氢气为 0.12mol,容器体
积为 4L,则 ts 内 H 的平均反应速率为 ,A 正确;
2
B.催化剂需要适宜温度,根据图像,约 1100℃,曲线Ⅱ、Ⅲ几乎重合,说明不论有无催化剂,平均
反应速率相同,则可能是催化剂失活,B 正确;
C.催化剂不影响平衡的移动,加入催化剂,乙苯的平衡转化率不变,延长反应时间乙苯的转化率不可
能到达 A 点,C 正确;
D.平衡常数只受温度影响。其他条件不变时,增大压强,平衡向左移动,但不能改变平衡常数,D 错
误;
答案选 D。
15.在 下,将 以物质的量之比 进行反应。发生的主要反应如下:I.
Ⅱ.
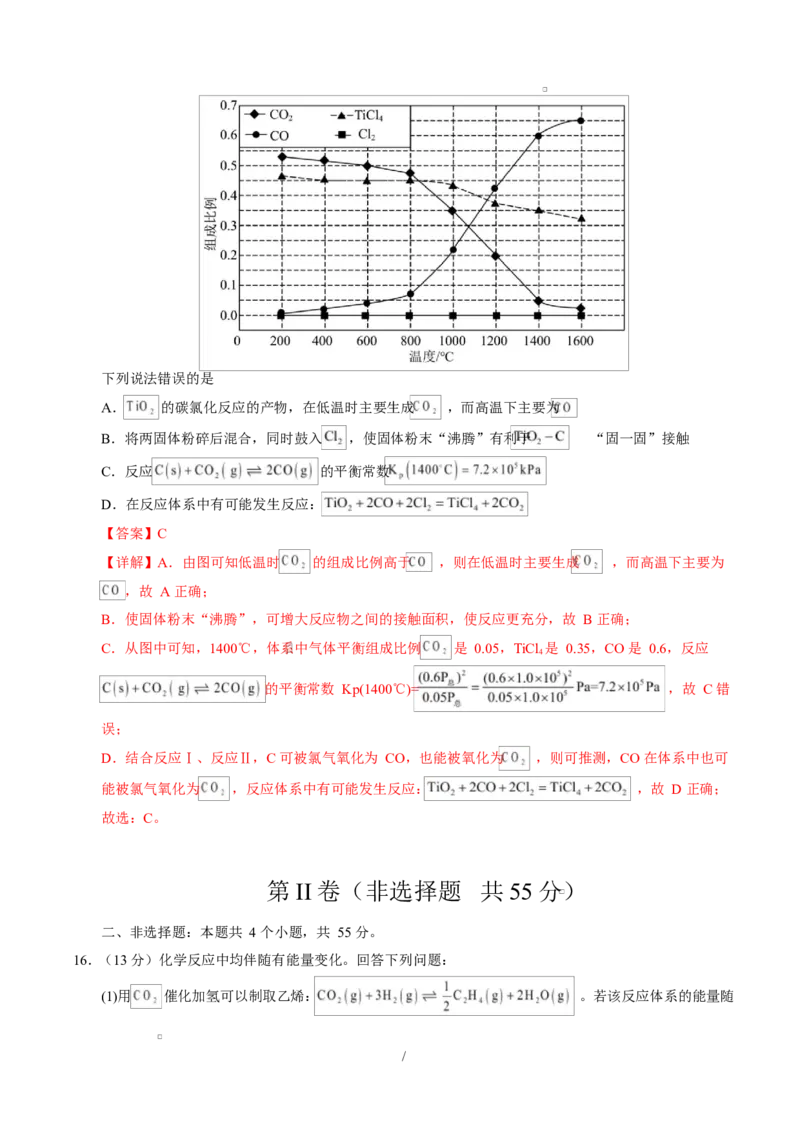
体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
/下列说法错误的是
A. 的碳氯化反应的产物,在低温时主要生成 ,而高温下主要为
B.将两固体粉碎后混合,同时鼓入 ,使固体粉末“沸腾”有利于 “固一固”接触
C.反应 的平衡常数
D.在反应体系中有可能发生反应:
【答案】C
【详解】A.由图可知低温时 的组成比例高于 ,则在低温时主要生成 ,而高温下主要为
,故 A 正确;
B.使固体粉末“沸腾”,可增大反应物之间的接触面积,使反应更充分,故 B 正确;
C.从图中可知,1400℃,体系中气体平衡组成比例 是 0.05,TiCl 是 0.35,CO 是 0.6,反应
4
的平衡常数 Kp(1400℃)= ,故 C 错
误;
D.结合反应Ⅰ、反应Ⅱ,C 可被氯气氧化为 CO,也能被氧化为 ,则可推测,CO 在体系中也可
能被氯气氧化为 ,反应体系中有可能发生反应: ,故 D 正确;
故选:C。
第 II 卷(非选择题 共 55 分)
二、非选择题:本题共 4 个小题,共 55 分。
16.(13 分)化学反应中均伴随有能量变化。回答下列问题:
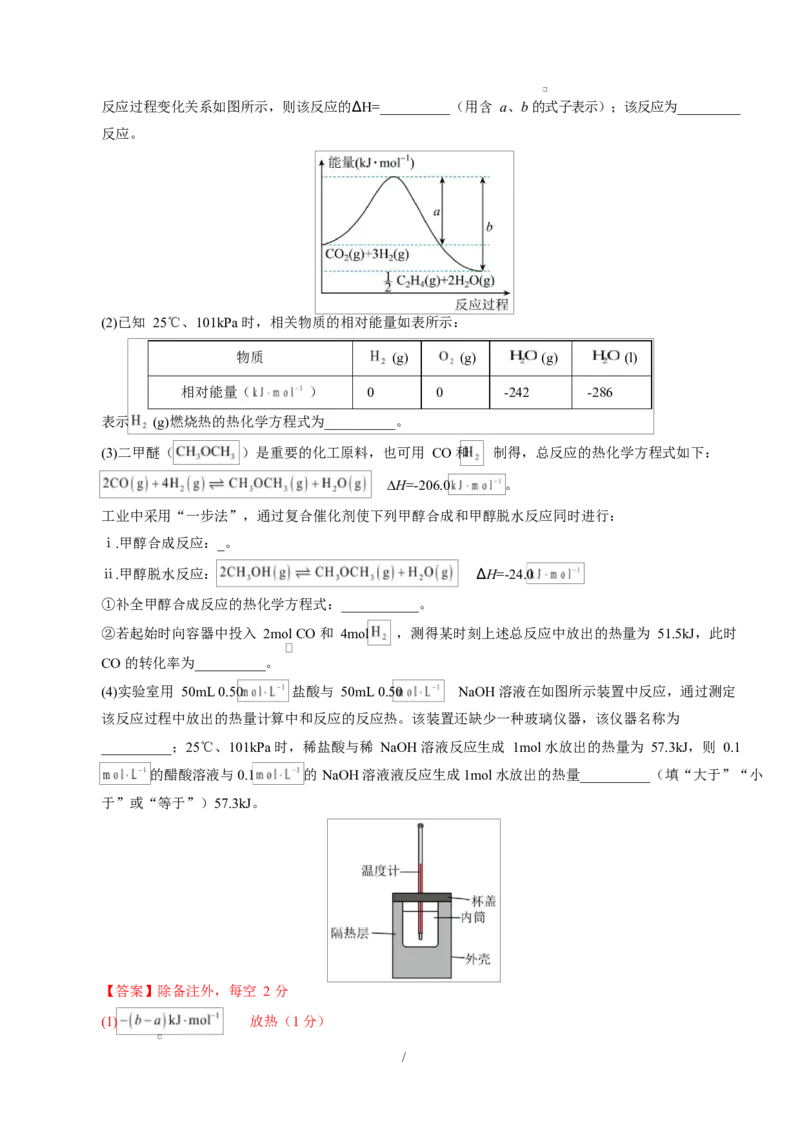
(1)用 催化加氢可以制取乙烯: 。若该反应体系的能量随
/反应过程变化关系如图所示,则该反应的∆H=__________(用含 a、b 的式子表示);该反应为_________
反应。
(2)已知 25℃、101kPa 时,相关物质的相对能量如表所示:
物质 (g) (g) (g) (l)
相对能量( ) 0 0 -242 -286
表示 (g)燃烧热的热化学方程式为__________。
(3)二甲醚( )是重要的化工原料,也可用 CO 和 制得,总反应的热化学方程式如下:
∆H=-206.0 。
工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行:
ⅰ.甲醇合成反应:_。
ⅱ.甲醇脱水反应: ∆H=-24.0
①补全甲醇合成反应的热化学方程式:___________。
②若起始时向容器中投入 2mol CO 和 4mol ,测得某时刻上述总反应中放出的热量为 51.5kJ,此时
CO 的转化率为__________。
(4)实验室用 50mL 0.50 盐酸与 50mL 0.50 NaOH 溶液在如图所示装置中反应,通过测定
该反应过程中放出的热量计算中和反应的反应热。该装置还缺少一种玻璃仪器,该仪器名称为
__________;25℃、101kPa 时,稀盐酸与稀 NaOH 溶液反应生成 1mol 水放出的热量为 57.3kJ,则 0.1
的醋酸溶液与0.1 的 NaOH溶液液反应生成1mol水放出的热量__________(填“大于”“小
于”或“等于”)57.3kJ。
【答案】除备注外,每空 2 分
(1) 放热(1 分)
/(2) ∆H=-286
(3) ∆H=-91 (或其他合理答案) 25%
(4) 玻璃搅拌器 小于
【详解】(1)由图可知,反应物的总能量高于生成物的总能量,故反应放出热量,∆H =-(b-a)kJ/mol;
(2)25℃ 和 101kPa 时,1molH 完全燃烧生成液态水所放出的热量为 H 的标准燃烧热,所以氢气的
2 2
标准燃烧热∆H =-286 ,表示 H(g)标准燃烧热的热化学方程式为 ∆
2
H =-286 ;
(3)①总反应减去反应ⅱ可得甲醇合成反应,故甲醇合成反应的热化学方程式
∆H =-91 ;
②由总反应可知,2molCO反应放出热量206kJ,则当放出热量为51.5kJ时,反应了 =0.5molCO,
故 CO 转化率为 ;
(4)酸碱混合反应需要搅拌,该装置缺少的玻璃仪器是环形玻璃搅拌棒;
醋酸是弱电解质,醋酸的电离过程吸热,所以 0.1mol/L 醋酸溶液与 0.1mol/LNaOH 溶液反应生成 1mL
水放出的热量小于 57.3kJ。
17.(14 分)甲醇是一种重要的化工原料,具有广阔的开发和应用前景。
I.工业上使用水煤气( 与 的混合气体)转化成甲醇( )。
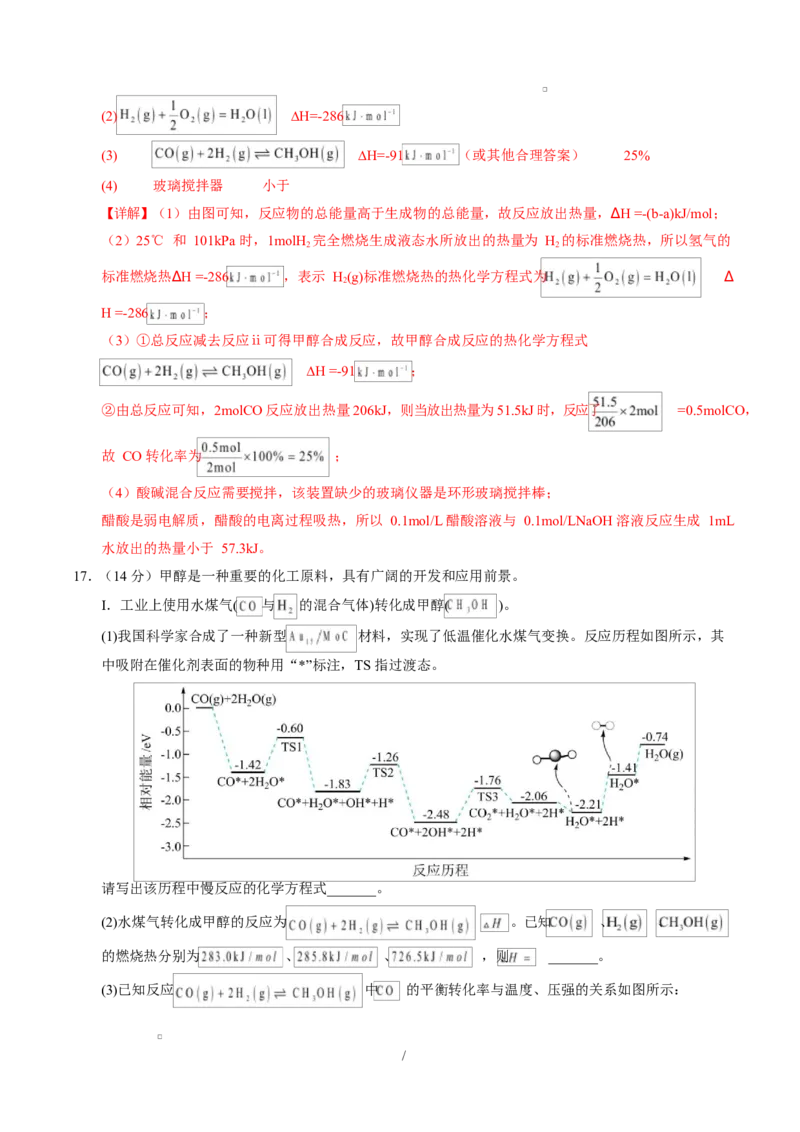
(1)我国科学家合成了一种新型 材料,实现了低温催化水煤气变换。反应历程如图所示,其
中吸附在催化剂表面的物种用“*”标注,TS 指过渡态。
请写出该历程中慢反应的化学方程式_______。
(2)水煤气转化成甲醇的反应为 。已知 、 、
的燃烧热分别为 、 、 ,则 _______。
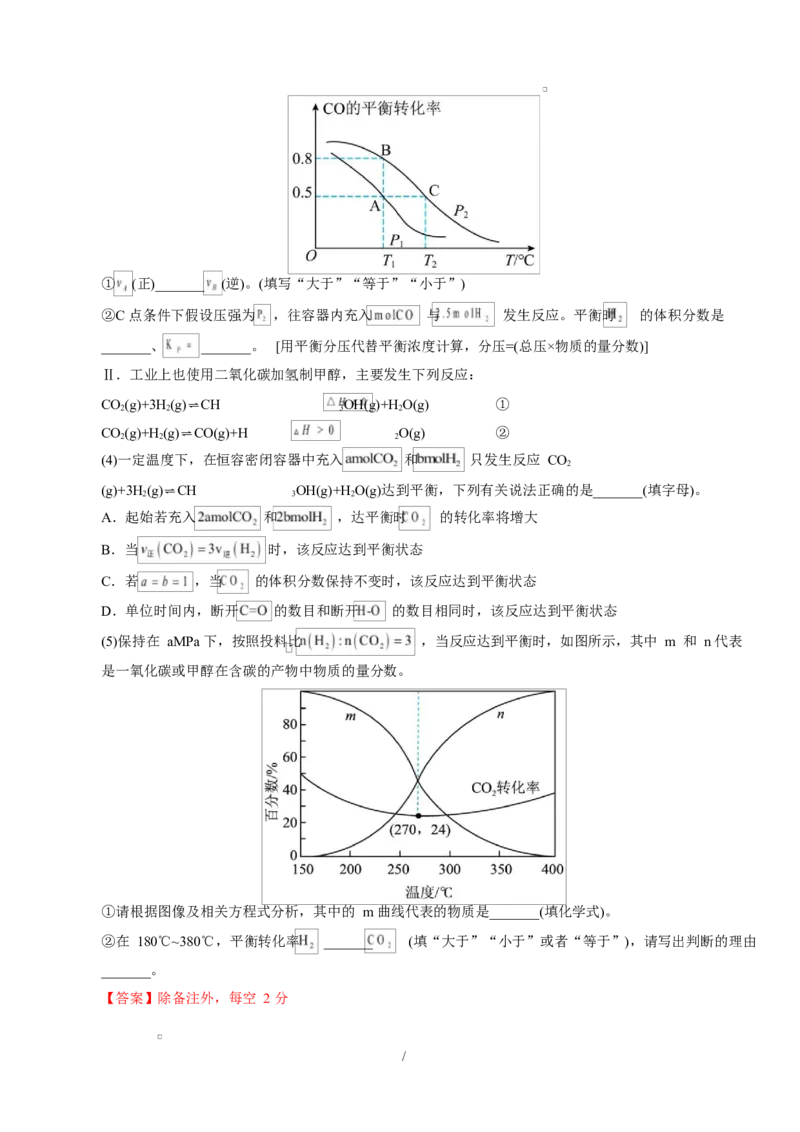
(3)已知反应 中 的平衡转化率与温度、压强的关系如图所示:
/① (正)_______ (逆)。(填写“大于”“等于”“小于”)
②C 点条件下假设压强为 ,往容器内充入 与 发生反应。平衡时 的体积分数是
_______、 _______。 [用平衡分压代替平衡浓度计算,分压=(总压×物质的量分数)]
Ⅱ.工业上也使用二氧化碳加氢制甲醇,主要发生下列反应:
CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) ①
CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ②
(4)一定温度下,在恒容密闭容器中充入 和 只发生反应 CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g)达到平衡,下列有关说法正确的是_______(填字母)。
A.起始若充入 和 ,达平衡时 的转化率将增大
B.当 时,该反应达到平衡状态
C.若 ,当 的体积分数保持不变时,该反应达到平衡状态
D.单位时间内,断开 的数目和断开 的数目相同时,该反应达到平衡状态
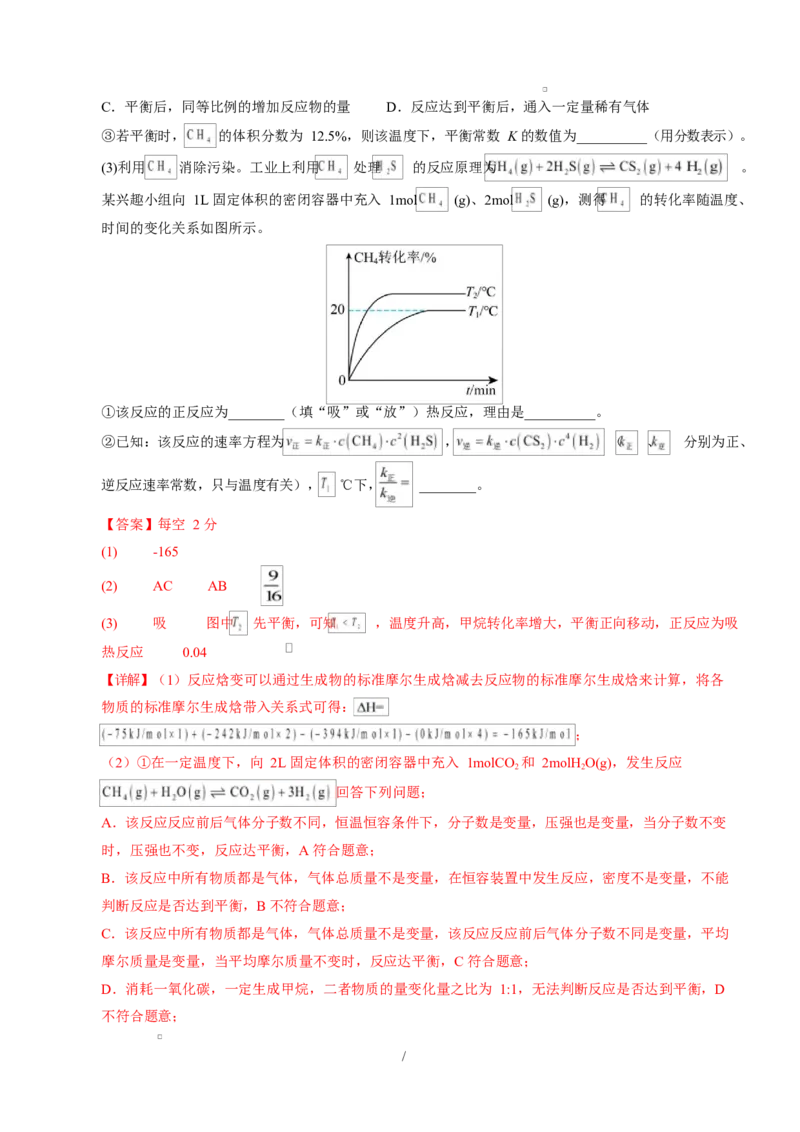
(5)保持在 aMPa 下,按照投料比 ,当反应达到平衡时,如图所示,其中 m 和 n 代表
是一氧化碳或甲醇在含碳的产物中物质的量分数。
①请根据图像及相关方程式分析,其中的 m 曲线代表的物质是_______(填化学式)。
②在 180℃~380℃,平衡转化率 _______ (填“大于”“小于”或者“等于”),请写出判断的理由
_______。
【答案】除备注外,每空 2 分
/(1)
(2)-128.1kJ/mol
(3) 小于(1 分) 60%
(4)A(1 分)
(5) CHOH (1 分) 低于(1 分) 起始 投料,只发生反应①时,CO 和
3 2
H 的转化率相同,只发生反应②时,CO 的转化率大于氢气的平衡转化率,当反应①②同时发生时,
2 2
H 的平衡转化率始终低于 CO
2 2
【详解】(1)根据图像可知,过渡态 TS1 的相对能量最大,此时的活化能最大,因此反应历程中活化
能最大的一步为: ;
故答案为:
(2)已知 CO(g)、H(g)、CHOH(g)的燃烧热分别为 283.0kJ/mol、285.8kJ/moll、726.5kJ/mol,则有
2 3
, ,
,
根据盖斯定律,①+2×②-③得 ;
故答案为:-128.1kJ/mol
(3)①AB 点均为平衡点,其 ,而 AB 两点温度相同,B 点 CO 转化率大,且反应为气体
分子数减少的反应,故 B 点压强比 A 点压强大,因此 B 点比 A 点的速率大;
故答案为:小于
②C 点条件下假设压强为 p,往容器中充入 1molCO 与 2.5mol 发生反应,平衡时 CO 的转化率为 0.5,
2
则反应 CO 为 0.5mol,则有:
反应后总的物质的量为 2.5mol, 的体积分数是 ,H 的体积分数为 ,CO 的
2
物质的量分数=CH OH 的物质的量分数= ,则
3
;
故答案为: ,
(4)A.恒容条件下,加倍投料,体系压强增大,二氧化碳的平衡转化率增大,A 正确;
/B.当 时,不符合化学计量数之比等于速率之比,正逆反应速率不相等,反应未达到平衡
状态,B 错误;
C.开始时等物质的量投料,CO 的体积分数始终保持不变,不能说明反应已达到平衡,C 错误;
2
D.单位时间内,断开 键的数目与断开 键数目不相等,因 和 中都有 键,因此
不能判断反应已经达到平衡,D 错误;
故答案选 A;
(5)①根据题目信息,其反应的产物为 时为放热反应,而生成 时为吸热反应,因此温度升
高,生成 平衡会逆向移动,从而使 的产量变少, 在含碳产物中物质的量分数减
小,则曲线 m 代表的物质为 ;
故答案为:CHOH
3
②起始 投料,只发生反应①时,CO 和 H 的转化率相同,只发生反应②时,CO 的转
2 2 2
化率大于氢气的平衡转化率,当反应①②同时发生时,H 的平衡转化率始终低于 CO;
2 2
故答案为:低于,起始 投料,只发生反应①时,CO 和 H 的转化率相同,只发生反应
2 2
②时,CO 的转化率大于氢气的平衡转化率,当反应①②同时发生时,H 的平衡转化率始终低于 CO
2 2 2
18.(14 分)将浓度均为 的 、 、 、 溶液及淀粉溶液混合,一定时间后溶
液变为蓝色。该实验是一种“碘钟实验”,某小组同学在室温下对其的原理进行探究。
资料:该“碘钟实验”的总反应为 ,反应分两步进行。
反应 A:_______;反应 B: 。
(1)反应 A 的离子方程式是_______。
(2)对于总反应,I-的作用相当于_______,I-可以改变单位体积内的_______(填标号),从而改变反应速
率。
a.活化分子数 b.活化分子百分数 c.分子总数
(3)为证明反应 A、B 的存在,进行实验Ⅰ。
实验 I:a.向酸化的 溶液中加入试剂 X 的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入 溶液,溶液的蓝色褪去。
试剂 X 是_______溶液。
(4)为探究硫酸浓度对溶液变蓝快慢的影响进行实验 II 和实验 III(各溶液浓度均为 )。
用量 溶液 溶液 溶液 试剂 X 溶液
实验 II 5 4 8 3 0
实验 III 5 2 x y z
溶液从混合时的无色变为蓝色的时间:实验 II 是 15min,实验 III 是 20min。
/①实验 III 中 x、y、z 所对应的数值分别是_______、_______、_______。
②对比实验 II 和实验 III,可得出的实验结论是_______。
【答案】除备注外,每空 2 分
(1)
(2) 催化剂(1 分) ab
(3)淀粉 KI
(4) 8(1 分) 3 2 其他条件不变,增大硫酸浓度可以加快反应速率
【详解】(1)该“碘钟实验“的总反应为 ,反应 B 为
,用总反应-反应 B 即得反应 A 的离子方程式为 ;
(2)对于总反应,I-的作用相当于催化剂;I-可以改变单位体积内的活化分子数和活化分子百分数,即
答案为 ab;
(3)过氧化氢具有氧化性,会将 KI 氧化为碘单质,碘单质遇到淀粉变蓝色,碘单质具有氧化性,可
以氧化 NaSO 溶液,发生反应: ,故 X 为淀粉 KI 溶液;
2 2 3
(4)①在反应中要采取控制变量的方法进行实验,即只改变一个反应条件,其它条件相同,依据表格
数据可知,实验Ⅲ跟实验 II 对比硫酸体积减少,所以其它条件都相同,而且混合后总体积也要相同,
故实验 III 中,x、y、z 所对应的数值分别是:8、3、2;
②对比实验 II、实验 III,可得出的实验结论是:其它条件不变,增大硫酸浓度可以加快反应速率。
19.(14 分)随着现代工业的发展, 作为一种可再生的能源在生产、生活中的作用越来越大。回答下列
问题:
(1)利用 合成 ,实现资源的再利用。已知:在 25℃、101kPa 下,由最稳定的单质生成 1mol 物
质的反应焓变,叫作该物质的标准摩尔生成焓,规定稳定单质的标准摩尔生成焓为 0。下表为几种常见
物质的标准摩尔生成焓的数值。
物质 CO(g) (g) (g) (g)
标准摩尔生成焓/ -283 -242 -75 -394
反应 ΔH=__________ 。
(2)利用 制备合成气(CO、 )。在一定温度下,向 2L 固定体积的密闭容器中充入 1mol 、
2mol (g),发生反应 。
①下列可以判断该反应达到平衡状态的是__________(填字母,下同)。
A.容器内压强不再变化 B.气体的密度不再变化
C.混合气的平均摩尔质量不再变化 D.
②下列可提高 平衡转化率的措施有__________。
A.升高温度 B.扩大容器体积
/C.平衡后,同等比例的增加反应物的量 D.反应达到平衡后,通入一定量稀有气体
③若平衡时, 的体积分数为 12.5%,则该温度下,平衡常数 K 的数值为__________(用分数表示)。
(3)利用 消除污染。工业上利用 处理 的反应原理为 。
某兴趣小组向 1L 固定体积的密闭容器中充入 1mol (g)、2mol (g),测得 的转化率随温度、
时间的变化关系如图所示。
①该反应的正反应为________(填“吸”或“放”)热反应,理由是__________。
②已知:该反应的速率方程为 , ( 、 分别为正、
逆反应速率常数,只与温度有关), ℃下, ________。
【答案】每空 2 分
(1) -165
(2) AC AB
(3) 吸 图中 先平衡,可知 ,温度升高,甲烷转化率增大,平衡正向移动,正反应为吸
热反应 0.04
【详解】(1)反应焓变可以通过生成物的标准摩尔生成焓减去反应物的标准摩尔生成焓来计算,将各
物质的标准摩尔生成焓带入关系式可得:
;
(2)①在一定温度下,向 2L 固定体积的密闭容器中充入 1molCO 和 2molH O(g),发生反应
2 2
回答下列问题;
A.该反应反应前后气体分子数不同,恒温恒容条件下,分子数是变量,压强也是变量,当分子数不变
时,压强也不变,反应达平衡,A 符合题意;
B.该反应中所有物质都是气体,气体总质量不是变量,在恒容装置中发生反应,密度不是变量,不能
判断反应是否达到平衡,B 不符合题意;
C.该反应中所有物质都是气体,气体总质量不是变量,该反应反应前后气体分子数不同是变量,平均
摩尔质量是变量,当平均摩尔质量不变时,反应达平衡,C 符合题意;
D.消耗一氧化碳,一定生成甲烷,二者物质的量变化量之比为 1:1,无法判断反应是否达到平衡,D
不符合题意;
/故答案选:AC。
②反应焓变可以通过生成物的标准摩尔生成焓减去反应物的标准摩尔生成焓来计算,带入关系式可得:
A.该反应为吸热反应,升高温度,化学平衡正向移动,甲烷的平衡转化率增大,A 符合题意;
B.扩大容器体积相当于减小压强,该反应后气体分子数增加,扩大体积,化学平衡正向移动,甲烷平
衡转化率增大,B 符合题意;
C.恒温恒容平衡后,同等比例的增加反应物的量,相当于在原平衡的基础上增大压强,化学平衡逆向
移动,甲烷的平衡转化率减小,C 不符合题意;
D.恒温恒容,反应达到平衡后,通入一定量稀有气体,反应物浓度不变,化学反应速率不变,化学平
衡不移动,甲烷平衡转化率不变,D 不符合题意;
故答案选 AB。
③设平衡时 转化的物质的量为 xmol,则有如下三段式
根据题意, 的体积分数为 12.5%,则有 ,解得
解得 ,代入平衡常数公式: ;故答案为: 。
(3)①根据图像结合先拐先平数值大,图中 先平衡,可知: ,且升高温度,甲烷的平衡转化
率增大,故 正向移动,该反应为吸热反应;
故答案为:吸;图中 先平衡,可知 ,温度升高,甲烷转化率增大,平衡正向移动,正反应为吸
热反应。
②平衡时正、逆反应速率相等,即 ,变形得到
,根据图像可以得到 T 温度下该反应平衡的三段式为:
1
,
,故答案为:0.04。
/