文档内容
2025-2026 学年高二年级化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第一章~第二章第二节(人教版 2019)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39
Ca-40 Ti-48 Cr-52 Fe-56 Ni-59 Cu-64 Ba-137
第Ⅰ卷(选择题 共 45 分)
一、选择题:本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.“嫦娥”揽月,“天和”驻空,“天问”探火,“奋斗者”号探秘深海,我国科技事业取得巨大成就。下列说法
不正
确的是
A.“嫦娥”六号运载火箭的助推器采用液氧-煤油发动机,燃料燃烧时存在化学能到热能的转化
B.“天和”核心舱的太阳能电池板主要成分是二氧化硅
C.“天问”一号火星车使用的保温材料为纳米气凝胶,具有丁达尔效应
D.“奋斗者”号潜水器含钛合金,其强度高于纯钛金属
2.下列应用涉及的反应属于吸热反应的是
A.NH 和 NO 反应作为火箭推进剂 B.Al 和 Fe O 反应焊接钢轨
2 4 2 2 3
C.煅烧石灰石制取生石灰 D.乙炔与氧气反应用于切割金属
3.在 反应中,表示该反应速率最快的是
A. B.
C. D.
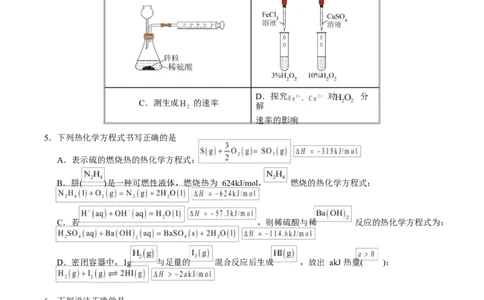
4.下列实验设计恰当的是
/A.准确测量中和反应反应热 B.探究温度对化学平衡的影响
D.探究 对 分
C.测生成 的速率
解
速率的影响
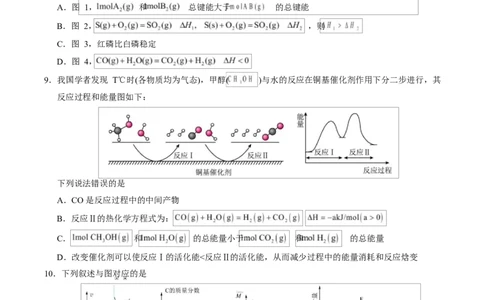
5.下列热化学方程式书写正确的是
A.表示硫的燃烧热的热化学方程式:
B.肼( )是一种可燃性液体,燃烧热为 624kJ/mol, 燃烧的热化学方程式:
C.若 ,则稀硫酸与稀 反应的热化学方程式为:
D.密闭容器中,1g 与足量的 混合反应后生成 ,放出 akJ 热量( ):
6.下列说法正确的是
A. 与 反应中, 能减小该反应的焓变
B. 制 反应中, 能加快化学反应速率
C.工业合成氨中,使用铁触媒能提高 N 的平衡转化率
2
D.豆科植物固氮过程中,固氮酶能提高该反应的活化能
7.下列事实不能用平衡移动原理解释的是
A.工业合成氨 ,采用 400℃~500℃的高温条件
B.工业制备 ,加入大量水,同时加热
/C.黄色的氯水在光照下颜色变浅
D.25℃~100℃,随温度升高,纯水的 减小
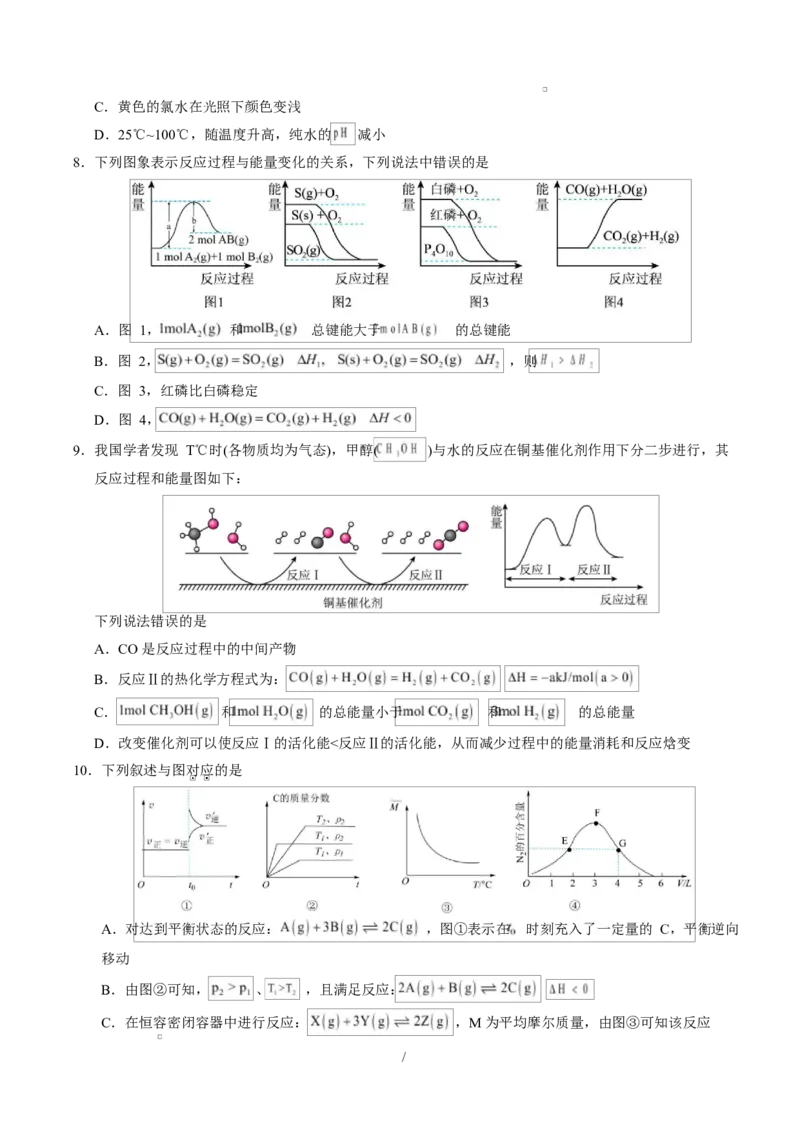
8.下列图象表示反应过程与能量变化的关系,下列说法中错误的是
A.图 1, 和 总键能大于 的总键能
B.图 2, ,则
C.图 3,红磷比白磷稳定
D.图 4,
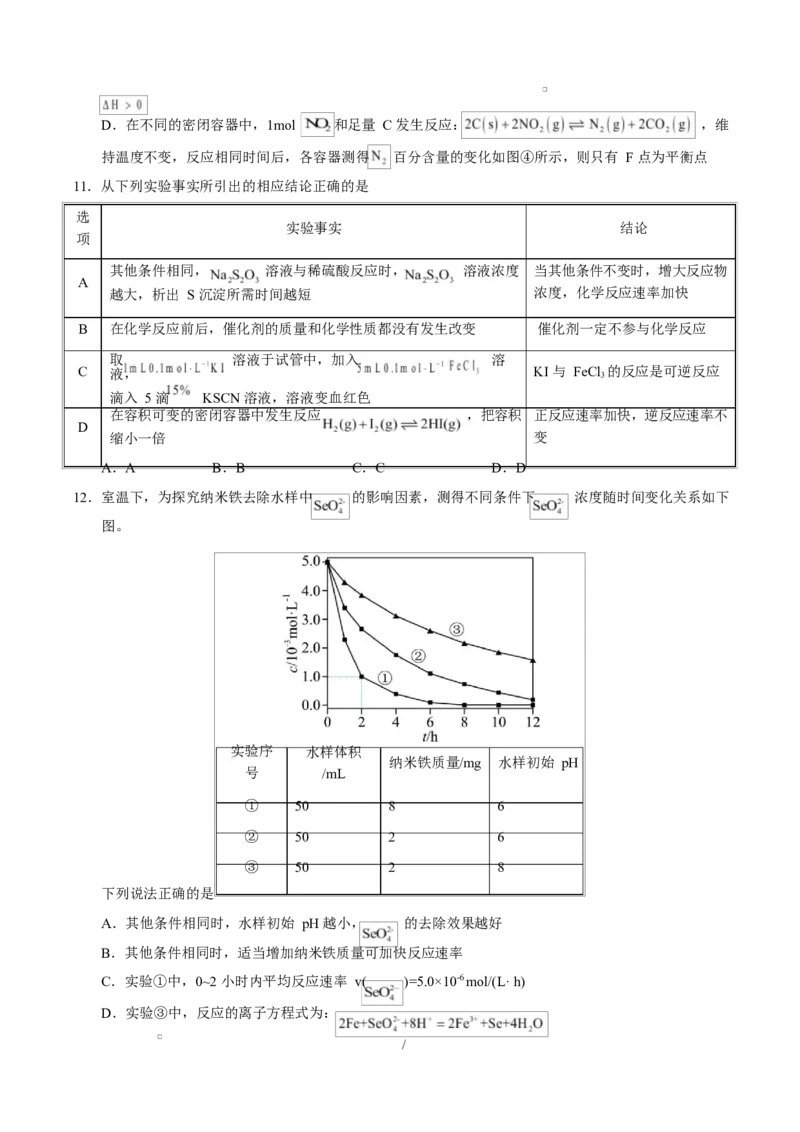
9.我国学者发现 T℃时(各物质均为气态),甲醇( )与水的反应在铜基催化剂作用下分二步进行,其
反应过程和能量图如下:
下列说法错误的是
A.CO 是反应过程中的中间产物
B.反应Ⅱ的热化学方程式为:
C. 和 的总能量小于 和 的总能量
D.改变催化剂可以使反应Ⅰ的活化能<反应Ⅱ的活化能,从而减少过程中的能量消耗和反应焓变
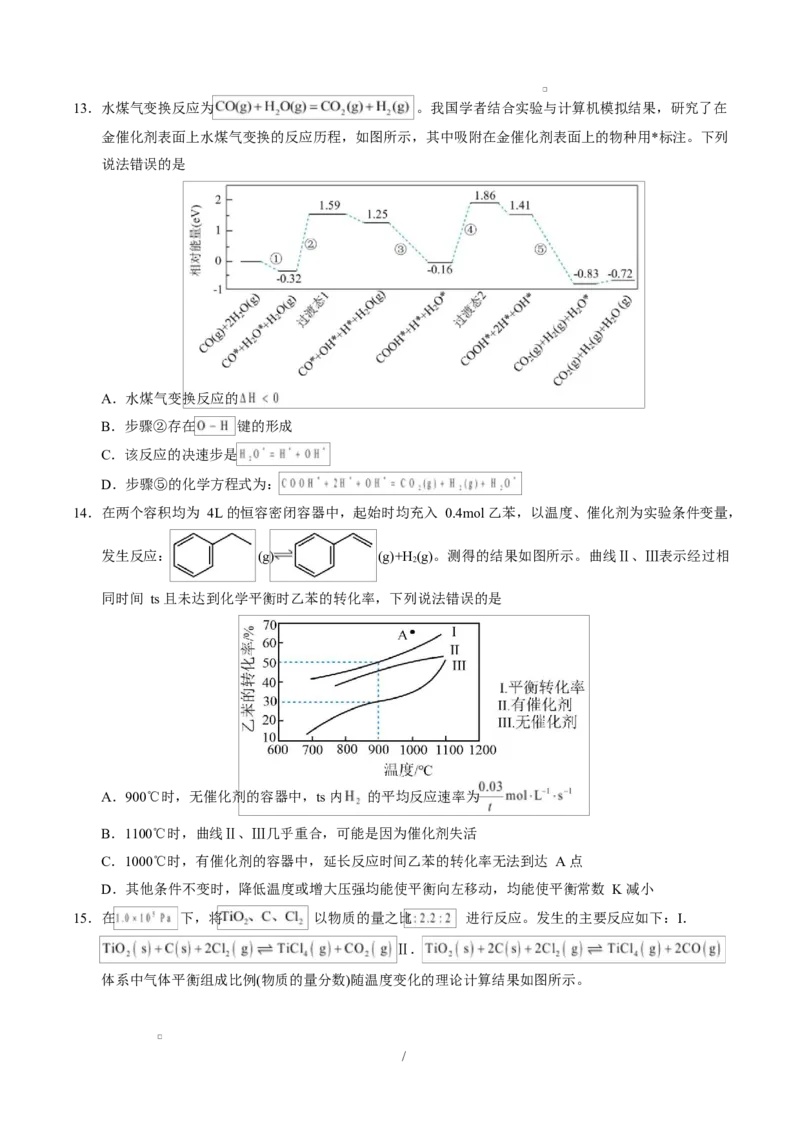
10.下列叙述与图对应的是
A.对达到平衡状态的反应: ,图①表示在 时刻充入了一定量的 C,平衡逆向
移动
B.由图②可知, 、 ,且满足反应:
C.在恒容密闭容器中进行反应: ,M 为平均摩尔质量,由图③可知该反应
/D.在不同的密闭容器中,1mol 和足量 C 发生反应: ,维
持温度不变,反应相同时间后,各容器测得 百分含量的变化如图④所示,则只有 F 点为平衡点
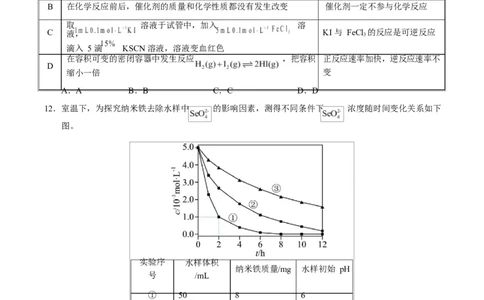
11.从下列实验事实所引出的相应结论正确的是
选
实验事实 结论
项
其他条件相同, 溶液与稀硫酸反应时, 溶液浓度 当其他条件不变时,增大反应物
A
越大,析出 S 沉淀所需时间越短 浓度,化学反应速率加快
B 在化学反应前后,催化剂的质量和化学性质都没有发生改变 催化剂一定不参与化学反应
取 溶液于试管中,加入 溶
C 液, KI 与 FeCl 的反应是可逆反应
3
滴入 5 滴 KSCN 溶液,溶液变血红色
在容积可变的密闭容器中发生反应 ,把容积 正反应速率加快,逆反应速率不
D
缩小一倍 变
A.A B.B C.C D.D
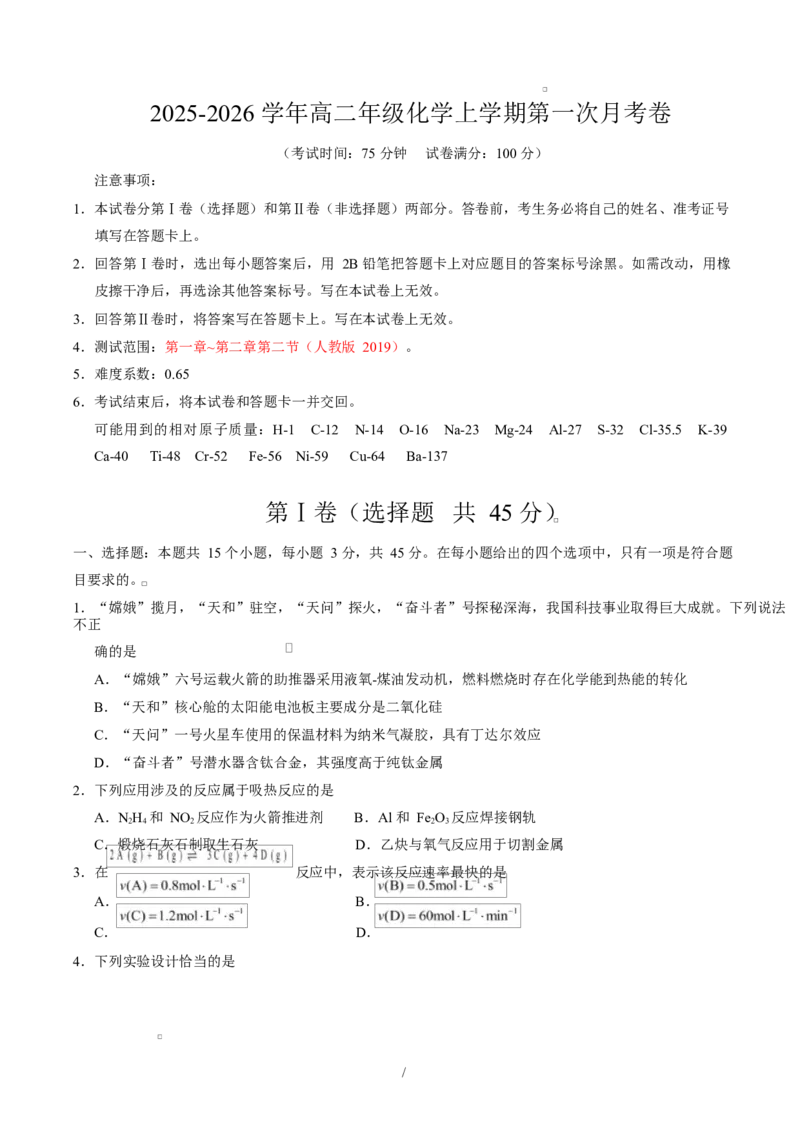
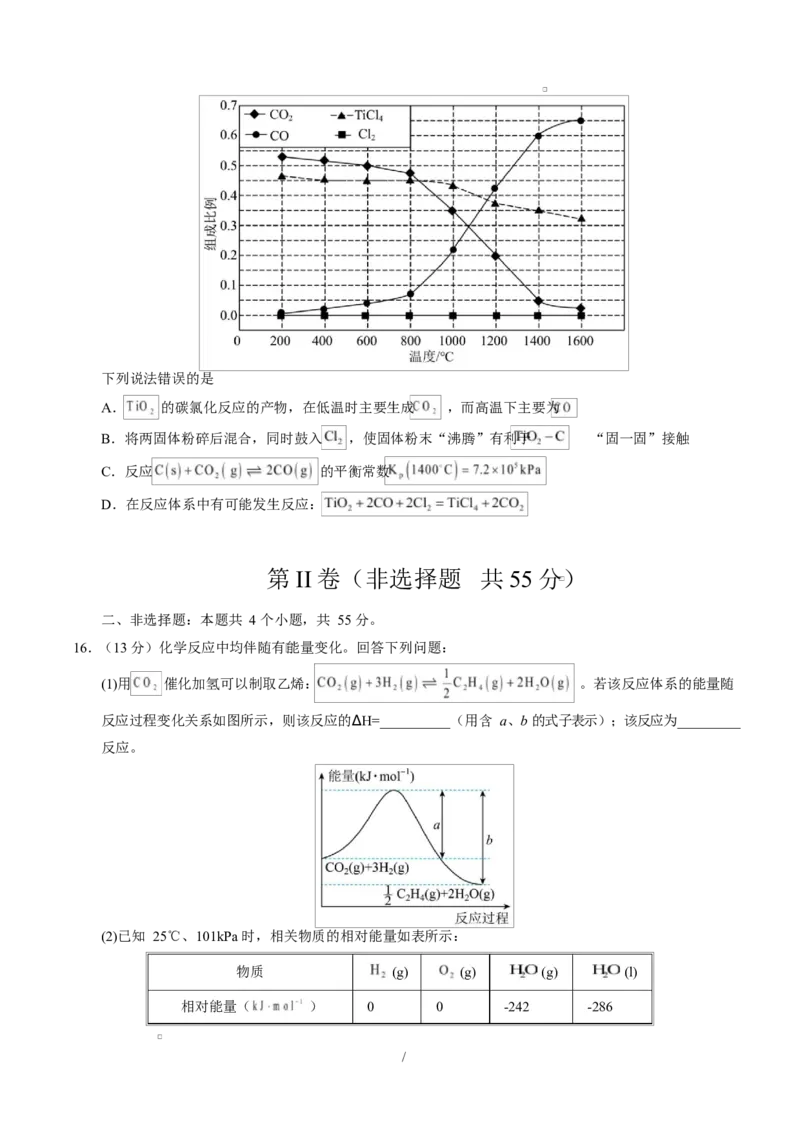
12.室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下 浓度随时间变化关系如下
图。
实验序 水样体积
纳米铁质量/mg 水样初始 pH
号 /mL
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.其他条件相同时,水样初始 pH 越小, 的去除效果越好
B.其他条件相同时,适当增加纳米铁质量可加快反应速率
C.实验①中,0~2 小时内平均反应速率 v( )=5.0×10-6 mol/(L· h)
D.实验③中,反应的离子方程式为:
/13.水煤气变换反应为 。我国学者结合实验与计算机模拟结果,研究了在
金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。下列
说法错误的是
A.水煤气变换反应的
B.步骤②存在 键的形成
C.该反应的决速步是
D.步骤⑤的化学方程式为:
14.在两个容积均为 4L 的恒容密闭容器中,起始时均充入 0.4mol 乙苯,以温度、催化剂为实验条件变量,
发生反应: (g) (g)+H(g)。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相
2
同时间 ts 且未达到化学平衡时乙苯的转化率,下列说法错误的是
A.900℃时,无催化剂的容器中,ts 内 的平均反应速率为
B.1100℃时,曲线Ⅱ、Ⅲ几乎重合,可能是因为催化剂失活
C.1000℃时,有催化剂的容器中,延长反应时间乙苯的转化率无法到达 A 点
D.其他条件不变时,降低温度或增大压强均能使平衡向左移动,均能使平衡常数 K 减小
15.在 下,将 以物质的量之比 进行反应。发生的主要反应如下:I.
Ⅱ.
体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
/下列说法错误的是
A. 的碳氯化反应的产物,在低温时主要生成 ,而高温下主要为
B.将两固体粉碎后混合,同时鼓入 ,使固体粉末“沸腾”有利于 “固一固”接触
C.反应 的平衡常数
D.在反应体系中有可能发生反应:
第 II 卷(非选择题 共 55 分)
二、非选择题:本题共 4 个小题,共 55 分。
16.(13 分)化学反应中均伴随有能量变化。回答下列问题:
(1)用 催化加氢可以制取乙烯: 。若该反应体系的能量随
反应过程变化关系如图所示,则该反应的∆H=__________(用含 a、b 的式子表示);该反应为_________
反应。
(2)已知 25℃、101kPa 时,相关物质的相对能量如表所示:
物质 (g) (g) (g) (l)
相对能量( ) 0 0 -242 -286
/表示 (g)燃烧热的热化学方程式为__________。
(3)二甲醚( )是重要的化工原料,也可用 CO 和 制得,总反应的热化学方程式如下:
∆H=-206.0 。
工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行:
ⅰ.甲醇合成反应:_。
ⅱ.甲醇脱水反应: ∆H=-24.0
①补全甲醇合成反应的热化学方程式:___________。
②若起始时向容器中投入 2mol CO 和 4mol ,测得某时刻上述总反应中放出的热量为 51.5kJ,此时
CO 的转化率为__________。
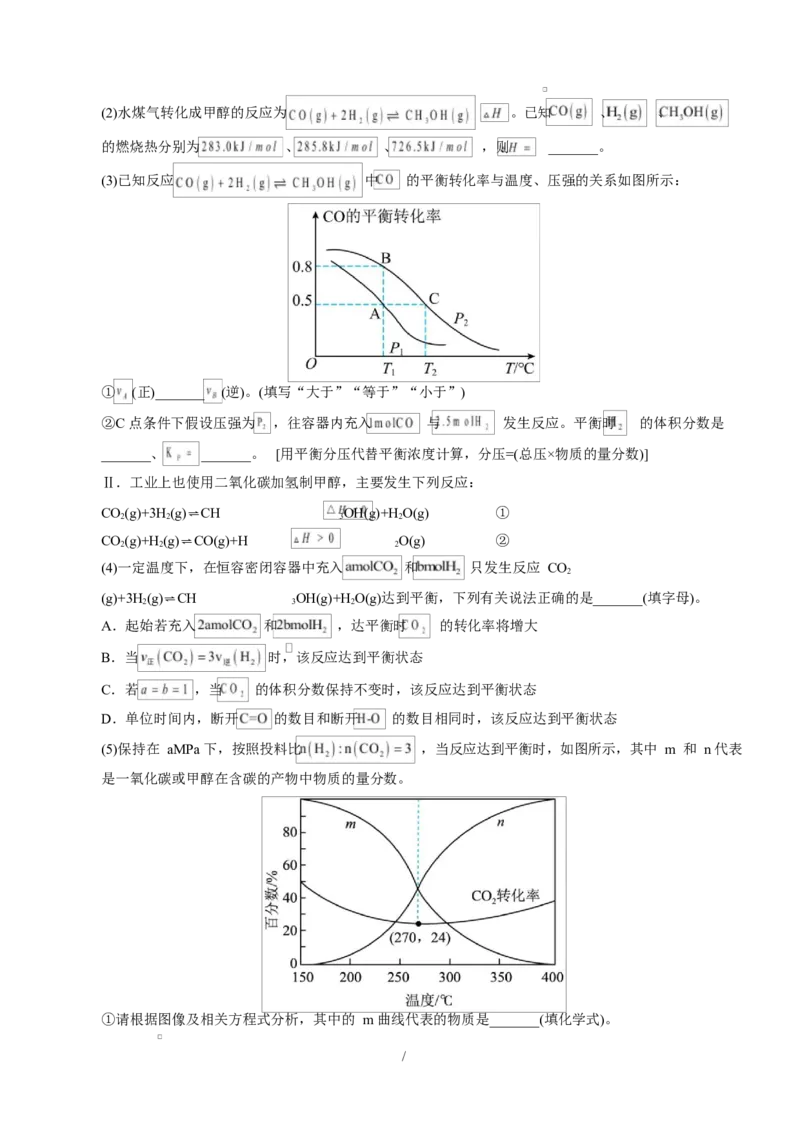
(4)实验室用 50mL 0.50 盐酸与 50mL 0.50 NaOH 溶液在如图所示装置中反应,通过测定
该反应过程中放出的热量计算中和反应的反应热。该装置还缺少一种玻璃仪器,该仪器名称为
__________;25℃、101kPa 时,稀盐酸与稀 NaOH 溶液反应生成 1mol 水放出的热量为 57.3kJ,则 0.1
的醋酸溶液与0.1 的 NaOH溶液液反应生成1mol水放出的热量__________(填“大于”“小
于”或“等于”)57.3kJ。
17.(14 分)甲醇是一种重要的化工原料,具有广阔的开发和应用前景。
I.工业上使用水煤气( 与 的混合气体)转化成甲醇( )。
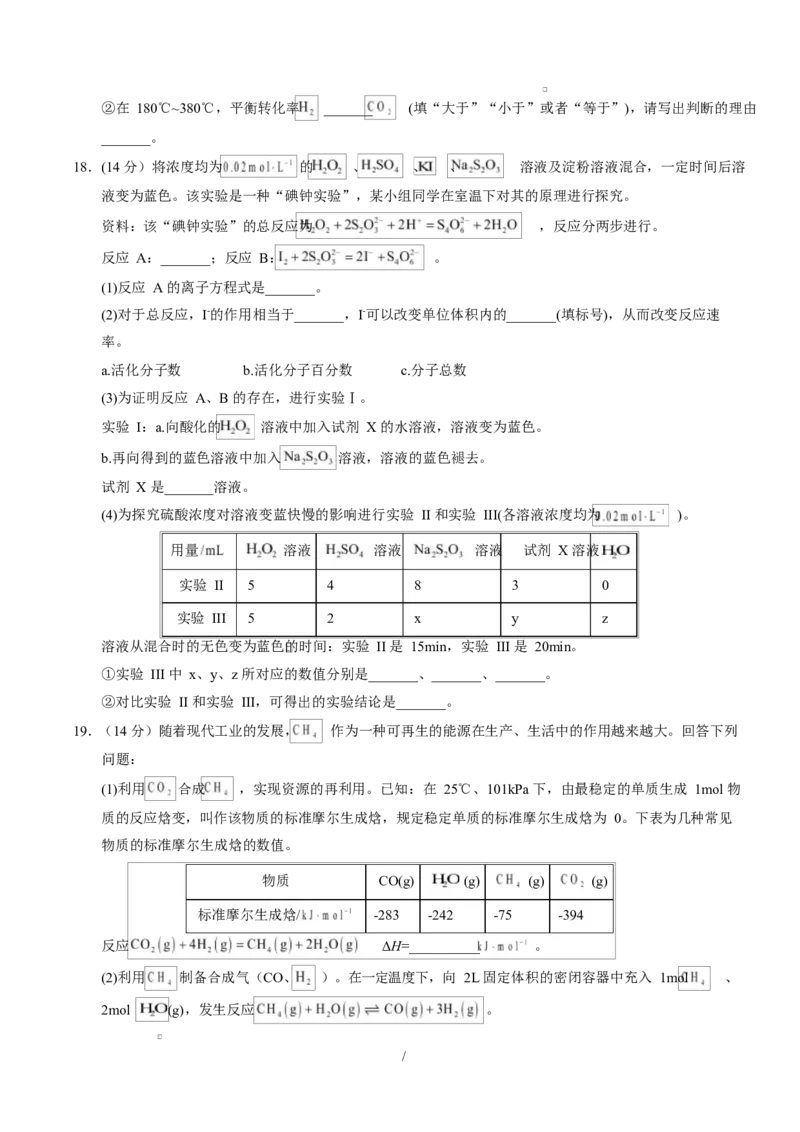
(1)我国科学家合成了一种新型 材料,实现了低温催化水煤气变换。反应历程如图所示,其
中吸附在催化剂表面的物种用“*”标注,TS 指过渡态。
请写出该历程中慢反应的化学方程式_______。
/(2)水煤气转化成甲醇的反应为 。已知 、 、
的燃烧热分别为 、 、 ,则 _______。
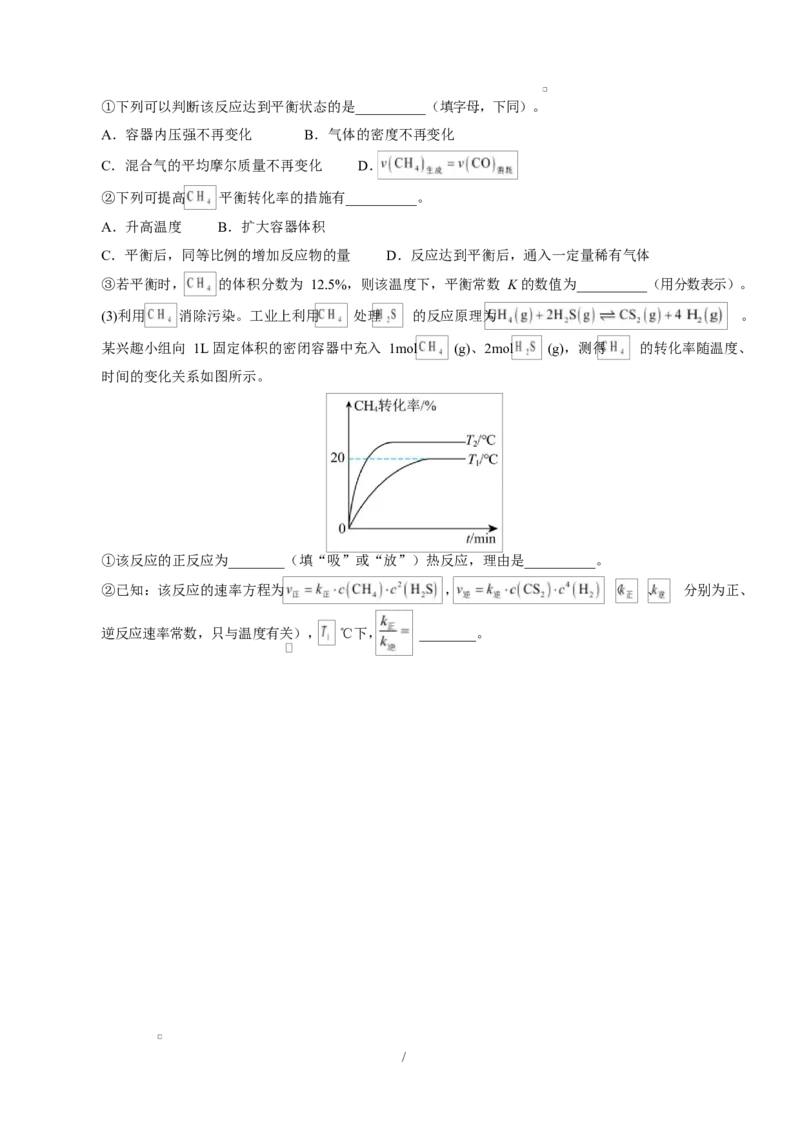
(3)已知反应 中 的平衡转化率与温度、压强的关系如图所示:
① (正)_______ (逆)。(填写“大于”“等于”“小于”)
②C 点条件下假设压强为 ,往容器内充入 与 发生反应。平衡时 的体积分数是
_______、 _______。 [用平衡分压代替平衡浓度计算,分压=(总压×物质的量分数)]
Ⅱ.工业上也使用二氧化碳加氢制甲醇,主要发生下列反应:
CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) ①
CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ②
(4)一定温度下,在恒容密闭容器中充入 和 只发生反应 CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g)达到平衡,下列有关说法正确的是_______(填字母)。
A.起始若充入 和 ,达平衡时 的转化率将增大
B.当 时,该反应达到平衡状态
C.若 ,当 的体积分数保持不变时,该反应达到平衡状态
D.单位时间内,断开 的数目和断开 的数目相同时,该反应达到平衡状态
(5)保持在 aMPa 下,按照投料比 ,当反应达到平衡时,如图所示,其中 m 和 n 代表
是一氧化碳或甲醇在含碳的产物中物质的量分数。
①请根据图像及相关方程式分析,其中的 m 曲线代表的物质是_______(填化学式)。
/②在 180℃~380℃,平衡转化率 _______ (填“大于”“小于”或者“等于”),请写出判断的理由
_______。
18.(14 分)将浓度均为 的 、 、 、 溶液及淀粉溶液混合,一定时间后溶
液变为蓝色。该实验是一种“碘钟实验”,某小组同学在室温下对其的原理进行探究。
资料:该“碘钟实验”的总反应为 ,反应分两步进行。
反应 A:_______;反应 B: 。
(1)反应 A 的离子方程式是_______。
(2)对于总反应,I-的作用相当于_______,I-可以改变单位体积内的_______(填标号),从而改变反应速
率。
a.活化分子数 b.活化分子百分数 c.分子总数
(3)为证明反应 A、B 的存在,进行实验Ⅰ。
实验 I:a.向酸化的 溶液中加入试剂 X 的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入 溶液,溶液的蓝色褪去。
试剂 X 是_______溶液。
(4)为探究硫酸浓度对溶液变蓝快慢的影响进行实验 II 和实验 III(各溶液浓度均为 )。
用量 溶液 溶液 溶液 试剂 X 溶液
实验 II 5 4 8 3 0
实验 III 5 2 x y z
溶液从混合时的无色变为蓝色的时间:实验 II 是 15min,实验 III 是 20min。
①实验 III 中 x、y、z 所对应的数值分别是_______、_______、_______。
②对比实验 II 和实验 III,可得出的实验结论是_______。
19.(14 分)随着现代工业的发展, 作为一种可再生的能源在生产、生活中的作用越来越大。回答下列
问题:
(1)利用 合成 ,实现资源的再利用。已知:在 25℃、101kPa 下,由最稳定的单质生成 1mol 物
质的反应焓变,叫作该物质的标准摩尔生成焓,规定稳定单质的标准摩尔生成焓为 0。下表为几种常见
物质的标准摩尔生成焓的数值。
物质 CO(g) (g) (g) (g)
标准摩尔生成焓/ -283 -242 -75 -394
反应 ΔH=__________ 。
(2)利用 制备合成气(CO、 )。在一定温度下,向 2L 固定体积的密闭容器中充入 1mol 、
2mol (g),发生反应 。
/①下列可以判断该反应达到平衡状态的是__________(填字母,下同)。
A.容器内压强不再变化 B.气体的密度不再变化
C.混合气的平均摩尔质量不再变化 D.
②下列可提高 平衡转化率的措施有__________。
A.升高温度 B.扩大容器体积
C.平衡后,同等比例的增加反应物的量 D.反应达到平衡后,通入一定量稀有气体
③若平衡时, 的体积分数为 12.5%,则该温度下,平衡常数 K 的数值为__________(用分数表示)。
(3)利用 消除污染。工业上利用 处理 的反应原理为 。
某兴趣小组向 1L 固定体积的密闭容器中充入 1mol (g)、2mol (g),测得 的转化率随温度、
时间的变化关系如图所示。
①该反应的正反应为________(填“吸”或“放”)热反应,理由是__________。
②已知:该反应的速率方程为 , ( 、 分别为正、
逆反应速率常数,只与温度有关), ℃下, ________。
/