文档内容
高二化学期末试题
一、单选题:本大题共16小题,共48分。
1. 明代宋应星所著《天工开物》中详细介绍了竹纸的制造工艺流程,其中“煮楻足火”工序是指加入石灰蒸煮以除去
竹料中的木质素、树胶等杂质。另外,为了防止书写时墨迹在纸面扩散,古代及现代造纸都要加入一些矿物性白粉填
充纸纤维之间的孔隙。下列说法中错误的是
A. 纸的主要化学成分为纤维素,纤维素属于多糖
B. 纸张中的纤维素之间是通过氢键和范德华力相结合的
C. 纸张燃烧后产生的灰白色部分主要成分为碳
D. 推测木质素分子中可能含有酸性官能团
2. 湖北省博物馆的镇馆之宝——曾侯乙编钟由青铜所铸。下列说法错误的是
.
A 青铜属于合金,硬度比纯铜大
B. 青铜器露置于空气中会发生电化学腐蚀而“生锈”
C. “青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
D. 现代工艺采用电解精炼提纯铜,用纯铜作阳极、粗铜作阴极
3. 利用CO可以合成化工原料COCl 、配合物Fe(CO) 等,下列说法不正确的是
2 5
A. COCl 分子内含有σ键和π键
2
B. 在一定条件下发生反应: ,过程中断裂配位键,形成金属键
C. CO分子与N、 含有相同电子数
2
D. Fe(CO) 中铁的化合价为0,其基态原子的价电子排布式3d6
5
4. 屠呦呦等人使用乙醚从中药中提取并分离得到青蒿素(相对分子质量为282,分子式为C H O),并测定了青蒿素
15 22 5
的分子结构。下列说法正确的是
A. 青蒿素是一种高分子化合物
B. “使用乙醚从中药中提取青蒿素”利用了萃取原理
C. 利用元素分析和红外光谱法能确定青蒿素的分子式
D. 仅利用核磁共振氢谱能确定青蒿素的相对分子质量
5. 化学与生产、生活密切相关。下列说法错误的是
A. 蛋白质、纤维素、核酸均属生物大分子,均能发生水解反应
B. 可用浓硝酸区分天然蚕丝与人造丝
C. 合成纤维、人造纤维及碳纤维不都属于有机高分子材料
D. 煮鸡蛋、以粮食为原料酿酒、紫外线杀菌消毒都主要涉及蛋白质变性
6. 按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转变成所需产物,原子利用率为100%。以下反应中符合绿色化学原则的是
A. 甲苯与氯气制备氯甲苯
B. 苯酚与甲醛制备酚醛树脂
.
C 环己醇与浓硫酸制备环己烯
D. 乙烯与氧气在银催化作用下生成环氧乙烷( )
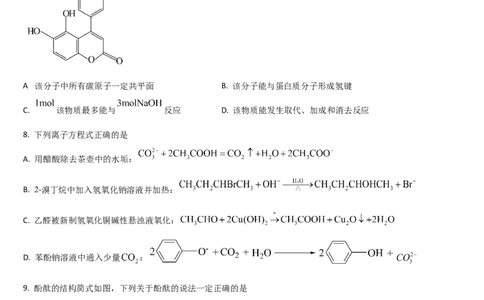
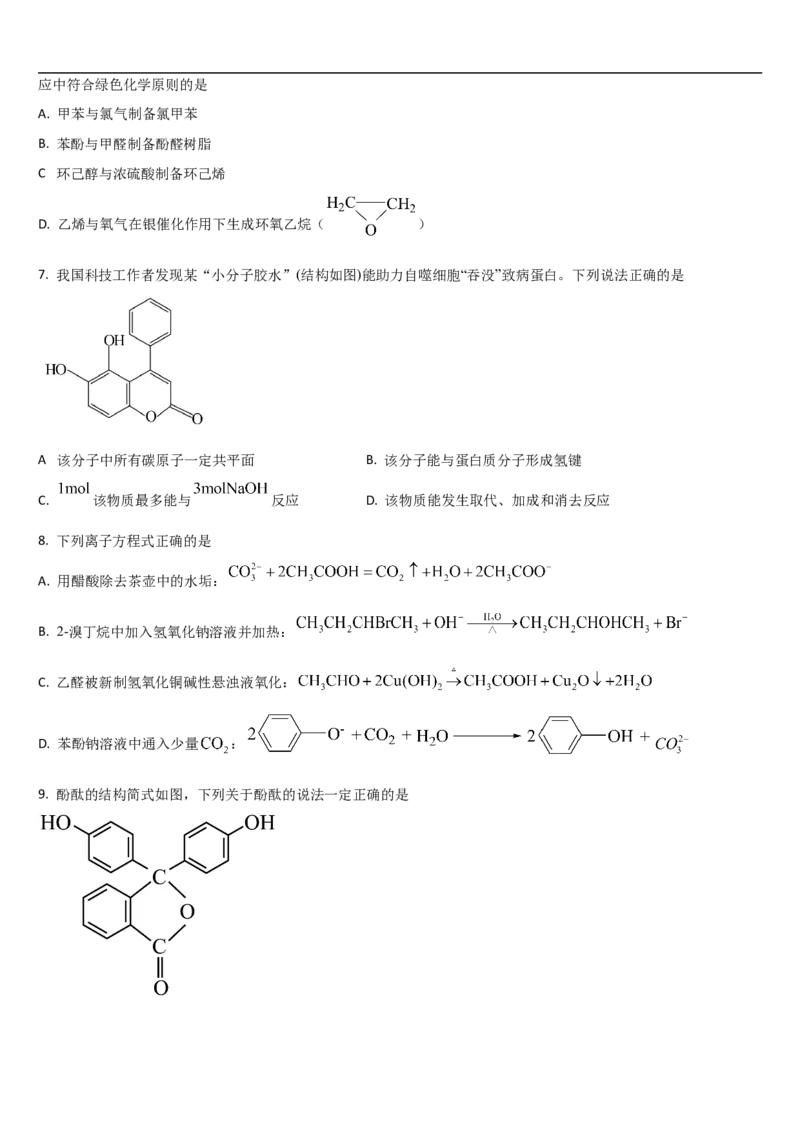
7. 我国科技工作者发现某“小分子胶水”(结构如图)能助力自噬细胞“吞没”致病蛋白。下列说法正确的是
.
A 该分子中所有碳原子一定共平面 B. 该分子能与蛋白质分子形成氢键
C. 该物质最多能与 反应 D. 该物质能发生取代、加成和消去反应
8. 下列离子方程式正确的是
A. 用醋酸除去茶壶中的水垢:
B. 2-溴丁烷中加入氢氧化钠溶液并加热:
C. 乙醛被新制氢氧化铜碱性悬浊液氧化:
D. 苯酚钠溶液中通入少量 :
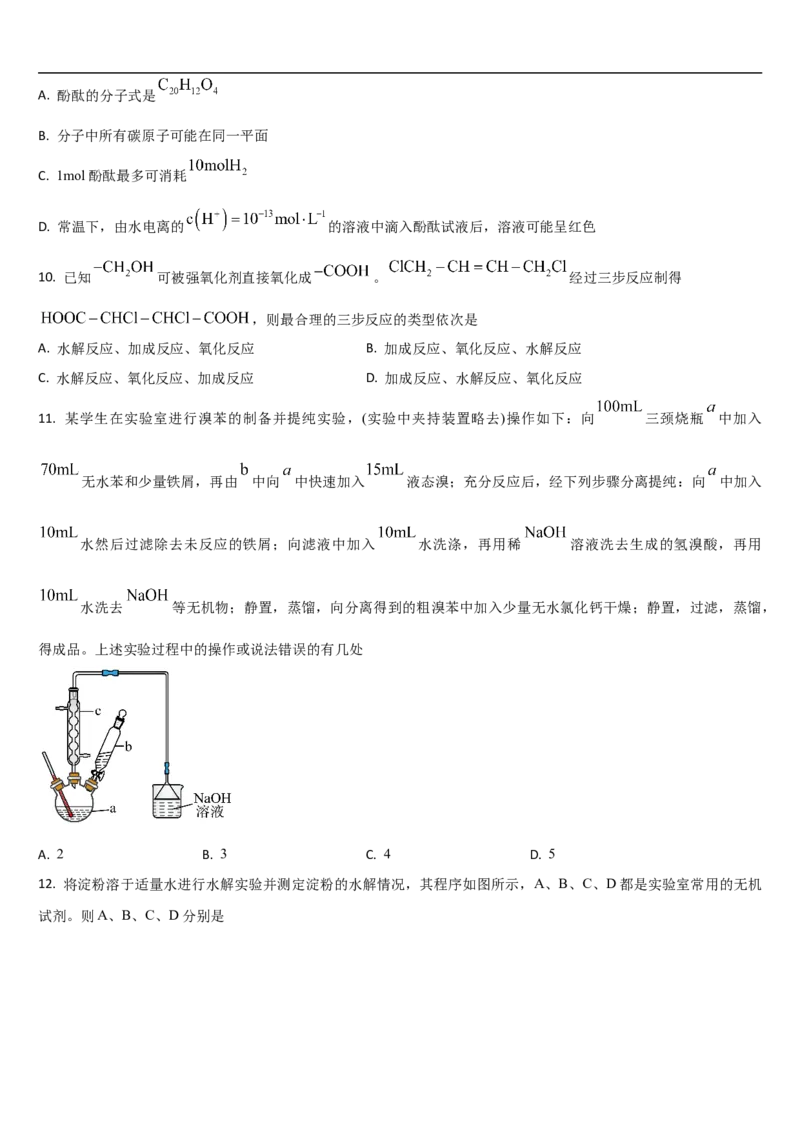
9. 酚酞的结构简式如图,下列关于酚酞的说法一定正确的是A. 酚酞的分子式是
B. 分子中所有碳原子可能在同一平面
C. 1mol酚酞最多可消耗
D. 常温下,由水电离的 的溶液中滴入酚酞试液后,溶液可能呈红色
10. 已知 可被强氧化剂直接氧化成 。 经过三步反应制得
,则最合理的三步反应的类型依次是
A. 水解反应、加成反应、氧化反应 B. 加成反应、氧化反应、水解反应
C. 水解反应、氧化反应、加成反应 D. 加成反应、水解反应、氧化反应
11. 某学生在实验室进行溴苯的制备并提纯实验,(实验中夹持装置略去)操作如下:向 三颈烧瓶 中加入
无水苯和少量铁屑,再由 中向 中快速加入 液态溴;充分反应后,经下列步骤分离提纯:向 中加入
水然后过滤除去未反应的铁屑;向滤液中加入 水洗涤,再用稀 溶液洗去生成的氢溴酸,再用
水洗去 等无机物;静置,蒸馏,向分离得到的粗溴苯中加入少量无水氯化钙干燥;静置,过滤,蒸馏,
得成品。上述实验过程中的操作或说法错误的有几处
A. 2 B. 3 C. 4 D. 5
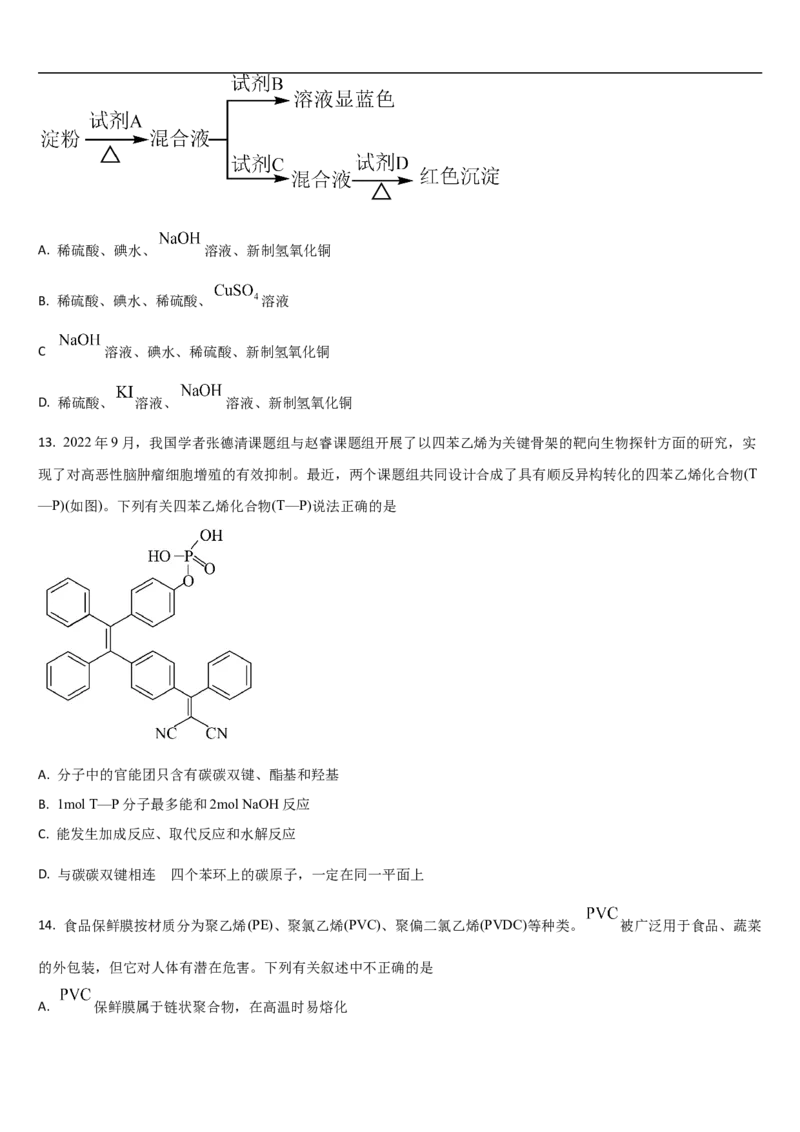
12. 将淀粉溶于适量水进行水解实验并测定淀粉的水解情况,其程序如图所示,A、B、C、D都是实验室常用的无机
试剂。则A、B、C、D分别是A. 稀硫酸、碘水、 溶液、新制氢氧化铜
B. 稀硫酸、碘水、稀硫酸、 溶液
.
C 溶液、碘水、稀硫酸、新制氢氧化铜
D. 稀硫酸、 溶液、 溶液、新制氢氧化铜
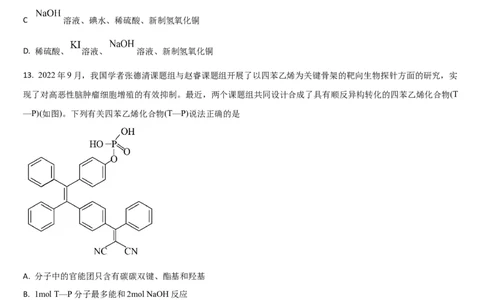
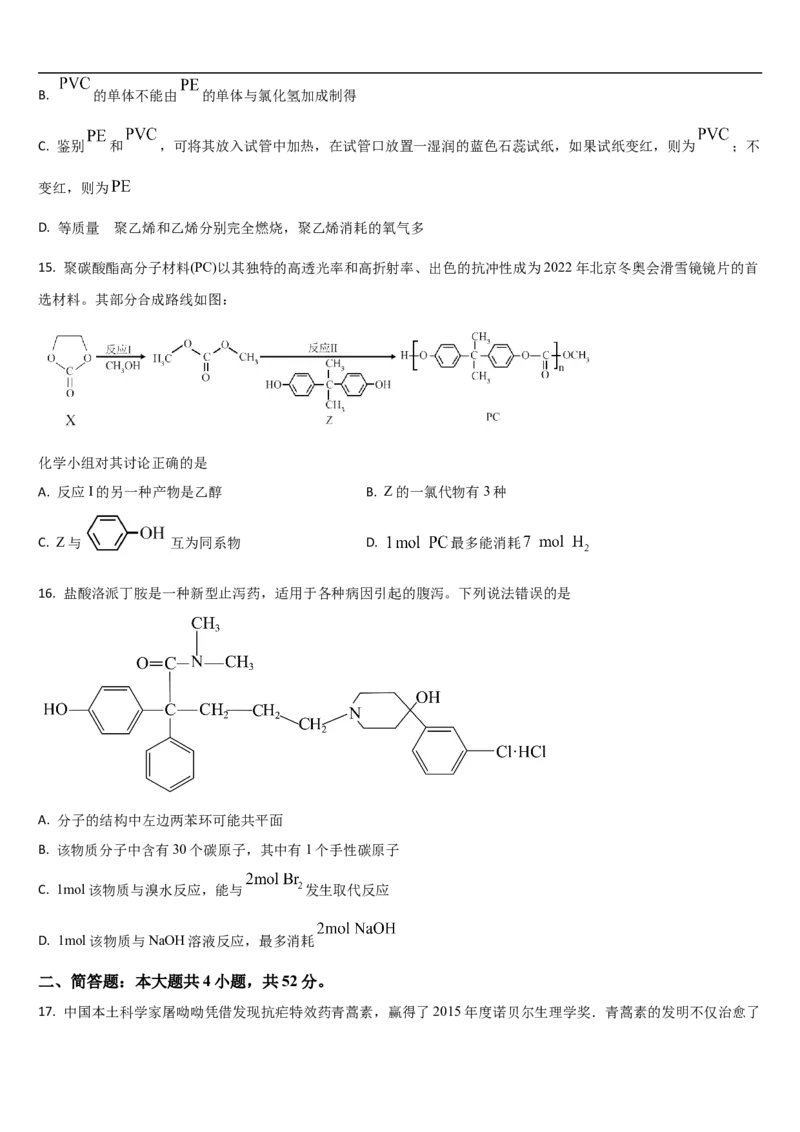
13. 2022年9月,我国学者张德清课题组与赵睿课题组开展了以四苯乙烯为关键骨架的靶向生物探针方面的研究,实
现了对高恶性脑肿瘤细胞增殖的有效抑制。最近,两个课题组共同设计合成了具有顺反异构转化的四苯乙烯化合物(T
—P)(如图)。下列有关四苯乙烯化合物(T—P)说法正确的是
A. 分子中的官能团只含有碳碳双键、酯基和羟基
B. 1mol T—P分子最多能和2mol NaOH反应
C. 能发生加成反应、取代反应和水解反应
的
D. 与碳碳双键相连 四个苯环上的碳原子,一定在同一平面上
14. 食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类。 被广泛用于食品、蔬菜
的外包装,但它对人体有潜在危害。下列有关叙述中不正确的是
A. 保鲜膜属于链状聚合物,在高温时易熔化B. 的单体不能由 的单体与氯化氢加成制得
C. 鉴别 和 ,可将其放入试管中加热,在试管口放置一湿润的蓝色石蕊试纸,如果试纸变红,则为 ;不
变红,则为
的
D. 等质量 聚乙烯和乙烯分别完全燃烧,聚乙烯消耗的氧气多
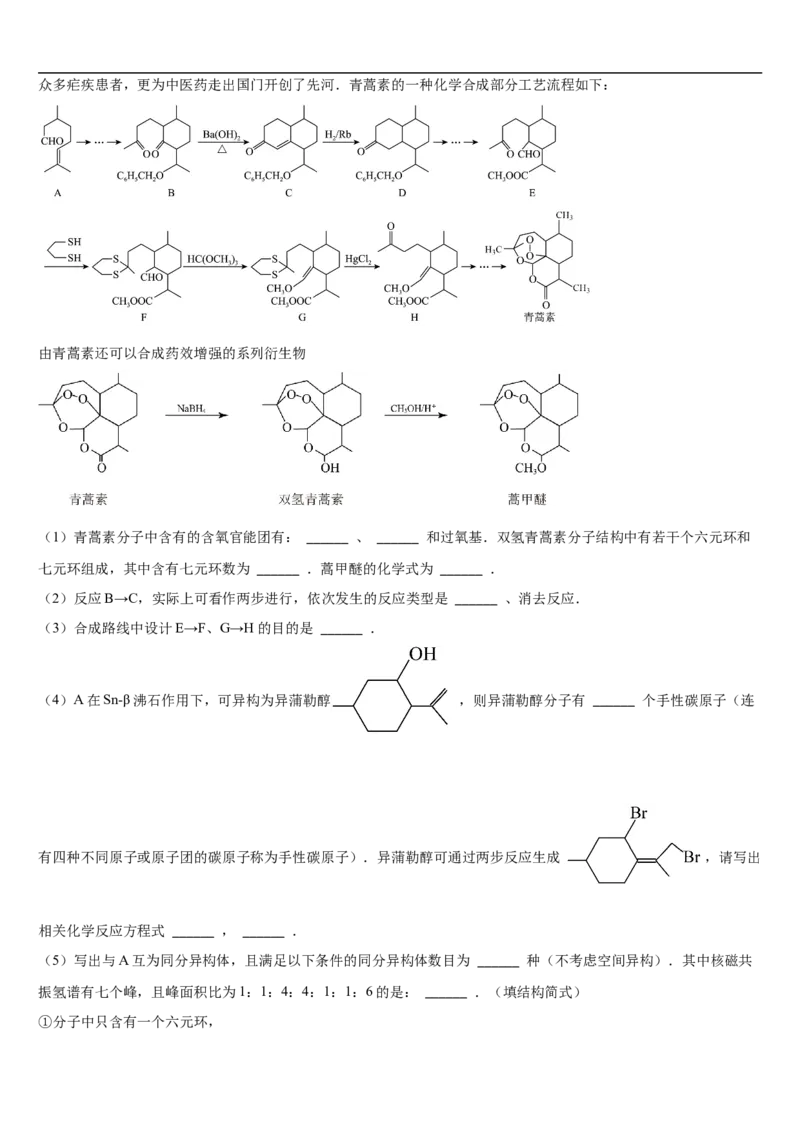
15. 聚碳酸酯高分子材料(PC)以其独特的高透光率和高折射率、出色的抗冲性成为2022年北京冬奥会滑雪镜镜片的首
选材料。其部分合成路线如图:
化学小组对其讨论正确的是
A. 反应I的另一种产物是乙醇 B. Z的一氯代物有3种
C. Z与 互为同系物 D. 最多能消耗
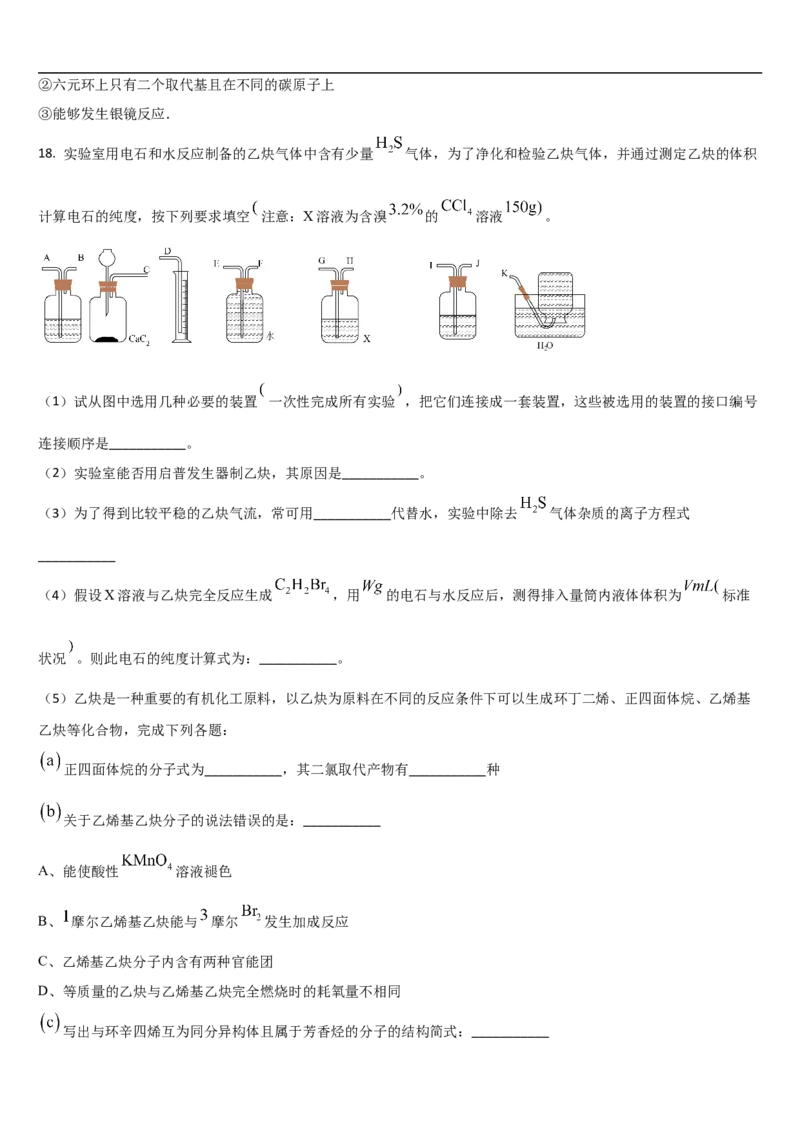
16. 盐酸洛派丁胺是一种新型止泻药,适用于各种病因引起的腹泻。下列说法错误的是
A. 分子的结构中左边两苯环可能共平面
B. 该物质分子中含有30个碳原子,其中有1个手性碳原子
C. 1mol该物质与溴水反应,能与 发生取代反应
D. 1mol该物质与NaOH溶液反应,最多消耗
二、简答题:本大题共4小题,共52分。
17. 中国本土科学家屠呦呦凭借发现抗疟特效药青蒿素,赢得了2015年度诺贝尔生理学奖.青蒿素的发明不仅治愈了众多疟疾患者,更为中医药走出国门开创了先河.青蒿素的一种化学合成部分工艺流程如下:
由青蒿素还可以合成药效增强的系列衍生物
(1)青蒿素分子中含有的含氧官能团有: ______ 、 ______ 和过氧基.双氢青蒿素分子结构中有若干个六元环和
七元环组成,其中含有七元环数为 ______ .蒿甲醚的化学式为 ______ .
(2)反应B→C,实际上可看作两步进行,依次发生的反应类型是 ______ 、消去反应.
(3)合成路线中设计E→F、G→H的目的是 ______ .
(4)A在Sn-β沸石作用下,可异构为异蒲勒醇 ,则异蒲勒醇分子有 ______ 个手性碳原子(连
有四种不同原子或原子团的碳原子称为手性碳原子).异蒲勒醇可通过两步反应生成 ,请写出
相关化学反应方程式 ______ , ______ .
(5)写出与A互为同分异构体,且满足以下条件的同分异构体数目为 ______ 种(不考虑空间异构).其中核磁共
振氢谱有七个峰,且峰面积比为1:1:4:4:1:1:6的是: ______ .(填结构简式)
①分子中只含有一个六元环,②六元环上只有二个取代基且在不同的碳原子上
③能够发生银镜反应.
18. 实验室用电石和水反应制备的乙炔气体中含有少量 气体,为了净化和检验乙炔气体,并通过测定乙炔的体积
计算电石的纯度,按下列要求填空 注意:X溶液为含溴 的 溶液 。
(1)试从图中选用几种必要的装置 一次性完成所有实验 ,把它们连接成一套装置,这些被选用的装置的接口编号
连接顺序是___________。
(2)实验室能否用启普发生器制乙炔,其原因是___________。
(3)为了得到比较平稳的乙炔气流,常可用___________代替水,实验中除去 气体杂质的离子方程式
___________
(4)假设X溶液与乙炔完全反应生成 ,用 的电石与水反应后,测得排入量筒内液体体积为 标准
状况 。则此电石的纯度计算式为:___________。
(5)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以生成环丁二烯、正四面体烷、乙烯基
乙炔等化合物,完成下列各题:
正四面体烷的分子式为___________,其二氯取代产物有___________种
关于乙烯基乙炔分子的说法错误的是:___________
A、能使酸性 溶液褪色
B、 摩尔乙烯基乙炔能与 摩尔 发生加成反应
C、乙烯基乙炔分子内含有两种官能团
D、等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:___________写出与苯互为同系物且一氯代物只有两种的物质的结构简式 举两例 :___________、___________。
19. 完成下列问题。
(1)在配合物[Cu(NH )]SO 中,___________是中心离子,提供电子对形成配位键的原子是___________。
3 4 4
(2)基态Cr原子的核外电子排布式为___________。
(3)下列羧酸:①CFCOOH ②CHCOOH ③CHFCOOH ④CHClCOOH ⑤CHCHCOOH,酸性由强到弱的顺序为
3 3 2 2 3 2
___________(填标号)。
(4)石墨晶体中横向与纵向的导电性不同,这说明晶体性质表现___________。
a.自范性 b.各向异性 c.各向同性
(5)基态硫原子占据最高能级的电子云轮廓图形状为___________。
(6)下列有关超分子的说法正确的是_______。。
A.超分子是由两个或两个以上分子通过分子间相互作用形成的分子聚集体
B.细胞膜中的磷脂分子的双层膜结构、冠醚与金属离子的聚集体都能看作超分子
C.分离C 和C 时,先是杯酚和C 形成超分子
60 70 70
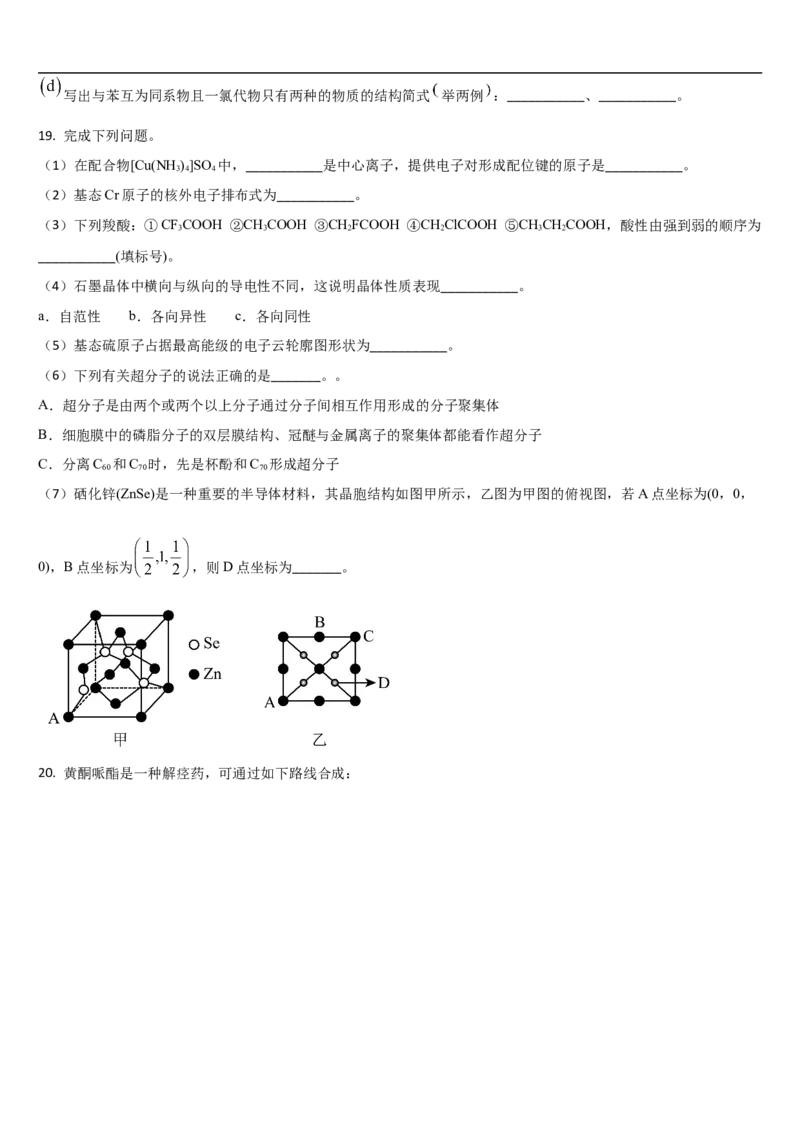
(7)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,
0),B点坐标为 ,则D点坐标为_______。
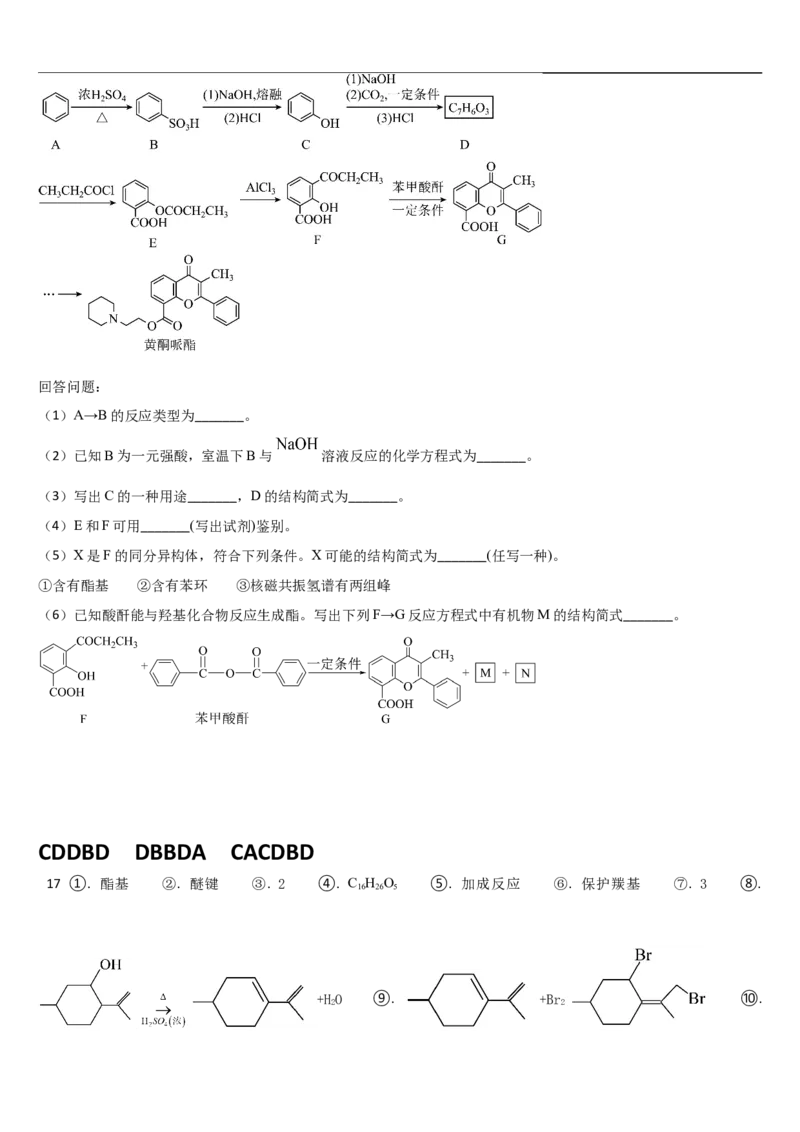
20. 黄酮哌酯是一种解痉药,可通过如下路线合成:回答问题:
(1)A→B的反应类型为_______。
(2)已知B为一元强酸,室温下B与 溶液反应的化学方程式为_______。
(3)写出C的一种用途_______,D的结构简式为_______。
(4)E和F可用_______(写出试剂)鉴别。
(5)X是F的同分异构体,符合下列条件。X可能的结构简式为_______(任写一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中有机物M的结构简式_______。
CDDBD DBBDA CACDBD
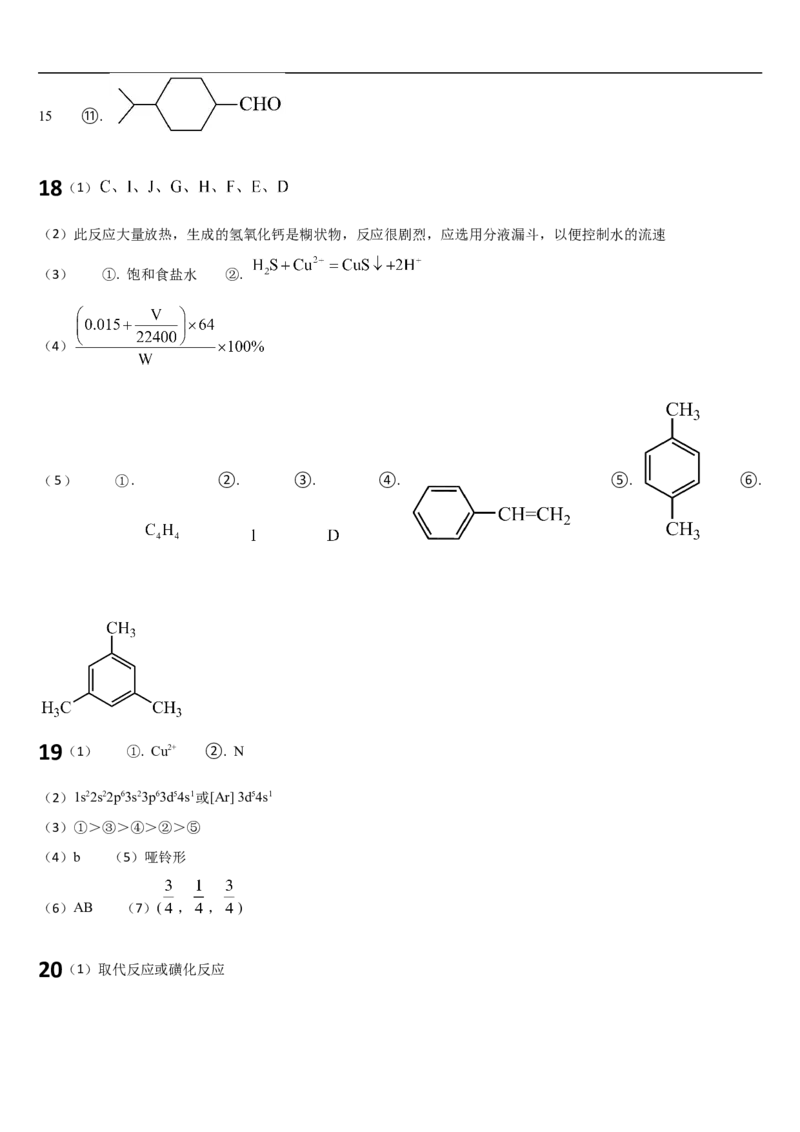
17 ①. 酯基 ②. 醚键 ③. 2 ④. C H O ⑤. 加成反应 ⑥. 保护羰基 ⑦. 3 ⑧.
16 26 5
+HO ⑨. +Br ⑩.
2 215 ⑪.
18(1)
(2)此反应大量放热,生成的氢氧化钙是糊状物,反应很剧烈,应选用分液漏斗,以便控制水的流速
(3) ①. 饱和食盐水 ②.
(4)
(5) ①. ②. ③. ④. ⑤. ⑥.
19(1) ①. Cu2+ ②. N
(2)1s22s22p63s23p63d54s1或[Ar] 3d54s1
(3)①>③>④>②>⑤
(4)b (5)哑铃形
(6)AB (7)( , , )
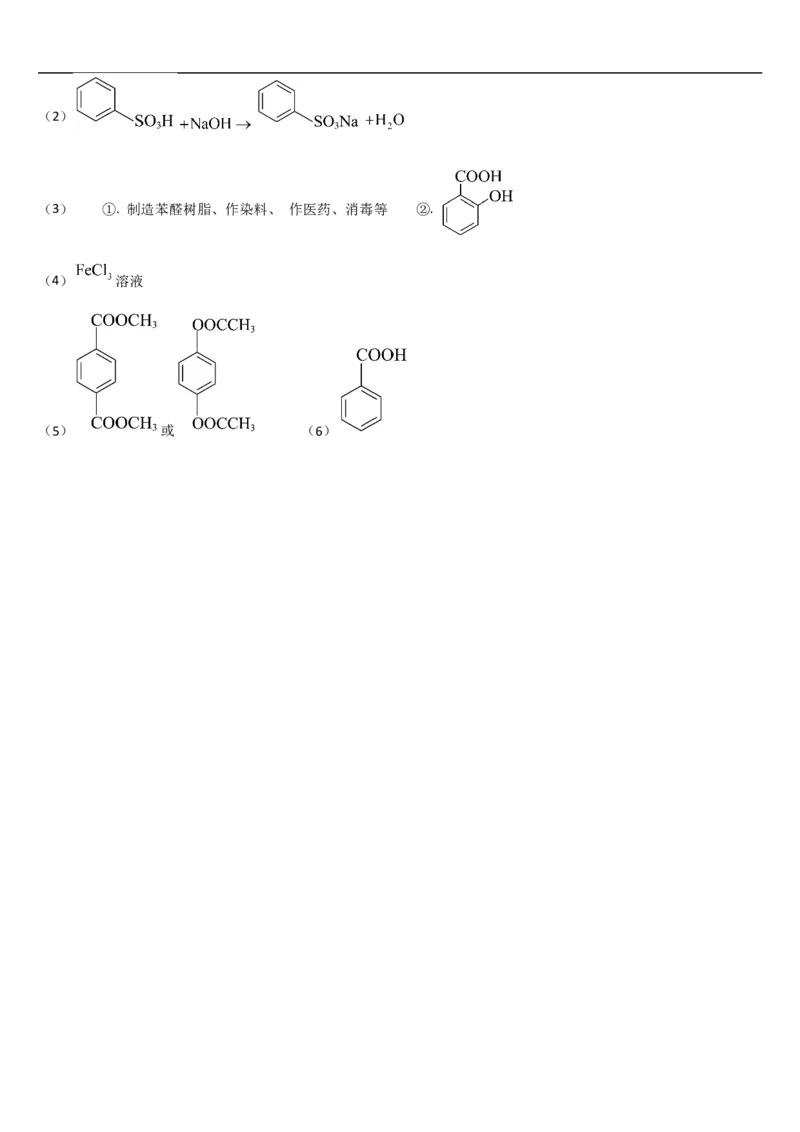
20(1)取代反应或磺化反应(2)
(3) ①. 制造苯醛树脂、作染料、 作医药、消毒等 ②.
(4) 溶液
(5) 或 (6)