文档内容
让更多的孩子得到更好的教育
中考总复习:综合计算技巧(提高)
撰稿:李伟 审稿:熊亚军
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
1.13.5g某不纯CuCl 样品溶于水后,与足量的AgNO 溶液反应,生成沉淀的质量为29g,则样品中可能混
2 3
有的杂质为( )
A.NaCl B. ZnCl C.KCl D.FeCl
2 3
2. 某硝酸铵(NH NO )样品,测知含氮量为37%,则样品中含有的杂质可能是( )
4 3
A.(NH )SO B. CO(NH ) C. NH HCO D. NHCl
4 2 4 2 2 4 3 4
3. 有一瓶久置的过氧化氢溶液,为测定其溶质的质量分数,取该溶液100g,向其中加入10g二氧化锰粉末.
过氧化氢全部反应后,称得剩余物质的质量为106.8g,则此瓶过氧化氢溶液中溶质的质量分数为( )
A.3.2% B.3.4% C.6.8% D.10.2%
4. (2012大庆)把2gMgO加入到100g7.3%的稀盐酸中,使其充分反应,再加入 10%的NaOH溶液使
Mg2+恰好沉淀完全,则所需NaOH溶液的质量为( )
A.60g B.40g C.80g D.100g
5. 经测定KClO、KCl、MnO 的混合物中钾元素质量分数为39%,某同学把100g该混合物充分加热完全
3 2
反应后,再将剩余固体完全溶于水经过滤洗涤干燥后称得黑色固体20.7g.请你推算加热该混合物时产生
氧气的总质量是( )
A.4.8 g B.9.6 g C.19.2 g D.48 g
6. 在托盘天平的烧杯中,分别盛有等质量,等质量分数足量的稀盐酸,天平平衡。向左盘烧杯中加入10.2g
碳酸镁和氢氧化镁的混合物,右盘烧杯中加入8g铜,充分反应后,天平重新平衡,则混合物中氢氧化镁的
质量为( )
A.1.8g B.2.2g C.6g D.8g
二、填空题
7. 2011年3月11日,日本发生里氏9.0级地震,地震造成当地很多人无家可归。为了防止灾后疫情的发生,
医务人员每天需要喷洒大量的过氧乙酸(化学式为C HO)消毒液。请计算:
2 4 3
(1)过氧乙酸中碳、氢、氧元素的质量比为__________。
(2)要配制280 kg溶质质量分数为0.5%的过氧乙酸消毒液,需要溶质质量分数为 20%的过氧乙酸溶液的
质量为_________kg。
8(. 2012铁岭)黄铜是铜和锌合金。某化学兴趣小组的同学在测定黄铜样品中铜的含量时,取黄铜样品20g
放入烧杯中,向其中加入100g稀硫酸,恰好完全反应.反应后烧杯中剩余物的总质量为119.8g。请计算:
(1)反应产生氢气的质量是______________g。
(2)黄铜样品中铜的质量分数___________。
三、计算题
9.氯化镁是制取镁的原料之一.现要测定某化工产品(含MgCl 和KCl)中所含的氯化镁质量分数,进行实
2
验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充
分振荡,实验所得数据见下表:
编号 1 2 3 4 5
加入氢氧化钾溶液的质量/g 10 10 10 10 10
生成沉淀的质量/g 0.58 a 1.74 2.32 2.32
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共6页让更多的孩子得到更好的教育
请分析上述数据,回答下列问题:
(1)表中a为________。
(2)样品中的氯化钾属于化肥中的______
肥,可回收利用。
(3)所用的氢氧化钾溶液中溶质的质量分数是____________。
(4)计算样品中氯化镁的质量分数是多少?(写出计算过程)
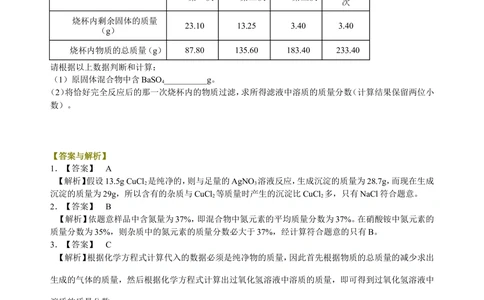
10. 有一包含有BaCO 、BaCl 、BaSO 的固体混合物40g。现进行如下实验:将该固体全部倒入烧坏内,再
3 2 4
分次加入稀盐酸,每次加50g,待每次充分反应后通过精密仪器测定有关的实验数据如下表:
第四
第一次 第二次 第三次
次
烧杯内剩余固体的质量
23.10 13.25 3.40 3.40
(g)
烧杯内物质的总质量(g) 87.80 135.60 183.40 233.40
请根据以上数据判断和计算:
(1)原固体混合物中含BaSO__________g。
4
(2)将恰好完全反应后的那一次烧杯内的物质过滤,求所得滤液中溶质的质量分数(计算结果保留两位小
数)。
【答案与解析】
1.【答案】 A
【解析】假设13.5g CuCl 是纯净的,则与足量的AgNO 溶液反应,生成沉淀的质量为28.7g,而现在生成
2 3
沉淀的质量为29g,所以含有的杂质与CuCl 等质量时产生的沉淀比CuCl 多,只有NaCl符合题意。
2 2
2.【答案】 B
【解析】依题意样品中含氮量为37%,即混合物中氮元素的平均质量分数为37%。在硝酸铵中氮元素的
质量分数为35%,则杂质中的氮元素的质量分数必大于37%,经计算符合题意的只有B。
3.【答案】 C
【解析】根据化学方程式计算代入的数据必须是纯净物的质量,因此首先根据物质的总质量的减少求出
生成的气体的质量,然后根据化学方程式计算出过氧化氢溶液中溶质的质量,即可得到过氧化氢溶液中
溶质的质量分数。
由于物质的总质量的减少就是因为生成了氧气,因此氧气的质量为:100g+10g-106.8g=3.2g。
设这瓶过氧化氢溶液中溶质的质量为x。
2HO 2HO+O↑
2 2 2 2
68 32
x 3.2g
x==6.8g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共6页让更多的孩子得到更好的教育
故过氧化氢溶液中溶质的质量分数为: ×100%=6.8%
4.【答案】 C
【解析】氧化镁可以和盐酸反应,反应后生成的氯化镁可以和氢氧化钠溶液反应,所以可以据此写出这
两个反应的化学方程式,然后找出氧化镁和氢氧化钠的关系,进行求算即可。设2g氧化镁消耗盐酸的质
量为x,则:
MgO+2HCl═MgCl +H O
2 2
40 73
2g x
解得:x=3.65g
剩余的氯化氢的质量为:100g×7.3%-3.65g=3.65g
设3.65g氯化氢所需NaOH的质量为y。
HCl + NaOH═H O+NaCl
2
36.5 40
3.65g y
解得:y=4g
①盐酸和氧化镁反应的化学方程式为:MgO+2HCl═MgCl +H O
2 2
②氢氧化钠和氯化镁反应的化学方程式为:MgCl +2NaOH═Mg(OH)↓+2NaCl
2 2
设使Mg2+沉淀完全需要氢氧化钠的质量为z,联立①②可得:
MgO ~ 2NaOH
40 80
2g z
解得:z=4g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共6页让更多的孩子得到更好的教育
所需NaOH溶液的质量为:(4g+4g)÷10%=80g
5.【答案】 A
【解析】根据反应前后元素质量不变分析,氯酸钾分解生成氧气的质量即为氯酸钾中氧元素的质量。黑
色固体为二氧化锰,因此原混合物中二氧化锰的质量为 20.7g,氯酸钾和氯化钾质量和为
100g-20.7g=79.3g,钾元素质量分数为39%,故钾元素质量为100g×39%=39g,由KClO、KCl的化学式可
3
以看出,钾元素和氯元素质量比为39:35.5,因此氯元素质量为35.5g,钾元素、氯元素和氧元素质量和为
79.3g,故氧元素质量为79.3g-35.5g-39g=4.8g。
6.【答案】 C
【解析】根据金属活动性,铜不能与稀盐酸发生反应,即天平右盘质量增加8g后,天平仍然平衡;因此天
平左盘加入10.2g混合物后质量也应增加8g,根据碳酸镁与盐酸反应会放出二氧化碳,可知二氧化碳气
体的质量=10.2g-8g=2.2g,据此可计算出碳酸镁的质量和氢氧化镁的质量。设混合物中碳酸镁的质量为x。
MgCO +2HCl=MgCl +H O+CO↑
3 2 2 2
84 44
x 2.2g
解得 x=4.2g
则混合物中氢氧化镁的质量为:10.2g-4.2g=6g
7.【答案】 (1)6:1:12 (2)7
【解析】(1)过氧乙酸(化学式为C HO)中C、H、O元素的质量比为:(12×2): (1×4):(16×3)=6∶1∶12。
2 4 3
(2)设需要20%的过氧乙酸溶液的质量为x,则:280 kg×0.5%=x·20%,解得:x=7 kg。
8.【答案】 0.2 67.5%
【解析】根据黄铜的成分铜和锌的性质可知,加入稀硫酸时,只有锌与硫酸反应生成了硫酸锌和氢气。
(1)根据质量守恒定律,产生氢气的质量为:20g+100g-119.8g=0.2g。
(2)设黄铜样品中锌的质量为x。
Zn+H SO =ZnSO +H ↑
2 4 4 2
65 2
x 0.2g
x=6.5g
黄铜样品中铜的质量分数为: ×100%=67.5%
9.【答案】 (1)1.16 (2)钾 (3)11.2%
(4)设原混合物中含有MgCl 的质量为y。
2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共6页让更多的孩子得到更好的教育
MgCl +2KOH=Mg(OH)↓+2KCl
2 2
95 58
y 2.32g
y=3.8g
则样品中氯化镁的质量分数为: ×100%=38%
答:样品中氯化镁的质量分数是38%。
【解析】(1)由表中1、3两次的数据可知,10g氢氧化钾溶液与氯化镁反应能生成0.58g沉淀,因此20g
氢氧化钠溶液能生成1.16g沉淀。
(2)氯化钾提供的主要营养元素是钾元素,属于钾肥。
(3)设10g氢氧化钾溶液中溶质氢氧化钾的质量为x。
MgCl +2KOH═2KCl+Mg(OH)↓
2 2
112 58
x 0.58g
x=1.12g
氢氧化钾溶液中溶质的质量分数为: ×100%═11.2%
(4)设原混合物中含有MgCl 的质量为y。
2
MgCl +2KOH=Mg(OH)↓+2KCl
2 2
95 58
y 2.32g
,y=3.8g。
则样品中氯化镁的质量分数是 ×100%=38%。
答:样品中氯化镁的质量分数是38%。
10.【答案】 (1)3.40
(2)从表中分析可知:第三次加入稀盐酸后物质恰好完全反应,根据质量恒定律,完全反应后生成CO 的
2
质量=40g+150 g-183.40 g=6.60g,设原混合物中BaCO 的质量为x,生成BaCl 的质量为y,则:
3 2
BaCO +2HCl═BaCl +H O+CO↑
3 2 2 2
197 208 44
x y 6.60g
x=29.55g y=31.2g
滤液中BaCl 中的质量分数为: ×100%=21.25%
2
答:恰好完全反应后过滤所得滤液中溶质的质量分数为21.25%。
【解析】(1)BaCO 、BaCl 、BaSO 的固体混合物中,只有硫酸钡既不溶于水也不溶于盐酸,因此烧杯内
3 2 4
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共6页让更多的孩子得到更好的教育
剩余固体是硫酸钡,质量是3.4g。
(2)从表中分析可知:第三次加入稀盐酸后物质恰好完全反应,根据质量恒定律,完全反应后生成CO 的
2
质量=40g+150 g-183.40 g=6.60g,设原混合物中BaCO 的质量为x,生成BaCl 的质量为y,则:
3 2
BaCO +2HCl═BaCl +H O+CO↑
3 2 2 2
197 208 44
x y 6.60g
x=29.55g y=31.2g
滤液中BaCl 的质量分数为: ×100%=21.25%
2
答:恰好完全反应后过滤所得滤液中溶质的质量分数为21.25%。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共6页