文档内容
2023 年高考考前押题密卷(辽宁卷)
化学·全解全析
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56 Ni 59 Ce 140
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求.
1.【答案】A
【详解】
A.朱砂的主要成分是HgS,选项A错误;
B.人工合成淀粉能减少二氧化碳的排放,有利于推进“碳中和”目标的实现,B正确;
C.铝合金密度小、强度高,通常具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料,C项正
确;
D.高铁酸钾(K FeO)氧化性,在水处理过程中能使蛋白质的变性、胶体聚沉、发生盐类水解、氧化还原反
2 4
应,D正确;
综上所述,答案为A。
2.【答案】B
【详解】
A. 中甲基在3号碳原子上,命名为:3-甲基丁酸,故A错误;
B.硼酸的分子式为 [或 ],其电子式为 ,B正确;
1
学科网(北京)股份有限公司C.反式聚异戊二烯结构简式: ,C错误;
D. 水解生成碳酸,水解方程式为: ,故A错误;
综上所述,答案为B。
3.【答案】D
【详解】
A.1个 中存在4个配位键,则1 mol 中配位键的数目为4 ,A错误;
B.酸性 溶液中存在平衡: ,1L pH=4的 溶液
中, 数目小于 ,故B错误;
C.没有明确溶液体积,不能计算悬浊液中的 数目,故C错误;
D.根据结构简式可知,分子中碳氧双键中含 键,所以 键数为 ,D正
确;
综上所述,答案为D。
4.【答案】D
【详解】微信搜索“高中试卷君”公众号 领取押题卷联考卷
A.共价单键是σ键,共价三键中含有2个π键1个σ键, 中含有的 键与 键的数目之比为 ,选
项A正确;
B.根据图中信息可知有离子反应 ,S元素由+2价变为-2价降了4,结合电荷守恒
和质量守恒配得离子反应为 ,故y=24,同理,由 中
S由+4价降为-2价降了6,结合电荷守恒和质量守恒配得离子反应为 ,故
x=21,选项B正确;
C. 参与的反应为 , 中S由-2价升高为+2价被氧化,C由+4价变为+2
价被还原,故 既被氧化又被还原,选项C正确;
D.根据反应 ,每生成 ,转移 ;反应
中每生成 ,转移 ,选项D错误;
2
学科网(北京)股份有限公司答案选D。
5.【答案】A
【详解】
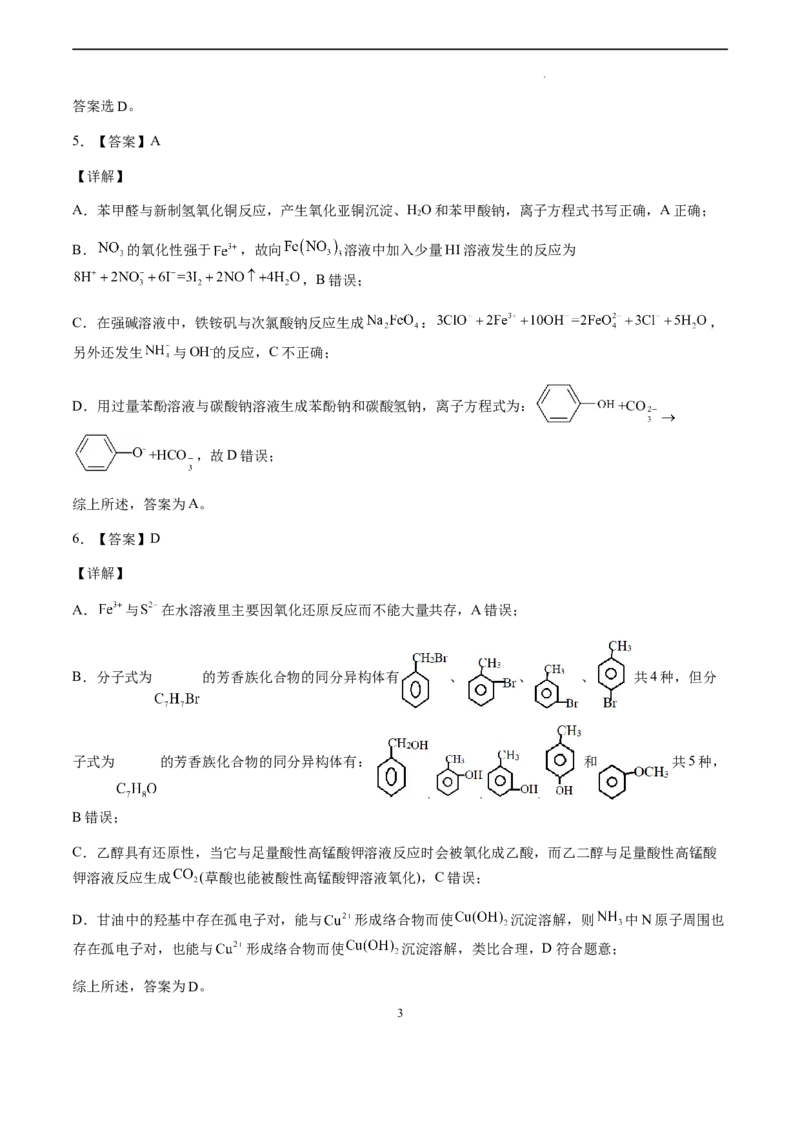
A.苯甲醛与新制氢氧化铜反应,产生氧化亚铜沉淀、HO和苯甲酸钠,离子方程式书写正确,A正确;
2
B. 的氧化性强于 ,故向 溶液中加入少量HI溶液发生的反应为
,B错误;
C.在强碱溶液中,铁铵矾与次氯酸钠反应生成 : ,
另外还发生 与OH-的反应,C不正确;
D.用过量苯酚溶液与碳酸钠溶液生成苯酚钠和碳酸氢钠,离子方程式为: +CO
+HCO ,故D错误;
综上所述,答案为A。
6.【答案】D
【详解】
A. 与 在水溶液里主要因氧化还原反应而不能大量共存,A错误;
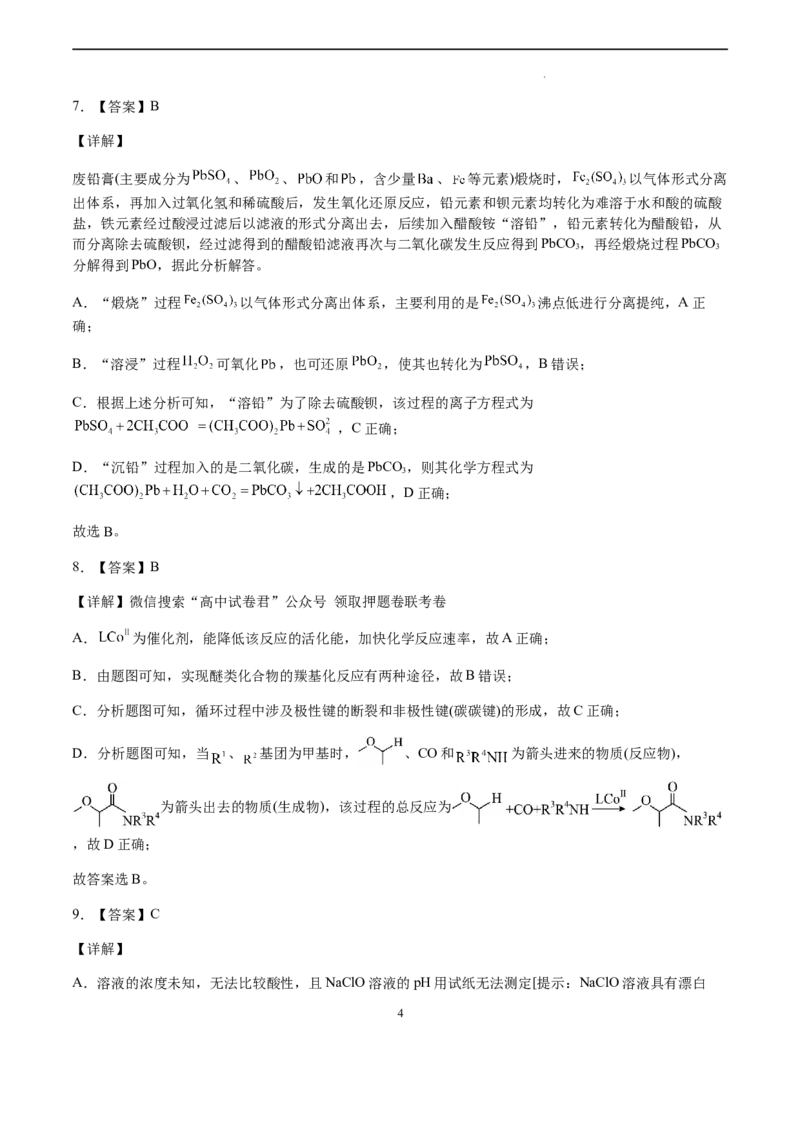
B.分子式为 的芳香族化合物的同分异构体有 、 、 、 共4种,但分
子式为 的芳香族化合物的同分异构体有: 和 共5种,
B错误;
C.乙醇具有还原性,当它与足量酸性高锰酸钾溶液反应时会被氧化成乙酸,而乙二醇与足量酸性高锰酸
钾溶液反应生成 (草酸也能被酸性高锰酸钾溶液氧化),C错误;
D.甘油中的羟基中存在孤电子对,能与 形成络合物而使 沉淀溶解,则 中N原子周围也
存在孤电子对,也能与 形成络合物而使 沉淀溶解,类比合理,D符合题意;
综上所述,答案为D。
3
学科网(北京)股份有限公司7.【答案】B
【详解】
废铅膏(主要成分为 、 、 和 ,含少量 、 等元素)煅烧时, 以气体形式分离
出体系,再加入过氧化氢和稀硫酸后,发生氧化还原反应,铅元素和钡元素均转化为难溶于水和酸的硫酸
盐,铁元素经过酸浸过滤后以滤液的形式分离出去,后续加入醋酸铵“溶铅”,铅元素转化为醋酸铅,从
而分离除去硫酸钡,经过滤得到的醋酸铅滤液再次与二氧化碳发生反应得到PbCO ,再经煅烧过程PbCO
3 3
分解得到PbO,据此分析解答。
A.“煅烧”过程 以气体形式分离出体系,主要利用的是 沸点低进行分离提纯,A正
确;
B.“溶浸”过程 可氧化 ,也可还原 ,使其也转化为 ,B错误;
C.根据上述分析可知,“溶铅”为了除去硫酸钡,该过程的离子方程式为
,C正确;
D.“沉铅”过程加入的是二氧化碳,生成的是PbCO ,则其化学方程式为
3
,D正确;
故选B。
8.【答案】B
【详解】微信搜索“高中试卷君”公众号 领取押题卷联考卷
A. 为催化剂,能降低该反应的活化能,加快化学反应速率,故A正确;
B.由题图可知,实现醚类化合物的羰基化反应有两种途径,故B错误;
C.分析题图可知,循环过程中涉及极性键的断裂和非极性键(碳碳键)的形成,故C正确;
D.分析题图可知,当 、 基团为甲基时, 、CO和 为箭头进来的物质(反应物),
为箭头出去的物质(生成物),该过程的总反应为
,故D正确;
故答案选B。
9.【答案】C
【详解】
A.溶液的浓度未知,无法比较酸性,且NaClO溶液的pH用试纸无法测定[提示:NaClO溶液具有漂白
4
学科网(北京)股份有限公司性,会使pH试纸褪色],A项错误;
B.浓盐酸也能与酸性高锰酸钾溶液反应使溶液褪色,则溶液褪色不能说明铁锈中是否含有二价铁,B错
误;
C.常温下,将 苯与 混合体积为 ,说明混合过程中削弱了 分子间
的氢键,且苯与 分子间的作用弱于氢键,导致分子间距离增大,从而使体积变大,C正确;
D.向过量的硝酸银溶液中先加入少量氯化钾溶液,再加入碘化钾溶液时,溶液中只存在沉淀的生成,没
发生沉淀的转化,所以无法比较氯化银和碘化银的溶度积大小,故D错误;
综上所述,答案为C。
10.【答案】B
【详解】
A.第一电离能是基态的气态原子失去最外层的一个电子所需能量,故Li的第一电离能为
,A项正确;
B.由LiO的晶胞图可知每个Li和4个O配位,其配位数为4,B项错误;
2
C.晶格能是指在标准状况下使离子晶体变成气态正离子和气态负离子时所吸收的能量,由图可知 晶
格能为 ,C项正确;
D.每个晶胞内含有8个Li和4个O,则 的密度为 ,D项正
确。
答案选B。
11.【答案】B
【详解】
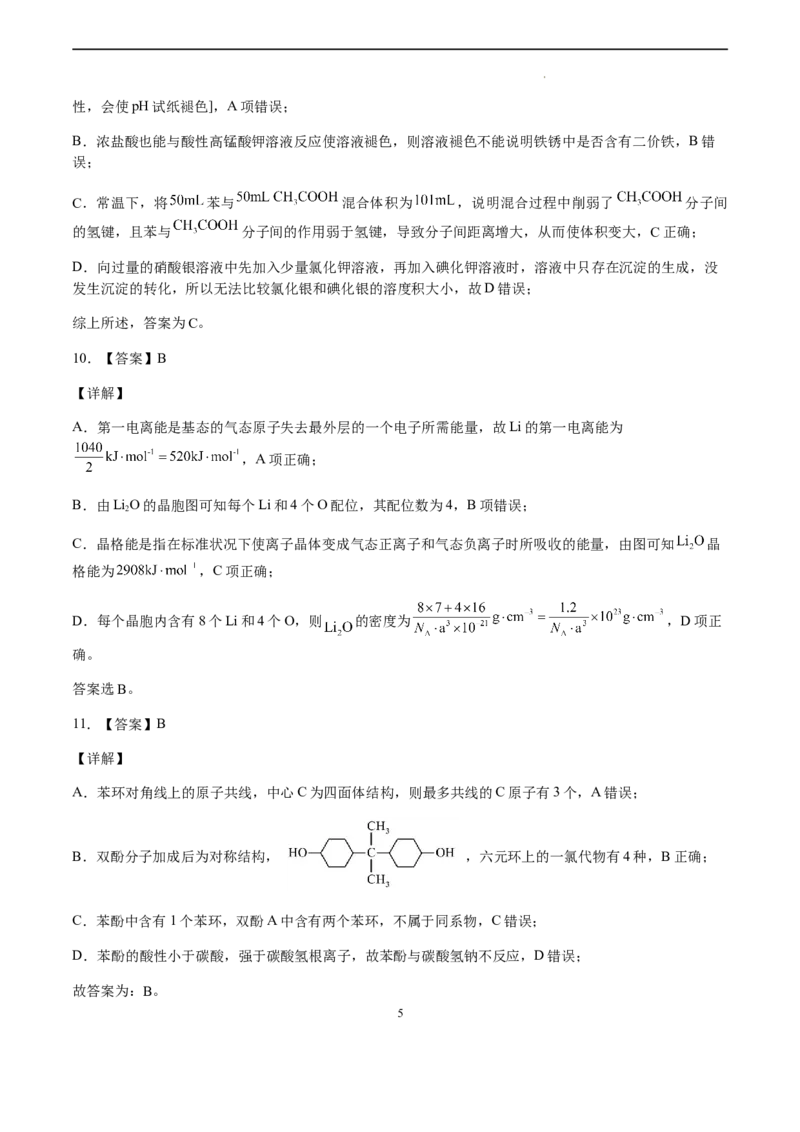
A.苯环对角线上的原子共线,中心C为四面体结构,则最多共线的C原子有3个,A错误;
B.双酚分子加成后为对称结构, ,六元环上的一氯代物有4种,B正确;
C.苯酚中含有1个苯环,双酚A中含有两个苯环,不属于同系物,C错误;
D.苯酚的酸性小于碳酸,强于碳酸氢根离子,故苯酚与碳酸氢钠不反应,D错误;
故答案为:B。
5
学科网(北京)股份有限公司12.【答案】D
【详解】
中间电极上产生CaP的组成为3Ca (PO ) CaHPO ·zHO,说明 中的氢被还原生成氢气,则该电极为
3 4 2· 4 2
阴极,连接电源的负极,两侧的电极就是阳极。据此解答。
A.中间的为阴极,两侧的为阳极,根据电子守恒分析,阳极失去的电子总数应该等于阴极得到电子总
数,故三电极流出或流入的电子数不相等,A错误;
B.工作时Ti/SnO -Sb电极与电源的正极相连,B错误;
2
C.Ti/SnO -Sb电极为阳极,水被氧化,氧化产物为氧气,氢离子不是氧化产物,C错误;
2
D.阴极是 中的氢得到电子生成氢气,同时生成 和 ,和钙离子和水结合形成
3Ca (PO ) CaHPO ·zHO,D正确;
3 4 2· 4 2
故选D。
13.【答案】D
【详解】微信搜索“高中试卷君”公众号 领取押题卷联考卷
T℃时,反应达到平衡时,正逆反应速率相等,则 ,反应的平衡常数
1
K= = ,设平衡时生成甲酸的浓度为amol/L,由题意可建立如下三段式:
由平衡常数可得:a(1-a)(1-a)=2,解得a=0.5,反应的平衡常数K= =2。
A.由反应热与反应物的键能之和和生成物的键能之和的差值相等可知,反应△H=(745kJ/mol×2+436kJ/
mol)-(745kJ/mol+426kJ/mol+413.4 kJ/mol+351 kJ/mol) <0,故A正确;
B.由分析可知,甲酸的体积分数为 ,故B正确;
C.由分析可知,反应的平衡常数K= =2,则k =0.5k ,故C正确;
逆 正
D.该反应为放热反应,升高温度,平衡向逆反应方向移动,化学平衡常数减小,由温度为T℃时,k
2 正
6
学科网(北京)股份有限公司=2.1k 可知,反应的平衡常数K'= =2.1>K,则反应温度T℃<T℃,故D错误;
逆 2 1
故选:D。
14.【答案】C
【详解】
X的原子半径在周期表中最小,X为H;W是地壳中含量第二的元素,W是Si;Y的p轨道上自旋方向不
的电子数之比为3:1,Y的原子序数比Si小,Y是O;根据 和正负化合价相等,Z为
Mg。
A.由分析可知,Y是O,Z是Mg,则离子半径: ,A错误;
B.由分析可知,Y是O,W是Si,二者形成的化合物为SiO,SiO 能与氢氟酸反应,B错误;
2 2
C.由分析可知,X是H,Z是Mg,二者形成的化合物为MgH ,MgH 与水反应生成 和H,C
2 2 2
正确;
D.由分析可知,X是H,Y是O,二者形成的化合物有HO和HO,HO 中含有非极性键,D错误;
2 2 2 2 2
故选C。
15.【答案】D
【详解】
A.柠檬酸的 ,柠檬酸三钠的 ,a点为柠檬酸三钠溶液,
, ,则溶液中 数量级为 ,选项A正确;
B.b点为 和 的混合溶液, 的电离平衡常数 , 的水解平衡常
数 , 的电离大于 的水解,溶液显酸性,选项B正确;
C.c点为 和 的混合溶液,二者的物质的量之比为1∶2,溶液满足:
,
,则
,选项C正确;
7
学科网(北京)股份有限公司D. 由题意可得, · = = ,则 =
, 时,溶液中 ,则 ,故
,则溶液满足: ,D错误;
答案选D。
二、非选择题:本题共4小题,共55分。
16.(14分)
【答案】
(1)将三价铈转化为四价铈,且将碳酸盐转化为二氧化碳,实现铈的富集
(2)6H++2CeO +H O=4H O+2Ce3++O ↑
2 2 2 2 2
(3)过滤
(4)浸出液中加入的SO 浓度越大, 增大,而 减小,因此D随浸出液中
增大而减小
(5)95.68%
(6)8 ×107
【详解】
(1)根据题意,四价铈不易进入溶液,而三价铈易进入溶液。故焙烧氟碳铈矿的目的是将三价铈转化为
四价铈,且将碳酸盐转化为二氧化碳,实现铈的富集。
(2) 转化为 ,则HO 转化为O:6H++2CeO +H O=4H O+2Ce3++O ↑。
2 2 2 2 2 2 2 2
故答案为:6H++2CeO +H O=4H O+2Ce3++O ↑。
2 2 2 2 2
(3)“操作I”为过滤。
故答案为:过滤。
(4)浸出液中加入的SO 浓度越大,根据化学平衡:Ce4++SO ,故而 增
8
学科网(北京)股份有限公司大,而 减小,因此D随浸出液中 增大而减小。
故答案为:浸出液中加入的SO 浓度越大, 增大,而 减小,因此D随
浸出液中 增大而减小。
(5)根据氧化还原反应得失电子守恒有n(Ce4+)×1+n(KMnO)×5=n(Fe2+)×1,解得n(Ce4+)=0.023mol,故w[
4
]= =95.68%。
故答案为95.68%。
(6)①由图可知,一个晶胞中,1个铈离子周围有4个氧离子,故铈离子的配位数为:4×2=8,
故答案为:8。
②在 晶胞中,N(Ce4+)= =4,N(O2-)=8×1=8,故每个晶胞中相当于有4个CeO,4M=ρ.v
2 晶
.N =ρ×(a×10-7)3×N 。故a= ×107nm。
胞 A A
故答案为: ×107。
17.(13分)
【答案】
(1)p-2q p (p-2q)
(2)66.5 1000 变大
(3)阳离子
【详解】
(1)
,
,则c(HNCO)=(p-2q)mol/L,则反应I的
9
学科网(北京)股份有限公司平衡常数K=c ( NH ) ×c ( HNCO ) =p (p-2q) ( mol/L )2。
3
(2)从图分析,过渡态3的相对能量为241-87=154kJ/mol,则ΔE1=154-87.5=66.5kJ/mol。从图分析,
HNCO(g)+NH
3
(g)⇌CO(NH
2
)
2
(g)
为放热反应,升温,平衡逆向移动,则右侧的线为
T℃的,取A点数值, kPa−1,若点A时继续投入等物质的量的
1
两种反应物,再次达到平衡时(温度不变),相当于加压,平衡正向移动,则CO(NH) 的体积分数变大。
2 2
(3)从图分析,c电极产生氮气,为阳极反应,d上产生氢气,为阴极反应,则a为负极,锌失去电子,
结合氢氧根离子,故该交换膜为阴离子交换膜,b为正极,与b极室相连的交换膜为阳离子交换膜,装置
Ⅱ阳极上的反应式为 。
18.(14分)
【答案】微信搜索“高中试卷君”公众号 领取押题卷联考卷
(1)恒压漏斗(或恒压分液漏斗) 饱和NaHS溶液
(2)H S+Ni2++2NH=NiS↓+2
2 3
(3)b
(4)4NiS+O+2H O= 4Ni(OH)S
2 2
(5) 偏高
【详解】
Ⅰ中硫化亚铁和盐酸反应生成硫化氢气体,硫化氢通过饱和NaHS溶液的装置Ⅱ除去氯化氢气体杂质后进
入装置Ⅲ,装置Ⅲ中硫化氢、氨气、氯化镍反应生成NiS,尾气有毒需要尾气处理装置;
(1)装置图中,仪器a的名称是恒压漏斗(或恒压分液漏斗);装置Ⅱ中的试剂为饱和NaHS溶液,饱和
NaHS溶液可以除去生成硫化氢气体中挥发的氯化氢气体杂质;
(2)装置Ⅲ中硫化氢、氨气、氯化镍反应生成NiS,反应为HS+Ni2++2NH=NiS↓+2 ;
2 3
(3)反应结束后关闭K、K,在b、c处分别连接下图两个装置,打开K、K 进行抽滤洗涤,抽滤洗涤
1 4 2 3
时,洗涤水进入装置Ⅲ然后通过抽气装置抽出达到洗涤目的,故连有抽气泵的装置Ⅳ接在b处以便能够抽
出洗涤水;
(4)已知,NiS在潮湿的空气中可转化为碱式硫化高镍[Ni(OH)S],从而降低除铜离子能力,故随时间延
长残留铜离子增加的原因是:4NiS+O+2H O= 4Ni(OH)S;
2 2
10
学科网(北京)股份有限公司(5)①由反应Ni2++H Y2- NiY2-+ 2H+可知, ,则样品的纯度为
2
;
②滴定过程中,缓冲溶液pH值过低,Ni2++H Y2- NiY2-+ 2H+,导致平衡逆向移动,则需要更多的标准
2
液参与反应,导致测得的产品纯度偏高。
19.(14分)
【答案】
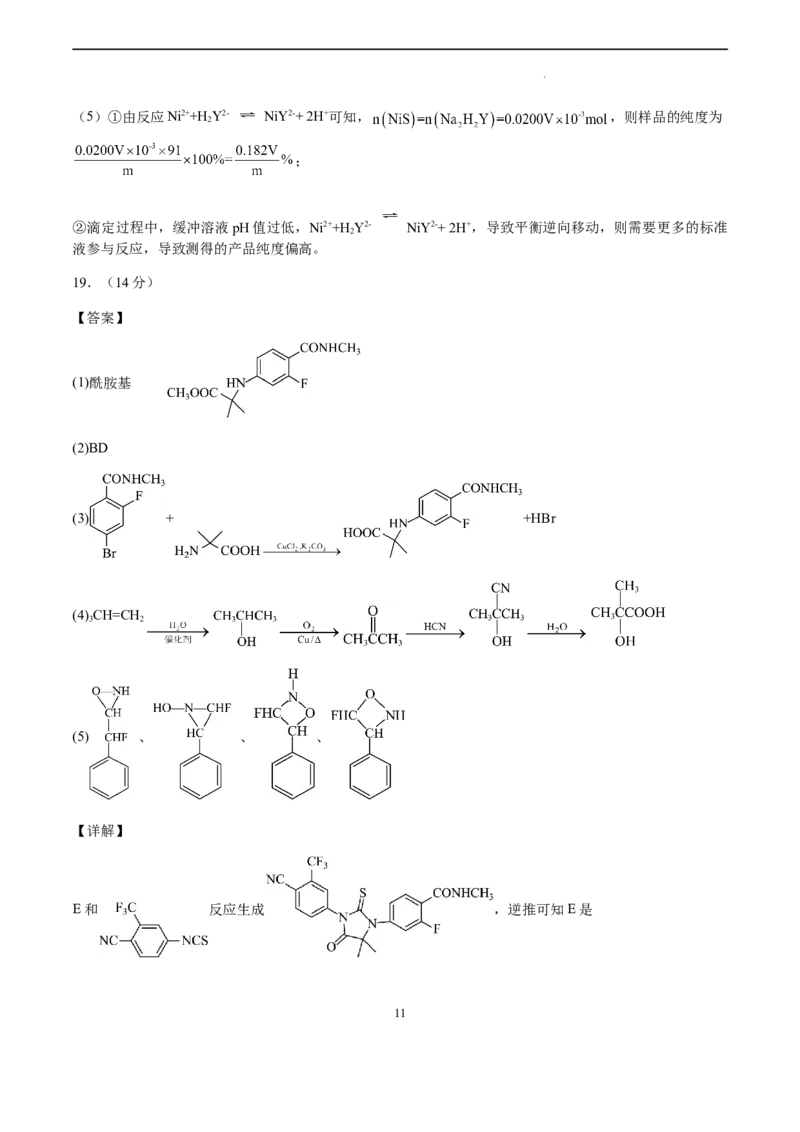
(1)酰胺基
(2)BD
(3) + +HBr
(4)CH=CH
3 2
(5) 、 、 、
【详解】
E和 反应生成 ,逆推可知E是
11
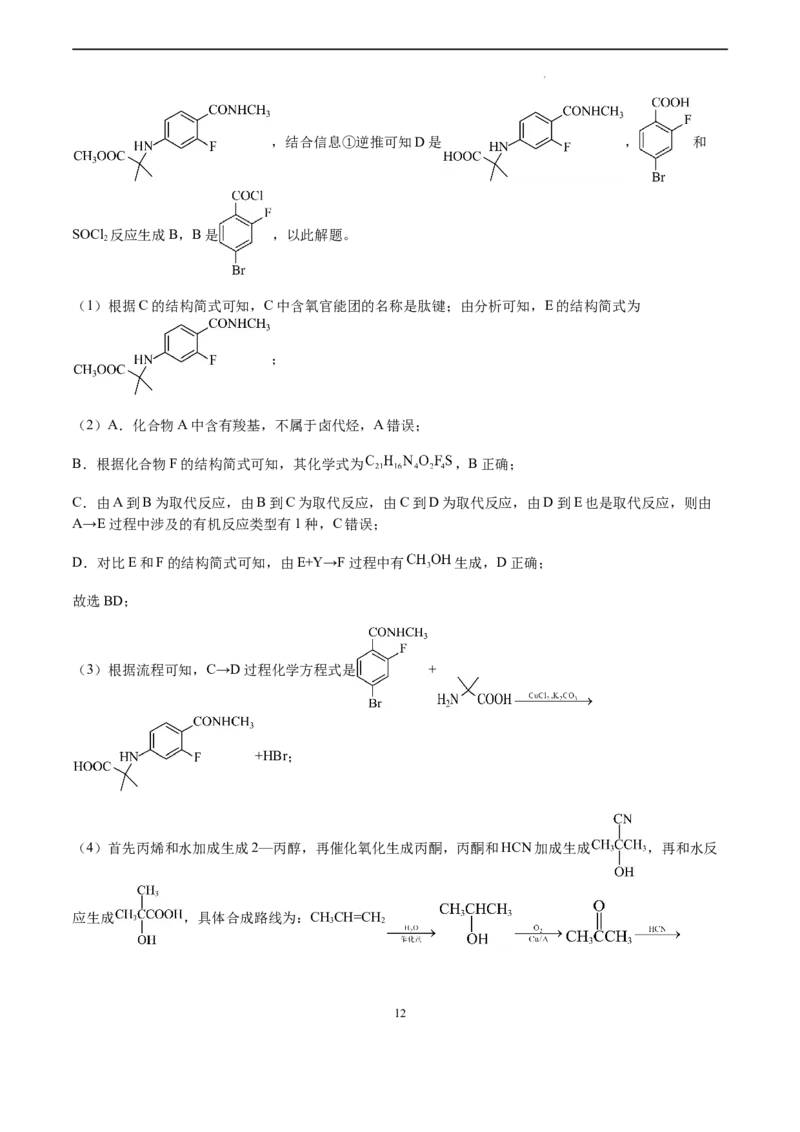
学科网(北京)股份有限公司,结合信息①逆推可知D是 , 和
SOCl 反应生成B,B是 ,以此解题。
2
(1)根据C的结构简式可知,C中含氧官能团的名称是肽键;由分析可知,E的结构简式为
;
(2)A.化合物A中含有羧基,不属于卤代烃,A错误;
B.根据化合物F的结构简式可知,其化学式为 ,B正确;
C.由A到B为取代反应,由B到C为取代反应,由C到D为取代反应,由D到E也是取代反应,则由
A→E过程中涉及的有机反应类型有1种,C错误;
D.对比E和F的结构简式可知,由E+Y→F过程中有 生成,D正确;
故选BD;
(3)根据流程可知,C→D过程化学方程式是 +
+HBr;
(4)首先丙烯和水加成生成2—丙醇,再催化氧化生成丙酮,丙酮和HCN加成生成 ,再和水反
应生成 ,具体合成路线为:CHCH=CH
3 2
12
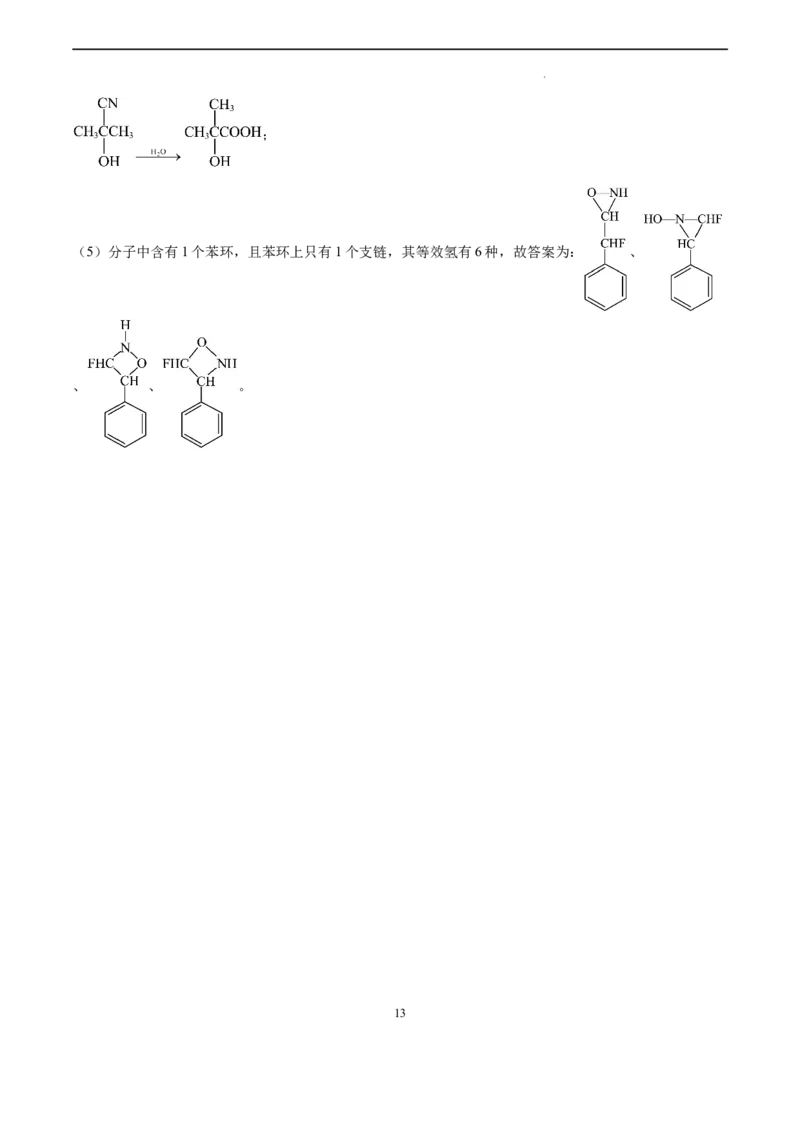
学科网(北京)股份有限公司;
(5)分子中含有1个苯环,且苯环上只有1个支链,其等效氢有6种,故答案为: 、
、 、 。
13
学科网(北京)股份有限公司14
学科网(北京)股份有限公司