文档内容
专题96 工艺流程——金属元素载体
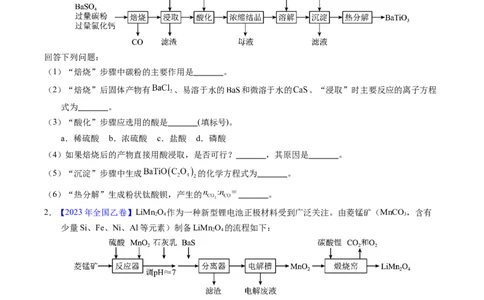
1.【2023年全国甲卷】 是一种压电材料。以 为原料,采用下列路线可制备粉状 。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是 。
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子方程
式为 。
(3)“酸化”步骤应选用的酸是 (填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行? ,其原因是 。
(5)“沉淀”步骤中生成 的化学方程式为 。
(6)“热分解”生成粉状钛酸钡,产生的 。
2.【2023年全国乙卷】LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有
2 4 3
少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为 。为提高溶矿速率,可采取的措施 (举1例)。
(2)加入少量MnO 的作用是 。不宜使用HO 替代MnO ,原因是 。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)= mol·L-1;用石灰乳调节至pH≈7,除去的
金属离子是 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有 。
(5)在电解槽中,发生电解反应的离子方程式为 。随着电解反应进行,为保持电解液成分稳定,
应不断 。电解废液可在反应器中循环利用。(6)煅烧窑中,生成LiMn O 反应的化学方程式是 。
2 4
3.【2023年全国新课标卷】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂
质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为 (填化学
式)。
(2)水浸渣中主要有SiO 和 。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9
3 4 4
以达到最好的除杂效果,若pH<9时,会导致 ;pH>9时,会导致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或
2 5 2 5
VO3+在碱性条件下,溶解为VO 或VO ,上述性质说明VO 具有 (填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为 。
2 2 5
4.【2023年1月浙江卷】某研究小组制备纳米 ,再与金属有机框架 )材料复合制备荧光材料
,流程如下:
已知:①含
锌组分间的转化关系:
② 是 的一种晶型, 以下稳定。
请回答:
(1)步骤Ⅰ,初始滴入 溶液时,体系中主要含锌组分的化学式是 。
(2)下列有关说法不正确的是___________。
A.步骤Ⅰ,搅拌的作用是避免反应物浓度局部过高,使反应充分
B.步骤Ⅰ,若将过量 溶液滴入 溶液制备 ,可提高 的利用率
C.步骤Ⅱ,为了更好地除去杂质,可用 的热水洗涤
D.步骤Ⅲ,控温煅烧的目的是为了控制 的颗粒大小
(3)步骤Ⅲ,盛放样品的容器名称是 。(4)用 和过量 反应,得到的沉淀可直接控温煅烧得纳米 ,沉淀无需洗涤
的原因是 。
(5)为测定纳米 产品的纯度,可用已知浓度的 标准溶液滴定 。从下列选项中选择合理的
仪器和操作,补全如下步骤[“___________”上填写一件最关键仪器,“(___________)”内填写一种操作,
均用字母表示]。
用___________(称量 样品 )→用烧杯(___________)→用___________(___________)→用移液管
(___________)→用滴定管(盛装 标准溶液,滴定 )
仪器:a、烧杯;b、托盘天平;c、容量瓶;d、分析天平;e、试剂瓶
操作:f、配制一定体积的Zn2+溶液;g、酸溶样品;h、量取一定体积的 溶液;i、装瓶贴标签
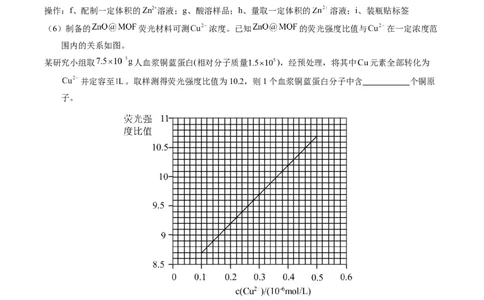
(6)制备的 荧光材料可测 浓度。已知 的荧光强度比值与 在一定浓度范
围内的关系如图。
某研究小组取 人血浆铜蓝蛋白(相对分子质量 ),经预处理,将其中 元素全部转化为
并定容至 。取样测得荧光强度比值为10.2,则1个血浆铜蓝蛋白分子中含 个铜原
子。
5.(2021·北京真题)铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
资料:
i.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ii.TiOSO
4
+(x+1)H
2
O⇌TiO
2
·xH
2
O↓+H
2
SO
4
iii.0.1 mol/L Fe2+生成Fe(OH) ,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
2
0.1 mol/L Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8(1)纯化
①加入过量铁粉的目的是_______。
②充分反应后,分离混合物的方法是_______。
(2)制备晶种
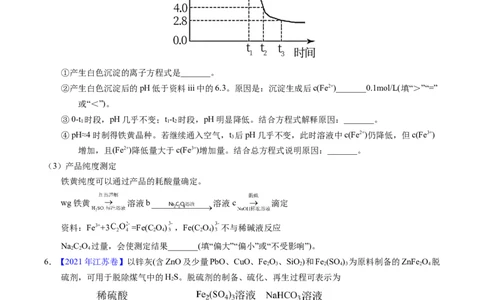
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO 溶液中加入氨水,产
4
生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe2+)_______0.1mol/L(填“>”“=”
或“<”)。
③0-t 时段,pH几乎不变;t-t 时段,pH明显降低。结合方程式解释原因:_______。
1 1 2
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)
3
增加,且(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄 溶液b 溶液c 滴定
资料:Fe3++3 =Fe(C O) ,Fe(C O) 不与稀碱液反应
2 4 2 4
NaC O 过量,会使测定结果_______(填“偏大”“偏小”或“不受影响”)。
2 2 4
6.【2021年江苏卷】以锌灰(含ZnO及少量PbO、CuO、Fe O、SiO)和Fe (SO ) 为原料制备的ZnFe O 脱
2 3 2 2 4 3 2 4
硫剂,可用于脱除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示为
2(1)“除杂”包括加足量锌粉、过滤加HO 氧化等步骤。除Pb2+和Cu2+外,与锌粉反应的离子还有
2 2
___(填化学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶
4 4
中,加水稀释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na HY)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3次,平均消耗
2 2
EDTA溶液25.00mL。计算ZnSO 溶液的物质的量浓度___(写出计算过程)。
4
(3)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反
2 2 2 2 4
应器。
①硫化过程中ZnFe O 与H、HS反应生成ZnS和FeS,其化学方程式为___。
2 4 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的反应,反应前
2 2
后ZnS的质量不变,该反应过程可描述为___。
(4)将硫化后的固体在N:O=95:5(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图
2 2
所示。在280~400℃范围内,固体质量增加的主要原因是___。
7.【2022年河北卷】以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝 颜
料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程
式为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,
不引入杂质)。
8.【2022年湖南卷】钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少
量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
物质
沸点/
136 127 57 180
回答下列问题:
(1)已知 , 的值只决定于反应体系的始态和终态,忽略 、 随温度的变化。若
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
A. B.
C. D.
(2) 与C. ,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:物质
分压
①该温度下, 与C. 反应的总化学方程式为_______;
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离 中含 、 杂质的方法
是_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼 的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰D.氧化汞分解制汞
9.【2022年北京卷】铵浸法由白云石[主要成分为 ,含 , 杂质]制备高纯度碳酸钙
和氧化镁。其流程如下:
已知:
物质
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
浸出率/ 浸出率/ 理论值/ 实测值/
98.4 1.1 99.7 -
98.8 1.5 99.2 99.5
98.9 1.8 98.8 99.5
99.1 6.0 95.6 97.6已知:i.对浸出率给出定义
ii.对 给出定义
①“沉钙”反应的化学方程式为___________。
② 浸出率远高于 浸出率的原因为___________。
③不宜选用的“ ”数值为___________。
④ 实测值大于理论值的原因为___________。
⑤蒸馏时,随馏出液体积增大, 浸出率可出 增加至 ,结合化学反应原理解释 浸出率
提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
10.【2022年辽宁卷】某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成分为
)联合焙烧法制备 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为___________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度(2) 在空气中单独焙烧生成 ,反应的化学方程式为___________。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出 和 ;②___________。
(4)滤渣的主要成分为___________(填化学式)。
(5)生成气体A的离子方程式为___________。
(6)加入金属 的目的是___________。
11.【2017新课标3卷】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为
FeO·Cr O,还含有硅、铝等杂质。制备流程如图所示:
2 3
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr O+Na CO+NaNO Na CrO+ Fe O+CO + NaNO
2 3 2 3 3 2 4 2 3 2 2
上述反应配平后FeO·Cr O 与NaNO 的系数比为_______。该步骤不能使用陶瓷容器,原因是_____。
2 3 3
(2)滤渣1中含量最多的金属元素是_______,滤渣2的主要成分是__________及含硅杂质。
(3)步骤④调滤液2的pH使之变____________(填“大”或“小”),原因是_____________(用
离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液 3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到
KCr O 固体。冷却到___________(填标号)得到的KCr O 固体产品最多。
2 2 7 2 2 7
a.80℃ b.60℃
c.40℃ d.10℃
步骤⑤的反应类型是___________________。
(5)某工厂用 m kg 铬铁矿粉(含 Cr O 40%)制备 KCr O ,最终得到产品 m kg,产率为
1 2 3 2 2 7 2
_____________。
12.(2020年新课标Ⅰ)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,
还包括钾、镁的铝硅酸盐,以及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是___________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有___________离子被氧化。写出VO+转化为
反应的离子方程式___________。
(3)“中和沉淀”中,钒水解并沉淀为 ,随滤液②可除去金属离子K+、Mg2+、Na+、
___________,以及部分的___________。
(4)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣③的主要成分是___________。
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是___________。
4 3 4
13.【2018新课标2卷】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO 和
2
少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Fe3+ Fe2+ Zn2+ Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO 外还有___________;氧化除杂工序中ZnO的作用是____________,若
2
不通入氧气,其后果是________________。(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返
回_______工序继续使用。
14.【2018江苏卷】以高硫铝土矿(主要成分为Al O 、Fe O 、SiO ,少量FeS 和金属硫酸盐)为原料,生
2 3 2 3 2 2
产氧化铝并获得Fe O 的部分工艺流程如下:
3 4
(1)焙烧过程均会产生SO ,用NaOH溶液吸收过量SO 的离子方程式为______________________。
2 2
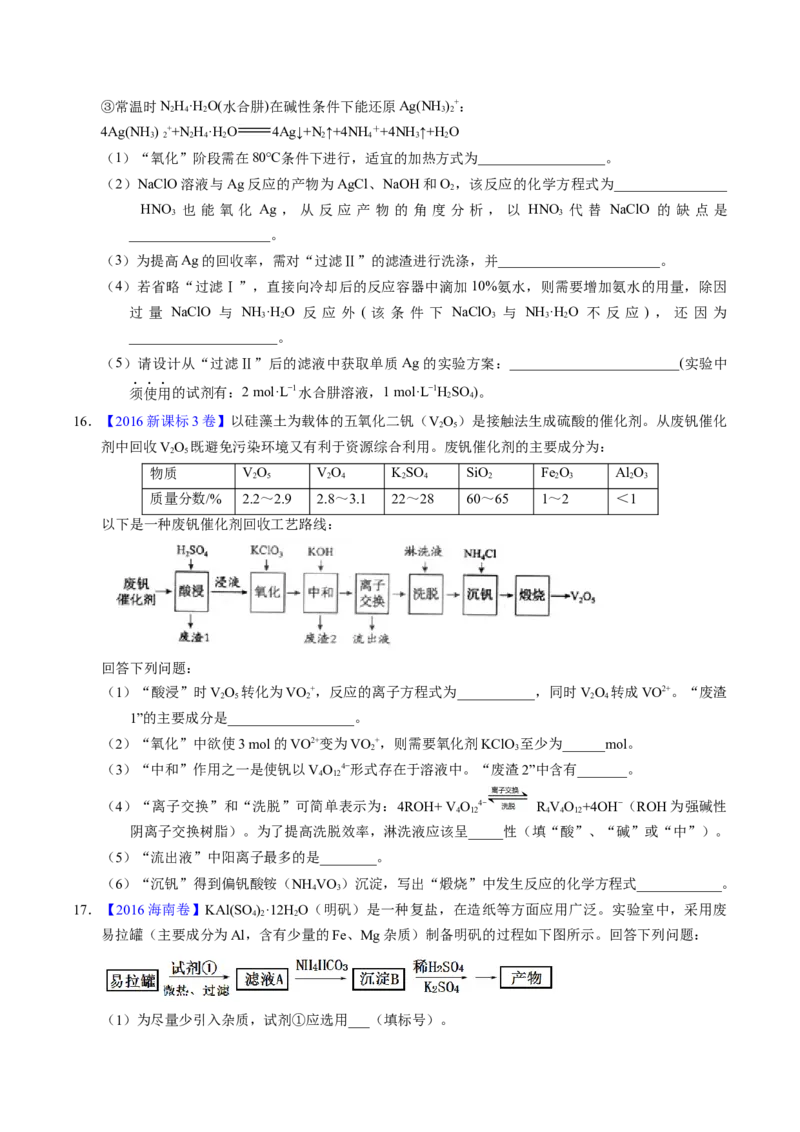
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题16图所示。
已知:多数金属硫酸盐的分解温度都高于600 ℃
焙烧后矿粉中硫元素总质量
硫去除率=(1— )×100%
焙烧前矿粉中硫元素总质量
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于__________________。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是
______________________________________________________。
(3)向“过滤”得到的滤液中通入过量CO ,铝元素存在的形式由_______________(填化学式)转
2
化为_______________(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe O 。Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和
2 3 2 3 2 3 4
SO ,理论上完全反应消耗的n(FeS)∶n(Fe O)=__________________。
2 2 2 3
15.【2017江苏卷】某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过
低,对实验的影响可忽略)。
已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO 2NaCl+NaClO
3
②AgCl可溶于氨水:AgCl+2NH·H O Ag(NH) ++ Cl− +2H O
3 2 3 2 2③常温时NH·H O(水合肼)在碱性条件下能还原Ag(NH)+:
2 4 2 3 2
4Ag(NH) ++N H·H O 4Ag↓+N↑+4NH++4NH↑+H O
3 2 2 4 2 2 4 3 2
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为__________________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O ,该反应的化学方程式为________________
2
HNO 也 能 氧 化 Ag , 从 反 应 产 物 的 角 度 分 析 , 以 HNO 代 替 NaClO 的 缺 点 是
3 3
____________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并_______________________。
(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因
过 量 NaClO 与 NH ·H O 反 应 外 ( 该 条 件 下 NaClO 与 NH ·H O 不 反 应 ) , 还 因 为
3 2 3 3 2
_____________________。
(5)请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:________________________(实验中
须使用的试剂有:2 mol·L−1水合肼溶液,1 mol·L−1HSO )。
2 4
16.【2016新课标3卷】以硅藻土为载体的五氧化二钒(VO )是接触法生成硫酸的催化剂。从废钒催化
2 5
剂中回收VO 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
2 5
物质 VO VO KSO SiO Fe O Al O
2 5 2 4 2 4 2 2 3 2 3
质量分数/% 2.2~2.9 2.8~3.1 22~28 60~65 1~2 <1
以下是一种废钒催化剂回收工艺路线:
回答下列问题:
(1)“酸浸”时VO 转化为VO +,反应的离子方程式为___________,同时VO 转成VO2+。“废渣
2 5 2 2 4
1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO +,则需要氧化剂KClO 至少为______mol。
2 3
(3)“中和”作用之一是使钒以VO 4−形式存在于溶液中。“废渣2”中含有_______。
4 12
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V O 4− R VO +4OH−(ROH为强碱性
4 12 4 4 12
阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH VO )沉淀,写出“煅烧”中发生反应的化学方程式____________。
4 3
17.【2016海南卷】KAl(SO )·12H O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废
4 2 2
易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
(1)为尽量少引入杂质,试剂①应选用___(填标号)。a.HCl溶液 b.HSO 溶液 c.氨水 d.NaOH溶液
2 4
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为___;将少量明矾溶于水,溶液呈弱酸性,其原因是_____。
(4)已知:K =1.0×10-14,Al(OH) AlO-+H++H O K=2.0×10-13。Al(OH) 溶于NaOH溶液反应
w 3 2 2 3
的平衡常数等于_________。