文档内容
辽宁省实验中学 2026 届高三第二次模拟考试
化学试卷
考试时间:75 分钟 试题满分:100 分
可能用到的相对原子质量: H—1 C—12 N—14 O—16 Ne—20 Na—23 Mg—24 Al—27 Cl—35.5 Ca—40 Fe
—56 Br—80
一、单选题(包含15小题,每小题3分,共45分。每题只有一个选项符合题意。)
1.分类是科学研究的重要方法,下列物质分类正确的是( )
A. 酸性氧化物: 、 、
B. 三元酸: 、 、
C. 电解质: 、氨水、
D.同素异形体: 、石墨烯、碳纳米管
2.下列陈述I与陈述II均正确,且具有因果关系的是 ( )
选项 陈述I 陈述Ⅱ
A 金属锂不能保存在煤油中 锂的密度比煤油小
B
加热 固体与浓 混合物可制备HI 比 酸性强
1一溴丁烷与足量 水溶液混合加热,充分反应后,滴加几滴硝酸
C 1—溴丁烷发生水解
银溶液,产生淡黄色沉淀
D 对盛有氢氧化铁胶体的U形管通电一段时间后,阴极区颜色变深 氢氧化铁胶体带正电
3. 表示阿伏加德罗常数的值,下列说法正确的是 ( )
A. 与足量的 反应, 转移电子数为
B.78g过氧化钠与足量水反应转移电子数为C.常温下,8.8g环氧乙烷 ( )中含有的共价键数目为
D.常温下, 与足量浓硫酸混合,转移的电子数目为
4.下列说法不正确的是 ( )
A. 同温同压条件下, 、 和 三种气体的密度关系:
B. 的乙醇与 的乙醇溶液等体积混合,混合后乙醇的质量分数小于 (乙醇密度小于水)
C. 某 溶液的密度为 , 的质量分数为 ,1L 该溶液中 的物质的量为
D. 氧气在放电条件下,有 转化为臭氧,则放电后混合气体对氢气的相对密度是35.6
5.下列反应的离子方程式正确的是 ( )
A. 将 等 体 积 、 等 浓 度 的 、 溶 液 和 氨 水 混 合 , 反 应 生 成 沉 淀 :
B.苯酚钠溶液中通入少量 :
C. 和 溶 液 以 物 质 的 量 之 比 1∶ 2 混 合 :
D. 固体与氢碘酸溶液反应:
6.室温下,下列各组离子一定能与指定溶液大量共存的是( )
A. 的 溶液: 、 、 、
B. 溶液: 、 、 、
C. 的氨水中: 、 、 、
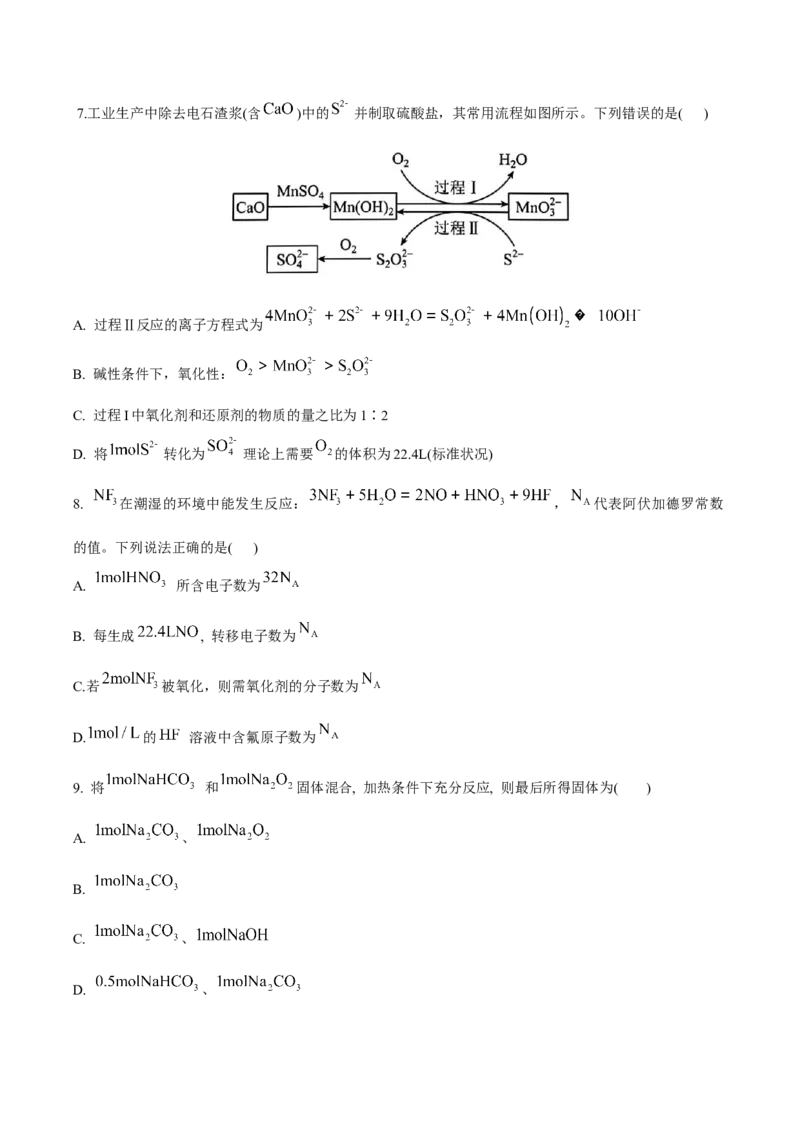
D. 溶液: 、 、 、7.工业生产中除去电石渣浆(含 )中的 并制取硫酸盐,其常用流程如图所示。下列错误的是( )
A. 过程Ⅱ反应的离子方程式为
B. 碱性条件下,氧化性:
C. 过程I中氧化剂和还原剂的物质的量之比为1∶2
D. 将 转化为 理论上需要 的体积为22.4L(标准状况)
8. 在潮湿的环境中能发生反应: , 代表阿伏加德罗常数
的值。下列说法正确的是( )
A. 所含电子数为
B. 每生成 , 转移电子数为
C.若 被氧化,则需氧化剂的分子数为
D. 的 溶液中含氟原子数为
9. 将 和 固体混合, 加热条件下充分反应, 则最后所得固体为( )
A. 、
B.
C. 、
D. 、10.自然界中存在一种尖晶石,可作为宝石,化学式为 ,该尖晶石中混有 。取一定量样品
,恰好与 一定浓度的盐酸完全反应,则该盐酸的浓度可能是( )
A. B.
C. D.
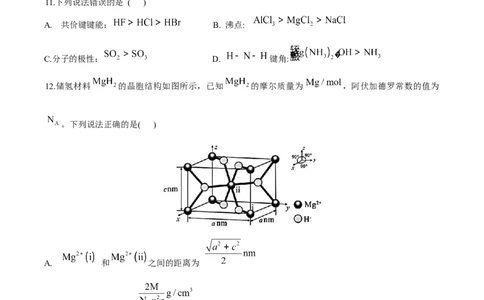
11.下列说法错误的是 ( )
A. 共价键键能: B. 沸点:
C.分子的极性: D. 键角:
12.储氢材料 的晶胞结构如图所示,已知 的摩尔质量为 ,阿伏加德罗常数的值为
。下列说法正确的是( )
A. 和 之间的距离为
B. 晶体密度的计算式为
C. 的配位数为3
D.晶胞中含有 2个
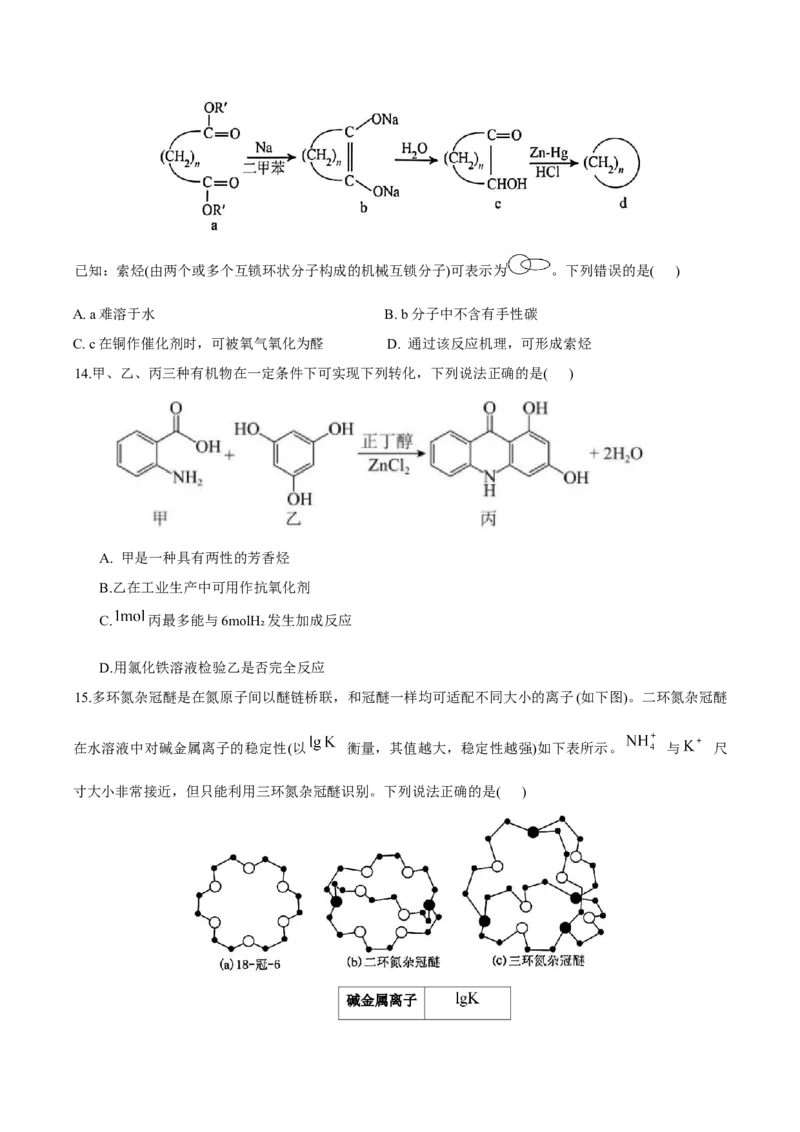
13.二元酸酯和金属钠在乙醚或二甲苯中,在纯氮气流存在下剧烈搅拌和回流,发生反应得到 一羟基环
酮(c),进一步还原可得到环烃(d)。反应机理如图:已知:索烃(由两个或多个互锁环状分子构成的机械互锁分子)可表示为 。下列错误的是( )
A. a难溶于水 B. b分子中不含有手性碳
C. c在铜作催化剂时,可被氧气氧化为醛 D. 通过该反应机理,可形成索烃
14.甲、乙、丙三种有机物在一定条件下可实现下列转化,下列说法正确的是( )
A. 甲是一种具有两性的芳香烃
B.乙在工业生产中可用作抗氧化剂
C. 丙最多能与6molH₂发生加成反应
D.用氯化铁溶液检验乙是否完全反应
15.多环氮杂冠醚是在氮原子间以醚链桥联,和冠醚一样均可适配不同大小的离子(如下图)。二环氮杂冠醚
在水溶液中对碱金属离子的稳定性(以 衡量,其值越大,稳定性越强)如下表所示。 与 尺
寸大小非常接近,但只能利用三环氮杂冠醚识别。下列说法正确的是( )
碱金属离子3.8
5.4
4.3
A. (a)分子中碳原子和氧原子杂化方式均为 且所有非氢原子共平面。
B. (a)和(b)分子的核磁共振氢谱的谱图相同
C. (b)分子与 形成的超分子相对更稳定
D. (c)分子中四个 原子构筑的空间有利于与 形成N—H…N氢键
二、填空题(包含4小题,共55分)
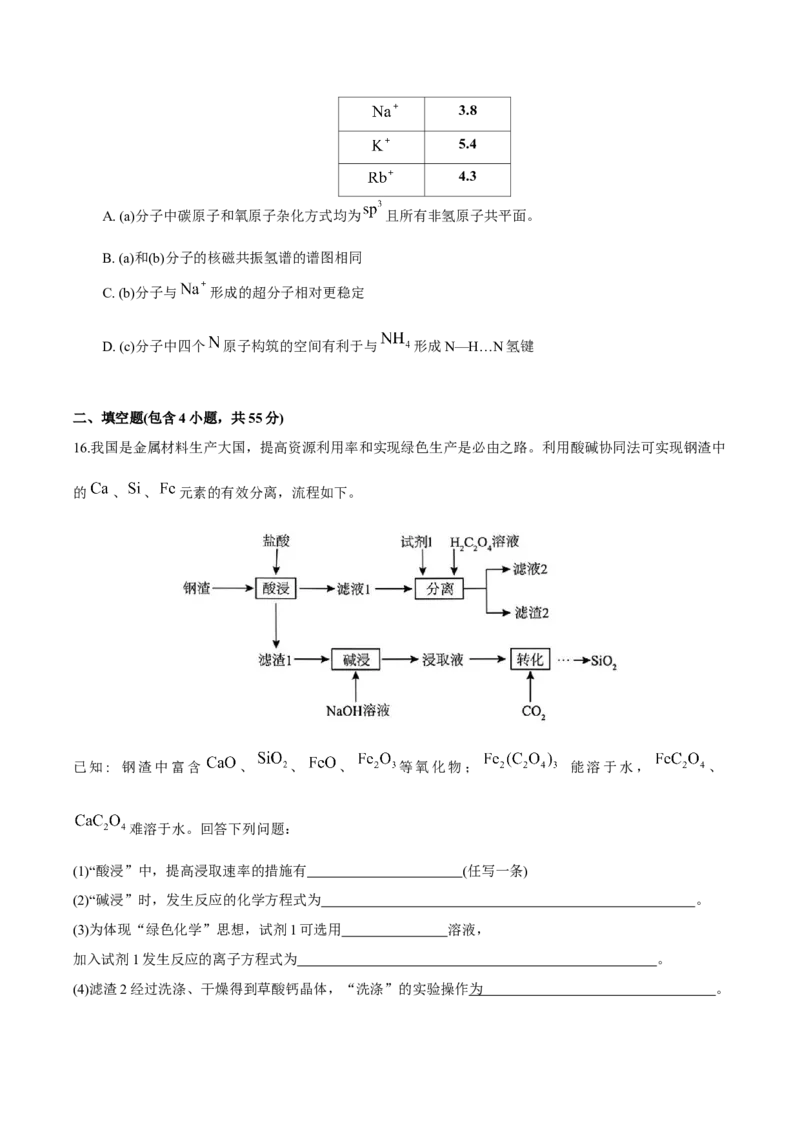
16.我国是金属材料生产大国,提高资源利用率和实现绿色生产是必由之路。利用酸碱协同法可实现钢渣中
的 、 、 元素的有效分离,流程如下。
已知: 钢渣中富含 、 、 、 等氧化物; 能溶于水, 、
难溶于水。回答下列问题:
(1)“酸浸”中,提高浸取速率的措施有 (任写一条)
(2)“碱浸”时,发生反应的化学方程式为 。
(3)为体现“绿色化学”思想,试剂1可选用 溶液,
加入试剂1发生反应的离子方程式为 。
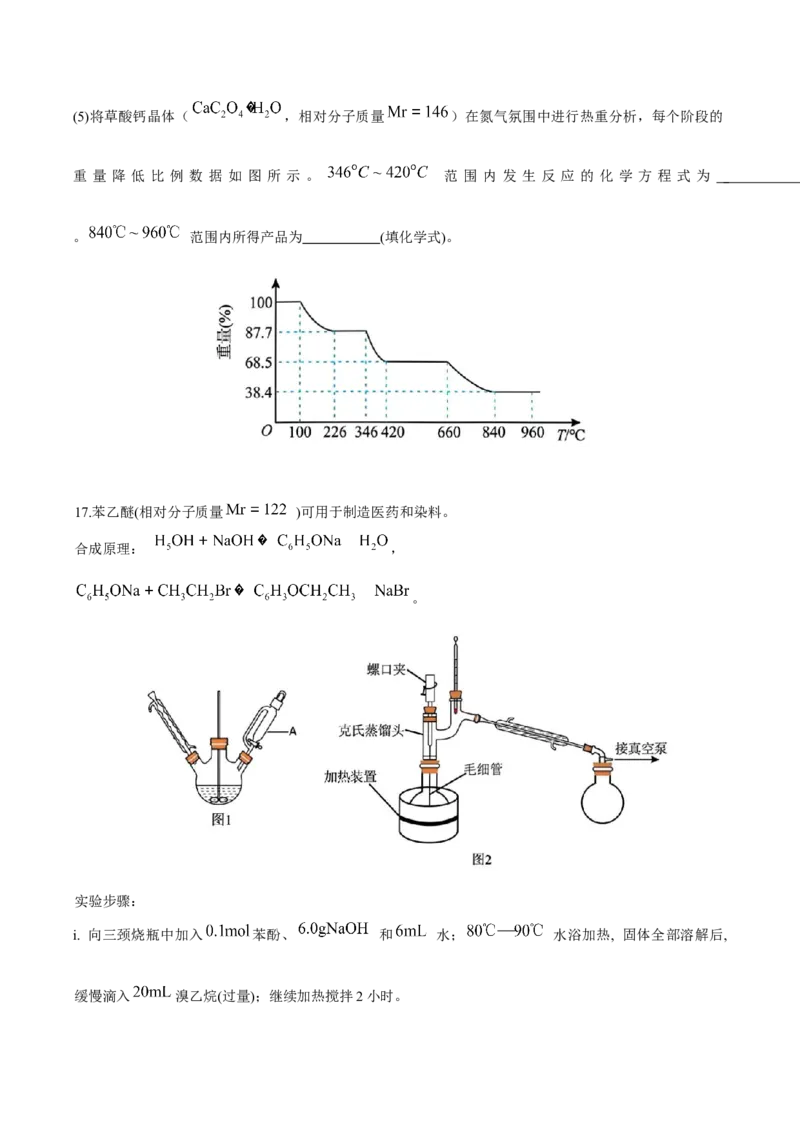
(4)滤渣2经过洗涤、干燥得到草酸钙晶体,“洗涤”的实验操作为 。(5)将草酸钙晶体( ,相对分子质量 )在氮气氛围中进行热重分析,每个阶段的
重 量 降 低 比 例 数 据 如 图 所 示 。 范 围 内 发 生 反 应 的 化 学 方 程 式 为
。 范围内所得产品为 (填化学式)。
17.苯乙醚(相对分子质量 )可用于制造医药和染料。
合成原理: ,
。
实验步骤:
i. 向三颈烧瓶中加入 苯酚、 和 水; 水浴加热, 固体全部溶解后,
缓慢滴入 溴乙烷(过量);继续加热搅拌2小时。ii. 冷却至室温,将三颈烧瓶中液体水洗分液,有机相用饱和食盐水洗涤两次,分离出有机相。
iii. 合并两次的洗涤液,用 乙醚提取一次,提取液与有机相合并,加入氯化钙并过滤,水浴蒸出乙
醚。常压蒸馏有机相,收集 左右的馏分,得10.7g粗产品,经过仪器测定,苯乙醚纯度为80%。
已知:①苯乙醚微溶于水,易溶于醇和醚。熔点——30℃,沸点172℃;溴乙烷沸点为38.4℃;溴乙烷和
乙醚都是易挥发的无色液体。②图2中克氏蒸馏头的螺口夹可调节毛细玻璃管的进气量。
回答下列问题:
(1)仪器A 的名称为 。
(2)步骤i温度控制在80—90℃,避免温度过高,除可能发生副反应外,另一重要原因
是 。
(3)步骤 ii中用饱和食盐水洗涤的优点是 。
(4)步骤 iii中加入氯化钙的目的是 。
(5)步骤 iii蒸馏可用如图2所示减压蒸馏装置,下列关于该装置的说法正确的是 (填标号)。
A. 毛细玻璃管可以起到防止暴沸的作用
B.克氏蒸馏头弯管的作用是防止液体剧烈沸腾冲入冷凝管
C.不可以将直形冷凝管替换为球形冷凝管
D.实施减压蒸馏时,应该先加热再启动真空泵减压
(6)苯乙醚的产率为 %(结果保留2位有效数字)
18.钛(Ti)是一种机械强度大、容易加工的耐高温金属,常用于制造合金。回答下列问题:
(1)基态 Ti原子核外电子的运动状态有 种,与Ti同周期且基态原子含有相同未成对电子数的主族元
素有 (填元素符号)。
(2)下列状态的 Ti原子中,失去最外层一个电子所需能量最大的是 (填字母)。
A. B.
C. D.
(3) 的极化能力强,不能从水溶液中获得其含氧酸正盐,只能得到水解产物如 和
。 的组成元素中第一电离能最大的是 (填元素符号)。
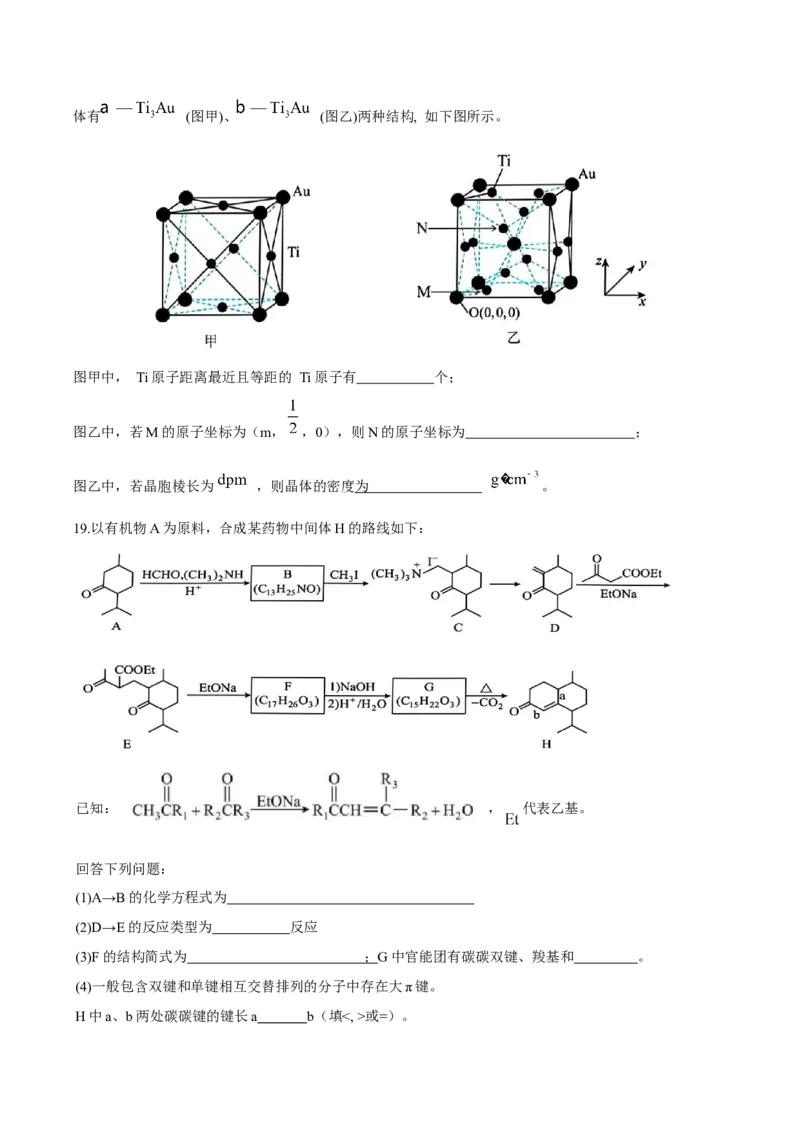
(4)超高硬度生物材料 (相对分子质量 )合金是理想的人工髋关节和膝关节材料,其晶体有 (图甲)、 (图乙)两种结构, 如下图所示。
图甲中, Ti原子距离最近且等距的 Ti原子有 个;
图乙中,若M的原子坐标为(m, ,0),则N的原子坐标为 ;
图乙中,若晶胞棱长为 ,则晶体的密度为 。
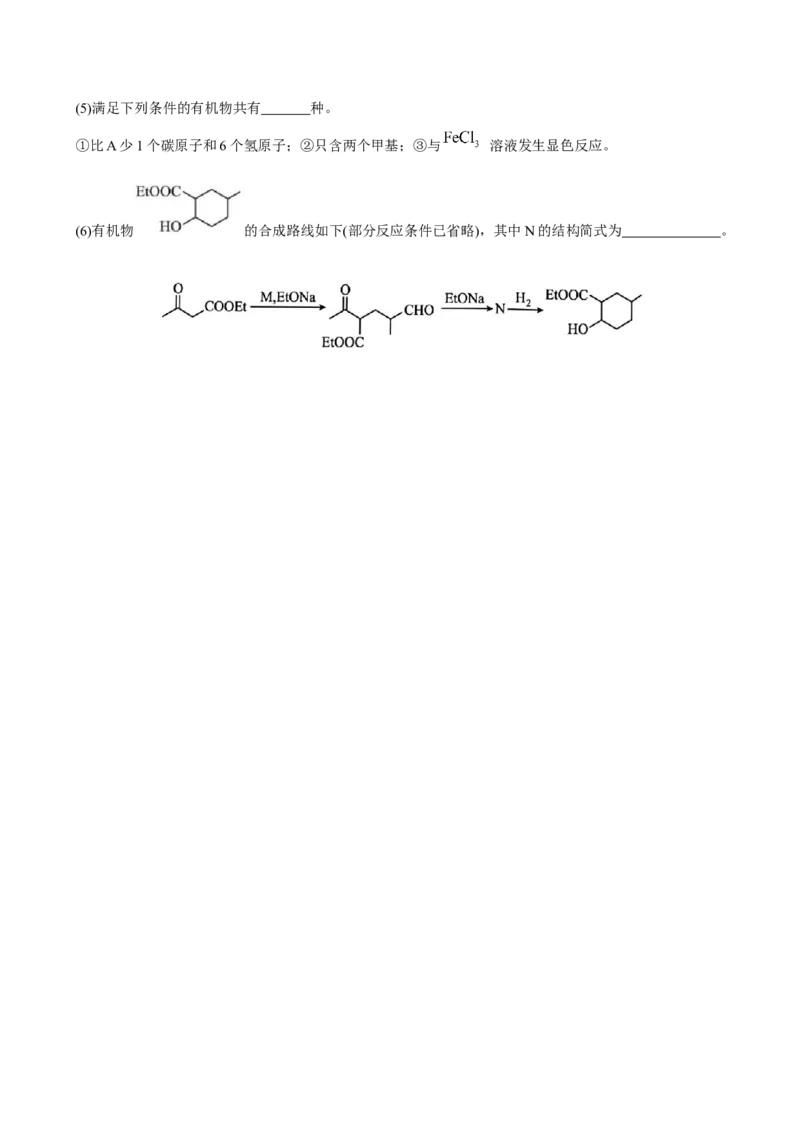
19.以有机物A为原料,合成某药物中间体H的路线如下:
已知: , 代表乙基。
回答下列问题:
(1)A→B的化学方程式为
(2)D→E的反应类型为 反应
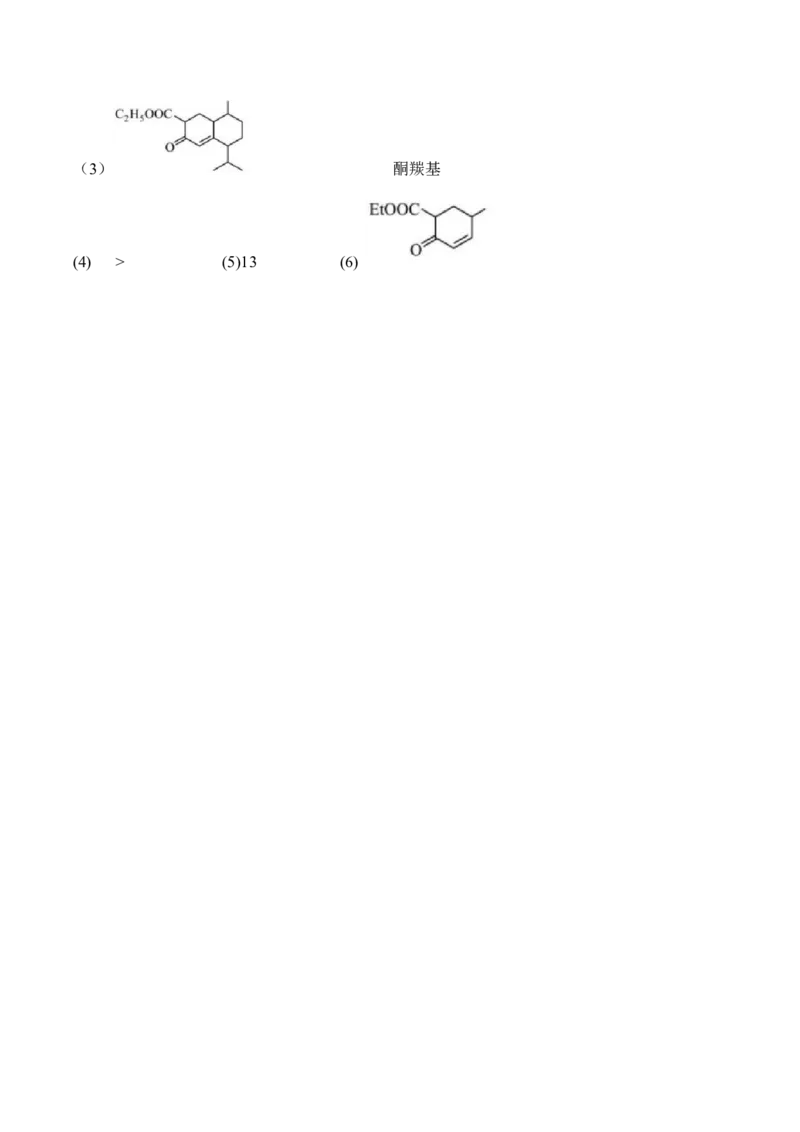
(3)F的结构简式为 ;G中官能团有碳碳双键、羧基和 。
(4)一般包含双键和单键相互交替排列的分子中存在大π键。
H中a、b两处碳碳键的键长a b(填<, >或=)。(5)满足下列条件的有机物共有 种。
①比A少1个碳原子和6个氢原子;②只含两个甲基;③与 溶液发生显色反应。
(6)有机物 的合成路线如下(部分反应条件已省略),其中N的结构简式为 。辽宁省实验中学2026届高三第二次模拟考试
化学试卷参考答案
1-5:DABDC 6-10:BDACA 11-15:BCCBD
16.(每空2分, 共14分)
(1)搅拌、粉碎钢渣、适当提高酸浸温度、适当增大盐酸浓度等(任写一条即可)
(2)
(3)
(4)向漏斗中加入蒸馏水至没过沉淀,待液体自然流净后重复操作两到三次(答案合理即可)
(5) ;
17.(前五个每空2分,最后一个空3分,共13分)
(1)恒压滴液漏斗 (2)防止溴乙烷大量挥发
(3)降低苯乙醚溶解度,便于分层且能减少其在水中的溶解损失
(4)除去有机相中的水 (5)ABC (6)70
18. (每空2分, 共14分)
(1)22 、
(2)D (3)N
(4) 8 ( )
19. (每空2分, 共14分)
(1)
(2)加成(3) 酮羰基
(4) > (5)13 (6)