文档内容
D.某溶液能与铝粉反应放出H : Na、 K、SO2、 Cl
北师大静海实验学校 2023-2024 学年第一学期高三年级 2 4
第一次阶段性评估
5.用N 表示阿伏加德罗常数,下列叙述正确的是( )
A
A.标准状况下,22.4LSO 中含有的分子数为N
化 学 试 题 3 A
B.标准状况下, 1molH O 的体积为22.4L
2 2
考试时间:60分钟 满分:100分
C.常温常压下,22.4LNH 含有的原子数目为0.4N
3 A
命题人: 审核人:
D.常温常压下,2gH 含有的原子数目2N
2 A
一、单选题(每题 3分,共计 60 分) 6.下列实验能达到目的的是( )
1.在无色透明强酸性溶液中,能大量共存的离子组是( )
A.将58.5gNaCl 溶于1L水中可得1mol/L的NaCl 溶液
A.Ca2+、K+、Cl-、NO B.Na+、OH-、Cl-、CO2
3 3 B.将标准状况下22.4LHCl 溶于1L水中可得1mol/L 盐酸
C.K+、Na+、MnO、SO2 D.Cl-、NH+、SO2、Ba2+ C.将40gNaOH 溶于水配成1L 溶液可得1mol/L 的NaOH 溶液
4 4 4 4
D.将78gNa O 溶于水配成1L溶液可得到浓度为1mol/L 的溶液
2.N 表示阿伏加 德罗常数,下列判断正确的是( ) 2 2
A
高温
A.在16g氧气中含有N 个分子
A 7.反应3SiO 6C2N Si N 6CO 中,氧化剂是
2 2 3 4
B.标准状况下,22.4L空气含有N 个分子
A
C.1molCl 参加反应转移电子数一定为2N A.N B.C C.Si N D.CO
2 A 2 3 4
D.含N A 个Na+的Na 2 O 溶解于1L水中,Na+的物质的量浓度为1mol·L—1 8.在溶液的配制过程中会引起浓度偏高的是( )
3.关于胶体的性质与应用,相关说法错误的是( ) A.配制500mL0.1mol/L 的硫酸铜溶液,用托盘天平称取胆矾8.0g
A.静电除尘器除去空气或工厂废气中的飘尘是利用胶体粒子的带电性而加以除 B.配制NaOH 溶液时,NaOH 固体放在烧杯中称量时间过长
去 C.定容时,仰视刻度线
B.明矾净水是利用胶体的吸附性 D.配制NaOH 溶液时,将称量好的NaOH 固体放入小烧杯中溶解,未经冷却立即转移
C.从颜色上无法区别 FeCl 溶液和Fe(OH) 胶体 到容量瓶中并定容
3 3
D.由于胶粒之间的排斥作用,胶粒不易聚集成大的颗粒,所以胶体的性质相对 9.下列化学反应中电子转移的表示方法正确的是( )
比较稳定
4.一定能在下列溶液中大量共存的离子组是( )
A.
A.使无色酚酞溶液呈红色的溶液中: Na、 K、 Cl、HCO
3
B.滴入KSCN溶液显现红色的溶液: K、Mg2、 Cl、 I
B.
C.使紫色石蕊溶液呈红色的溶液中: ClO、 Na、 Fe2、SO2
4
第1页(共4页)
{#{QQABbYiQogioABAAAQhCQwEQCgCQkAEAAIoGBBAIoAAAwAFABAA=}#}A.向FeSO 溶液中滴加NaOH 溶液,先生成白色沉淀
4
C.
B.在坩埚中对钠块加热,钠块熔化并燃烧,残留淡黄色固体
C.向脱脂棉包裹的干燥过氧化钠粉末滴几滴水,棉花燃烧
D.向硫酸铜稀溶液中加入绿豆大小的钠块,能置换出铜单质
D.
15.下列有关物质的性质与用途,不具有对应关系的是( )
A.FeCl 溶液呈酸性,可用于刻蚀铜板
3
10.氢化钠可以作为生氢剂(其中NaH 中氢元素为-1 价),反应方程式如下:
B.Al O 的熔点高,常用作耐火、耐高温材料
NaHH ONaOHH ,其中水的作用是( ) 2 3
2 2
A.既不是氧化剂也不是还原剂 B.是氧化剂 C.Na
2
O
2
与CO
2
反应,可用于潜艇中的供氧剂
C.是还原剂 D.既是氧化剂又是还原剂 D.NaClO具有强氧化性,常作为杀菌、消毒剂
11.由反应I +2KClO =2KIO +Cl 可推知的是( ) 16.下列关于除杂试剂的选择不 . 正 . 确 . 的是(括号中的物质为杂质)( )
2 3 3 2
A.氧化产物:Cl 2 B.氧化性:KIO 3 >KClO 3 A.Fe 2 O 3 Al 2 O 3 :NaOH溶液 B.Cl 2 (HCl):饱和食盐水
C.还原性:I 2 >Cl 2 D.每消耗0.1molI 2 ,转移0.2mol 电子 C.NaHCO Na CO :澄清石灰水 D.FeCl FeCl :Cl
3 2 3 3 2 2
12.同温同压下,1mol H 和1mol O ,下列有关它们的说法正确的是( )
2 2 17.下列离子方程式书写正确的是( )
A.质量相同,体积不同 B.分子数相同,质量不同
A.钠和冷水反应:Na+2H O=Na++2OH+H ↑
2 2
C.体积相同,分子数不同 D.体积相同,原子数不同
B.氯气通入水溶液中:Cl +H O=Cl-+ClO-+2H+
2 2
13.中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
C.Al O 粉末溶于NaOH 溶液中:Al O +2OH-=2AlO- +H O
2 3 2 3 2 2
选项 陈述Ⅰ 陈述Ⅱ 判断
D.FeCl 溶液通入足量的Cl 反应:Fe2++Cl =Fe3++2Cl-
2 2 2
A 碳酸钠溶液可用于治疗胃病 Na CO 可与盐酸反应 Ⅰ对,Ⅱ对,有
2 3
18.相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出
向Na O 的水溶液中滴入酚酞变
2 2
B Na O 与水反应生成氢氧化钠 Ⅰ对,Ⅱ错,无 的氢气在同温同压下体积之比为( )
2 2
红色
A.1:1 B.1:2 C.1:3 D.2:1
高压钠灯发出透雾能力强的
C 金属钠具有强还原性 Ⅰ对,Ⅱ对,有 19.侯德榜是我国杰出的化学家,“侯氏制碱法”的创始人。1926年,塘沽
黄光
“红三角”牌纯碱在万国博览会获金质奖章。反应:
Na O 能与CO 和H O反应生
2 2 2 2
D 过氧化钠可为航天员供氧 Ⅰ对,Ⅱ对,有
NaClCO NH H ONaHCO NH Cl ,是“侯氏制碱法”的重要反应。
成O 2 3 2 3 4
2
14.关于钠及其化合物的实验叙述错误的是( ) 下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确
第2页(共4页)
{#{QQABbYiQogioABAAAQhCQwEQCgCQkAEAAIoGBBAIoAAAwAFABAA=}#}的是( )
①根据实验目的,虚线框中的装置所用的试剂为 。
②装置C 中观察到的现象是 ,反应的化学方程式
A.小韩同学说:该条件下NaHCO 的溶解度较小
3
是 。
B.小韦同学说:NaHCO 不是纯碱
3 ③装置A 的作用是制备CO ,写出A中发生反应的化学方程式
2
C.小羊同学说:析出NaHCO 固体后的溶液中只含氯化铵,可做化肥 是 。
3
D.小任同学说:该反应是在饱和食盐水中先通入氨气,再通入二氧化碳
22.A~H分别表示中学化学中常见的某种物质,它们之间的相互转化关系如下图所示(部分
20. 某500mL溶液中含0.1mol Fe2+,0.2mol Fe3+,加入0.2mol铁粉,待Fe3+完 反应物、生成物未列出)。已知:C、D、E、F、G 五种物质中均含有同一种元素;A 为淡黄
全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)( )
色固体化合物;G为红褐色固体。
A.0.4mol/L B.0.6mol/L C.0.8mol/L D.1.0mol/L
二、综合题(每空 2分,共计 40 分)
21. 钠、碳及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有NaN 、Fe O 、KClO 、NaHCO
3 2 3 4 3
等物质。当汽车发生碰撞时,NaN 迅速分解产生N 和Na,同时放出大量的热。
3 2
(1)写出反应的化学方程式:
N 使气囊迅速膨胀,从而起到保护作用。
2
② 。
①KClO 的名称是 ,具有 (填“还原性”或“氧化性”)。
4
②Fe 2 O 3 可处理产生的Na,反应为6Na+Fe 2 O 3 =3Na 2 O+2Fe,反应中Na作 ⑥ 。
(填“还原剂”或“氧化剂”)。
(2)写出离子方程式:
(2)Na O 可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装
2 2
③ 。
置探究Na O 与CO 的反应。请回答下列问题:
2 2 2
⑤ 。
第3页(共4页)
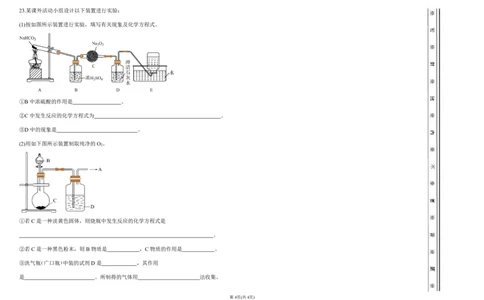
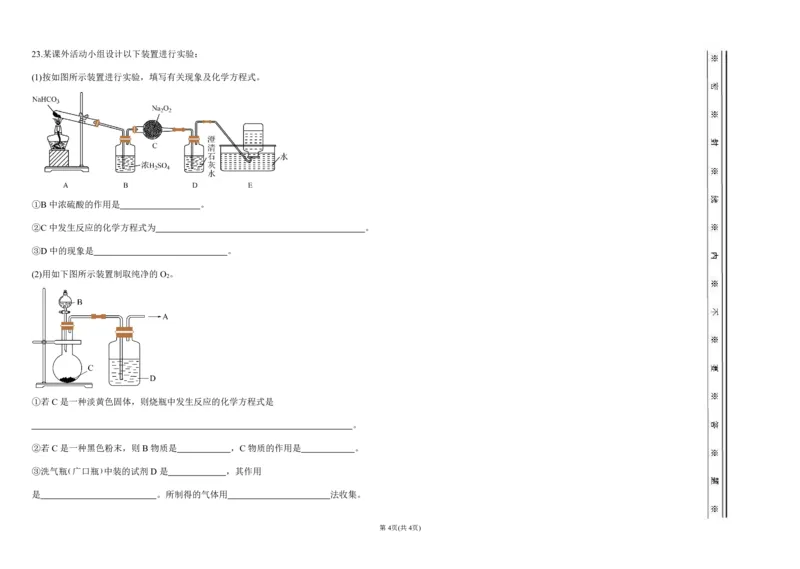
{#{QQABbYiQogioABAAAQhCQwEQCgCQkAEAAIoGBBAIoAAAwAFABAA=}#}23.某课外活动小组设计以下装置进行实验:
(1)按如图所示装置进行实验,填写有关现象及化学方程式。
①B 中浓硫酸的作用是 。
②C 中发生反应的化学方程式为 。
③D中的现象是 。
(2)用如下图所示装置制取纯净的O 。
2
①若 C 是一种淡黄色固体,则烧瓶中发生反应的化学方程式是
。
②若 C 是一种黑色粉末,则 B物质是 ,C 物质的作用是 。
③洗气瓶(广口瓶)中装的试剂D是 ,其作用
是 。所制得的气体用 法收集。
第4页(共4页)
{#{QQABbYiQogioABAAAQhCQwEQCgCQkAEAAIoGBBAIoAAAwAFABAA=}#}