文档内容
化学参考答案与解析
1.C 【解析】竹编和根雕所用材料均为纤维素,是有机高分子材料,A和 B选项错误;糖人所用材料为麦芽糖,
不是有机高分子材料,C正确;刺绣所用棉线由植物纤维素构成,丝线由蚕丝蛋白构成,均为有机高分子,D错
误;故答案选C。
2.D 【解析】金属钠、钾着火生成的过氧化钠、超氧化钾与泡沫灭火器喷出的二氧化碳反应生成氧气,故不能用泡
沫灭火器灭火,A错误;蒸馏过程忘加沸石,应该停止加热,冷却后补加沸石,B错误;高锰酸钾具有强氧化性,乙
醇具有还原性,二者不能放在同一橱窗,C错误;Cl是有毒气体,制备时应在通风橱中进行,D正确;故答案选D。
2
3.B 【解析】体积分数为75%的医用酒精可以使蛋白质变性,但没有强氧化性,A错误;泡沫灭火器灭火是利
用Al3+与HCO-互促水解生成CO 和大量泡沫,粘附在可燃物上,隔绝空气,从而达到灭火的目的,B正确;
3 2
用FeCl溶液刻蚀铜制电路板,2FeCl+Cu2FeCl+CuCl,利用了FeCl的氧化性比 CuCl强或者 Cu的
3 3 2 2 3 2
还原性比FeCl强的性质,C错误;热的纯碱溶液水解显碱性,油污在碱性条件下水解生成易溶于水的物质,
2
油污和纯碱之间无直接反应,D错误;故答案选B。
·· ··
4.A 【解析】HF分子之间的氢键结构为 ,A正确;HClO的电子式为 H:O:Cl:,B错
·· ··
误;HCl分子中共价键电子云轮廓图为 ,C错误;SO 的VSEPR模型为 ,D错误;故答案选A。
3
5.C 【解析】CH 可能是环戊烷或者戊烯,若为环戊烷,其σ键的数目为15N,A错误;标准状况下,NO 为液
5 10 A 2
态,22.4L不是1mol,B错误;120gNaHSO 晶体,其物质的量为1mol,阳离子为Na+,阴离子为HSO-,离子
4 4
总数为2N,C正确;随着反应的进行,浓盐酸变稀,反应停止,转移电子数小于0.6N,D错误;故答案选C。
A A
6.B 【解析】根据原子序数依次增大,Y与W同主族,结合Y形成2个共价键,W形成6个共价键,所以Y为氧
元素,W为硫元素,X比Y的原子序数小,比同周期相邻元素的第一电离能高,且X得到1个电子后尚能形成
2个共价键,所以X为氮元素,Z形成1个共价键,为氟元素,R带一个正电荷,为钠元素,据此作答。该化合
物阴离子半径比F-大,离子键弱,熔点低,A正确;核外电子排布相同时,核电荷数越大,对核外电子的吸引
力越强,离子半径越小,故离子半径为:O2->F->Na+,B错误;Y的氢化物为HO和HO,均为极性分子,C
2 2 2
正确;SO 和 SO 的中心原子均采用 sp2杂化,但 SO 的中心原子有一对孤电子对,对成键电子产生的斥力
2 3 2
大,键角小,D正确;故答案选B。
7.B 【解析】T分子中有2个手性碳原子,存在对映异构,不存在顺反异构,A错误;M与足量 H 加成后,产物
2
分子中除羧基碳原子外,其余8个碳原子均采用sp3杂化,B正确;1molT消耗5molBr,1molM消耗4mol
2
Br,物质的量之比为5∶4,C错误;T和M在一定条件下均可发生缩聚反应,但 T不能发生加聚反应,D错误;
2
故答案选B。
8.C 【解析】将凡士林涂在b端和d端,将旋塞推入时会堵塞液体通道,A错误;酸碱中和滴定时需加入指示剂
指示终点,B错误;采用控制变量法探究HO 溶液浓度对反应速率的影响,C正确;氯水具有漂白性,不能用
2 2
pH试纸测定其pH,D错误;故答案选C。
【化学答案 第1页(共5页)】
{#{QQABbQQAogigAIIAABgCAQX4CAKYkAGCAAgGAFAcoAAAgRFABAA=}#}
书书书9.D 【解析】F的电负性大于 Cl,吸电子能力强,导致 CFCOOH中羟基极性大,易电离,酸性强,pK 小,A正
3 a
确;NH 分子中心氮原子有一对孤电子对,[Cu(NH)]2+中氮原子无孤电子对,孤电子对与成键电子对之间
3 3 4
的斥力大于成键电子对与成键电子对之间的斥力,导致 NH 分子中 H—N—H键角减小,B正确;H—F键的
3
键能大于H—O键的键能,不易断裂,稳定性强,C正确;O 为弱极性分子,所以在非极性溶剂 CCl中的溶解
3 4
度大于在极性溶剂HO中的溶解度,D错误;故答案选D。
2
10.B 【解析】电解时Mn2+转化为 MnO,发生氧化反应,则 Y极为阳极,N为正极,M为负极,发生氧化反应,
2
A正确;N为正极,Li+嵌入,当N极质量增加1.4g时,增加0.2molLi+,转移0.2mol电子,同时有0.2mol
Cl-由b区移动至c区,B错误;X极电极反应式为2HO+2e-H↑ +2OH-,a区溶液的 OH-浓度增
2 2
大,pH增大,C正确;Y极电极反应式为Mn2+-2e-+2HOMnO +4H+,D正确;故答案选B。
2 2
11.A 【解析】Al(SO)溶液水解生成的硫酸无挥发性,加热蒸干后得到的白色固体为 Al(SO),A正确;向
2 4 3 2 4 3
含有酚酞的NaCO 溶液中加入BaCl溶液,溶液红色变浅,有可能是稀释引起的,不能证明存在水解平衡,
2 3 2
B错误;将盛有NO 与NO 混合气体的密闭容器体积压缩至原来的一半,增大压强,气体颜色先变深再变
2 2 4
浅,但比原来深,C错误;5mL0.1mol·L-1KI溶液加入6mL0.1mol·L-1FeCl溶液,Fe3+过量,加入KSCN
3
溶液,溶液肯定会变成血红色,不能证明Fe3+与I-发生的反应为可逆反应,D错误;故答案选A。
12.D 【解析】由图2的投影,结合铁元素的常见化合价可知,Na+在晶胞的12条棱心、体心及晶胞分割成的
1
8个小立方体的体心位置,个数为12× +1+8=12,A正确;由图1知阴离子在晶胞顶点和面心位置,个数
4
1 1
为8× +6× =4,故该晶体的化学式为 NaFeF,根据正负化合价代数和为零,可知铁元素的化合价为
8 2 3 6
4×M(NaFeF) 9.56×1032
+3,B正确;该晶体的密度为 3 6 g·cm-3= g·cm-3,C正确;距离最近的阴、阳离子
N(a×10-10)3 Na3
A A
槡3
是顶点的阴离子和小立方体体心的阳离子,阴、阳离子之间的最短距离为 apm,D错误;故答案选D。
4
13.C 【解析】路径 1的最大能垒是 73.33kJ·mol-1-(-37.63)kJ·mol-1=110.96kJ·mol-1,决速步骤为
CHOHCHO +H,A错误;路径 1的最大能垒是 110.96kJ·mol-1,路径 2的最大能垒是
3 3
106.1kJ·mol-1-(-37.63)kJ·mol-1=143.73kJ·mol-1,所以路径1更容易进行,路径1是甲醇脱氢制甲醛
的主要路径,B错误;过渡态1路径1断裂O—H键,路径2断裂C—H键,路径1比路径2能垒低,更容易进
行,O—H键比C—H键易断裂,C正确;最后一步除了 H—H键的形成还有分子脱附时能量的变化,所以
H—H键的键能不是22.25kJ·mol-1,D错误;故答案选C。
14.D 【解析】由图2可知,HAsO 的电离常数K =1×10-2.2,K =1×10-7.0,K =1×10-11.5,所以 NaAsO
3 4 a1 a2 a3 3 4
的K =K/K =1×10-2.5,数量级为10-3,A正确;根据电荷守恒:3c(AsO3-)+2c(HAsO2-)+c(HAsO-)
h1 w a3 4 4 2 4
+c(OH-)=c(Na+)+c(H+),pH=7时,c(H+)=c(OH-),c(HAsO2-)=c(HAsO-),所以3c(AsO3-)+
4 2 4 4
3c(HAsO2-)=c(Na+),B正确;已知吸附原理为吸附剂的带电基团可吸附异性离子,由图 1、图 2可知,
4
+3和+5两种价态的含砷微粒在不同pH时以分子或阴离子存在,所以吸附剂带正电荷越多、含砷微粒带
负电荷越多时,吸附效果越好,结合图像,pH在4~7时,吸附剂X带正电荷,而三价砷主要以中性分子形式
存在,所以,吸附剂对三价砷几乎不吸附,此时,五价砷几乎都以阴离子形式存在,吸附剂对五价砷的吸附量
比较大,可以加入氧化剂将三价砷转化为五价砷,提高吸附剂的吸砷量,C正确;当 pH>7时,吸附剂带负电
荷且pH越大,所带负电荷越多,而五价砷阴离子所带负电荷也增多,负电荷之间的斥力随之增大,吸附量陡
然降低,所以当pH>7之后,pH越大,吸附剂X对五价砷的吸附量越小,D错误;故答案选D。
【化学答案 第2页(共5页)】
{#{QQABbQQAogigAIIAABgCAQX4CAKYkAGCAAgGAFAcoAAAgRFABAA=}#}15.(14分,除注明外,每空2分)
△
【答案】(1)分液漏斗(1分) 防倒吸(1分) Cu+2HSO(浓)CuSO +SO↑+2HO
2 4 4 2 2
(2)防止氨水挥发、防止生成的(NH)SO 分解 溶液由红色变为无色
4 2 3
(3)SO +2OH-SO2-+HO
2 3 2
cV
(4)cV-2 2
1 1 2
(5)装置中O 会将生成的(NH)SO 氧化为(NH)SO,产率降低
2 4 2 3 4 2 4
【解析】甲装置制备SO,乙装置制备(NH)SO,由于SO 易溶于水,所以用仪器b防倒吸,丙装置吸收尾气
2 4 2 3 2
SO,乙装置反应温度不宜过高,否则氨水挥发或生成的(NH)SO 分解均可导致产品产率降低。如果反应
2 4 2 3
过程通入SO 过多,会生成NHHSO,通入SO 过少,氨水反应不完全,所以结合0.1mol·L-1(NH)SO 溶
2 4 3 2 4 2 3
液pH约为 8.5,当含有酚酞的氨水溶液由红色变为无色,表明氨水恰好生成(NH)SO。100mL
4 2 3
0.2mol·L-1的氨水理论上可生成100×10-3×0.1mol(NH)SO,通过滴定可计算生成的(NH)SO 为
4 2 3 4 2 3
( cV) ( cV)
cV-2 2 ×10-3×10mol,所以产率为 cV-2 2 ×100%,如果不先排出装置中的空气,装置中的 O
1 1 2 1 1 2 2
会将生成的(NH)SO 氧化为(NH)SO,产率降低。
4 2 3 4 2 4
16.(14分,每空2分)
【答案】(1)1s22s22p63s23p63d104s24p4(或[Ar]3d104s24p4)
△
(2)CuTe+6HSO(浓)2CuSO +4SO↑+TeO +6HO
2 2 4 4 2 2 2
(3)AgSO 微溶于水,存在沉淀溶解平衡:AgSO(s)幑幐2Ag+(aq)+SO2-(aq),加入少量 NaCl固体,Cl-
2 4 2 4 4
与Ag+反应,生成更难溶的AgCl,可防止银元素进入脱铜液。 BaSO、AgCl
4
(4)1∶2
(5)TeO2-+2SO2-+HOTe↓+2SO2-+2OH-
3 3 2 4
(6)蒸发浓缩、冷却结晶
【解析】(1)O、S、Se、Te均为ⅥA族元素,Se在第四周期,所以电子排布式为1s22s22p63s23p63d104s24p4(或
[Ar]3d104s24p4)。
(2)根据已知信息①并结合流程可知,含碲物料“焙烧”后,CuTe和浓 HSO 反应生成 CuSO、TeO、SO 和
2 2 4 4 2 2
△
HO,化学方程式为CuTe+6HSO(浓)2CuSO +4SO↑+TeO +6HO。
2 2 2 4 4 2 2 2
(3)“焙烧”后,所得烧渣为TeO、CuSO、PbSO 和AgSO,AgSO 微溶于水,存在沉淀溶解平衡:AgSO(s)
2 4 4 2 4 2 4 2 4
幑幐2Ag+(aq)+SO2-(aq),“水浸”时加入少量 NaCl固体,Cl-与 Ag+反应,生成更难溶的 AgCl,可防止银
4
元素进入脱铜液;CuSO 溶于水进入脱铜液,TeO 和PbSO 难溶于水,和生成的 AgCl进入下一步“碱溶”工
4 2 4
序,“碱溶”时TeO 和NaOH溶液反应生成NaTeO 溶液,所得滤渣为PbSO 和AgCl。
2 2 3 4
(4)“吸收”工序SeO、SO 与水反应转化为HSO 和Se,氧化剂和还原剂物质的量之比为1∶2。
2 2 2 4
(5)“碱溶”后所得溶液为NaTeO 溶液,用NaSO“还原”后得到碲粉,离子方程式为 TeO2-+2SO2-+HO
2 3 2 3 3 3 2
Te↓+2SO2-+2OH-。
4
(6)从“脱铜液”中得到CuSO·5HO的“系列操作”是蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
4 2
【化学答案 第3页(共5页)】
{#{QQABbQQAogigAIIAABgCAQX4CAKYkAGCAAgGAFAcoAAAgRFABAA=}#}17.(15分,除注明外,每空2分)
【答案】(1)2CO(g)+6H(g)幑幐CH(g)+4HO(g)ΔH=-128.1kJ·mol-1 低温(1分)
2 2 2 4 2
(2)bc
(3)L(1分) 降低(1分) 由图像可知随温度降低,反应②的平衡常数增大更快,所以低温时生成更多的
1
主产物,相当于抑制了副反应
(4p)4( p)
7 7
(4)>(1分)
(3p)6( p)2
14 14
(5)9CO +8e-+6HOCH +8HCO- CO 和O(1分,不全、有错不得分)
2 2 4 3 2 2
【解析】(1)根据盖斯定律,由① ×2+②计算可得 2CO(g)+6H(g)幑幐CH(g)+4HO(g)ΔH=
2 2 2 4 2
-128.1kJ·mol-1。该反应是气体分子数减少的反应,ΔS<0,ΔH<0,所以低温条件下自发进行。
(2)选取的物理量要满足的条件:未达到平衡时一直在变化,达到平衡后不变。
a.整个体系全是气体,质量和体积不变,密度一直不变。错误。
b.由反应②和③可以看出,反应过程分子数减少,压强会降低,达到平衡后压强不变。正确。
c.未达到平衡时,HO(g)的浓度一直在增加,达到平衡后不变。正确。
2
d.反应过程中CH 和CHOH物质的量相等是一个特殊的点,不代表达到平衡。错误。故选bc。
2 4 3
ΔH ΔH
(3)根据lnK=- +C的图像,斜率 - 越大说明反应的 -ΔH越大,即 ΔH越小,已知 ΔH <ΔH;由图
RT R 2 3
像可知随温度降低,反应②的平衡常数增大更快,所以低温时生成更多的主产物,相当于抑制了副反应。
(4)由第(1)问可知,2CO(g)+6H(g)幑幐CH(g)+4HO(g)ΔH<0,升高温度,平衡逆向移动,H 的平
2 2 2 4 2 2
衡转化率降低,观察图2可知,a点后升温,H 转化率升高,故 a点时反应未达平衡,正在向正向建立平衡,
2
所以v >v。c点后升温H 转化率降低,平衡逆向移动,故c点为平衡点,该点对应温度T的平衡常数K
正 逆 2 3 p
计算过程如下:
根据题中数据列三段式: 2CO(g)+6H(g)幑幐CH(g)+4HO(g)
2 2 2 4 2
开始/mol 1 3
变化/mol 0.8 2.4 0.4 1.6
平衡/mol 0.2 0.6 0.4 1.6 共2.8
p 3p p 4p
分压
14 14 7 7
(4p)4( p)
p4(HO)p(CH)
7 7
K = 2 2 4 = 。
p p6(H)p2(CO) (3p)6( p)2
2 2
14 14
(5)阴极:9CO +8e-+6HOCH +8HCO-;阳极:2HO-4e-O↑ +4H+,H++HCO-HO+
2 2 4 3 2 2 3 2
CO↑,所以阳极产生的气体是CO 和O。
2 2 2
18.(15分,除注明外,每空2分)
【答案】(1)对氯甲苯(4氯甲苯)(1分) 光照(1分)Cl(1分)
2
師師
(2) 帨帨
師師
Cl
【化学答案 第4页(共5页)】
O
師師
帨帨 羰基、醚键、羧基 C H ClO(1分,不考查Cl和O的顺序)
師師OCH 20 21 4
3
{#{QQABbQQAogigAIIAABgCAQX4CAKYkAGCAAgGAFAcoAAAgRFABAA=}#}浓HSO
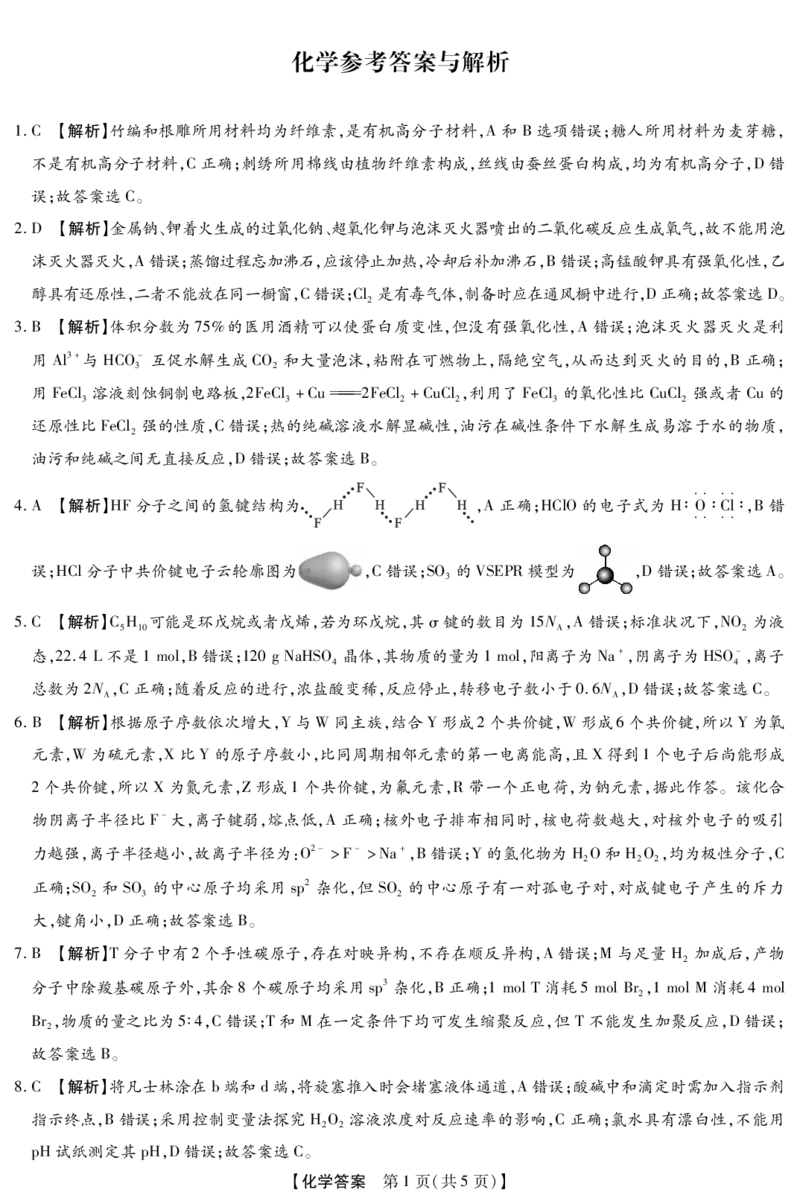
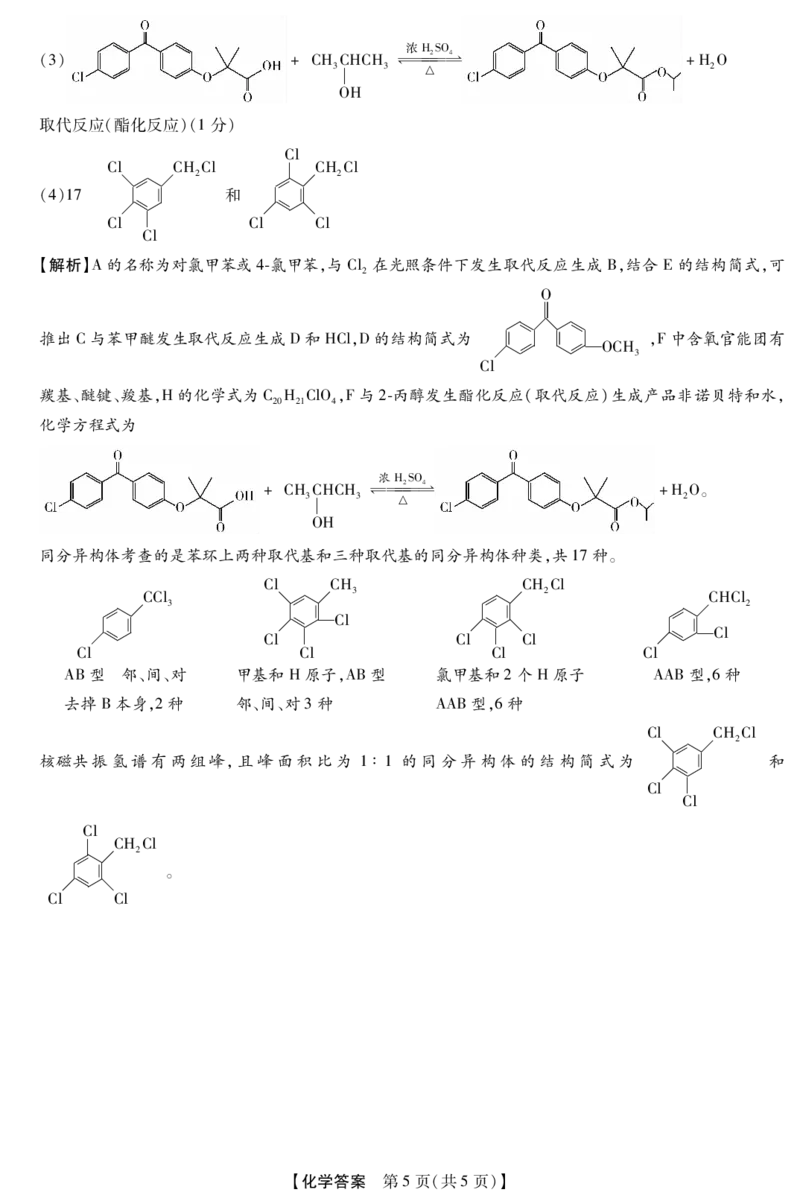
(3) +CHCHCH 幑帯帯帯2 幐4 +HO
3 3 △ 2
OH
取代反应(酯化反应)(1分)
Cl
Cl CHCl CHCl
師師 2 師師 2
(4)17 帪帪 和 帪帪
師師 師師
Cl Cl Cl
Cl
【解析】A的名称为对氯甲苯或4氯甲苯,与Cl在光照条件下发生取代反应生成 B,结合 E的结构简式,可
2
師師
推出C与苯甲醚发生取代反应生成D和HCl,D的结构简式为 帨帨
師師
Cl
【化学答案 第5页(共5页)】
O
師師
帨帨 ,F中含氧官能团有
師師OCH
3
羰基、醚键、羧基,H的化学式为C H ClO,F与2丙醇发生酯化反应(取代反应)生成产品非诺贝特和水,
20 21 4
化学方程式为
浓HSO
+CHCHCH 幑帯帯帯2 幐4 +HO。
3 3 △ 2
OH
同分异构体考查的是苯环上两种取代基和三种取代基的同分异构体种类,共17种。
Cl CH CHCl
CCl 師師 3 師師 2 CHCl
師師 3 帪帪 帪帪 師師 2
師師 Cl 師師
帪帪 帪帪
師師 Cl Cl Cl 師師 Cl
Cl Cl Cl Cl
AB型 邻、间、对 甲基和H原子,AB型 氯甲基和2个H原子 AAB型,6种
去掉B本身,2种 邻、间、对3种 AAB型,6种
Cl CHCl
師師 2
核磁共振氢谱有两组峰,且峰面积比为 1∶1的同分异构体的结构简式为 帪帪 和
師師
Cl
Cl
Cl
CHCl
師師 2
帪帪 。
師師
Cl Cl
{#{QQABbQQAogigAIIAABgCAQX4CAKYkAGCAAgGAFAcoAAAgRFABAA=}#}