文档内容
江苏省百校联考高三年级第一次考试
化 学 试 卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Mn 55 Zn 65
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
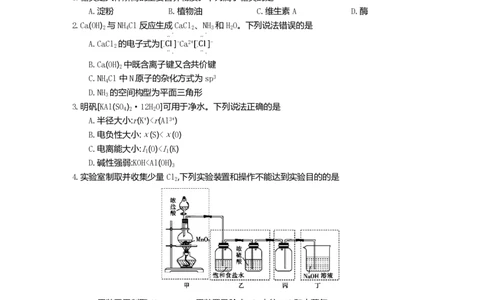
1.糖类是人体所需的重要营养物质。下列属于糖类的是
A.淀粉 B.植物油 C.维生素A D.酶
2.Ca(OH) 与NH Cl反应生成CaCl 、NH 和H O。下列说法错误的是
2 4 2 3 2
· ·
·· ··
A.CaCl 的电子式为[·Cl]-Ca2+[·Cl]-
2 · ·
··· ···
B.Ca(OH) 中既含离子键又含共价键
2
C.NH Cl中N原子的杂化方式为sp3
4
D.NH 的空间构型为平面三角形
3
3.明矾[KAl(SO ) ·12H O]可用于净水。下列说法正确的是
4 2 2
A.半径大小:r(K+)0
𝑐2(CO)·𝑐2(NO)
B.上述反应平衡常数为K=
𝑐2(CO )·𝑐(N )
2 2
C.上述反应中消耗1 mol NO时转移电子的数目为2×6.02 ×1023
D.将部分CO 分离出来,v(正)和NO平衡时转化率均增大
2
11.室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
A
向
静
盛
置
有
,观察
KBr
CC
溶
l 4
液
层
的
颜
试
色
管 中滴加几滴新制氯水,再加入CCl 4溶液,振荡、
Cl 2的氧化性比Br 2的强
B
向
化
盛 有SO 2水溶液的试管中滴加几滴酸性KMnO 4溶液,观察溶液颜色变
SO 2具有漂白性
C 向久置的FeSO 4溶液中滴加几滴KSCN溶液,振荡,观察溶液颜色变化 FeSO 4已全部变质
D 用pH试纸测得: CH
3
COONa溶液的pH约为9,NaNO 2溶液的pH约为8
H
C
N
H
O
3 C
2
O
电
OH
离
的
出
强
H +的能力比
12.室温下用0.1 mol·L-1 NaOH溶液吸收SO ,若通入SO 所引起的溶液体积变化和H O
2 2 2
挥发可忽略,溶液中含硫物种的浓度c =c(H SO )+c(HSO-)+c(SO2-)。H SO 电离常数分别为
总 2 3 3 3 2 3
K =1.54×10-2、K =1.00×10-7。下列说法正确的是
a1 a2
A.NaOH溶液吸收SO 所得到的溶液中:c(SO2-)>c(HSO-)>c(H SO )
2 3 3 2 3
B.NaOH完全转化为NaHSO 时,溶液中:c(H+)+c(SO2-)=c(OH-)+c(H SO )
3 3 2 3
C.NaOH完全转化为Na SO 时,溶液中:c(Na+)>c(SO2-)>c(OH-)>c(HSO-)
2 3 3 3
D.NaOH溶液吸收SO ,c =0.1 mol·L-1 溶液中:c(H SO ) >c(SO2-)
2 总 2 3 3
13.CO 催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
2
反应①:CO (g)+3H (g) CH OH(g)+H O(g) ΔH=-49.5 kJ·mol-1
2 2 3 2
反应②:CO (g)+H (g) CO(g)+H O(g) ΔH=41.2 kJ·mol-1
2 2 2
学科网(北京)股份有限公司在0.5 MPa条件下,将n(CO )∶n(H )为1∶3的混合气体以一定流速通过装有催化剂的反应器,
2 2
𝑛 (CH OH)
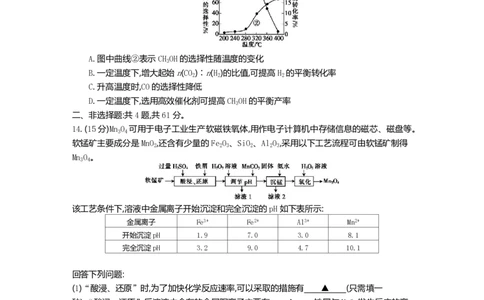
实验测得CO 的转化率、CH OH的选择性[ 生成 3 ×100%]与温度的关系如图所示。下列有
2 3 𝑛 (CO )
总转化 2
关说法正确的是
A.图中曲线②表示CH OH的选择性随温度的变化
3
B.一定温度下,增大起始n(CO )∶n(H )的比值,可提高H 的平衡转化率
2 2 2
C.升高温度时,CO的选择性降低
D.一定温度下,选用高效催化剂可提高CH OH的平衡产率
3
二、非选择题:共4题,共61分。
14.(15分)Mn O 可用于电子工业生产软磁铁氧体,用作电子计算机中存储信息的磁芯、磁盘等。
3 4
软锰矿主要成分是MnO ,还含有少量的Fe O 、SiO 、Al O ,采用以下工艺流程可由软锰矿制得
2 2 3 2 2 3
Mn O 。
3 4
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸、还原”时,为了加快化学反应速率,可以采取的措施有 ▲ (只需填一
种),“酸浸、还原”后溶液中含有的金属阳离子主要有 ▲ ,铁屑与MnO 发生反应的离
2
子方程式为 ▲ 。
(2)“调节pH”时加入H O 溶液的目的是 ▲ ,“调节pH”的范围为 ▲ 。
2 2
(3)“沉锰”时,其他条件一定,沉锰过程中锰离子的沉淀率与溶液温度的关系如图所示。50 ℃
后,溶液温度越高,锰离子的沉淀率越低的原因是 ▲ 。
学科网(北京)股份有限公司(4)“氧化”时一般控制温度在80 ℃~85 ℃,可以采取的加热方法是 ▲ ,反应化学方程
式为 ▲ 。
15.(15分)有机物F具有抗氧化性、抗肿瘤作用,其合成路线如图所示:
CHO C
6 6
A B D
E F
已知: CH CH Br CH CH MgBr
3 2 3 2
回答下列问题:
(1)B分子中碳原子的杂化轨道类型为 ▲ 。
(2)已知C的分子式为C H O ,C的结构简式为 ▲ 。
7 6 2
(3)反应⑤的类型为 ▲ 。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式: ▲ 。
①能与FeCl 溶液发生显色反应
3
②能发生银镜反应
③核磁共振氢谱显示有4种不同化学环境的氢,其峰面积比为6∶2∶1∶1
(5)请设计以乙醛和甲苯为原料制 的合成路线流程图。(无机试剂任用,合
成路线流程图示例见本题题干)
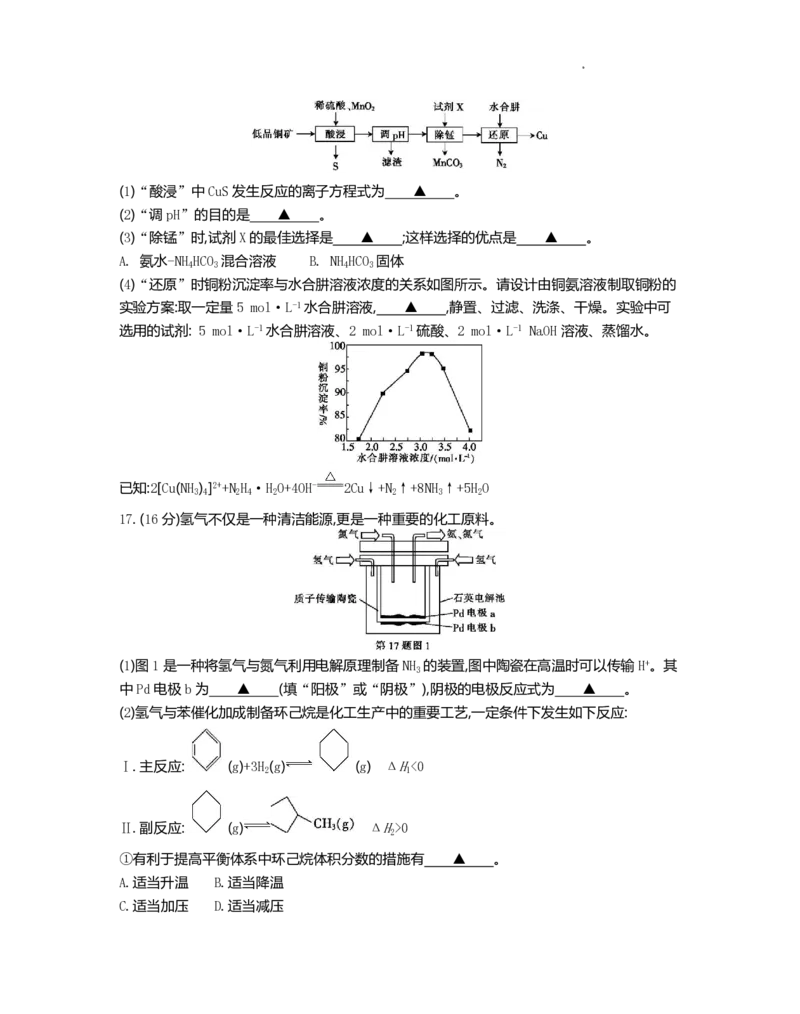
16.(15分)用低品铜矿(主要含CuS、FeO)制备铜粉的一种工艺流程如下:
学科网(北京)股份有限公司(1)“酸浸”中CuS发生反应的离子方程式为 ▲ 。
(2)“调pH”的目的是 ▲ 。
(3)“除锰”时,试剂X的最佳选择是 ▲ ;这样选择的优点是 ▲ 。
A. 氨水-NH HCO 混合溶液 B. NH HCO 固体
4 3 4 3
(4)“还原”时铜粉沉淀率与水合肼溶液浓度的关系如图所示。请设计由铜氨溶液制取铜粉的
实验方案:取一定量5 mol·L-1水合肼溶液, ▲ ,静置、过滤、洗涤、干燥。实验中可
选用的试剂: 5 mol·L-1水合肼溶液、2 mol·L-1硫酸、2 mol·L-1 NaOH溶液、蒸馏水。
已知:2[Cu(NH ) ]2++N H ·H O+4OH- 2Cu↓+N ↑+8NH ↑+5H O
3 4 2 4 2 2 3 2
17.(16分)氢气不仅是一种清洁能源,更是一种重要的化工原料。
(1)图1是一种将氢气与氮气利用电解原理制备NH 的装置,图中陶瓷在高温时可以传输H+。其
3
中Pd电极b为 ▲ (填“阳极”或“阴极”),阴极的电极反应式为 ▲ 。
(2)氢气与苯催化加成制备环己烷是化工生产中的重要工艺,一定条件下发生如下反应:
Ⅰ.主反应: (g)+3H (g) (g) ΔH<0
2 1
Ⅱ.副反应: (g) ΔH>0
2
①有利于提高平衡体系中环己烷体积分数的措施有 ▲ 。
A.适当升温 B.适当降温
C.适当加压 D.适当减压
学科网(北京)股份有限公司②反应Ⅰ在管式反应器中进行,实际投料往往在n(H )∶n(C H )=3∶1的基础上适当增大H 用量,
2 6 6 2
其目的是 ▲ 。
③图2是氢气与苯反应的机理,该过程可描述为 ▲ ;当H 中混有微量H S或CO等杂质
2 2
时,会导致反应Ⅰ的产率降低,推测其可能原因为 ▲ 。
④催化剂载体中的酸性中心能催化苯及环己烷的裂解。已知酸性中心可结合孤电子对,图3中
可作为酸性中心的原子的标号是 ▲ (填“a”、“b”或“c”)。
学科网(北京)股份有限公司江苏省百校联考高三年级第一次考试
化学试卷参考答案
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.A 2.D 3.B 4.C 5.A 6.B 7.C 8.D 9.D 10.C 11.A 12.C 13.B
二、非选择题:共4题,共61分。
14.(15分)
(1)粉碎软锰矿、搅拌、加热、适当增大硫酸的浓度(2分) Mn2+、Fe2+、Al3+(2分)
3MnO
2
+12H++2Fe 3Mn2++2Fe2++6H
2
O(2分)
(2)把Fe2+氧化为Fe3+(2分) 4.7~8.1(或4.7≤pH<8.1)(2分)
(3)温度升高,氨水发生分解并挥发(2分)
(4)水浴加热(1分) 3Mn(OH)2 +H
2
O
2
Mn
3
O
4
+4H
2
O(2分)
15.(15分)
(1)sp2、sp3(2分)
(2) (3分)
(3)取代反应(2分)
(4) 或 (3分)
(5)
(5分)
16.(15分)
(1)CuS+MnO
2
+4H+ Mn2++Cu2++S+2H
2
O (3分)
学科网(北京)股份有限公司(2)将Fe3+转化为Fe(OH)3除去(2分)
(3)A(2分) 使用碳酸氢铵时会有二氧化碳放出,导致碳元素利用率低,且有液体外溢的危险(3分)
(4)加入蒸馏水稀释至3 mol·L-1~3.25 mol·L-1,加入适量2 mol·L-1 NaOH溶液,边搅拌边逐滴加入铜氨溶液,
加热使其充分反应,同时用2 mol·L-1硫酸吸收反应中放出的NH 3,直至溶液中无气泡产生,停止滴加(5分)
17.(16分)
(1)阳极(2分) N
2
+6H++6e- 2NH 3(3分)
(2)①BC(2分)
②提高苯的利用率(2分)
③氢气在金属催化剂表面转化为氢原子,氢原子和苯分子吸附在催化剂表面活性中心,发生反应生成环己烷(3
分) 金属催化剂会与H 2 S或CO反应从而失去催化活性或者H 2 S、CO导致催化剂中毒而失去催化活性(2分)
④b(2分)
学科网(北京)股份有限公司