文档内容
2024 年兰州市高三诊断考试
化学
注意事项:
1.答卷前。考生务必将自已的姓名、准考证号填写在答题卡上。
2.回答选择题时。选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号框涂黑。如需
改动。用橡皮擦干净后,再选涂其它答案标号框。回答非选择题时,将答案写在名题卡上。写
在木试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Be-9 C-12 N-14 O-16 P-31
S-32 Cl-35.5
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
符合题目要求。
1.我国古代劳动人民对化学发展做出了重要贡献。下列有关文献记载中蕴含的化学知识叙述不正确的是( )
A.唐代韩愈的《晚春二首·其二》中写到:“榆荚只能随柳絮,等闲撩乱走空园”,诗词中的“柳絮”主要成
分为纤维素
B.东晋葛洪《肘后备急方》记载:“青蒿一握,以水二升渍,绞取汁”,用此法提取青蒿素的操作中“渍”
和“绞”分别表示浸取、过滤,涉及的操作均为物理方法
C.《荀子·劝学》写到:冰,水为之,而寒于水。冰变为水属于吸热反应
D.《本草纲目》记载:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次...价值数倍也”涉及的操作为蒸馏
2.2023年中国“大国重器”频频问世,彰显了中国科技发展的巨大成就。下列有关说法正确的是( )
A.“天问一号”火星车的保温材料为纳米气凝胶,能产生丁达尔效应
B.“梦天实验舱”原子钟利用电子跃迁计时,工作时发生化学变化
C.长征2号运载火箭的整流罩端头材料玻璃钢属于金属材料
D.中国天眼发现纳赫兹引力波,其使用的碳化硅材料为有机高分子材料
3.化学用语是表述化学学科知识的专业语言符号。下列说法不正确的是( )
A.基态Cr原子的价电子排布式:3d54s1
B.ClO的电子式:
2
C.OF 和ClO-的VSEPR模型均为四面体形
2 2
D.ICl和NH 均为极性分子
3
4.下图装置可用于收集气体并验证其某些化学性质,下列相关的选项正确的是( )
选项 气体 试剂 现象 结论
学科网(北京)股份有限公司A NH 酚酞溶液 溶液变红色 氨气显碱性
3
B SO 酸性KMnO 溶液 溶液褪色 SO 具有漂白性
2 4 2
C HCl 硅酸钠溶液 生成白色沉淀 Cl的非金属性比Si强
D Cl Kl-淀粉溶液 溶液变蓝 Cl 具有氧化性
2 2
5.有机小分子X通过选择性催化聚合可分别得到聚合物Y和Z,下列说法正确的是( )
A.Y和Z互为同系物
B.X的结构可表示为:
C.Y和Z均能使酸性高锰酸钾溶液褪色
D.Y和Z均能在NaOH溶液中降解为小分子
6.磷烷(PH )是集成电路、太阳能电池等电子工业生产的原材料。工业上制备PH 的反应原理为:
3 3
。N 表示阿伏加德罗常数,下列说法正确的
A
是( )
A.常温下pH=13的NaOH溶液中水电离出的c(OH-)=0.1mol/L
B.0.1mol/L的NaH PO 溶液中HPO -的数目小于0.1N
2 2 2 2 A
C.3.1g白磷中共价键的数目为0.6N
A
D. 每转移3个电子,生成 磷烷
7.海洋中有丰富的“食品、矿产、能源、药物和水产资源”等,下列说法正确的是( )
A.“氯碱工业”制碱的离子方程式:
B.第③步的反应可在“直接加热”的条件下实现
C.第⑤步、第⑥步中试剂可以选用SO 水溶液和稀硫酸
2
学科网(北京)股份有限公司D.第②步中应向“精盐”水溶液中先通入NH ,再通入CO
3 2
8.阿散酸(XWQYZ )被用作畜禽饲料的抗菌剂,所含W、X、Y、Z、Q是核电荷数依次增大的前四周期主
6 8 3
族元素。其中X、Y、Z同周期,Y、Q同主族,Q的最高能层为N层。基态X原子s轨道上的电子数是p轨
道上的电子数2倍,且与基态Z原子具有相同的未成对电子数。下列说法不正确的是( )
A.X、Y、Q的最高价氧化物对应水化物的酸性,Y的最强
B.X、Y、Z第一电离能大小顺序为:Z>Y>X
C.X、Y、Z分别与W形成的化合物可能均含极性键和非极性键
D.简单氢化物的沸点高低顺序为:Z>Y>X
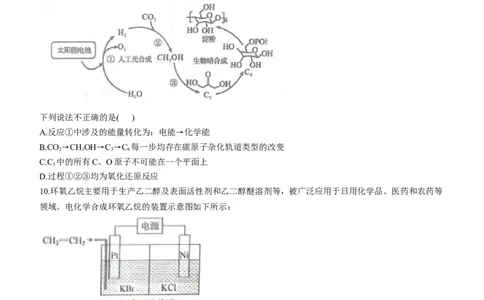
9.我国科学家实现了CO 到淀粉的人工合成,有利于“碳中和”的实现。其物质转化过程示意图如下:
2
下列说法不正确的是( )
A.反应①中涉及的能量转化为:电能→化学能
B.CO →CHOH→C →C 每一步均存在碳原子杂化轨道类型的改变
2 3 3 6
C.C 中的所有C、O原子不可能在一个平面上
3
D.过程①②③均为氧化还原反应
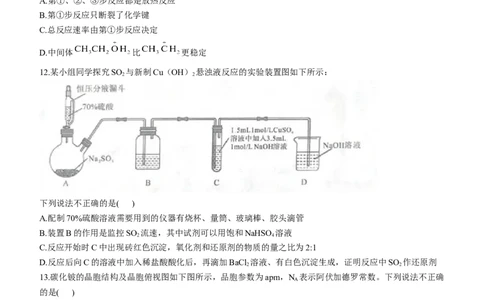
10.环氧乙烷主要用于生产乙二醇及表面活性剂和乙二醇醚溶剂等,被广泛应用于日用化学品、医药和农药等
领域。电化学合成环氧乙烷的装置示意图如下所示:
已知:
下列说法不正确的是
A.Pt电极接电源正极
B.Pt电极区的反应方程式为:
C.制备1mol环氧乙烷,Ni电极区产生标准状况下22.4LH
2
D.电解完成后,将阳极区和阴极区溶液混合才可得到环氧乙烷
学科网(北京)股份有限公司11.乙烯在酸催化下水合制乙醇的反应机理、能量与反应进程的关系加下图所示:
下列叙述正确的是( )
A.第①、②、③步反应都是放热反应
B.第①步反应只断裂了化学键
C.总反应速率由第①步反应决定
D.中间体 比 更稳定
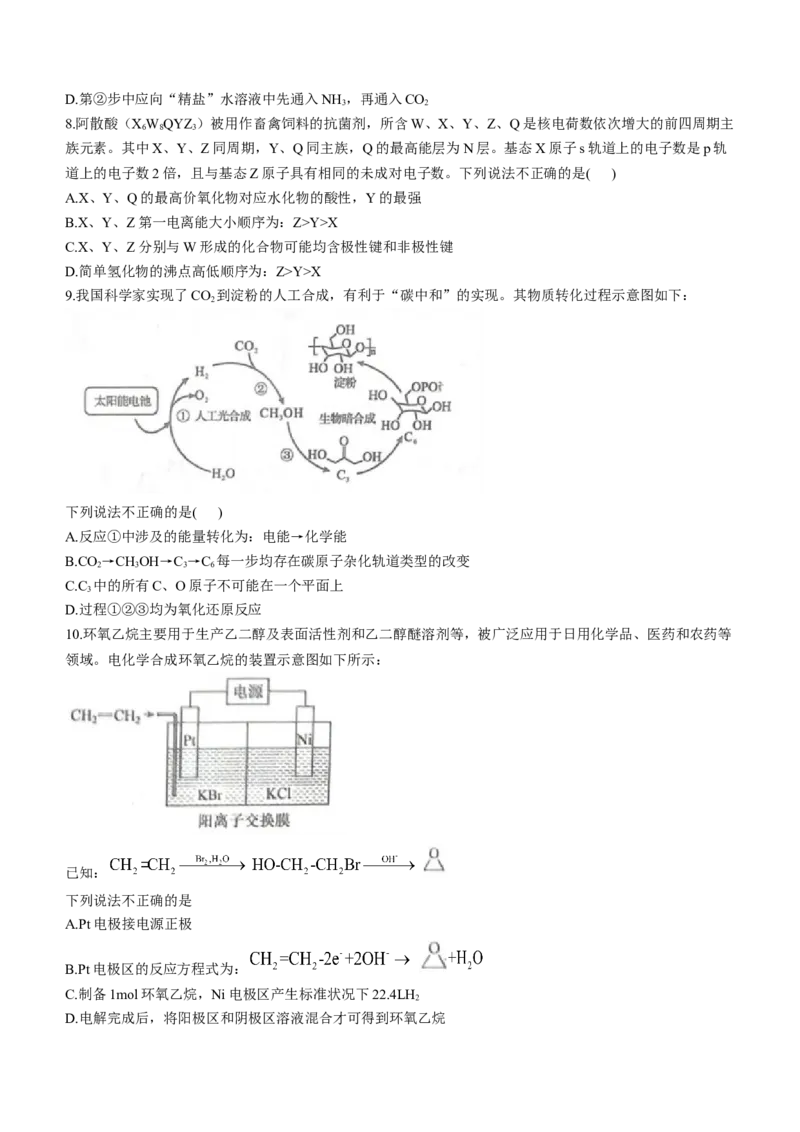
12.某小组同学探究SO 与新制Cu(OH) 悬浊液反应的实验装置图如下所示:
2 2
下列说法不正确的是( )
A.配制70%硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管
B.装置B的作用是监控SO 流速,其中试剂可以用饱和NaHSO 溶液
2 4
C.反应开始时C中出现砖红色沉淀,氧化剂和还原剂的物质的量之比为2:1
D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl 溶液、有白色沉淀生成,证明反应中SO 作还原剂
2 2
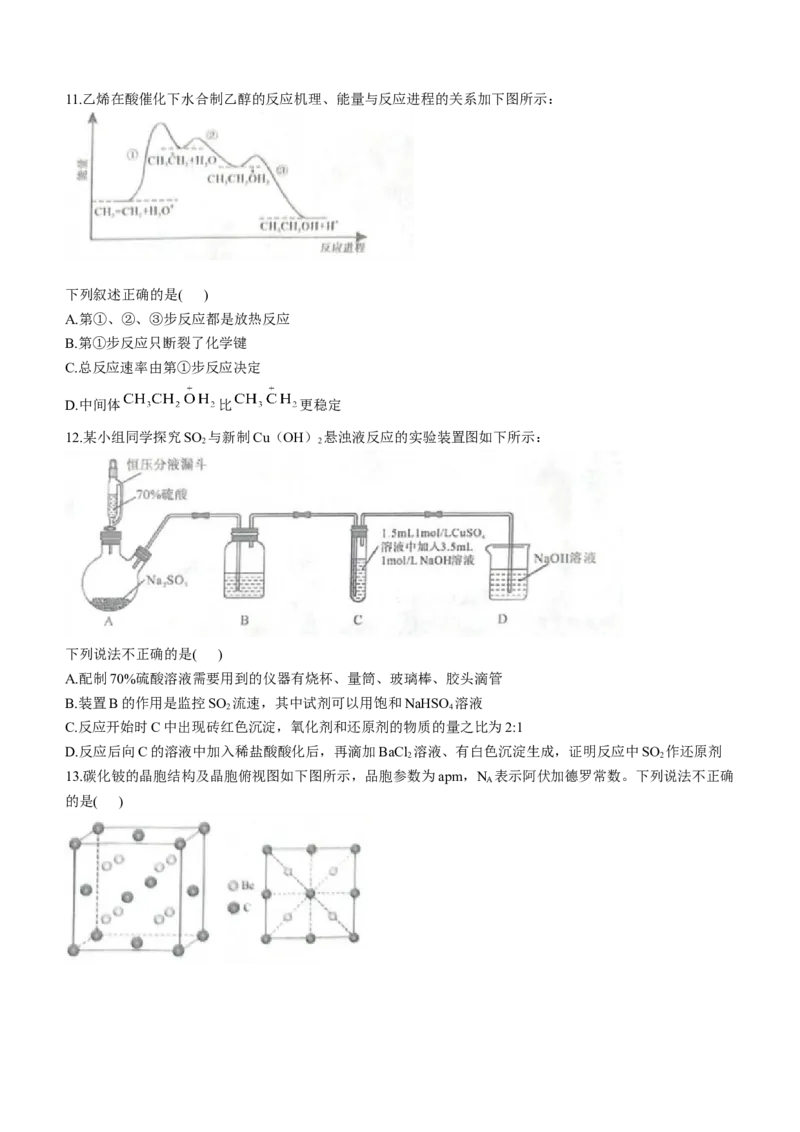
13.碳化铍的晶胞结构及晶胞俯视图如下图所示,品胞参数为apm,N 表示阿伏加德罗常数。下列说法不正确
A
的是( )
学科网(北京)股份有限公司A. 铍原子和碳原子之间的最近距离为 a pm
B.与碳原子周围距离最近的铍原子有8个
C.碳化铍的密度为
D.碳化铍与水反应的方程式为
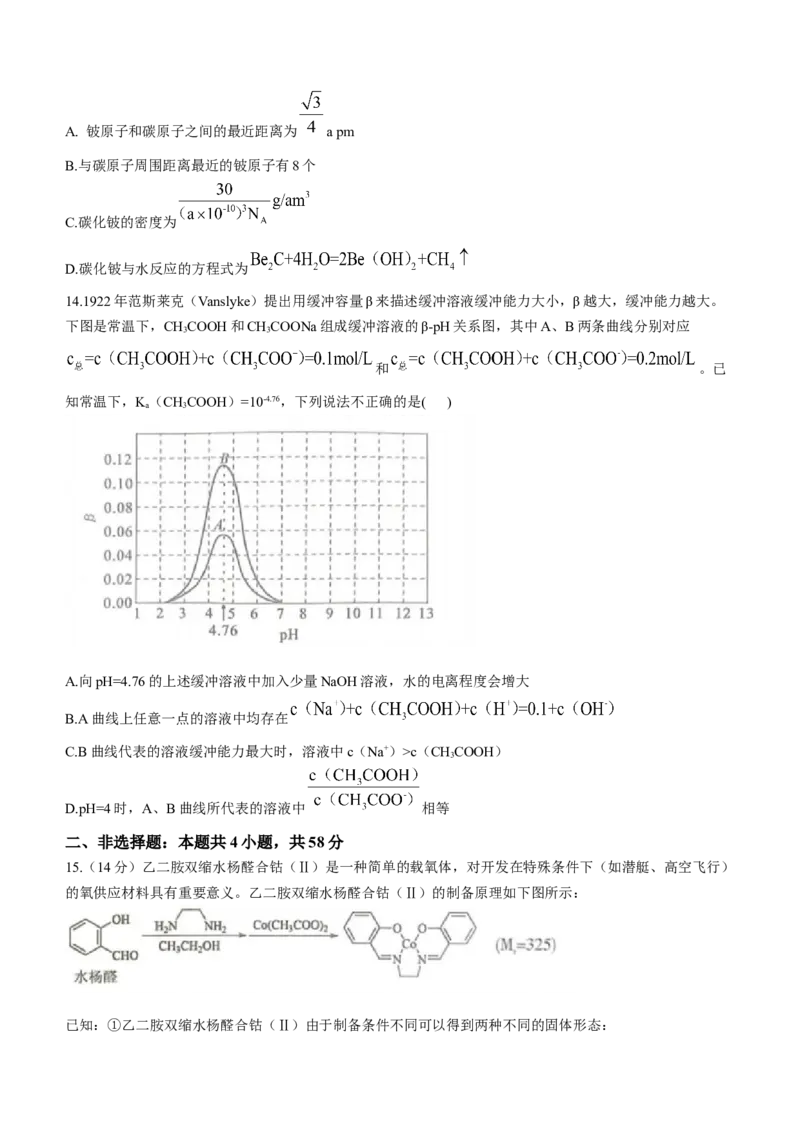
14.1922年范斯莱克(Vanslyke)提出用缓冲容量β来描述缓冲溶液缓冲能力大小,β越大,缓冲能力越大。
下图是常温下,CHCOOH和CHCOONa组成缓冲溶液的β-pH关系图,其中A、B两条曲线分别对应
3 3
和 。已
知常温下,K(CHCOOH)=10-4.76,下列说法不正确的是( )
a 3
A.向pH=4.76的上述缓冲溶液中加入少量NaOH溶液,水的电离程度会增大
B.A曲线上任意一点的溶液中均存在
C.B曲线代表的溶液缓冲能力最大时,溶液中c(Na+)>c(CHCOOH)
3
D.pH=4时,A、B曲线所代表的溶液中 相等
二、非选择题:本题共4小题,共58分
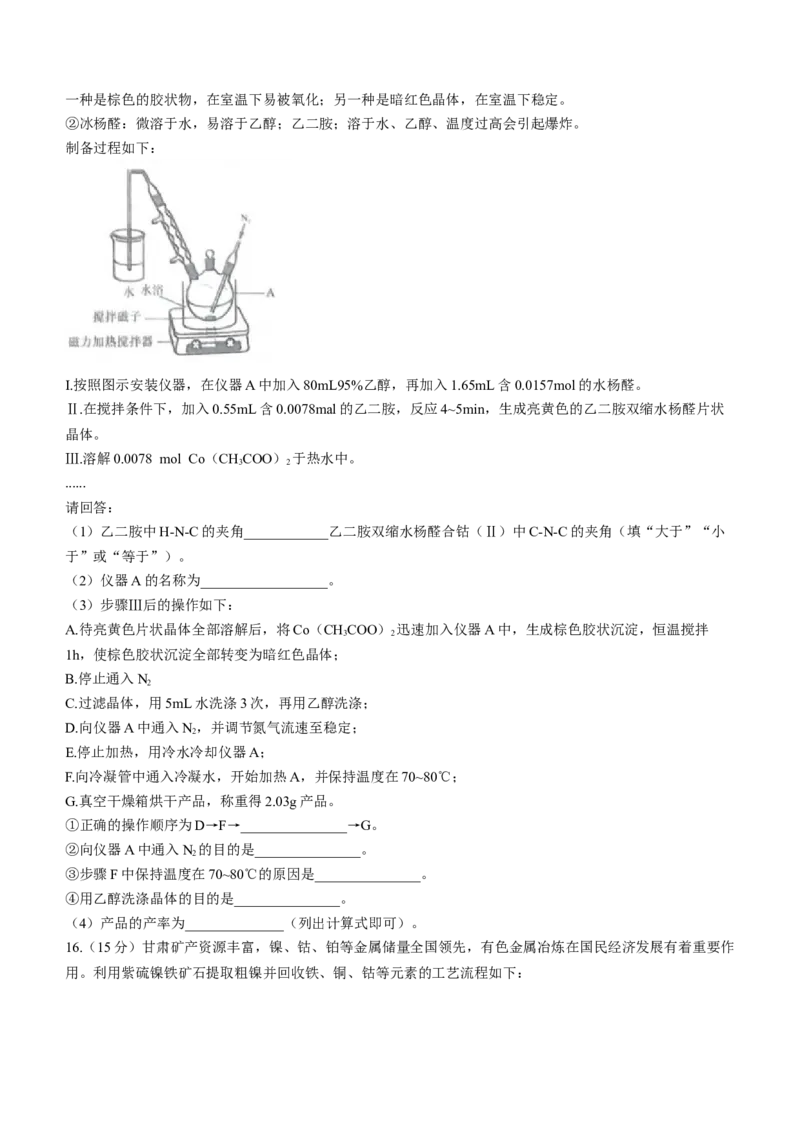
15.(14分)乙二胺双缩水杨醛合钴(Ⅱ)是一种简单的载氧体,对开发在特殊条件下(如潜艇、高空飞行)
的氧供应材料具有重要意义。乙二胺双缩水杨醛合钴(Ⅱ)的制备原理如下图所示:
已知:①乙二胺双缩水杨醛合钴(Ⅱ)由于制备条件不同可以得到两种不同的固体形态:
学科网(北京)股份有限公司一种是棕色的胶状物,在室温下易被氧化;另一种是暗红色晶体,在室温下稳定。
②冰杨醛:微溶于水,易溶于乙醇;乙二胺;溶于水、乙醇、温度过高会引起爆炸。
制备过程如下:
I.按照图示安装仪器,在仪器A中加入80mL95%乙醇,再加入1.65mL含0.0157mol的水杨醛。
Ⅱ.在搅拌条件下,加入0.55mL含0.0078mal的乙二胺,反应4~5min,生成亮黄色的乙二胺双缩水杨醛片状
晶体。
Ⅲ.溶解0.0078 mol Co(CHCOO) 于热水中。
3 2
......
请回答:
(1)乙二胺中H-N-C的夹角____________乙二胺双缩水杨醛合钴(Ⅱ)中C-N-C的夹角(填“大于”“小
于”或“等于”)。
(2)仪器A的名称为__________________。
(3)步骤Ⅲ后的操作如下:
A.待亮黄色片状晶体全部溶解后,将Co(CHCOO) 迅速加入仪器A中,生成棕色胶状沉淀,恒温搅拌
3 2
1h,使棕色胶状沉淀全部转变为暗红色晶体;
B.停止通入N
2
C.过滤晶体,用5mL水洗涤3次,再用乙醇洗涤;
D.向仪器A中通入N,并调节氮气流速至稳定;
2
E.停止加热,用冷水冷却仪器A;
F.向冷凝管中通入冷凝水,开始加热A,并保持温度在70~80℃;
G.真空干燥箱烘干产品,称重得2.03g产品。
①正确的操作顺序为D→F→_______________→G。
②向仪器A中通入N 的目的是_______________。
2
③步骤F中保持温度在70~80℃的原因是_______________。
④用乙醇洗涤晶体的目的是_______________。
(4)产品的产率为______________(列出计算式即可)。
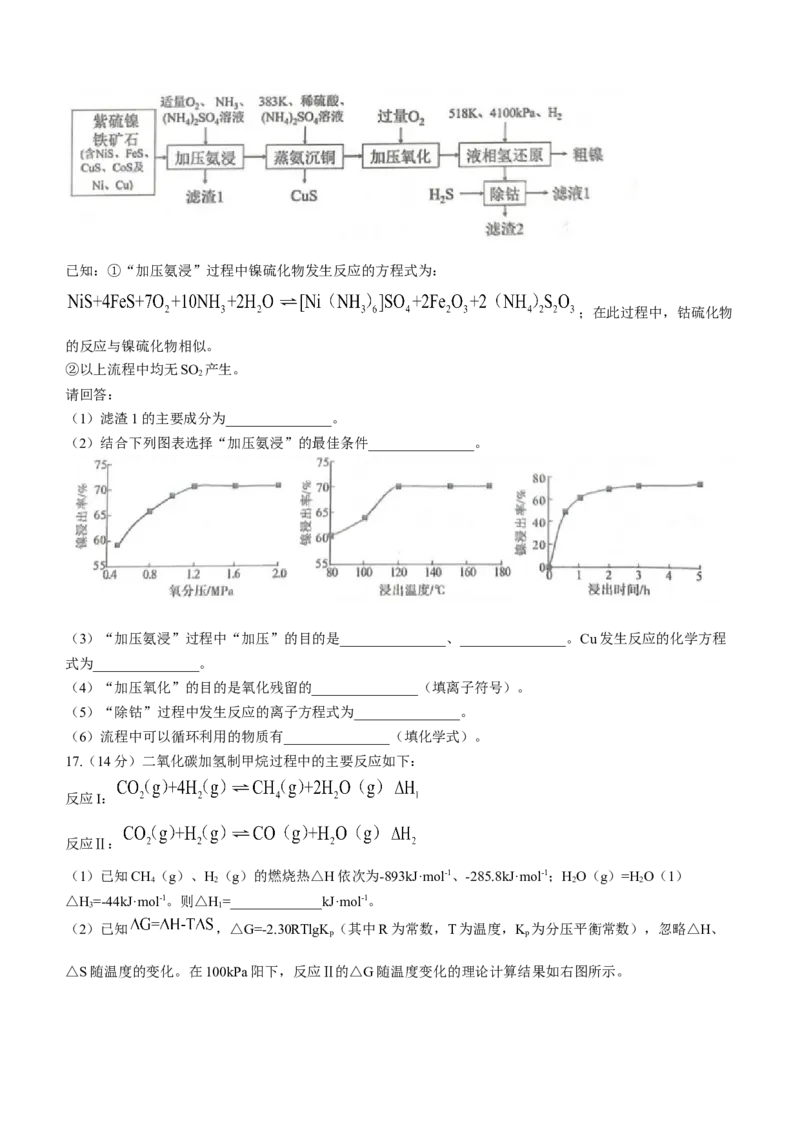
16.(15分)甘肃矿产资源丰富,镍、钴、铂等金属储量全国领先,有色金属冶炼在国民经济发展有着重要作
用。利用紫硫镍铁矿石提取粗镍并回收铁、铜、钴等元素的工艺流程如下:
学科网(北京)股份有限公司已知:①“加压氨浸”过程中镍硫化物发生反应的方程式为:
;在此过程中,钴硫化物
的反应与镍硫化物相似。
②以上流程中均无SO 产生。
2
请回答:
(1)滤渣1的主要成分为_______________。
(2)结合下列图表选择“加压氨浸”的最佳条件_______________。
(3)“加压氨浸”过程中“加压”的目的是_______________、_______________。Cu发生反应的化学方程
式为_______________。
(4)“加压氧化”的目的是氧化残留的_______________(填离子符号)。
(5)“除钴”过程中发生反应的离子方程式为_______________。
(6)流程中可以循环利用的物质有_______________(填化学式)。
17.(14分)二氧化碳加氢制甲烷过程中的主要反应如下:
反应I:
反应Ⅱ:
(1)已知CH(g)、H(g)的燃烧热△H依次为-893kJ·mol-1、-285.8kJ·mol-1;HO(g)=H O(1)
4 2 2 2
△H=-44kJ·mol-1。则△H=_____________kJ·mol-1。
3 1
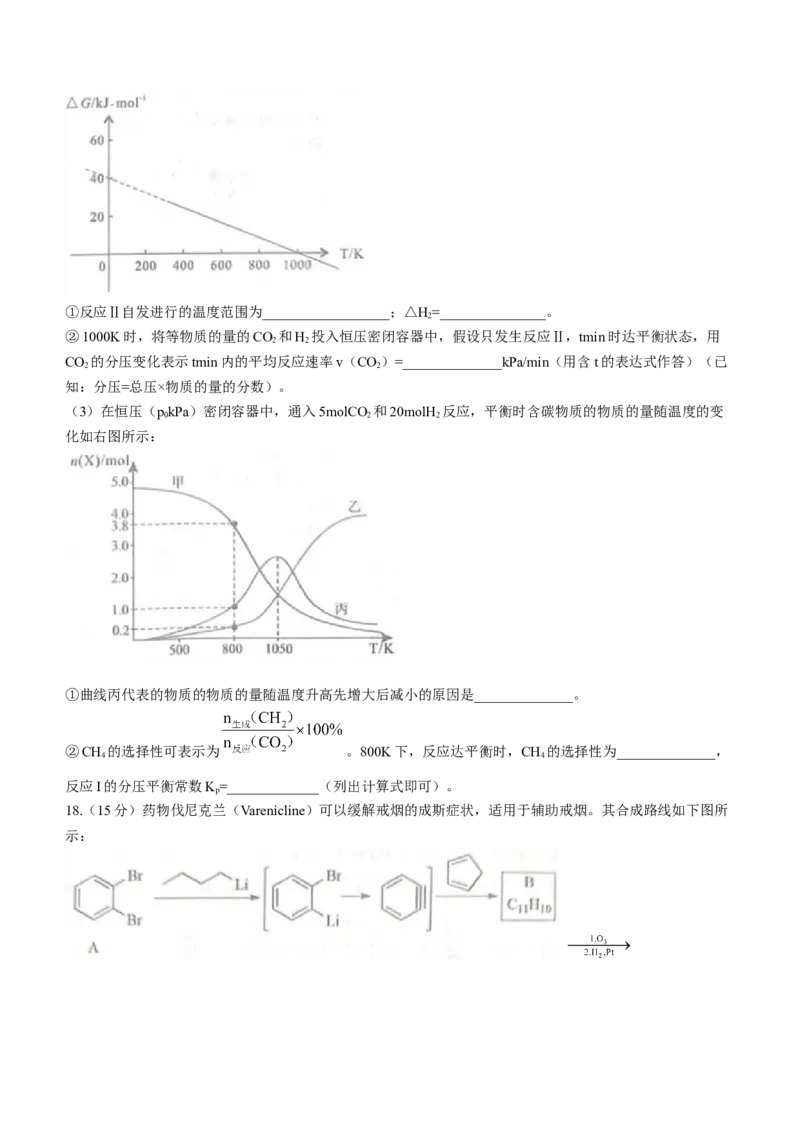
(2)已知 ,△G=-2.30RTlgK(其中R为常数,T为温度,K 为分压平衡常数),忽略△H、
p p
△S随温度的变化。在100kPa阳下,反应Ⅱ的△G随温度变化的理论计算结果如右图所示。
学科网(北京)股份有限公司①反应Ⅱ自发进行的温度范围为__________________;△H=_______________。
2
②1000K时,将等物质的量的CO 和H 投入恒压密闭容器中,假设只发生反应Ⅱ,tmin时达平衡状态,用
2 2
CO 的分压变化表示tmin内的平均反应速率v(CO)=______________kPa/min(用含t的表达式作答)(已
2 2
知:分压=总压×物质的量的分数)。
(3)在恒压(pkPa)密闭容器中,通入5molCO 和20molH 反应,平衡时含碳物质的物质的量随温度的变
0 2 2
化如右图所示:
①曲线丙代表的物质的物质的量随温度升高先增大后减小的原因是______________。
②CH 的选择性可表示为 。800K下,反应达平衡时,CH 的选择性为______________,
4 4
反应I的分压平衡常数K=_____________(列出计算式即可)。
p
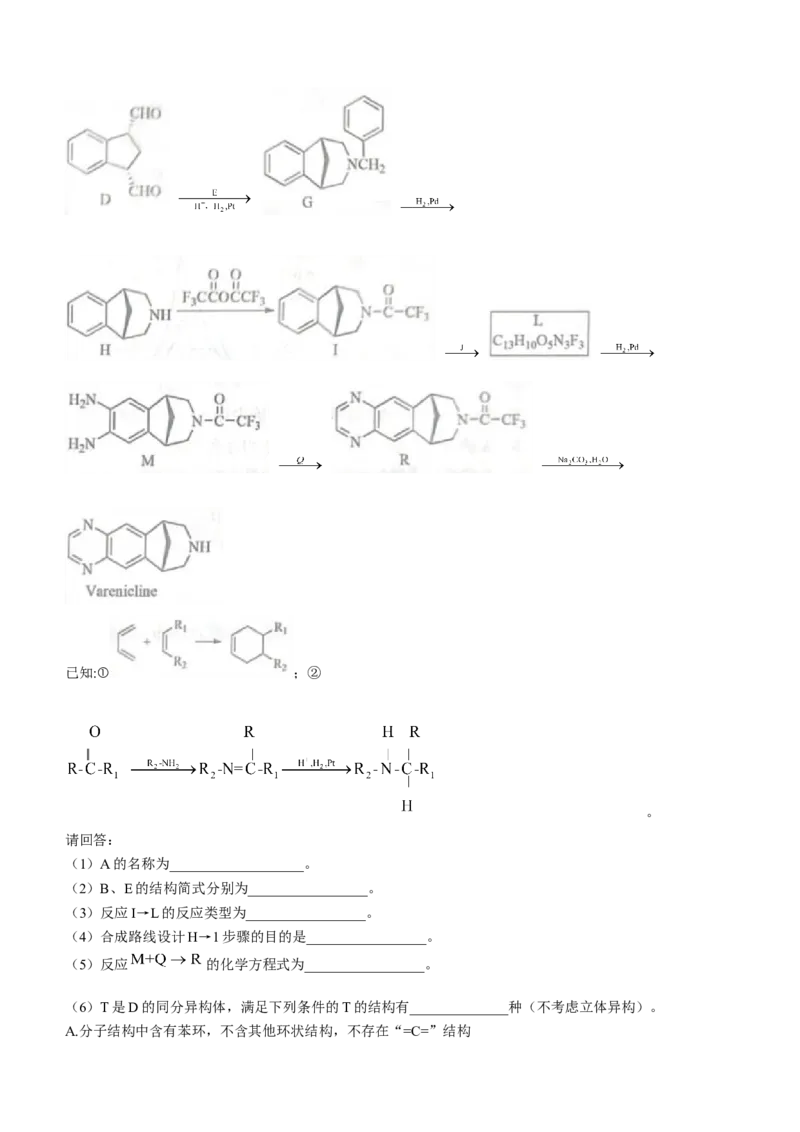
18.(15分)药物伐尼克兰(Varenicline)可以缓解戒烟的成斯症状,适用于辅助戒烟。其合成路线如下图所
示:
学科网(北京)股份有限公司已知:① ;②
。
请回答:
(1)A的名称为___________________。
(2)B、E的结构简式分别为_________________。
(3)反应I→L的反应类型为_________________。
(4)合成路线设计H→1步骤的目的是_________________。
(5)反应 的化学方程式为_________________。
(6)T是D的同分异构体,满足下列条件的T的结构有______________种(不考虑立体异构)。
A.分子结构中含有苯环,不含其他环状结构,不存在“=C=”结构
学科网(北京)股份有限公司B.苯环上只有两个取代基
C.能发生银镜反应,能发生水解反应,且水解产物遇FeCl 显紫色
3
其中核磁共振氢谱有5组峰,峰面积之比为1:2:2:2:3的结构简式为______________(任写一种即可)。
学科网(北京)股份有限公司