文档内容
4.1.2 化学电源 练习(解析版)
1.某氨气燃料电池,如图所示,下列说法错误的是( )
A.正极的电极反应式为O +4e﹣+4H+═2H O
2 2
B.电子流向:电极1→负载→电极2
C.Na+由左向右移动
D.NH 在电极1上发生氧化反应
3
【答案】A
【解析】A.通入氧气的一极为正极,电解质溶液为碱性,所以氧气得电子生成氢氧根,电极方程
式为O +4e﹣+2H O=4OHˉ,故A错误;
2 2
B.原电池中电子由负极经导线流向正极,根据分析可知电极 1为负极,电极2为正极,所以电子
的流向为电极1→负载→电极2,故B正确;
C.原电池中阳离子流向正极,所以钠离子自左向右移动,故C正确;
D.据图可知NH 在电极1上转化为N 和H O,失电子发生氧化反应,故D正确;故选:A。
3 2 2
2.氢氧燃料电池以氢气为燃料,氧气为氧化剂,电极是多孔镍电极,电解质溶液为质量分数 30%
的KOH溶液。下列叙述正确的是( )
A.通入O 的极是负极
2
B.负极反应式为2H ﹣4e﹣═4H+
2
C.工作时溶液中OH﹣移向负极
D.氢氧燃料电池将化学能转化为热能
【答案】C
【解析】A、氧碱性燃料电池中,通入O 的电极为正极,通入H 的电极为负极,故A错误;
2 2
B、通入H 的电极为负极,负极发生失去电子的氧化反应生成H O,负极反应为:H +2OH﹣﹣2e﹣
2 2 2
=2H O,故B错误;
2
C、原电池工作时,阳离子移向正极,阴离子移向负极,即工作时溶液中OH﹣移向负极,故C正确;
D、氢氧碱性燃料电池是原电池,能量转化主要是化学能转化为电能,故D错误;故选:C。
3.Li﹣MnO 电池放电时反应为Li+MnO ═LiMnO ,下列说法不正确的是( )
2 2 2A.Li电极发生氧化反应
B.溶液中Li﹣向MnO 电极移动
2
C.可用水代替电池中的有机物
D.正极反应式为Li++e﹣+MnO ═LiMnO
2 2
【答案】C
【解析】A、该原电池中,Li电极为负极,发生失电子的氧化反应,故A正确;
B、原电池工作时,阳离子移向正极,即溶液中Li﹣向MnO 电极移动,故B正确;
2
C、金属Li是活泼金属,能与水反应,所以不能用水代替电池中的有机物,故C错误;
D、MnO 电极为正极,正极上Mn元素得到电子,电极反应式为Li++e﹣+MnO ═LiMnO ,故D正
2 2 2
确;故选:C。
4.化学与生产、生活密切相关,下列有关说法正确的是( )
A.锌锰干电池是二次电池
B.医用酒精与工业酒精的主要成分相同,都可用于伤口消毒
C.夏天面粉发酵速度与冬天面粉发酵速度相差不大
D.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
【答案】D
【解析】A、锌锰干电池不能充电,属于一次电池,不是二次电池,故A错误;
B、工业酒精中含有甲醛,甲醛是有毒的,故B错误;
C、夏天温度高,面粉发酵的速度快,故C错误;
D、煤油来自石油的分馏,可用作航空燃料,也可用于保存Na,故D正确;故选:D。
5.锰﹣锂锂离子电池结构如图所示。放电时总反应为:C(Li)+LiMn O ═C+Li Mn O [C(Li)
2 4 2 2 4
表示锂原子嵌入石墨形成的复合材料].下列说法错误的是( )A.放电时,C(Li)为电池的负极
B.电解质溶液用稀H SO 效果更好
2 4
C.放电时,电极LiMn O 发生还原反应
2 4
D.负极反应为C(Li)﹣e﹣═C+Li+
【答案】B
【解析】A、原电池总反应中,Li化合价升高、发生失电子的氧化反应,则C(Li)为负极,故A
正确;
B、金属Li是活泼金属,能与水反应,发生自损耗现象,所以电解质不能用稀H SO 溶液,故B错
2 4
误;
C、原电池总反应中,Mn的化合价由+3.5→+3,LiMn O 发生得电子的还原反应,故C正确;
2 4
D、C(Li)为电池的负极,电极反应式为C(Li)﹣e﹣═C+Li+,故D正确;故选:B。
6.镁﹣空气电池是一种新型燃料电池,其工作原理如图所示。下列说法错误的是( )
A.金属Mg电极为负极,其电势低于空气电极的电势
B.电子流向:Mg电极→导线→空气电极→电解质溶液→Mg电极
C.电池总反应为2Mg+O +2H O═2Mg(OH)
2 2 2
D.回收后的氢氧化镁经一系列转化,可重新制成镁锭循环利用
【答案】B
【解析】A、该原电池中,Mg为负极、空气电极为正极,则Mg电极电势低于空气电极的电势,故
A正确;
B、原电池工作时,电子流向:Mg电极→导线→空气电极,阴离子:空气电极→Mg电极,形成闭
合回路,但电子不能进入电解质溶液中,故B错误;
C、负极反应为Mg﹣2e﹣+2OH﹣=Mg(OH) 、正极反应为O +4e﹣+2H O=4OH﹣,原电池总反应
2 2 2式为2Mg+O +2H O=2Mg(OH) ,故C正确;
2 2 2
D、Mg(OH) →MgCl →熔融MgCl Mg,即回收后的氢氧化镁经一系列转化,可重新制成镁
2 2 2
锭循环利用,故D正确;故选:B。
7.一种镁氧电池电极材料为金属膜和吸附氧气的活性炭,电解液为 KOH浓溶液,如图所示。下列
说法不正确的是( )
A.正极反应式为:O +4e﹣+2H O═4OH﹣
2 2
B.负极反应式为:Mg﹣2e﹣+2OH﹣═Mg(OH)
2
C.电子的移动方向是由a经外电路到b
D.该电池在工作过程中,电解液KOH的浓度保持不变
【答案】D
【解析】A.Mg电极a作负极、活性炭b电极作正极,正极反应式为O +4e﹣+2H O=4OH﹣,故A
2 2
正确;
B.Mg作负极、Mg失电子生成Mg(OH) ,电极反应式为Mg﹣2e﹣+2OH﹣=Mg(OH) ,故B
2 2
正确;
C.Mg作负极、活性炭作正极,即 a电极为负极,b电极为正极,电子从负极 a经外电路到正极
b,故C正确;
D.负极反应为Mg﹣2e﹣+2OH﹣=Mg(OH) 、正极反应为O +4e﹣+2H O=4OH﹣,原电池总反应
2 2 2
为2Mg+O +2H O=2Mg(OH) ,消耗水使KOH的浓度增大,故D错误;故选:D。
2 2 2
8.锌﹣空气燃料电池可用作电动车动力电源,电池的电解质溶液为 KOH溶液,放电时反应为:
2Zn+O +4OH﹣+2H O═2Zn(OH) 2﹣.下列说法正确的是( )
2 2 4
A.放电时,正极反应为:Zn+4OH﹣﹣2e﹣═Zn(OH) 2﹣
4
B.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
C.充电时,电解质溶液中c(OH﹣)逐渐增大
D.充电时,电子的运动方向为:电源负极→电解池阴极→电解质溶液→电解池阳极→电源正极
【答案】C
【解析】A.放电时,负极上锌失电子生成 Zn(OH) 2﹣,负极反应式为Zn+4OH﹣﹣2e﹣═Zn
4
(OH) 2﹣,故A错误;
4B.放电时,1mol氧气得到4mol电子,则电路中通过2mol 电子,消耗0.5mol氧气,即消耗标况
下11.2L氧气,故B错误;
C、充电是放电的逆过程,则电解反应式为:Zn(OH) 2﹣═Zn+4OH﹣﹣2e﹣,则氢氧根离子的浓
4
度变大,故C正确;
D、充电时,是电解池,电子经外电路由电解池的阳极→电源正极→电源负极→电解池阴极,电子
不能再溶液中传递,故D错误;故选:C。
9.锌﹣空气燃料电池可用作电动车动力电源,电池的电解质溶液为 KOH溶液,电池总反应为
2Zn+O +4OH﹣+2H O═2Zn(OH) 2﹣.下列说法正确的是( )
2 2 4
A.锌极发生还原反应
B.电子从锌极经KOH溶液移向充空气的电极
C.锌极需定期更换
D.该电池是电能转化为化学能的装置
【答案】C
【解析】A、锌极发生氧化反应,故A错误;
B、电子从锌极经导线流向充空气的电极,故B错误;
C、锌失电子不断消耗,所以锌极需定期更换,故C正确;
D、原电池化学能转化为电能,故D错误;故选:C。
10.铅蓄电池反应原理为:Pb(s)+PbO (s)+2H SO (aq) 2PbSO (s)+2H O(l),下
2 2 4 4 2
列说法正确的是( )
A.放电时,正极附近pH减小
B.充电时,铅蓄电池的负极连接电源的正极
C.放电时,负极的电极反应式为:Pb﹣2e﹣═Pb2+
D.充电时,阴极的电极反应式为:PbSO +2e﹣═Pb+SO 2﹣
4 4
【答案】D
【解析】A、由总方程式可知,为原电池时,Pb为负极,PbO 为正极,发生还原反应,电极方程
2
式为PbO +4H++SO 2﹣﹣2e﹣=2H O+PbSO ,正极附近pH增大,故A错误;
2 4 2 4
B、充电时,该装置是电解池,电池的负极和外加电源的负极相连,为阴极,发生还原反应,故 B
错误;
C、由总方程式可知,为原电池时,Pb为负极,发生氧化反应,电极方程式为Pb+SO 2﹣﹣2e﹣=
4
PbSO ,故C错误;
4
D、在充电时,该装置是电解池,阴极发生的还原反应:PbSO +2e﹣=Pb+SO 2﹣,故D正确。故选:
4 4D。
11.燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。如图为氢氧燃料
电池构造示意图。下列说法中正确的是( )
A.a极为电池的正极,电极反应式为:O +4e﹣+2H O=4OH﹣
2 2
B.b极为电池的负极,电极反应式为:H ﹣2e﹣═2H+
2
C.电解质溶液中K+离子向a极移动
D.当生成1mol H O时,电路中流过电子的物质的量为2mol
2
【答案】D
【解析】A、a极为负极,电极反应为:2OH﹣+H ﹣2e﹣═2H O,故A错误;
2 2
B、b极为电池的正极,电极反应式:O +2H O+4e﹣═4OH﹣,故B错误;
2 2
C、电解质溶液中K+离子向正极b移动,故C错误;
D、总反应方程式为:2H +O =2H O,生成2mol水转移4mol电子,则当生成1mol H O时,电路
2 2 2 2
中流过电子的物质的量为2mol,故D正确;故选:D。
12.普通锌锰干电池的构造如图所示,其电池反应的方程式为:Zn+2NH Cl+2MnO ═Zn(NH )
4 2 3
Cl +2MnO(OH),下列说法不正确的是( )
2 2
A.石墨作正极
B.锌发生氧化反应
C.电池工作时,电子从石墨经导线流向锌
D.正极的电极反应为:NH ++MnO +e﹣═MnO(OH)+NH
4 2 3
【答案】C
【解析】A、锌筒为负极,石墨作正极,故A正确;B、电池中锌失去电子,发生氧化反应,故B正确;
C、电池中电子从负极流向正极即从锌经导线流向石墨,故C错误;
D、正极得电子发生还原反应,所以正极的电极反应为NH ++MnO +e﹣=MnO(OH)+NH ,故D
4 2 3
正确;故选:C。
13.将铂电极放置在KOH溶液中,然后分别向两极通入CH 和O ,即产生电流,称为甲烷燃料电
4 2
池。下列有关说法中错误的是( )
A.CH 在负极上反应,O 在正极上反应
4 2
B.放电过程中电解质溶液的碱性减弱
C.此电池属于环境友好型电池
D.此电池中化学能100%转化为电能
【答案】D
【解析】A.在燃料电池中,通入燃料甲烷的电极为负极,失去电子,发生氧化反应,通入氧气的
电极为正极,正极上氧气得到电子,发生还原反应,故A正确;
B.在甲烷燃料电池中,负极电极反应式为CH ﹣8e﹣+10OH﹣=CO 2﹣+7H O,正极的电极反应式
4 3 2
为O +4e﹣+2H O=4OH﹣,总反应方程式为CH +2O +2OH﹣=CO 2﹣+3H O,可见在放电过程中,
2 2 4 2 3 2
反应消耗KOH,产生H O,使溶液中溶质的物质的量浓度减小,因而溶液的碱性减弱,故B正确;
2
C.反应产生H O,无污染,因此电池属于环境友好型电池,故C正确;
2
D.电池在工作时,除转化为电能外,还产生了热量,有热能产生,因此化学能不可能 100%转化
为电能,故D错误;故选:D。
14.DBFC燃料电池的结构如图,该电池的总反应为NaBH +4H O ═NaBO +6H O.下列关于电池
4 2 2 2 2
工作时的相关分析不正确的是( )
A.X极为正极,电流经X流向外电路
B.Y极发生的还原反应为H O +2e﹣═2OH﹣
2 2
C.X极区溶液的pH逐渐减小
D.每消耗1.0L 0.50mol/L的H O 电路中转移1.0mol e﹣
2 2
【答案】A
【解析】由电池的总反应为NaBH +4H O ═NaBO +6H O可知,X电极上NaBH 发生失去电子的
4 2 2 2 2 4氧化反应,作负极,则Y极作正极,
A.该电池中X极为负极,Y极作正极,电子经X流向外电路流入Y,电流经Y流向外电路,故A
错误;
B.该电池中Y极为正极,正极上H O 发生还原反应,电极反应为H O +2e﹣=2OH﹣,故B正确;
2 2 2 2
C.X极为负极,发生失去电子的氧化反应,电极反应式为BH ﹣+8OH﹣﹣8e﹣=BO ﹣+6H O,所以
4 2 2
X极区溶液的pH逐渐减小,故C正确;
D.由电极反应式 H O +2e﹣=2OH﹣可知,每消耗 1molH O 电路中转移 2mole﹣,所以每消耗
2 2 2 2
1.0L0.50mol/L即0.50molH O ,电路中转移1.0mole﹣,故D正确;故选:A。
2 2
15.铅蓄电池放电时发生的化学反应:PbO +Pb+2H SO ═2PbSO +2H O,其电极材料分别是PbO
2 2 4 4 2 2
和Pb,电解质为H SO 溶液,下列说法不正确的是( )
2 4
A.电池工作过程中,H SO 溶液浓度降低
2 4
B.电池工作过程中,电解质溶液中H+向正极移动
C.每当有2mol电子通过电路时,负极材料增重96g
D.正极发生反应为:PbO +4H++2e﹣═Pb2++2H O
2 2
【答案】D
【解析】A、铅蓄电池工作时,硫酸参加反应生成硫酸铅同时生成水,导致硫酸浓度降低,故 A正
确;
B、原电池放电时阴离子向负极移动,阳离子向正极移动,即电解质溶液中 H+向正极移动,故B正
确;
C、蓄电池中,负极上金属Pb失电子,发生氧化反应Pb+SO 2﹣﹣2e﹣=PbSO ,每当有2mol电子
4 4
通过电路时,负极材料增重96g,故C正确;
D、铅蓄电池正极上PbO 得电子发生还原反应PbO +4H++SO 2﹣+2e﹣═PbSO +2H O,故D错误。
2 2 4 4 2
故选:D。
16.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y O )的氧
2 3
化锆(ZrO )晶体,在熔融状态下能传导O2﹣.下列对该燃料电池说法不正确的是( )
2
A.在熔融电解质中,O2﹣移向负极
B.电池的总反应是:2C H +13O ═8CO +10H O
4 10 2 2 2
C.通入丁烷的一极是负极,电极反应为:C H ﹣26e﹣+13O2﹣═4CO ↑+5H O
4 10 2 2
D.通入空气的一极是正极,电极反应为:O +4e﹣+4H+═2H O
2 2
【答案】D
【解析】A、原电池中阴离子向负极移动,阳离子向正极移动,所以O2﹣移向负极,故A正确;B、电池的总反应与丁烷燃烧的化学方程式一致,为2C H +13O =8CO +10H O,故B正确;
4 10 2 2 2
C、通入丁烷一极是负极,失电子被氧化,电极反应式为C H +13O2﹣﹣26e﹣=4CO +5H O,故C
4 10 2 2
正确;
D、通入空气的一极为原电池的正极,发生还原反应,电极反应式为O +4e﹣=2O2﹣,故D错误;
2
故选:D。
17.2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的结构如图所示,
电池反应式为Li x C 6 +Li 1﹣x CoO 2 C 6 +LiCoO 2 (x<1)。下列说法正确的是( )
A.放电时,a极为负极
B.充电时,Li 1﹣x CoO 2 /LiCoO 2 电极发生Li+脱嵌,放电时发生Li+嵌入
C.充电时,若转移0.3mol电子,石墨电极将减轻2.1g
D.放电时,Li+在电解质中由a极向b极迁移
【答案】B
【解析】A、原电池中b电极为负极,a电极为正极,故A错误;
B、充电时,Li 1﹣x CoO 2 /LiCoO 2 电极反应为:LiCoO 2 ﹣xe﹣=Li 1﹣x CoO 2 +xLi+,电极发生Li+脱嵌,
而放电时发生:Li 1﹣x CoO 2 +xLi++xe﹣=LiCoO 2 ,Li+嵌入,故B正确;
C、放电时负极反应式为Li C ﹣xe﹣=C +xLi+,充电时阴极反应式为C +xLi++xe﹣=Li C ,所以充
x 6 6 6 x 6
电时若转移0.3mol电子,石墨电极将增重0.3mol×7gmol/L=2.1g,故C错误;
D、放电时,阳离子移向正极、阴离子移向负极,即Li+在电解质中由b极向a极迁移,故D错误;
故选:B。
18.乙醇做为可再生能源比化石能源具有较大的优势,如图为乙醇燃料电池,该电池的总反应方程
式为C H OH+3O ═2CO +3H O.下列关于该电池叙述错误的是( )
2 5 2 2 2A.a极与用电器的正极相接
B.该装置将化学能转化为电能
C.质子(H+)由装置左侧向右侧移动
D.该装置的电解质溶液呈酸性
【答案】C
【解析】A、氧气得电子发生还原反应,是原电池的正极,则a极与用电器的正极相接,故A正确;
B、该装置是原电池,是将化学能转化为电能的装置,故B正确;
C、原电池中阳离子向正极移动,则质子(H+)由装置右侧向左侧移动,故C错误;
D、负极的电极产物为二氧化碳,则应装置中电解溶液呈酸性,故D正确;故选:C。
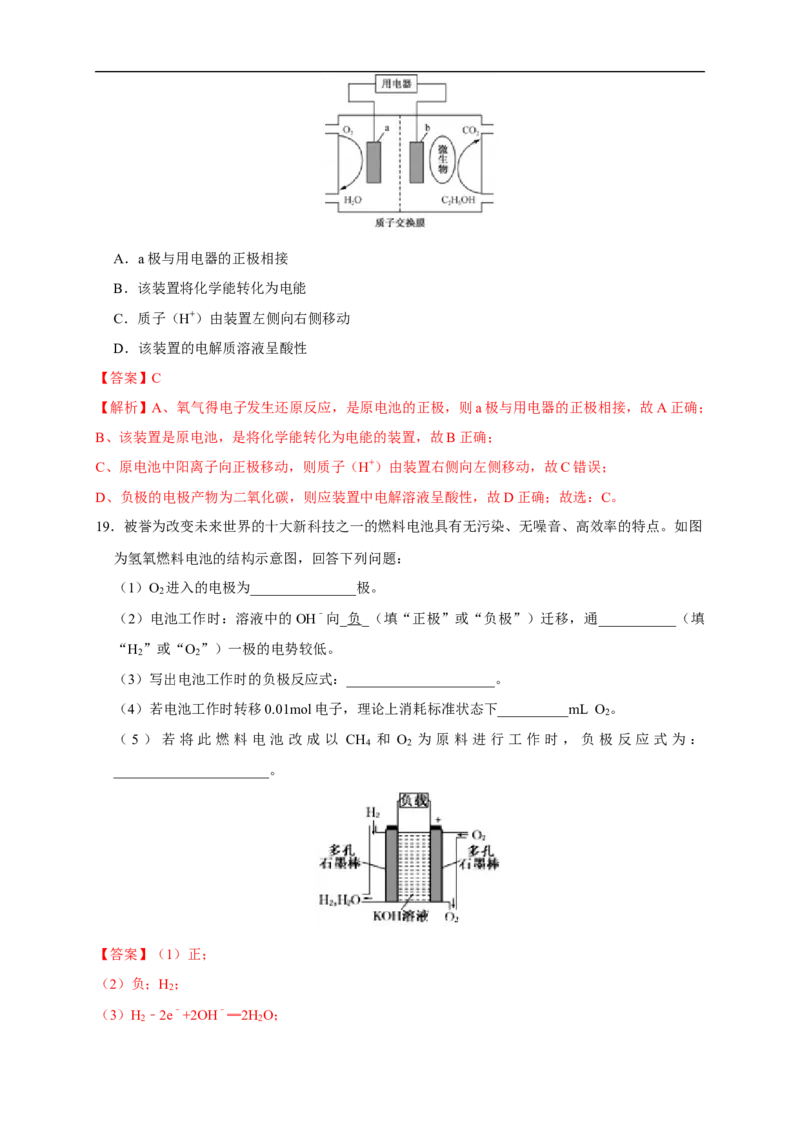
19.被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图
为氢氧燃料电池的结构示意图,回答下列问题:
(1)O 进入的电极为_______________极。
2
(2)电池工作时:溶液中的OH﹣向_负_(填“正极”或“负极”)迁移,通___________(填
“H ”或“O ”)一极的电势较低。
2 2
(3)写出电池工作时的负极反应式:_____________________。
(4)若电池工作时转移0.01mol电子,理论上消耗标准状态下__________mL O 。
2
(5)若将此燃料电池 改成以 CH 和 O 为原料 进行 工作时,负极反应式为:
4 2
______________________。
【答案】(1)正;
(2)负;H ;
2
(3)H ﹣2e﹣+2OH﹣═2H O;
2 2(4)56;
(5)CH +10OH﹣﹣8e﹣═CO 2﹣+7H O。
4 3 2
【解析】通常在原电池反应中,O 只能得电子,所以通O 的电极为正极,在碱性电解质溶液中,
2 2
O 得电子的产物与溶液反应生成OH﹣,电极反应式为O +4e﹣+2H O═4OH﹣,通H 的电极为负极
2 2 2 2
H 失电子的产物与电解质溶液反应生成H O,电极反应式为H ﹣2e﹣+2OH﹣═2H O。
2 2 2 2
(1)由以上分析知,O 进入的电极为正极,
2
故答案为:正;
(2)电池工作时:阴离子向负极移动,则溶液中的OH﹣向负极迁移;在原电池中,负极的电势较
低,则通H 一极的电势较低,
2
故答案为:负;H ;
2
(3)电池工作时,通H 的电极为负极,H 失电子的产物与电解质溶液反应生成H O,电极反应式
2 2 2
为H ﹣2e﹣+2OH﹣═2H O,
2 2
故答案为:H ﹣2e﹣+2OH﹣═2H O;
2 2
(4)在正极1molO 转移电子4mol,若电池工作时转移0.01mol电子,理论上消耗标准状态下O
2 2
的体积为 =56mL,
故答案为:56;
(5)若将此燃料电池改成以CH 和O 为原料进行工作时,负极为通CH 的电极,CH 失电子的产
4 2 4 4
物与OH﹣反应生成CO 2﹣和水,电极反应式为:CH +10OH﹣﹣8e﹣═CO 2﹣+7H O,
3 4 3 2
故答案为:CH +10OH﹣﹣8e﹣═CO 2﹣+7H O。
4 3 2
20.通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,负极反应的物质为___________,正极反应的物质为____________,酸式
电池的电极反应:
负极:_____________________,正极:______________________。电解质溶液 pH 的变化
____________(填“变大”,“变小”,“不变”)。
(2)在碱式介质中,碱式电池的电极反应:
负极:______________________,正极:_____________________。电解质溶液 pH 的变化
__________(填“变大”,“变小”,“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是_C_。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H SO 、KOH为介质的氢氧燃料电池的负极电极反应式相同
2 4D.以稀H SO 、KOH为介质的氢氧燃料电池的总反应式相同
2 4
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:
3Zn+2K FeO +8H O 3Zn(OH) +2Fe(OH) +4KOH。
2 4 2 2 3
该电池放电时负极反应式为_______________________________。
①放电时每转移3mol电子,正极有____________mol K
2
FeO
4
被还原。
② 放 电 时 , 正 极 发 生 _ 还 原 _ ( 填 “ 氧 化 ” 或 “ 还 原 ” ) 反 应 ; 正 极 反 应 为
③________________________________。
放电时,___________(填“正”或“负”)极附近溶液的碱性增强。
【答④案】(1)氢气;氧气;2H
2
﹣4e﹣=4H+;O
2
+4e﹣+4H+=2H
2
O;变大;
(2)2H ﹣4e﹣+4OH﹣=4H O;O +4e﹣+2H O=4OH﹣;变小;
2 2 2 2
(3)C;
(4) Zn﹣2e﹣+2OH﹣═Zn(OH) ;
2
1;①
②还原;FeO
4
2﹣+3e﹣+4H
2
O═Fe(OH)
3
+5OH﹣;
③正。
④【解析】(1)在酸性氢氧燃料电池中,石墨作电极,在负极上氢气失电子生成氢离子,电极反应
为2H ﹣4e﹣=4H+;在正极由氧气得电子生成水,电极反应为O +4e﹣+4H+=2H O,由于正负极消
2 2 2
耗与生成的氢离子等量,所以氢离子的总量不变,而总电极反应式为2H +O 2H O,水的总量增加,
2 2 2
故pH变大,
故答案为:氢气;氧气;2H ﹣4e﹣=4H+;O +4e﹣+4H+=2H O;变大;
2 2 2
(2)在碱式介质中,氢气在负极失去电子生成氢离子,氢离子结合氢氧根离子生成水,电极反应
式为2H ﹣4e﹣+4OH﹣=2H O;氧气在正极得电子生成氢氧根离子,电极反应式为O +4e﹣+2H O=
2 2 2 2
4OH﹣,由于正负极消耗与生成的氢氧根离子等量,所以氢氧根离子的总量不变,而总电极反应式
为2H +O =2H O,水的总量增加,故pH变小,
2 2 2
故答案为:2H ﹣4e﹣+4OH﹣=4H O;O +4e﹣+2H O=4OH﹣;变小;
2 2 2 2
(3)A.电解获得H 消耗较多的能量,而在催化剂作用下利用太阳能来分解H O获得H 更为科学,
2 2 2
故A正确;
B.氢氧燃料电池产物H O无污染,能有效保护环境,所以氢氧燃料电池作为汽车动力更能保护环境,
2
故B正确;
C.以稀H SO 、KOH为介质的氢氧燃料电池的负极电极反应式分别为:H ﹣2e﹣═4H+,H ﹣2e﹣
2 4 2 2+2OH﹣=2H O,不相同,故C错误;
2
D.以稀H SO 、KOH为介质的氢氧燃料电池的总反应式均为2H +O =2H O,故D正确,
2 4 2 2 2
故答案为:C;
(4) 放电时,负极上锌失电子发生氧化反应,电极反应式为:Zn﹣2e﹣+2OH﹣═Zn(OH) ,
2
故答案①为:Zn﹣2e﹣+2OH﹣═Zn(OH) ;
2
放电时,正极上1molK FeO 得3mol电子发生还原反应生成1molFe(OH) ,所以每转移3 mol
2 4 3
②电子,正极有1molK FeO 被还原,
2 4
故答案为:1;
放电时,正极上K FeO 得电子,发生还原反应,正极的电极方程式为 FeO 2﹣+3e﹣+4H O═Fe
2 4 4 2
③(OH) +5OH﹣,
3
故答案为:还原;FeO 2﹣+3e﹣+4H O═Fe(OH) +5OH﹣;
4 2 3
负极电极方程式电极反应式为:Zn﹣2e﹣+2OH﹣═Zn(OH) ,正极的电极方程式为FeO 2﹣+3e
2 4
④﹣+4H O═Fe(OH) +5OH﹣,所以正极附近溶液的碱性增强,
2 3
故答案为:正。
21.燃料电池是一种具有应用前景的绿色电源。图为燃料电池的结构示意图,电解质溶液为NaOH
溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
(1)若该燃料电池为氢氧燃料电池。
a极通入的物质为____________,电解质溶液中的OH﹣移向_负_极(填“负”或“正”)。
①写出此氢氧燃料电池工作时,负极的电极反应式:___________。
②(2)若该燃料电池为甲烷燃料电池。已知电池的总反应为CH
4
+2O
2
+2OH﹣═CO
3
2﹣+3H
2
O
下列有关说法正确的是__________。(填字母代号)
①A.燃料电池将电能转变为化学能
B.负极的电极反应式为CH +10OH﹣﹣8e﹣═CO 2﹣+7H O
4 3 2
C.正极的电极反应式为O +4H++4e﹣═2H O
2 2
D.通入甲烷的电极发生还原反应
当消耗甲烷11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子
②的物质的量为____________mol。【答案】(1) 氢气;负;
H
2
﹣2e﹣+2O①H﹣=2H
2
O;
②(2) B;
3.2。①
②【解析】(1) 燃料电池中,负极上失电子发生氧化反应,通入燃料氢气的电极是负极,据图示
可知a电极是负①极,故a极通入的物质为氢气;原电池中阴离子移向负极故OH﹣移向负极,
故答案为:氢气;负;
电解质溶液为NaOH溶液,为碱性环境,故此氢氧燃料电池工作时,负极的电极反应式:H ﹣
2
②2e﹣+2OH﹣=2H O,
2
故答案为:H ﹣2e﹣+2OH﹣=2H O;
2 2
(2) A.燃料电池为原电池原理,应为将化学能转变为电能,故A错误;
B.电①解质溶液为NaOH溶液,为碱性环境,故负极的电极反应式为 CH
4
+10OH﹣﹣8e﹣=CO
3
2﹣
+7H O,故B正确;
2
C.碱性环境中正极的电极反应式应为:为O +2H O+4e﹣=4OH﹣,故C错误;
2 2
D.通入甲烷的电极失电子发生氧化反应,故D错误;
故答案为:B;
据电池的总反应CH +2O +2OH﹣=CO 2﹣+3H O可知:消耗甲烷22.4L(标准状况下)时,假设
4 2 3 2
②电池的能量转化效率为100%,则导线中转移的电子的物质的量为8mol,则当消耗甲烷11.2L(标
准状况下)时,假设电池的能量转化效率为100%,则导线中转移的电子的物质的量4mol,故电池
的能量转化效率为80%时,导线中转移的电子的物质的量为4×0.8=3.2mol,
故答案为:3.2。
22.氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,负极通入___________,正极通
入____________,总反应为____________;电极反应特别要注意电解质,有下列三种情况:
(1)电解质是KOH溶液(碱性电解质)
负极发生的反应为:H ﹣2e﹣═2H+,2H++2OH﹣═2H O,所以:负极的电极反应式为:
2 2
①_______________________________。
正极是O 得到电子,即:O +4e﹣═2O2﹣,O2﹣在碱性条件下不能单独存在,只能结合H O生
2 2 2
②成OH﹣即:2O2﹣+2H O═4OH﹣,因此,正极的电极反应式为______________________。
2
(2)电解质是H SO 溶液(酸性电解质)
2 4
负极的电极反应式为__________。
①正极是O
2
得到电子,即:O
2
+4e﹣═2O2﹣,O2﹣在酸性条件下不能单独存在,只能结合H+生
②成H O即:O2﹣+2H+═H O,因此正极的电极反应式为____________________。
2 2【答案】氢气;氧气;2H +O =2H O;
2 2 2
(1) H ﹣2e﹣=2H+; H ﹣2e﹣=2H+;O +4e﹣+4H+=2H O。
2 2 2 2
【解析①】燃料电池中燃料作②为负极,发生氧化反应,总反应的产物和燃料燃烧时产物相同,所以氢
氧燃料电池,以惰性金属铂(Pt)或石墨做电极材料时,负极通入氢气,正极通入氧气,总反应为:
2H +O =2H O,故答案为:氢气;氧气;2H +O =2H O;
2 2 2 2 2 2
(1) 负极发生的反应为:H ﹣2e﹣=2H+,2H++2OH﹣=2H O,则总的负极的电极反应式为:H
2 2 2
﹣2e﹣①+2OH﹣=2H O; 正极是O 得到电子,即:O +4e﹣=2O2﹣,O2﹣在碱性条件下不能单独存
2 2 2
在,只能结合H O生成②OH﹣即:2O2﹣+2H O=4OH﹣,因此,正极的电极反应式为:O +4e﹣+2H O
2 2 2 2
=4OH﹣;故答案为:H ﹣2e﹣+2OH﹣=2H O;O +4e﹣+2H O=4OH﹣;(2) 电解质为酸时,负
2 2 2 2
极的电极反应式为:H ﹣2e﹣=2H+; ①
2
正极是O 得到电子,即:O +4e﹣=2O2﹣,O2﹣在酸性条件下不能单独存在,只能结合 H+生成
2 2
②H O即:O2﹣+2H+=H O,因此正极的电极反应式为:O +4e﹣+4H+=2H O;故答案为:H ﹣2e﹣=
2 2 2 2 2
2H+;O +4e﹣+4H+=2H O。
2 2