文档内容
2024 年 2 月红色十校高三联考·化学参考答案
1.答案B,解析:A选项正确;
B选项错误,酒精没有强氧化性;
C选项正确,氯化钙溶解放热,加速冰雪的融化,且盐水凝固点比水更低;
D选项正确,使用含氟牙膏,牙齿成分中羟基磷灰石Ca (PO ) OH与F-反应转化为更难溶
5 4 3
于水的氟磷灰石Ca (PO ) F和OH-
5 4 3
2.答案D,解析:A选项错误,溶液如果显酸性,NO -会氧化Fe2+导致二者无法大量共存;
3
溶液如果显碱性,OH-与NH +不能大量共存;
4
B选项错误,S2-与Cu2+反应,生成黑色的CuS沉淀;
C选项错误,大量的氨水会和铝离子反应,生成氢氧化铝沉淀;
D选项正确,溶液是否澄清透明和离子是否有颜色无关。
3.答案A,解析:A选项正确, Mg(价电子3s2)失去一个电子后,价电子排布式为3s1(半充满),
Al(价电子3s23p1)失去一个电子后,价电子排布式为3s2(全充满),而稳定性:全充满>半充
满,所以第二电离能:Al>Mg;
B选项错误,稳定性HF>HCl,所以共价键的键能H-F>H-Cl;
C选项错误,共价键键长越短,原子晶体的共价键强度越大,熔点越高,所以熔点:
金刚石>SiC>晶体硅;
D选项错误,CCl 呈现sp3杂化,属于正四面体对称的非极性分子晶体,H O中,中心原
4 2
子O价层电子对数为4,呈现不等性sp3杂化,空间构型是V型,所以分子的极性:CCl K;
D选项正确,同周期的这两种元素,如果都在第二或第三周期,则原子序数为a+3,如果
都在第四或第五周期,则原子序数为a+13(多出10种过渡元素),如果都在第六或第七周
1
{#{QQABLYIEggCoAAAAAQgCAwHYCEAQkAAAAIoGAFAAMAIBCRNABAA=}#}期,则原子序数为a+27(镧系、锕系再分别多出15种元素)。
8.答案C,解析:A选项错误,A中含有氧原子,不属于烃类;
B选项错误,当R是乙基时,A中不存在手性碳原子;
C选项正确,两个双键碳原子上均连接不同的基团,所以存在顺反异构,而A中含有-Cl,
可以在碱性条件发生水解反应;
D 选项错误,将苯环记为 ph-,属于苯甲酸同系物的同分异构体有以下情况:
①ph-CH -CH -COOH② ③ph-CH -COOH 和一个-CH ,共 3种④ph-COOH
2 2 2 3
和一个-C H ,有3种;⑤ph-COOH和两个-CH ,有6种,合计14种。
2 5 3
9.答案D,解析:A选项正确,无水CaCl 或P O 可以吸收多余的氨气;
2 2 5
B选项正确,长颈漏斗和空气相通,可以防止堵塞、NH 不溶于CCl ,可以控制氨气的流
3 4
速;
C 选项正确,氨气极易溶于水,a 装置可以防倒吸,本实验涉及转化关系
Cr O 2-+H O 2CrO 2-+2H+,Cr O 2-显橙色,CrO 2-显黄色,实验时溶液颜色会发生变
2 7 2 4 2 7 4
化;
D选项错误,由于常温下K Cr O 的溶解度远小于K CrO ,且该反应可逆,无法实现将
2 2 7 2 4
K Cr O 全部转化为K CrO 。
2 2 7 2 4
10.答案C,解析:A选项错误,电负性F>N>Cl, 所以NF 中N的化合价为+3价,NCl 中N
3 3
的化合价是-3价;
B选项错误,HI还原性很强,会被浓硫酸氧化(可以换做用浓磷酸制HI);
C选项正确,Zn和Cd属于同一族的过渡元素,性质相似,都能与氨水反应,生成配合物;
D选项错误,2SO +O 2SO 中反应物可用空气代替O ,因为空气中的其他主要成
2 2 3 2
分(主要考虑N ) 不与SO 反应,但是工业合成氨:N +3H 2NH ,反应物不能用空
2 2 2 2 3
气代替N ,因为空气中存在大量的O ,在高温高压条件下,O 与H 反应,可能发生爆
2 2 2 2
炸。
11.答案D, 解析:结合题目信息和Q只形成一个共价键,可知Q只能是F,再根据物质的
结构,可以推测出Y、M、Q 、Z、X分别为 B、N、F、Si、Cl。
A选项正确,YQ 是BF ,构型为平面正三角形,键角120°,ZX 是SiCl ,构型是空间正
3 3 4 4
四面体结构,键角109°28′,所以键角:YQ >ZX ;
3 4
B选项正确,Y原子(B原子)通过配位键,也达到8电子稳定结构;
C选项正确,SiO 可以用作耐高温坩埚;
2
D选项错误,第二周期元素中,由于N原子价电子构型是2s22p3,p能级半充满,第一电
离能:F>N>O>C,所以第二周期不存在任何元素的第一电离能数值介于M与Q之间。
12.答案D,解析:通过均摊法得知该立方体晶胞中K、I、O的原子个数分别是1,1,3,所以
晶胞化学式为KIO 。
3
A选项正确,加碘盐中含有KIO ;
3
B选项正确,2处的O原子,位于侧面的面心,通过x、y、z三个方向投影,得到的坐标
1 1
是 a,a, a ;
2 2
C选项正确,KIO
3
的摩尔质量M=214g/mol,一个晶胞的体积V=(a×10-10cm)3,所以晶胞
M 214
密度 (g/cm3);
V N (a1010)3N
A A
2
{#{QQABLYIEggCoAAAAAQgCAwHYCEAQkAAAAIoGAFAAMAIBCRNABAA=}#}4 4
(x3 y3)3 z3
3 3
4(x3 y3 3z3)
D选项错误,该晶胞的原子空间利用率
a3 3a3
13.答案C,解析:从图示来看,A电极产生N ,应为电解池的阳极,左边浓差电池Ag(2)
2
连接电极A,做原电池的正极,NO -向丁室迁移。
3
A选项错误,阴离子交换膜允许OH-通过,A电极上的反应为2NH -6e-+6OH-=N ↑+6H O;
3 2 2
B选项错误,A极电极反应为:2NH -6e-+6OH-=N ↑+6H O,OH-从甲移到乙进行补充,但
3 2 2
反应生成了水,故乙池NaOH溶液pH会减小;
C选项正确,产生1.12LH (标况) 时,转移0.1mol 电子,丙室会有0.1molAg+生成Ag单
2
质,同时有0.1molNO -从丙室移向丁室,一共减少17g;
3
D选项错误,由于浓差电池中,Ag(2)电极的Ag+浓度已经减小,若要使电池恢复到初始
状态,Ag(2)电极需发生氧化反应(活性电极)产生Ag+,则Ag(2)需要和电源正极相连,D
错误。
14.答案D, 解析:①③两条曲线平行,所以物质类型相同,则曲线②代表HA溶液,b=5.5, 结
合纵坐标的意义可知:b点时,可算出K (HA)=c(H+)=1×10-5.5, 而a=4.0,此时c(OH-)=10-10
a
mol/L,此时金属阳离子浓度为1mol/L,所以曲线①的K =10-20, 同理可知,曲线③的
sp
K =10-11, 而题目已知Ksp[Mg(OH) ]>Ksp[Cu(OH) ],所以Ksp[Mg(OH) ]=10-11(对应曲线
sp 2 2 2
③), Ksp[Cu(OH) ]=10-20(对应曲线①),K (HA)=c(H+)=1×10-5.5(对应曲线②)
2 a
A选项正确;
B选项正确,当Cu2+刚好完全沉淀时,c(Cu2+)=10-5mol/L,则
K [Cu(OH) ] 1020
c(OH) sp 2 107.5mol/L
c(Cu2) 105
此时c(H+)=10-6.5mol/L,即溶液pH=6.5;
C选项正确:Mg(OH) +2HA=Mg2++2A-+2H O, 该反应的平衡常数
2 2
c(Mg2)c2(A) c(Mg2)c2(OH)c2(A)c2(H) K [Mg(OH) ]K2(HA) 1011(105.5)2
k sp 2 a 106 105
c2(HA) c2(HA)K2 K2 (1014)2
w w
所以C正确;
D选项错误,②③两条曲线相交时,N点的两条曲线的纵坐标相等,
c(HA) K c(H)
c(Mg2) ,即 sp ,
c(A) c2(OH) K
a
K c(H)c(OH) 1014
所以 sp ,而K 1011,则c(OH)102.5mol/L, pH11.5
c(OH) K 105.5 sp
a
所以选项D错误(也可以用数学方法分别求出两条曲线的函数方程,求出交点对应的横坐
标)。
15.(16分,除标注的地方外,其他每空2分)
(1)d(1分),3d24s2(1分)
(2)3(或三)(1分); CaSO 和SiO (2分,写化学式才给分,写对一个给1分,写了三个
4 2
的,错写一个扣1分,扣完为止,写了四种物质的不给分)。
(3)3.2≤pH<4.0(答[3.2,4)或3.2~4.0给2分,答3.2T (高温)时,以反应①
1 2 1
为主,CO 的转化率减小。
2
②79.1(MPa)-2(没有单位、单位写错不扣分,要求保留三位有效数字)
(5)①>(1分,写“大于”不给分) ②<(1分,写“小于”不给分)
解析:
(2)反应②-反应①,可得:CH 4 (g)+H 2 O(g) CO(g)+3H 2 (g) △H 3 = △H 2 -
△H=+207kJ/mol,该反应△H>0,△S>0,所以反应③在高温下自发(△G<0);
设 CO 的 键 能 是 xkJ/mol , 则 △H =(4×414kJ/mol+2×463kJ/mol) -
3
(x+3×436kJ/mol)=+207kJ/mol,可得x=1067。
(3)反应②的△H >0,适合高温条件,反应①的△H <0,适合于低温条件,但是温度太
2 1
低,反应速率太慢。
(4)①反应①的△H <0,反应②的△H >0,温度升高,反应①平衡向左移动,CO 的转化
1 2 2
率减小,而反应②平衡向右移动,CO 的转化率增大。在TT (高温)时,以反应①为主,CO 的转化率减小。
2 1 2
②设初始投料为1molCO 和2molH ,T 时,CO 转化0.6mol,CH 选择性为60%,则此
2 2 1 2 4
时n(CH )=0.36mol,n(CO)=0.24mol,n(CO )=0.4mol,设此时体系中n(H O)=xmol,
4 2 2
n(H )=ymol,由于存在三个反应,运用三段式法不方便,可以利用原子守恒建立等式:
2
n(H)=2x+2y+0.36×4=4mol,n(O)=x+0.4×2+0.24=2mol,解得x=0.96mol,y=0.32mol。
2mol0.32mol
H 的转化率 100%84%;
2 2mol
T 时刻,n(CH )=0.36mol,n(CO)=0.24mol,n(CO )=0.4mol,n(H O)=0.96mol,n(H )=0.32mol,
1 4 2 2 2
体系中五种气体的总物质的量为2.28mol,而P =2.28MPa,所以:
总
p(CH )=0.36MPa,p(CO)=0.24MPa,p(CO )=0.4MPa,p(H O)=0.96MPa,p(H )=0.32MPa,
4 2 2 2
(0.36MPa)(0.96MPa)2
则反应①的K = 79.1(MPa)2
p (0.4MPa)(0.32MPa)4
(5)①在恒温恒容条件下, 乙和丙相对于甲的投料而言,乙增加1molCO (提高H 的平衡
2 2
转化率),丙增加1molH (降低了H 的平衡转化率),所以平衡时H 的转化率:乙>甲>
2 2 2
丙。
②在绝热恒容条件下,甲从正方向投料,正反应吸热(温度越高,平衡常数越大),导
致温度减低,正反应平衡常数减小,丁从反方向投料(放热方向),温度升高,平衡常
数增大,所以正反应的平衡常数:甲<丁。
18(14分,除了标注之外每空2分)
(1)2-溴苯丙酸(1分,2-溴-3-苯基丙酸,也给分); 2(或两)(1分)
(2)氰基、羧基(2分,答对一个给1分); 17 (3)
5
{#{QQABLYIEggCoAAAAAQgCAwHYCEAQkAAAAIoGAFAAMAIBCRNABAA=}#}(4)36
(5)
(一共4分,每一步1分,如果第一步写错就不给分)
解析:
反应①为α-卤代反应,则A是 ,再用-CN取代-Br,结合B的分
子 式 可 知 B 是 , 再 用 SOCl 和 NH 取 代 , 得 到
2 3
,最后用H 还原-CN(酰胺基不与H 反应),得到C的结构简式
2 2
是 。
(1)A中碳原子有苯环和羧基碳原子的sp2杂化以及饱和碳原子的sp3杂化,一共两种。
(2)B分子共平面问题:苯环上12个原子一定共平面, 结构中,四个原子也
共平面,而sp3杂化的饱和碳原子,最多只能与周围2个原子共平面,-OH上的H原子可
以通过单键旋转而与之共平面,所以 B 分子中,最多共平面的原子数有 17 个。
(4)观察C的结构,苯环外的不饱和度为1(只含一个不饱和键),现要求苯环上三个位置被
取代,-CH CHO占据一个位置,剩下2个-NH 和2个碳原子,通过组合,符合条件的同
2 2
分异构有四大类:
6
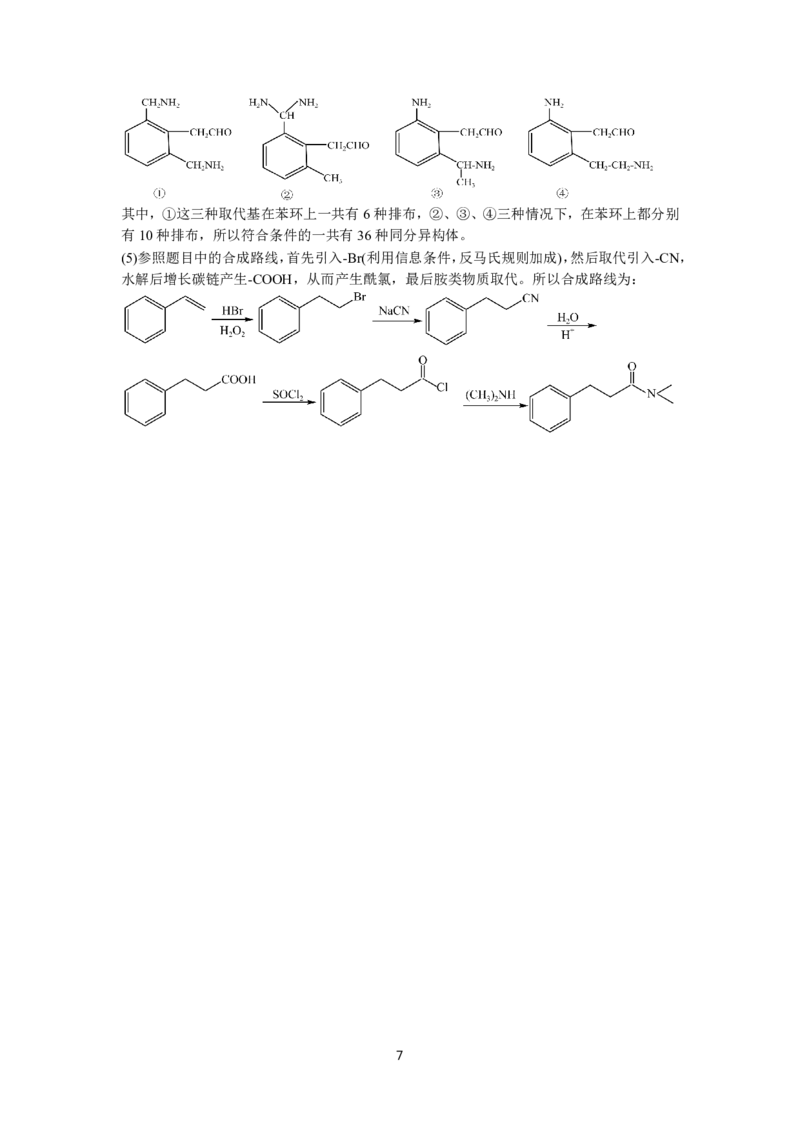
{#{QQABLYIEggCoAAAAAQgCAwHYCEAQkAAAAIoGAFAAMAIBCRNABAA=}#}其中,①这三种取代基在苯环上一共有6种排布,②、③、④三种情况下,在苯环上都分别
有10种排布,所以符合条件的一共有36种同分异构体。
(5)参照题目中的合成路线,首先引入-Br(利用信息条件,反马氏规则加成),然后取代引入-CN,
水解后增长碳链产生-COOH,从而产生酰氯,最后胺类物质取代。所以合成路线为:
7
{#{QQABLYIEggCoAAAAAQgCAwHYCEAQkAAAAIoGAFAAMAIBCRNABAA=}#}