文档内容
高一化学试题
2024.7
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分.满分100分,考试时间90分钟.
注意事项:
1.每小题选出答案后,用2B铅笔把答题卡上对应题目答案标号涂黑.如需改动,用橡皮擦干
净后,再选涂其他答案标号,不能将答案直接答在试卷上.
2.考试结束后,请将答题卡一并交回.
可能用到的相对原子质量:
第Ⅰ卷(选择题 共40分)
一、选择题:本题共10小题,每小题2分,共20分.每小题只有一个选项符合题目要求.
1.青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践.下列有关解释合理的是( )
A.清洗铁锅后及时擦干,能减缓铁锅因发生析氢腐蚀而生锈
B.烹煮食物的后期加入食盐,能避免 长时间受热而分解
C.用盐卤(主要成分 )点豆腐,能使得豆浆中的蛋白质胶体发生聚沉
D.制作面点时加入食用小苏打,利用 中和发酵过程产生的酸
2.下列过程中不涉及氧化还原反应的是( )
A.灼烧干海带 B.乙醚浸取青蒿素 C.雷雨发庄稼 D.氯碱工业
3.鉴别浓度均为 的 溶液,下列方法不可行的是( )
A.焰色试验 B.滴加醋酸 C.滴加 溶液 D.滴加硫酸钠溶液
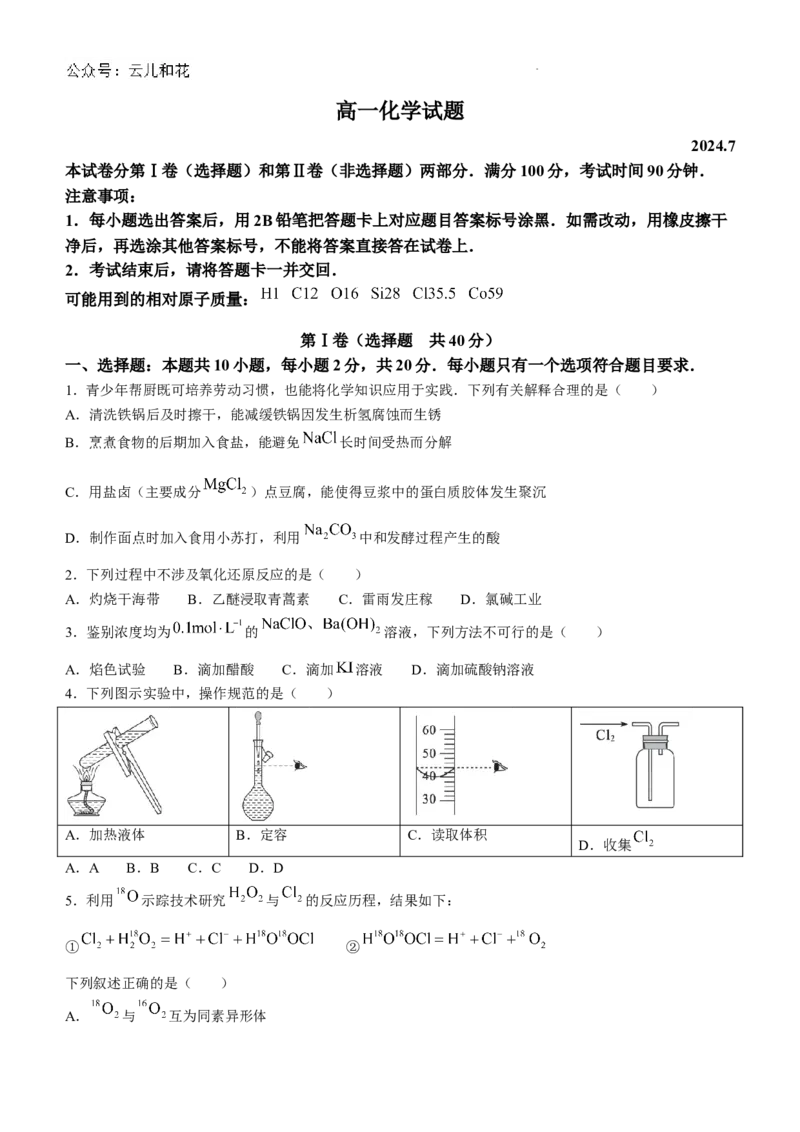
4.下列图示实验中,操作规范的是( )
A.加热液体 B.定容 C.读取体积
D.收集
A.A B.B C.C D.D
5.利用 示踪技术研究 与 的反应历程,结果如下:
① ②
下列叙述正确的是( )
A. 与 互为同素异形体
学科网(北京)股份有限公司B.1个 分子中含20个质子
C.反应历程②中未涉及非极性共价键的断裂
D.用电子式表示 的形成过程
6.下列叙述Ⅰ和叙述Ⅱ均正确,且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A 石墨能导电且化学性质不活泼 阴极电保护法中可用石墨作辅助阳极
B 用于制造光导纤维
的导电性介于导体和绝缘体之间
C 五氧化二磷可吸水 可用作食品干燥剂
D 断裂氨分子中的化学键需要吸收热量 工业上用液氨作制冷剂
A.A B.B C.C D.D
7.X、Y、Z、W为短周期主族元素,原子序数依次增大,最外层电子数之和为15.X的单质可以在W的单
质中燃烧,火焰为苍白色,Y是金属元素,Z的最外层电子数是次外层电子数的一半.下列说法错误的是(
)
A.稳定性 B.原子半径
C.最高价含氧酸的酸性 D.W的一种氧化物可用于自来水的杀菌消毒
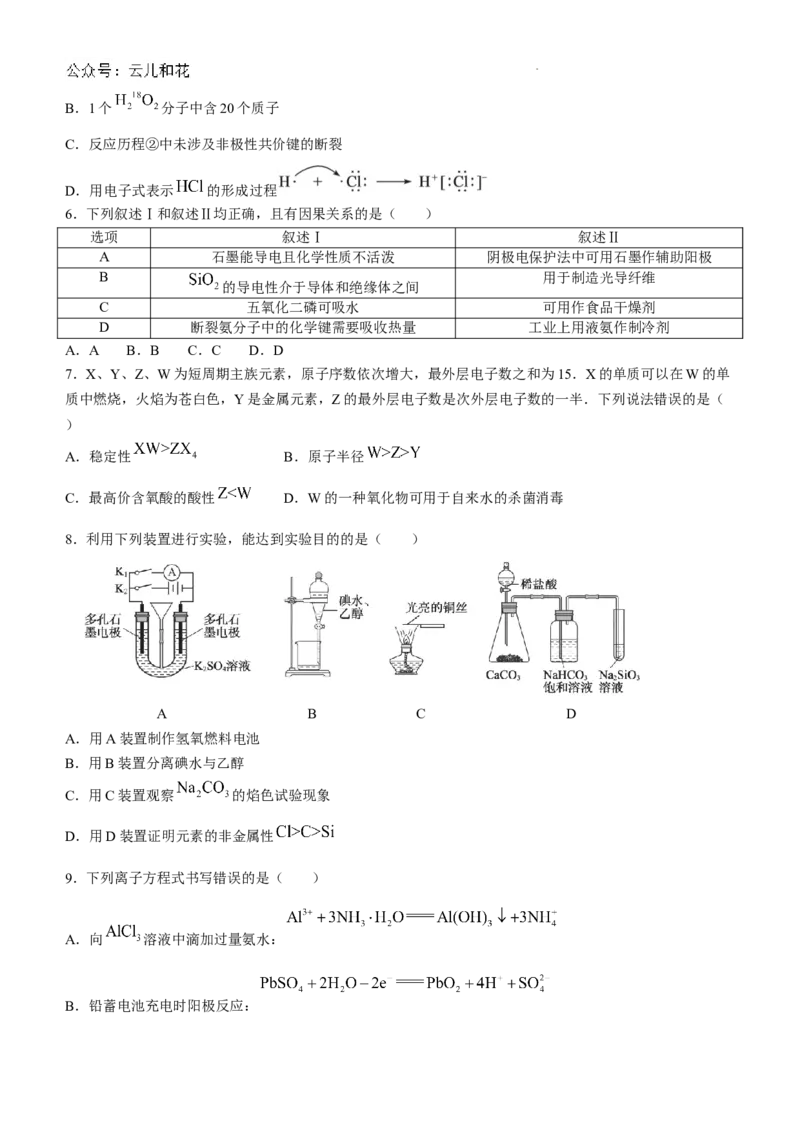
8.利用下列装置进行实验,能达到实验目的的是( )
A B C D
A.用A装置制作氢氧燃料电池
B.用B装置分离碘水与乙醇
C.用C装置观察 的焰色试验现象
D.用D装置证明元素的非金属性
9.下列离子方程式书写错误的是( )
A.向 溶液中滴加过量氨水:
B.铅蓄电池充电时阳极反应:
学科网(北京)股份有限公司C.用惰性电极电解硝酸银溶液离子方程式:
D.海水提溴过程中将溴吹入 吸收塔:
10.探究 反应速率的影响因素,
有关实验数据如下表所示:
编号 温度℃
催化剂 酸性 溶液 溶液 溶
液褪色平均
体积 浓度 体积 浓度 时间
1 25 0.5 4 0.1 8 0.2 12.7
2 80 0.5 4 0.1 8 0.2 a
3 25 0.5 4 0.01 8 0.2 6.7
4 25 0 4 0.01 8 0.2 b
下列说法错误的是( )
A.通过实验可得到“其他条件相同时,温度升高,可加快反应速率”的结论,证据是
B.可通过比较相同时间收集 体积来判断反应速率快慢
C.实验3和4探究的是催化剂对反应速率的影响,
D.实验3中用 表示该反应速率
二、选择题:本题共5小题,每小题4分,共20分.每小题有一个或两个选项符合题意,全部
选对得4分,选对但不全的得2分,有选错的得0分.
11.根据实验操作或现象所得结论正确的是( )
实验操作或现象 结论
A
取 溶液于试管中,加入 溶 与 反应有定限度
液,充分反应后,分为两份,一份滴入 溶液,溶液变红;另一
份加淀粉,变蓝
B
向 溶液中滴加过量氯水,再加入淀粉 溶液,溶液先变橙黄色
氧化性
后变蓝色
C 醋酸的电离需要吸收热量
用 溶液分别与等体积等浓度 溶液、
盐酸反应,测得反应热依次为
D
向锌和稀硫酸反应的试管中滴加几滴 溶液,气泡生成速率加快 是该反应的催化剂
A.A B.B C.C D.D
12.以 为催化剂的光热化学循环分解 的反应机理如图所示;已知:常温常压下,由最稳定的单质
学科网(北京)股份有限公司合成 某物质的反应焓变叫做该物质的摩尔生成焓,最稳定的单质的摩尔生成焓为0. 和 的摩尔
生成焓分别为 .
下列说法错误的是( )
A.过程①吸收能量
B.反应过程中 元素的化合价未发生变化
C.该过程中存在的能量转化形式:光能→化学能,热能→化学能
D.二氧化碳分解的热化学方程式为
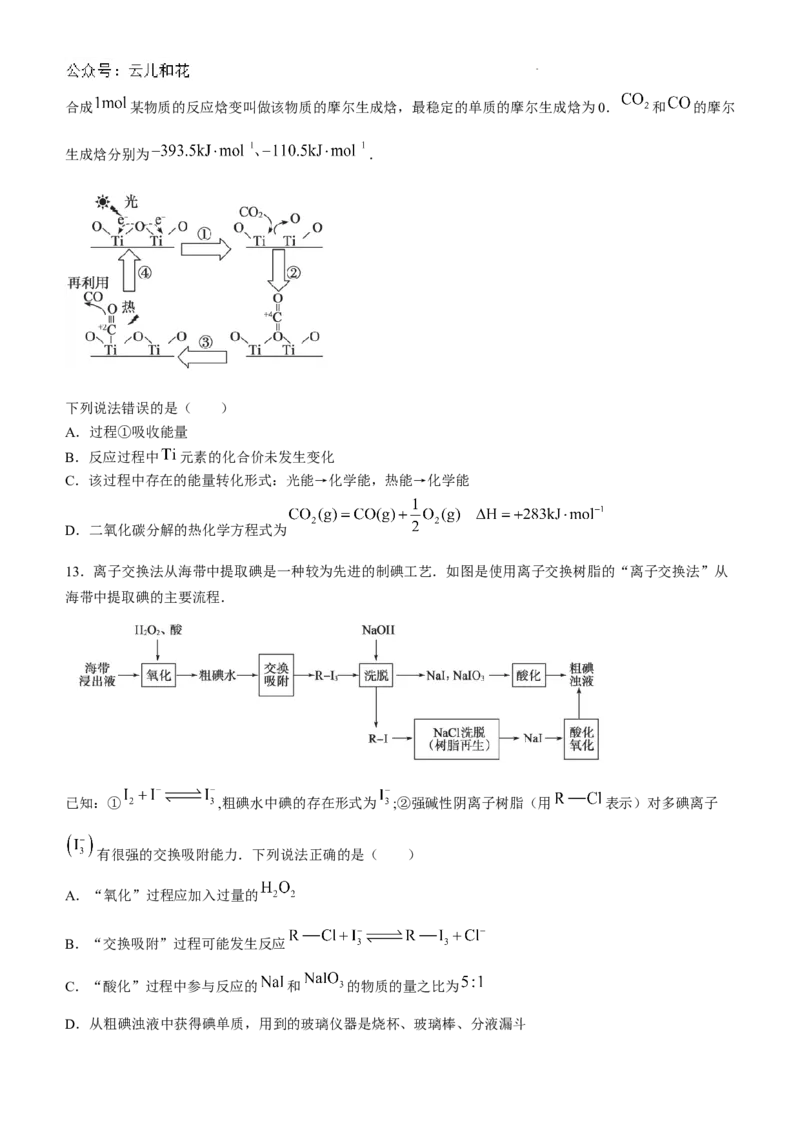
13.离子交换法从海带中提取碘是一种较为先进的制碘工艺.如图是使用离子交换树脂的“离子交换法”从
海带中提取碘的主要流程.
已知:① ,粗碘水中碘的存在形式为 ;②强碱性阴离子树脂(用 表示)对多碘离子
有很强的交换吸附能力.下列说法正确的是( )
A.“氧化”过程应加入过量的
B.“交换吸附”过程可能发生反应
C.“酸化”过程中参与反应的 和 的物质的量之比为
D.从粗碘浊液中获得碘单质,用到的玻璃仪器是烧杯、玻璃棒、分液漏斗
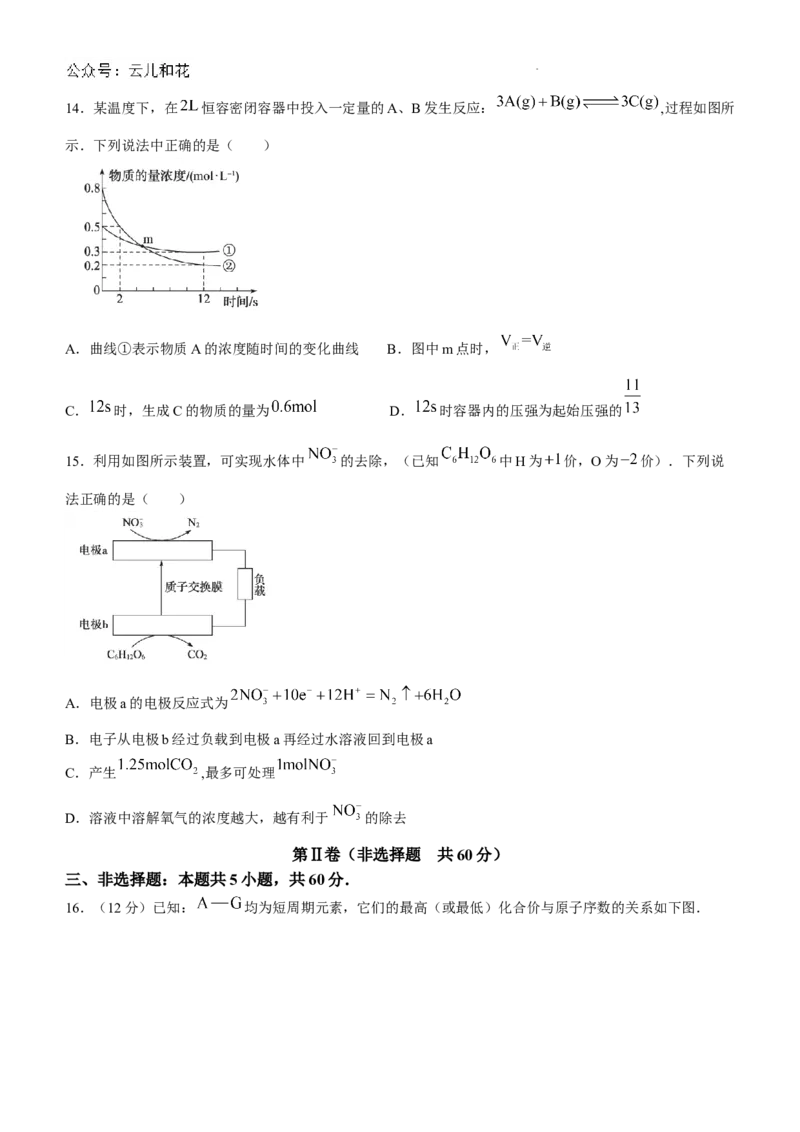
学科网(北京)股份有限公司14.某温度下,在 恒容密闭容器中投入一定量的A、B发生反应: ,过程如图所
示.下列说法中正确的是( )
A.曲线①表示物质A的浓度随时间的变化曲线 B.图中m点时,
C. 时,生成C的物质的量为 D. 时容器内的压强为起始压强的
15.利用如图所示装置,可实现水体中 的去除,(已知 中H为 价,O为 价).下列说
法正确的是( )
A.电极a的电极反应式为
B.电子从电极b经过负载到电极a再经过水溶液回到电极a
C.产生 ,最多可处理
D.溶液中溶解氧气的浓度越大,越有利于 的除去
第Ⅱ卷(非选择题 共60分)
三、非选择题:本题共5小题,共60分.
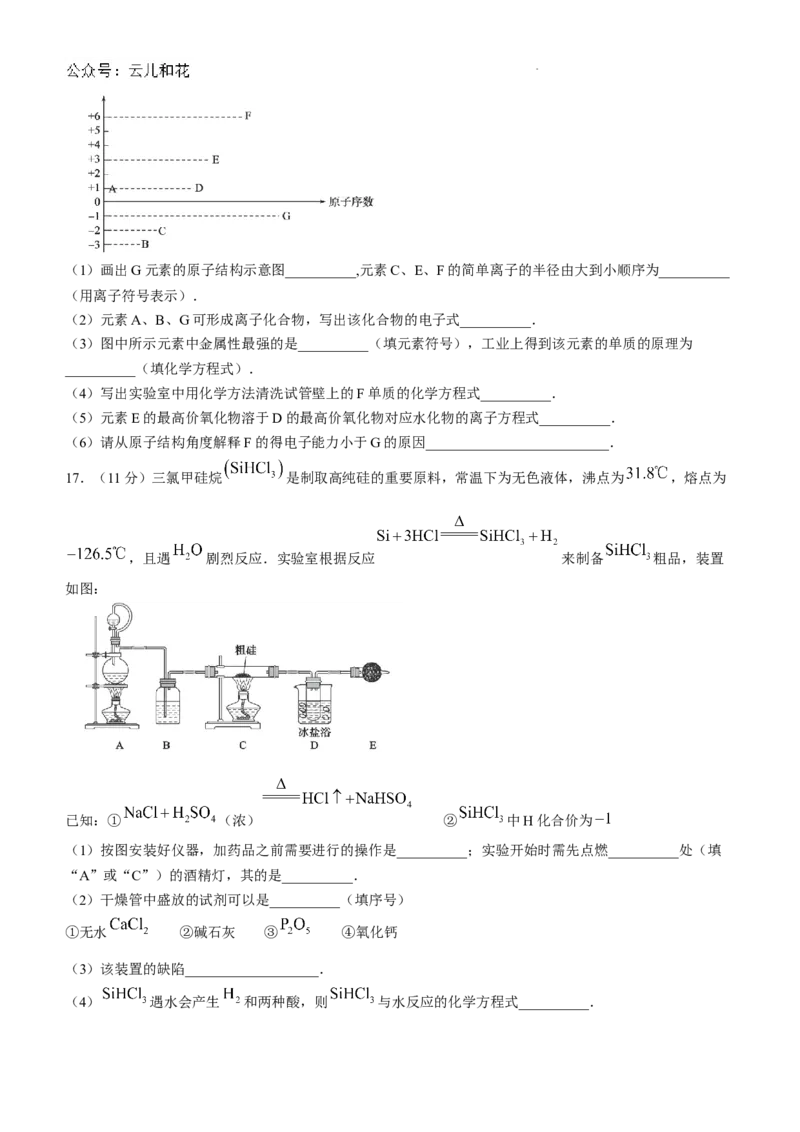
16.(12分)已知: 均为短周期元素,它们的最高(或最低)化合价与原子序数的关系如下图.
学科网(北京)股份有限公司(1)画出G元素的原子结构示意图__________,元素C、E、F的简单离子的半径由大到小顺序为__________
(用离子符号表示).
(2)元素A、B、G可形成离子化合物,写出该化合物的电子式__________.
(3)图中所示元素中金属性最强的是__________(填元素符号),工业上得到该元素的单质的原理为
__________(填化学方程式).
(4)写出实验室中用化学方法清洗试管壁上的F单质的化学方程式__________.
(5)元素E的最高价氧化物溶于D的最高价氧化物对应水化物的离子方程式__________.
(6)请从原子结构角度解释F的得电子能力小于G的原因__________________________.
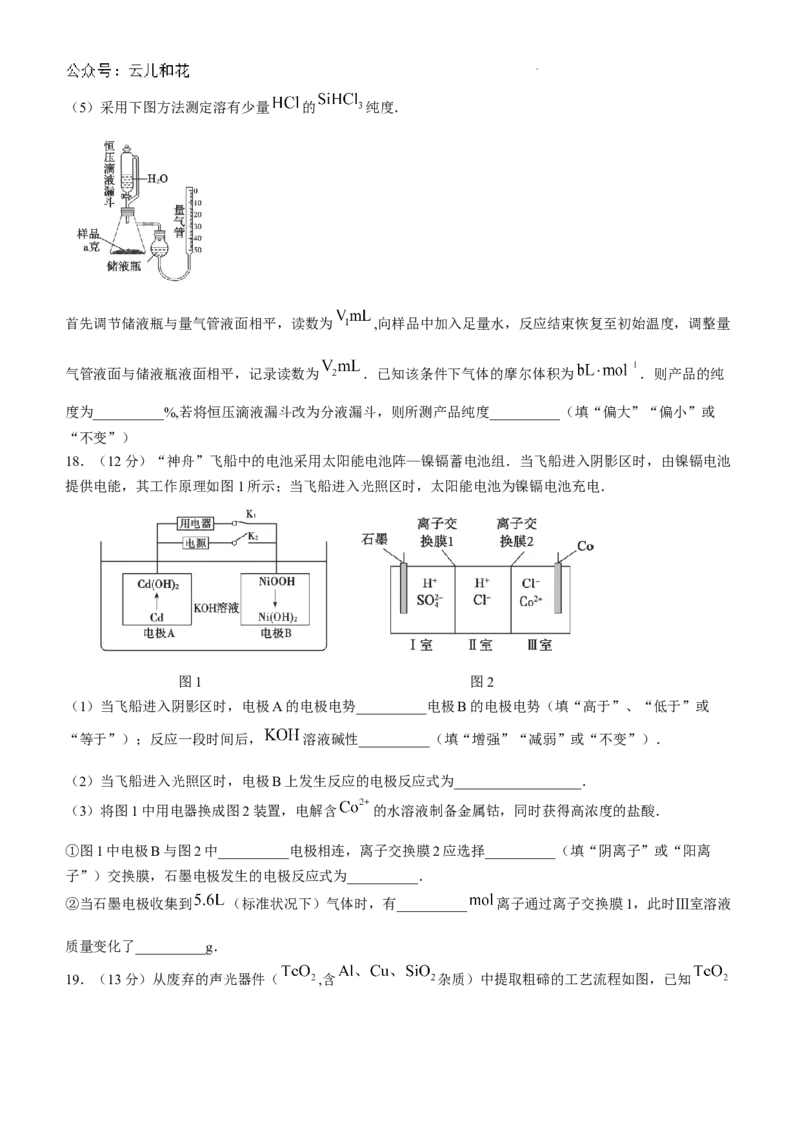
17.(11分)三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,且遇 剧烈反应.实验室根据反应 来制备 粗品,装置
如图:
已知:① (浓) ② 中H化合价为
(1)按图安装好仪器,加药品之前需要进行的操作是__________;实验开始时需先点燃__________处(填
“A”或“C”)的酒精灯,其的是__________.
(2)干燥管中盛放的试剂可以是__________(填序号)
①无水 ②碱石灰 ③ ④氧化钙
(3)该装置的缺陷___________________.
(4) 遇水会产生 和两种酸,则 与水反应的化学方程式__________.
学科网(北京)股份有限公司(5)采用下图方法测定溶有少量 的 纯度.
首先调节储液瓶与量气管液面相平,读数为 ,向样品中加入足量水,反应结束恢复至初始温度,调整量
气管液面与储液瓶液面相平,记录读数为 .已知该条件下气体的摩尔体积为 .则产品的纯
度为__________%,若将恒压滴液漏斗改为分液漏斗,则所测产品纯度__________(填“偏大”“偏小”或
“不变”)
18.(12分)“神舟”飞船中的电池采用太阳能电池阵—镍镉蓄电池组.当飞船进入阴影区时,由镍镉电池
提供电能,其工作原理如图1所示;当飞船进入光照区时,太阳能电池为镍镉电池充电.
图1 图2
(1)当飞船进入阴影区时,电极A的电极电势__________电极B的电极电势(填“高于”、“低于”或
“等于”);反应一段时间后, 溶液碱性__________(填“增强”“减弱”或“不变”).
(2)当飞船进入光照区时,电极B上发生反应的电极反应式为__________________.
(3)将图1中用电器换成图2装置,电解含 的水溶液制备金属钴,同时获得高浓度的盐酸.
①图1中电极B与图2中__________电极相连,离子交换膜2应选择__________(填“阴离子”或“阳离
子”)交换膜,石墨电极发生的电极反应式为__________.
②当石墨电极收集到 (标准状况下)气体时,有__________ 离子通过离子交换膜1,此时Ⅲ室溶液
质量变化了__________g.
19.(13分)从废弃的声光器件( ,含 杂质)中提取粗碲的工艺流程如图,已知
学科网(北京)股份有限公司性质与 相似.回答下列问题.
(1)碲 在元素周期表的位置为__________.
(2)为加快“碱性浸出”的反应速率可采取的措施有__________(写出一条即可).
“碱性浸出”所得滤渣的主要成分为__________.
(3)“氧化沉碲”过程中氧化剂所含的化学键类型为__________,氧化剂与还原剂的物质的量之比为
__________.
(4)“溶解还原”中离子方程式为__________,“溶解还原”后的浊液经__________、洗涤、干燥得到粗碲.
判断洗涤干净的实验操作和现象是__________.
(5)电解法提纯粗碲时,先将上述流程得到的粗碲溶于 溶液,生成 电解液,再用适当的电
极进行电解,阴极的电极反应式为__________.
20.(12分)碳中和作为一种新型环保形式可推动社会绿色发展.下图为科学家研究的一种二氧化碳新循环
体系,主要分为4个过程.
(1)过程Ⅰ的原理: ,根据下表数据回答:
化学键
436 496 463
键能/
由过程Ⅰ制备 需__________(填“放出”或“吸收”)能量__________ .
(2)常温下,在过程Ⅲ中 在氧气中充分燃烧生成 和液态水放出 的热量,则甲
醇的摩尔燃烧焓的热化学方程式为____________________.
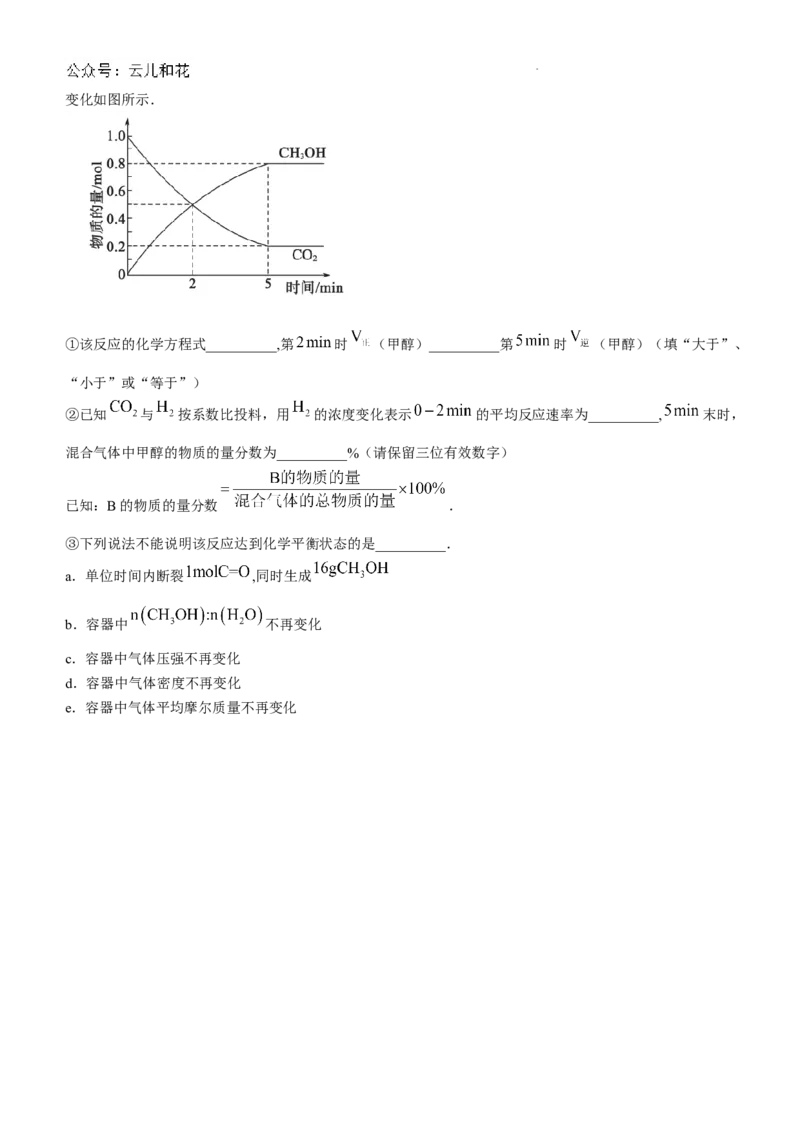
(3) 时,在 密闭容器中充入 和 发生过程Ⅱ中的反应, 和 的物质的量随时间
学科网(北京)股份有限公司变化如图所示.
①该反应的化学方程式__________,第 时 (甲醇)__________第 时 (甲醇)(填“大于”、
“小于”或“等于”)
②已知 与 按系数比投料,用 的浓度变化表示 的平均反应速率为__________, 末时,
混合气体中甲醇的物质的量分数为__________%(请保留三位有效数字)
已知:B的物质的量分数 .
③下列说法不能说明该反应达到化学平衡状态的是__________.
a.单位时间内断裂 ,同时生成
b.容器中 不再变化
c.容器中气体压强不再变化
d.容器中气体密度不再变化
e.容器中气体平均摩尔质量不再变化
学科网(北京)股份有限公司高一化学试题参考答案
一、选择题:本题共10小题,每小题2分,共20分.每小题只有一个选项符合题目要求.
1.C 2.B 3.B 4.D 5.C 6.A 7.B 8.A 9.C 10.D
二、选择题:本题共5小题,每小题4分,共20分.每小题有一个或两个选项符合题意,全部
选对得4分,选对但不全的得2分,有选错的得0分.
11.AC 12.B 13.BC 14.D 15.AC
三、非选择题:本题共5小题,共60分.
16.(12分,除标注外,每空2分)
(1) (1分) (1分) (2) (1分)
(3) (1分) (熔融)
(4)
(5)
(6)S原子与 原子电子层数相同,半径 ,核电荷数 ,对最外层电子的吸引力 ,得电子能
力
17.(11分,除标注外,每空2分)
(1)检验装置的气密性(1分) A(1分) 排尽装置中的空气(1分)
(2)②④
(3)无 的尾气处理装置(1分)
(4)
(5) 偏大(1分)
18.(12分,除标注外,每空2分)
(1)低于(1分) 增强(1分)
(2)
学科网(北京)股份有限公司(3)①石墨(1分) 阴离子(1分) ②1 65
19.(13分,除标注外,每空2分)
(1)第5周期 族(1分)
(2)适当提高 浓度、适当提高温度、搅拌(1分)(任写1条即得1分) (1分)
(3)离子键、(极性)共价键(1分)
(4)
过滤(1分) 取最后一次洗涤液于试管中,加入 溶液,若无白色沉淀生成,则说明洗涤干净
(5)
20.(12分,除标注外,每空2分)
(1)吸收(1分) 242(1分)
(2)
(3)① (1分) 大于(1分)
② 33.3 ③
学科网(北京)股份有限公司