文档内容
第 04 课 离子反应 离子方程式
[学习目标]
课标要点 学科素养
离子反应及离子方程式 通过离子方程式的书写,培养用化学符号说明物质变化的能力
通过分析、推理等方法认识离子反应的本质特征、构成要素及其
离子反应的条件
相互关系
1.通过实验事实认识离子反应。
2.认识并掌握离子反应发生的条件。
3.掌握离子方程式的书写方法,学会判断离子方程式的正误。
[学习过程]
教材学习
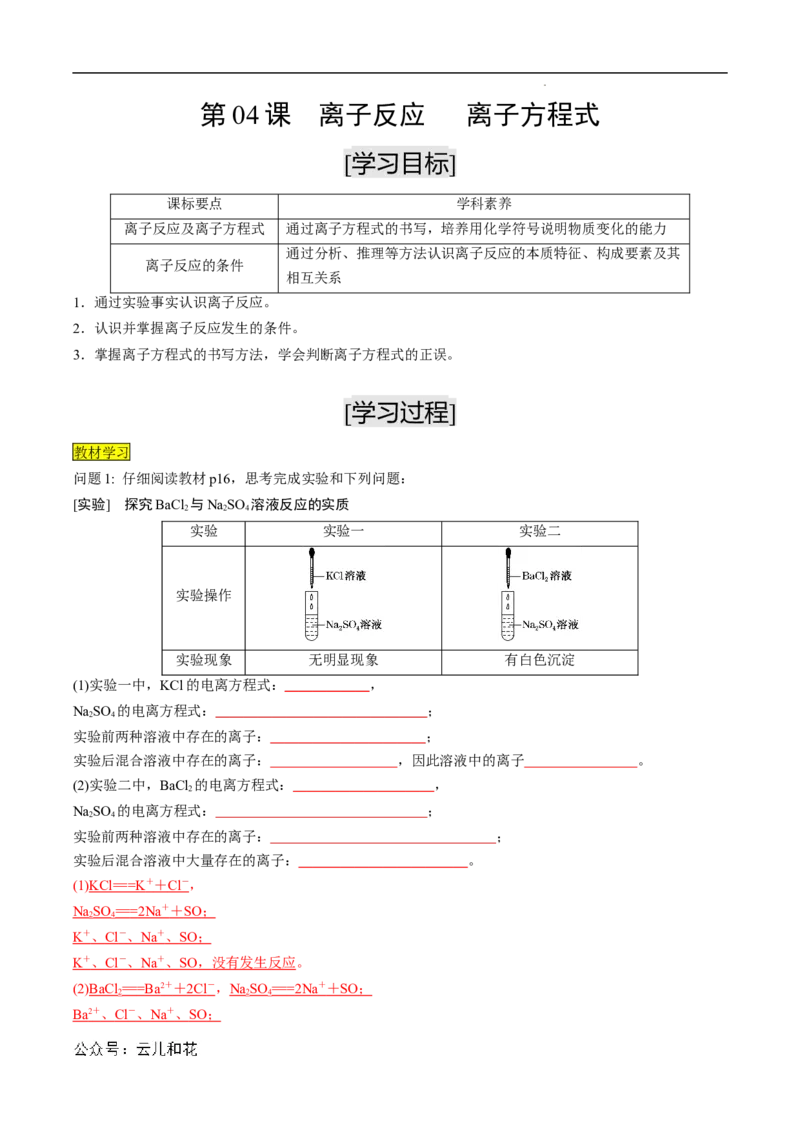
问题1: 仔细阅读教材p16,思考完成实验和下列问题:
[实验] 探究BaCl 与NaSO 溶液反应的实质
2 2 4
实验 实验一 实验二
实验操作
实验现象 无明显现象 有白色沉淀
(1)实验一中,KCl的电离方程式:______,
NaSO 的电离方程式:_______________;
2 4
实验前两种溶液中存在的离子:___________;
实验后混合溶液中存在的离子:_________,因此溶液中的离子________。
(2)实验二中,BaCl 的电离方程式:__________,
2
NaSO 的电离方程式:_______________;
2 4
实验前两种溶液中存在的离子:________________;
实验后混合溶液中大量存在的离子:____________。
(1) KCl == = K + + Cl - ,
NaSO == = 2Na + + SO ;
2 4
K + 、 Cl - 、 Na + 、 SO ;
K + 、 Cl - 、 Na + 、 SO , 没有发生反应 。
(2)BaCl == = Ba 2 + + 2Cl - ,NaSO == = 2Na + + SO ;
2 2 4
Ba 2 + 、 Cl - 、 Na + 、 SO ;
学科网(北京)股份有限公司Na + 、 Cl - 。
上述实验过程可用如图表示:
(3)由上述实验得出的结论是BaCl 与NaSO 溶液之间的反应,实质上是Ba2+与SO之间的反应。
2 2 4
即电解质在溶液中的反应,实质上是离子之间的反应。
问题2:仔细阅读教材p17,思考下列问题:
(1)对于反应Ba(OH) +H SO =BaSO ↓+2H O,从微观角度来看,实质是
2 2 4 4 2
。
(2)电解质在溶液中的反应实质上是 ,这样的反应属于 。
(3) 来表示反应的式子叫做 。
(4)离子方程式正确书写步骤:(以NaSO 溶液和BaCl 溶液的反应为例)
2 4 2
写出反应的化学方程式:NaSO +BaCl ===BaSO ↓+2NaCl。
2 4 2 4
把易溶于水且易电离的物质写成离子的形式。难溶的物质、气体和水等仍用化学式表示:
。
删去方程式两边 :SO+Ba2+===BaSO ↓
4
查: 。
(1)Ba2++2OH−+2H++SO=BaSO ↓+2H O
4 2
(2)离子之间的反应 离子反应
(3)用实际参加反应的离子符号 离子方程式
(4)2Na++SO+Ba2++2Cl−===BaSO ↓+2Na++2Cl− 不参加反应的离子,并化为最简 检查方程式两边
4
各元素的原子个数和电荷总数是否相等
[知识精讲]
一. 离子反应
1.概念:有离子参加或生成的化学反应。
2.本质:离子反应总是向着某种离子浓度减小的方向进行。
3.发生条件
(1)反应中有难溶物质生成,如生成BaSO。
4
(2)反应中有难电离物质生成,如生成CHCOOH。
3
(3)反应中有易挥发物质生成,如生成CO。
2
(4)溶液中的某些离子发生氧化还原反应,如Cl 与NaBr反应。
2
二.离子方程式
1.概念:用实际参加反应的离子符号来表示反应的式子叫作离子方程式。
2.书写步骤(以NaSO 溶液与BaCl 溶液的反应为例)
2 4 2
学科网(北京)股份有限公司3.离子方程式的书写及判断的核心
在书写离子方程式和判断离子方程式的正误时要从“两易”“两等”和“两查”入手:
4.书写离子方程式时的拆分原则
(1)强酸、强碱和易溶于水的盐改写成离子形式,难溶物质、难电离物质、易挥发物质、单质、氧化物等均
写化学式。
(2)改写微溶物时要看清题目要求
①作为反应物,若是澄清溶液写离子符号,若是悬浊液写化学式,如石灰水和石灰乳,石灰水写成离子形
式而石灰乳则写成化学式。
②作为生成物,一般写化学式(标“↓”号)。
(3)氨水作反应物写NH ·H O;作生成物,若有加热条件或浓度很大时,可写NH (标“↑”号)。
3 2 3
(4)容易出现错误的几类物质的改写
①多元弱酸的酸式酸根离子不能拆开写,如NaHCO 不能拆写成Na+、H+和CO,应拆写成Na+和HCO。
3
②浓硫酸作为反应物不能拆开写,应写成化学式;在溶液中的NaHSO 应拆写成Na+、H+和SO。
4
5.离子方程式的意义
反应物 化学方程式 离子方程式
HCl+NaOH HCl+NaOH===NaCl+HO
2
HCl+KOH HCl+KOH===KCl+HO
2
H++OH-===HO
2
HSO +NaOH HSO +2NaOH===NaSO +2HO
2 4 2 4 2 4 2
HSO +KOH HSO +2KOH===KSO +2HO
2 4 2 4 2 4 2
可以看出,离子方程式不仅可以表示某个具体的化学反应,还可以表示同一类型的离子反应。
意义:表示一类化学反应。
学科网(北京)股份有限公司[典题例析]
[例1]下列有关反应中不属于离子反应的是( )
A.NaCO 溶液与澄清石灰水的反应
2 3
B.氢氧化铜与稀硫酸的反应
C.锌与氯化铜溶液的反应
D.二氧化碳与生石灰作用生成碳酸钙的反应
[例2]下列离子方程式书写正确的是( )
A.碳酸钠溶液与盐酸反应:NaCO+2H+===2Na++HO+CO↑
2 3 2 2
B.氨水中加盐酸:H++OH-===H O
2
C.硫酸铜溶液中放入铁片:Cu2++Fe===Fe2++Cu
D.碳酸钙溶于硝酸:CO+2H+===H O+CO↑
2 2
[例3]下列化学方程式对应的离子方程式正确的是( )
A.CuCO+2NaOH===Cu(OH) ↓+NaCO Cu2++2OH-===Cu(OH) ↓
3 2 2 3 2
B.Ba(OH) +HSO ===BaSO ↓+2HO Ba2++SO===BaSO ↓
2 2 4 4 2 4
C.AgNO+NaCl===AgCl↓+NaNO Ag++Cl-===AgCl↓
3 3
D.Cu(OH) +HSO ===CuSO+2HO OH-+H+===H O
2 2 4 4 2 2
[例4]下列各反应能用H++OH-===H O表示的是( )
2
A.Ba(OH) 溶液和稀硫酸的反应
2
B.NaOH溶液和稀盐酸的反应
C.Cu(OH) 和稀硫酸的反应
2
D.NaOH溶液和CO 的反应
2
[例5]离子反应方程式书写:(注意写化学方程式不给分)
(1)用盐酸中和烧碱,请写出其反应的离子方程式: 。
(2)用稀硫酸清洗铁锈(Fe O),请写出其反应的离子方程式: 。
2 3
(3)用足量的澄清石灰水检验二氧化碳,请写出其反应的离子方程式: 。
(4)用铝片与硝酸汞溶液反应,请写出其反应的离子方程式: 。
(5)用醋酸可以溶解碳酸钙,请写出其反应的离子方程式: 。
[例6]判断下列反应的离子方程式是否正确,在括号中打“√”或“×”。
(1)盐酸与碳酸钡反应:CO2-
+ 2H+ === CO↑ + H O( )
3 2 2
(2)铝与盐酸反应:Al + 6H+ === Al3+ +3H↑( )
2
(3)硝酸银溶液中加入铜粉:Ag+ + Cu === Cu2+ + Ag( )
(4)Mg与醋酸溶液反应:Mg + 2H+ === Mg2+ + H ↑( )
2
(5)碳酸氢钙溶液与盐酸反应:Ca(HCO ) + 2H+ === Ca2+ + 2H O + 2CO ↑( )
3 2 2 2
(6)澄清石灰水与盐酸反应:Ca(OH) + 2H+ === 2HO + Ca2+( )
2 2
(7)碳酸钠与氯化钙混合:CO2-
+ Ca2+ === CaCO ↓( )
3 3
(8)稀硫酸与氢氧化钡溶液混合:H+ + SO2- + Ba2+ + OH- === HO + BaSO↓( )
4 2 4
学科网(北京)股份有限公司(9)氧化铁与稀盐酸混合: Fe O + 6H+ === 2Fe3+ + 3H O( )
2 3 2
[例1] 【答案】D
【解析】离子反应指的是有离子参加或生成的反应。酸、碱、盐在溶液中相互之间的反应都有离子参加,
活泼金属可以把较不活泼的金属从它们的盐溶液中置换出来(K、Ca、Na除外),在这些反应中也都有离子
参加,因此这些反应都属于离子反应。由此推出A、B、C项都正确;二氧化碳与生石灰的反应没有离子
参加或生成,不属于离子反应,D项错误。
[例2] 【答案】C
【解析】NaCO 易溶,应拆成离子形式,A项错误;NH ·H O为弱碱,应写化学式,B项错误;CaCO 难
2 3 3 2 3
溶于水,应写化学式,D项错误。
[例3]【答案】C
【解析】CuCO 是难溶性盐,在书写离子方程式时不能拆开,故A错误;有HO生成,离子方程式为Ba2+
3 2
+2OH-+2H++SO===BaSO ↓+2HO,故B错误;AgNO 和NaCl反应的实质为Ag++Cl-===AgCl↓,化
4 2 3
学方程式与离子方程式相对应,故C正确;Cu(OH) 难溶于水,不能拆成离子形式,故D错误。
2
[例4] 【答案】B
【解析】A项,Ba2++2OH-+SO+2H+===BaSO ↓+2HO;C项,Cu(OH) +2H+===Cu2++2HO;D项,
4 2 2 2
CO+2OH-===CO+HO。
2 2
【例5】
【答案】(1) H++OH- = HO(2分) (2) Fe O+6H+=2Fe3++3H O(2分)
2 2 3 2
(3) CO + Ca2++2OH-= CaCO ↓+H O(2分)(4)2Al+3Hg2+= 2Al3++3Hg(2分)
2 3 2
(5)CaCO+ 2CHCOOH=Ca2++2CH COO- +CO ↑+H O(2分)
3 3 3 2 2
【解析】(1)盐酸和烧碱发生中和反应产生NaCl和HO,反应的离子方程式是H++OH- === HO;(2)稀硫酸
2 2
清洗铁锈(Fe O),发生反应产生硫酸铁和水,反应的离子方程式是 Fe O+6H+=== 2Fe3++3H O;(3)二氧化
2 3 2 3 2
碳与氢氧化钙发生反应产生碳酸钙和水,反应的离子方程式是CO + Ca2++2OH-=== CaCO ↓+H O;(4)铝活
2 3 2
动性比Hg强,所以铝与硝酸汞发生置换反应产生汞和硝酸铝,根据电子守恒和电荷守恒可得,反应的离
子方程式是:2Al+3Hg2+=== 2Al3++3Hg;(5)由于醋酸的酸性比碳酸强,所以醋酸可以溶解碳酸钙,该反应
的离子方程式是CaCO + 2CHCOOH=== Ca2++2CH COO- +CO ↑+H O。
3 3 3 2 2
考点:考查离子方程式书写的知识。
【例6】
【答案】(1)~(3)××× ; (4)~(6)××× ; (7)~(9)√×√
[效果检测]
1.下列离子反应不能发生的是( )
A.KCl+NaOH===NaCl+KOH
B.AgNO+NaCl===AgCl↓+NaNO
3 3
C.NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
D.CaCO +HO+CO===Ca(HCO )
3 2 2 3 2
学科网(北京)股份有限公司2.下列各组物质间的反应中,不属于离子反应的是( )
A.Zn和HSO (稀)反应
2 4
B.NaCl溶液和AgNO 溶液反应
3
C.C和O 反应
2
D.Fe和CuSO 溶液反应
4
3.能正确表示下列化学反应的离子方程式的是( )
A.澄清的石灰水与盐酸的反应:OH−+H+===H O
2
B.氧化镁与稀硝酸反应:O2−+2H+===H O
2
C.硫酸镁溶液与氢氧化钡溶液混合:Ba2++SO===BaSO ↓
4
D.碳酸钙溶于稀盐酸中:CO+2H+===H O+CO↑
2 2
4.与铁、石灰水、石灰石都能发生离子反应的是( )
A.盐酸 B.CO C.O D.NaCO 溶液
2 2 2 3
5.NaHCO 和NaHSO 的溶液混合后,实际参加反应的离子是( )
3 4
A.H+和CO B.HCO和HSO
C.Na+、HCO和H+ D.HCO和H+
6.下列反应可以用同一离子方程式表示的是( )
A.HCl溶液+NaCO 溶液 HCl溶液+NaHCO 溶液
2 3 3
B.NaOH溶液+HCl溶液 Ba(OH) 溶液+HSO 溶液
2 2 4
C.BaCl 溶液+HSO 溶液 Ba(OH) 溶液+NaSO 溶液
2 2 4 2 2 4
D.CaCO +HCl溶液 NaCO 溶液+HSO 溶液
3 2 3 2 4
7.下列离子方程式的书写正确的是( )
A.稀醋酸与NaOH溶液的反应:H++OH−=H O
2
B.铜粉与稀盐酸的反应:Cu+2H+=Cu2++H↑
2
C.氯气与碘化钾溶液的反应:Cl+I−=Cl−+I
2 2
D.碳酸钠溶液与足量稀盐酸的反应:CO+2H+=CO↑+HO
2 2
8.下表中评价合理的是( )
选项 化学反应及其离子方程式 评价
石灰乳与NaCO 溶液混合:Ca2+
2 3
A 正确
+CO=CaCO ↓
3
向碳酸镁中加入稀盐酸:
B 错误,碳酸镁不应该写成离子形式
CO+2H+=CO↑+HO
2 2
向硫酸铜溶液中加入氢氧化钡溶液:Ba2+
C 正确
+SO=BaSO↓
4
氢氧化钙溶液与稀硫酸混合:Ca2++2OH−
D 错误,反应物和产物的配比不正确
+2H++SO=CaSO↓+2HO
4 2
9.氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道稀硫酸中的哪种粒子(H O、H+、SO)能使氧化铜
2
学科网(北京)股份有限公司溶解。请你和他一起通过下图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
(1)通过实验Ⅰ可以证明__________________________。
(2)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进
一步确认的实验操作是:在Ⅲ中先加入______________________,再加入____________________。
(3)探究结果为_______________________________。
(4)反应的离子方程式为__________________________________。
10.(1)书写下列反应的离子方程式。
①NaCl 溶液和 AgNO 溶液_____
3
②Ba(OH) 溶液和 HSO 溶液_____
2 2 4
③MgO 与稀盐酸反应_____
④NaHSO 与 NaHCO 溶液_____
4 3
(2)写出一个下列离子方程式表示的化学方程式。
①CO +2H+=CO ↑+HO:_____
2 2
②Ag++Cl-=AgCl↓:_____
③Cu2++2OH-=Cu(OH) ↓:_____
2
④SO +2OH-=SO +HO:_____
2 2
1.【答案】A
【解析】因KCl溶液与NaOH溶液相互交换成分,不生成水、气体、沉淀,则物质不能发生化学反应。
2. 【答案】C
【解析】A、B、D选项中的反应都是在溶液中进行的反应,且每一组中都有拆写出的离子参与反应,所以
都是离子反应;C与O 反应无论产物是CO还是CO ,都没有离子参加反应或者有离子生成,故不属于离
2 2
子反应。
3.【答案】A
【解析】单质、氧化物、难溶于水的物质、难电离的物质不能写成离子形式,B、D均错误;C项还生成
氢氧化镁沉淀。
4. 【答案】A
【解析】铁与盐酸发生置换反应、石灰水与盐酸发生中和反应、石灰石与盐酸发生复分解反应,都是离子
反应;铁与CO、NaCO 溶液不反应,与O 能反应但不是离子反应。
2 2 3 2
5.【答案】D
【解析】NaHCO 和NaHSO 的电离方程式分别如下:NaHCO =Na++HCO;NaHSO=Na+
3 4 3 4
学科网(北京)股份有限公司+H++SO,故D项正确。
6. 【答案】C
【解析】A项第1组反应为2H++CO=CO↑+HO,第2组反应为H++HCO=CO↑+HO,两者不同;B项第1
2 2 2 2
组反应为H++OH−=HO,第2组反应为Ba2++2OH−+2H++SO=BaSO↓+2
2 4
HO,两者不同;C项两组反应均为Ba2++SO=BaSO↓;D项第1组反应为CaCO +2H+=Ca2+
2 4 3
+CO↑+HO,第2组反应为CO+2H+=CO ↑+HO,两者不同。
2 2 2 2
7.【答案】D
【解析】离子方程式正误判断的方法是“三查”:一查电荷是否守恒,原子数是否守恒;二查物质拆分是
否正确;三查物质间的反应是否符合客观事实。据此可知 A中CHCOOH应写成化学式;B中铜不与盐酸
3
反应,不符合客观事实;C中原子不守恒。
8.【答案】B
【解析】A项离子方程式错误,微溶于水的氢氧化钙以石灰乳形式存在时,不能写成离子形式;C项漏掉
生成氢氧化铜沉淀的部分反应;D项离子方程式正确,评价错误。
9. 【答案】(1)H O不能使氧化铜溶解
2
(2)可溶性硫酸盐 稀硫酸
(3)H+能溶解氧化铜,而HO、SO两种粒子都不能使CuO溶解
2
(4)CuO+2H+===Cu2++HO
2
【解析】(2)在Ⅲ中应先加入可溶性的硫酸盐,以证明CuO的溶解过程中SO不起作用,然后再加入稀硫酸,
从而证明CuO溶解是硫酸中的H+起作用。
10.(【答案】Ag++Cl-=AgCl↓
AgNO+HCl=AgCl↓+HNO
3 3
【详解】
(1)①NaCl和AgNO 反应生成氯化银和硝酸钠,反应的离子方程式为:Ag++Cl-=AgCl↓,故答案为:Ag+
3
+Cl-=AgCl↓;
②Ba(OH) 溶液和 HSO 溶液反应生成硫酸钡沉淀和水,反应的离子方程式为:
2 2 4
,故答案为: ;
③MgO 与稀盐酸反应生成氯化镁和水,反应的离子方程式为: ,故答案为:
;
④NaHSO 与 NaHCO 溶液硫酸钠、二氧化碳和水,反应的离子方程式为: ,故答
4 3
案为: ;
(2) ①CO +2H+=CO ↑+HO代表可溶性碳酸盐和强酸反应,可以是碳酸钠和盐酸的反应,反应的方程
2 2
式为: ,故答案为: ;
学科网(北京)股份有限公司②Ag++Cl-=AgCl↓代表可溶性银盐和盐酸或可溶性氯化物的反应,可是硝酸银和盐酸的反应,反应方程式
为:AgNO+HCl=AgCl↓+HNO ,故答案为:AgNO+HCl=AgCl↓+HNO ;
3 3 3 3
③Cu2++2OH-=Cu(OH) ↓代表可溶性铜盐和强碱反应生成氢氧化铜和可溶性盐的过程,可以是氯化铜和氢
2
氧化钠的反应,反应方程式为: ,故答案为:
;
④SO +2OH-=SO +HO代表二氧化硫和强碱反应生成可溶性亚硫酸盐和水的反应,可以是二氧化硫和
2 2
强氧化钠的反应,反应方程式为: ,故答案为: ;
学科网(北京)股份有限公司学科网(北京)股份有限公司