文档内容
江西赣州市 2025—2026 学年高二年级 10 月月考化学试卷
试卷共8页,18小题,满分100分。考试用时75分钟。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.月饼是中秋佳节必不可少的美食。下列月饼制作过程的主要目的是减小反应速率的是( )
A.熟绿豆制作豆沙馅 B.月饼印花 C.分散烘烤 D.阴凉干燥处保存
A.A B.B C.C D.D
2. 在不同条件下的反应速率如下,其中表示反应速率最
快的是( )
A. B.
C. D.
3.下列事实不能用勒夏特列原理解释的是( )
A.工业上用熔融的 和熔融的 反应制备
B.工业合成氨时一般采用的压强为
C.天热时,打开冰镇可乐瓶盖产生大量泡沫
D.实验室不能用铁桶盛装 溶液
4.利用下列装置进行实验,其中能到达实验目的的是( )
A.用浓硫酸代替稀硫酸加快生成 的反应速率 B.实验室制备并收集C.探究稀盐酸与锌粒反应的热效应 D.探究浓度对化学反应速率的影响
A.A B.B C.C D.D
5.往烧杯中加入 碳酸氢钠固体、 柠檬酸及少量蒸馏水,搅拌,体系温度随时间变化曲线如图所示。
下列关于该反应的说法正确的是( )
A.为放热反应
B.正反应的活化能大于逆反应的活化能
C.反应物的总能量大于生成物的总能量
D.反应过程中能量变化趋势和生石灰与 反应的能量变化趋势相同
6. 时,往密闭容器中通入 ,发生反应:
。下列说法正确的是( )
A.充分反应后,混合气体的物质的量为
B.到达平衡时,降低温度,混合气体总物质的量会增大
C.反应体系中, 的值始终为2
D.平衡时,
7.劳动是人类生存的基石。下列劳动过程对应的化学知识正确且有关联的是( )
选项 劳动过程 化学知识
A 野炊时,往柴火堆中鼓入空气
空气中的 具有可燃性
B 酿酒时,在合适的温度下添加酒曲发酵 酒曲在合适的温度下具有催化作用
C 煤炭工对煤炭进行脱硫处理 脱硫后的煤炭燃烧效率更高
D 利用铝与氧化铁反应焊接铁轨 铝的熔点低
A.A B.B C.C D.D
8.软脂酸 和蔗糖 的燃烧热分别为 、。下列说法错误的是( )
A.在 时, 纯物质完全然烧生成指定产物时所放出的热量,叫做物质的然烧热
B.表示 燃烧热的热化学方程式为
C. 完全燃烧生成 和 ,放出的热量为
D.相同物质的量的软脂酸和蔗糖完全燃烧,蔗糖释放的热量更多
9.利用如图装置测定 的 。每次用 盐酸和
溶液进行反应,重复实验多次,测得反应前后温度差的平均值为 。已知
反应后溶液的比热容 ,盐酸与 溶液的密度近似为 ,且忽略由反应引起
的体积变化。下列说法正确的是( )
A.仪器a为金属搅拌器
B.实验过程中,若盐酸和 溶液少量多次混合,则测得的 会偏小
C.该实验测得的
D.将 溶液与盐酸混合后,立即测混合液的温度,该温度为反应前的初始温度
10.下列陈述I与陈述Ⅱ均正确,且两者间具有因果关系的是( )
选项 陈述I 陈述Ⅱ
增大强, 平衡正向
A 压缩封装有 和 混合气体的注射器,混合
移动,最终平衡时的 大于未压缩
气体的颜色先变深又逐渐变浅
时的
B 与稀硫酸反应,溶液变为棕黄色
C 浓硝酸保存在棕色试剂瓶中 浓硝酸具有强氧化性浓度增大,活化分子百分数增多,有效碰
D 反应物的浓度增大,化学反应速率增大
撞次数增多
A.A B.B C.C D.D
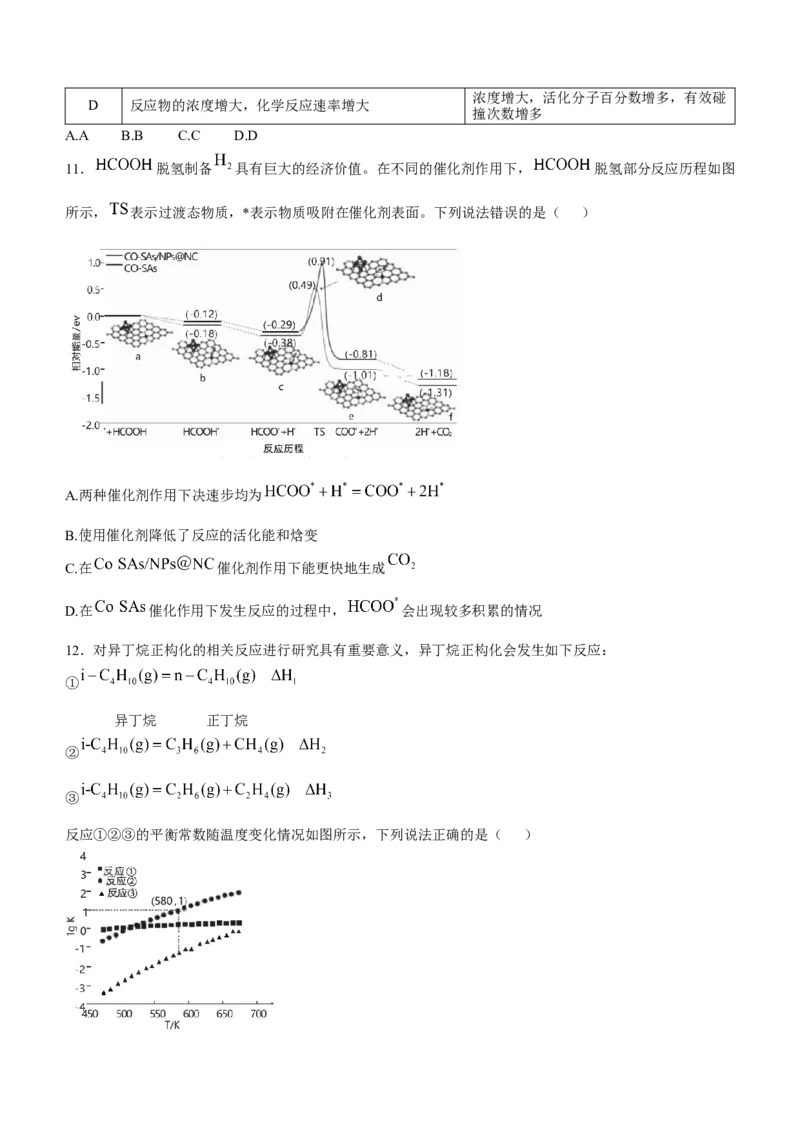
11. 脱氢制备 具有巨大的经济价值。在不同的催化剂作用下, 脱氢部分反应历程如图
所示, 表示过渡态物质,*表示物质吸附在催化剂表面。下列说法错误的是( )
A.两种催化剂作用下决速步均为
B.使用催化剂降低了反应的活化能和焓变
C.在 催化剂作用下能更快地生成
D.在 催化作用下发生反应的过程中, 会出现较多积累的情况
12.对异丁烷正构化的相关反应进行研究具有重要意义,异丁烷正构化会发生如下反应:
①
异丁烷 正丁烷
②
③
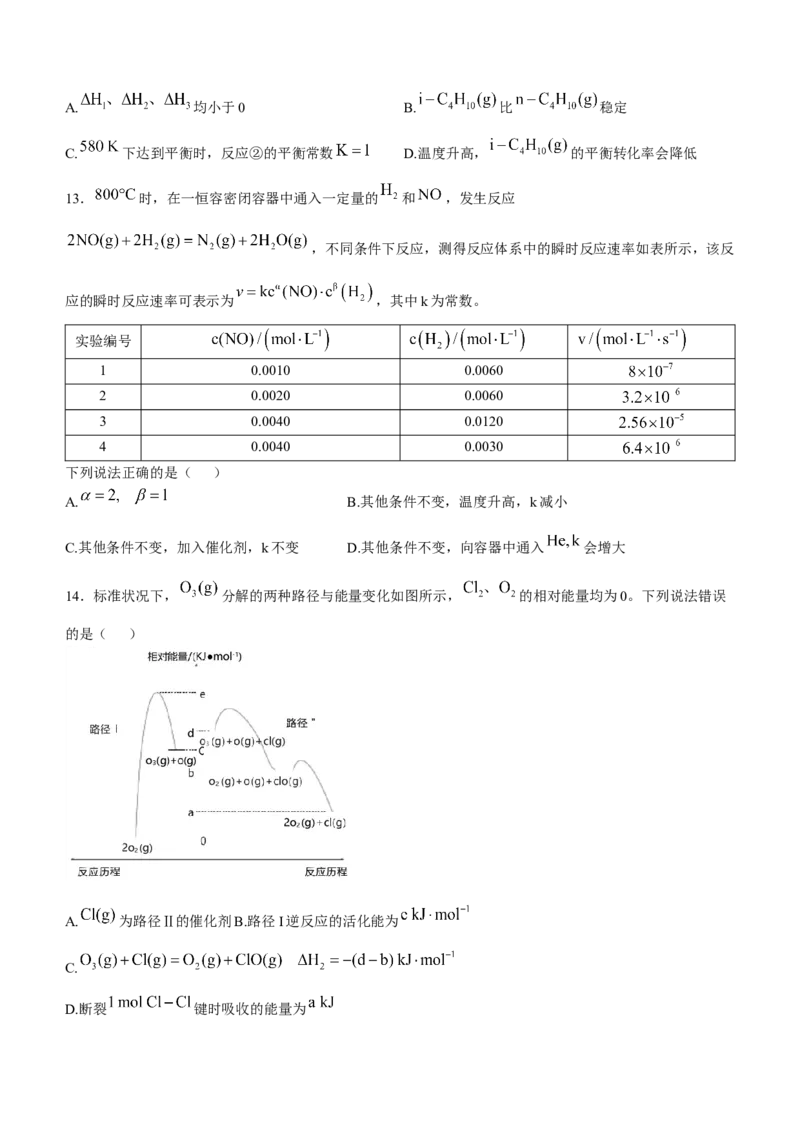
反应①②③的平衡常数随温度变化情况如图所示,下列说法正确的是( )A. 均小于0 B. 比 稳定
C. 下达到平衡时,反应②的平衡常数 D.温度升高, 的平衡转化率会降低
13. 时,在一恒容密闭容器中通入一定量的 和 ,发生反应
,不同条件下反应,测得反应体系中的瞬时反应速率如表所示,该反
应的瞬时反应速率可表示为 ,其中k为常数。
实验编号
1 0.0010 0.0060
2 0.0020 0.0060
3 0.0040 0.0120
4 0.0040 0.0030
下列说法正确的是( )
A. B.其他条件不变,温度升高,k减小
C.其他条件不变,加入催化剂,k不变 D.其他条件不变,向容器中通入 会增大
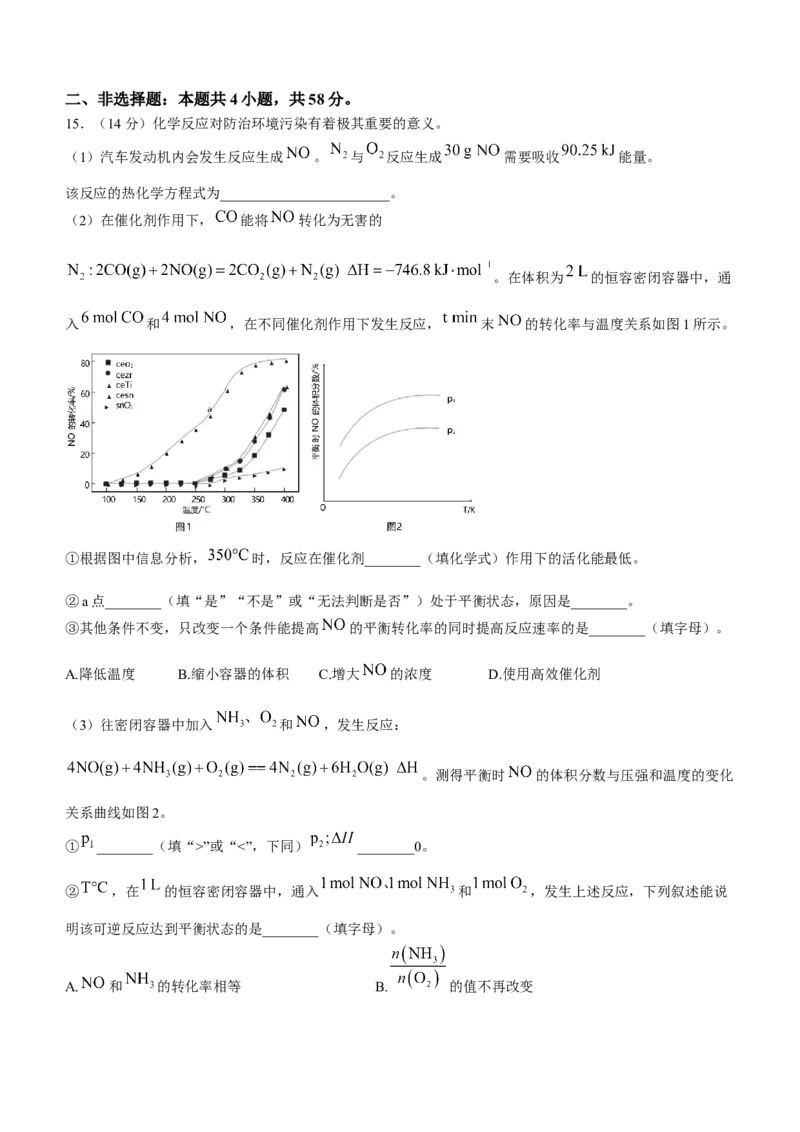
14.标准状况下, 分解的两种路径与能量变化如图所示, 的相对能量均为0。下列说法错误
的是( )
A. 为路径Ⅱ的催化剂B.路径I逆反应的活化能为
C.
D.断裂 键时吸收的能量为二、非选择题:本题共4小题,共58分。
15.(14分)化学反应对防治环境污染有着极其重要的意义。
(1)汽车发动机内会发生反应生成 。 与 反应生成 需要吸收 能量。
该反应的热化学方程式为________________________。
(2)在催化剂作用下, 能将 转化为无害的
。在体积为 的恒容密闭容器中,通
入 和 ,在不同催化剂作用下发生反应, 末 的转化率与温度关系如图1所示。
①根据图中信息分析, 时,反应在催化剂________(填化学式)作用下的活化能最低。
②a点________(填“是”“不是”或“无法判断是否”)处于平衡状态,原因是________。
③其他条件不变,只改变一个条件能提高 的平衡转化率的同时提高反应速率的是________(填字母)。
A.降低温度 B.缩小容器的体积 C.增大 的浓度 D.使用高效催化剂
(3)往密闭容器中加入 和 ,发生反应:
。测得平衡时 的体积分数与压强和温度的变化
关系曲线如图2。
① ________(填“>”或“<”,下同) ________0。
② ,在 的恒容密闭容器中,通入 和 ,发生上述反应,下列叙述能说
明该可逆反应达到平衡状态的是________(填字母)。
A. 和 的转化率相等 B. 的值不再改变C.消耗 的同时消耗 D.容器内总压强不再改变
16.(14分)化学是一门以实验为基础的学科。
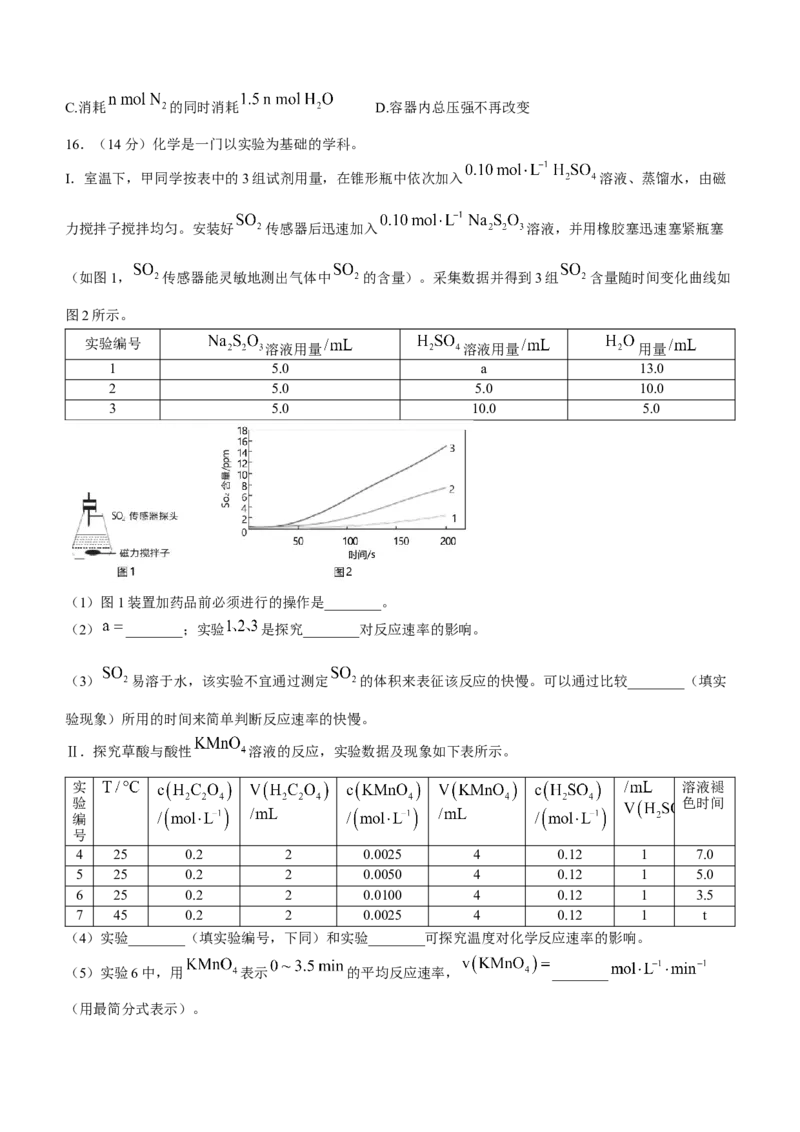
I.室温下,甲同学按表中的3组试剂用量,在锥形瓶中依次加入 溶液、蒸馏水,由磁
力搅拌子搅拌均匀。安装好 传感器后迅速加入 溶液,并用橡胶塞迅速塞紧瓶塞
(如图1, 传感器能灵敏地测出气体中 的含量)。采集数据并得到3组 含量随时间变化曲线如
图2所示。
实验编号
溶液用量 溶液用量 用量
1 5.0 a 13.0
2 5.0 5.0 10.0
3 5.0 10.0 5.0
(1)图1装置加药品前必须进行的操作是________。
(2) ________;实验 是探究________对反应速率的影响。
(3) 易溶于水,该实验不宜通过测定 的体积来表征该反应的快慢。可以通过比较________(填实
验现象)所用的时间来简单判断反应速率的快慢。
Ⅱ.探究草酸与酸性 溶液的反应,实验数据及现象如下表所示。
实 溶液褪
验 色时间
编
号
4 25 0.2 2 0.0025 4 0.12 1 7.0
5 25 0.2 2 0.0050 4 0.12 1 5.0
6 25 0.2 2 0.0100 4 0.12 1 3.5
7 45 0.2 2 0.0025 4 0.12 1 t
(4)实验________(填实验编号,下同)和实验________可探究温度对化学反应速率的影响。
(5)实验6中,用 表示 的平均反应速率, ________
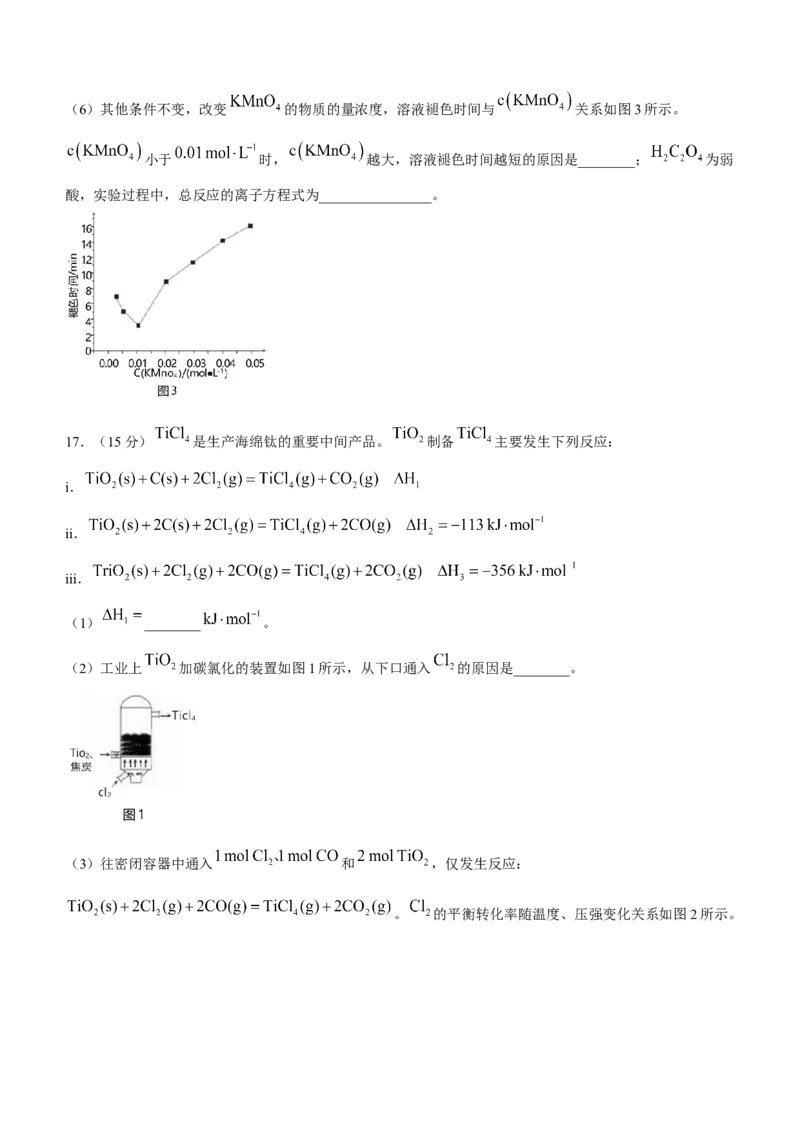
(用最简分式表示)。(6)其他条件不变,改变 的物质的量浓度,溶液褪色时间与 关系如图3所示。
小于 时, 越大,溶液褪色时间越短的原因是________; 为弱
酸,实验过程中,总反应的离子方程式为________________。
17.(15分) 是生产海绵钛的重要中间产品。 制备 主要发生下列反应:
i.
ii.
iii.
(1) ________ 。
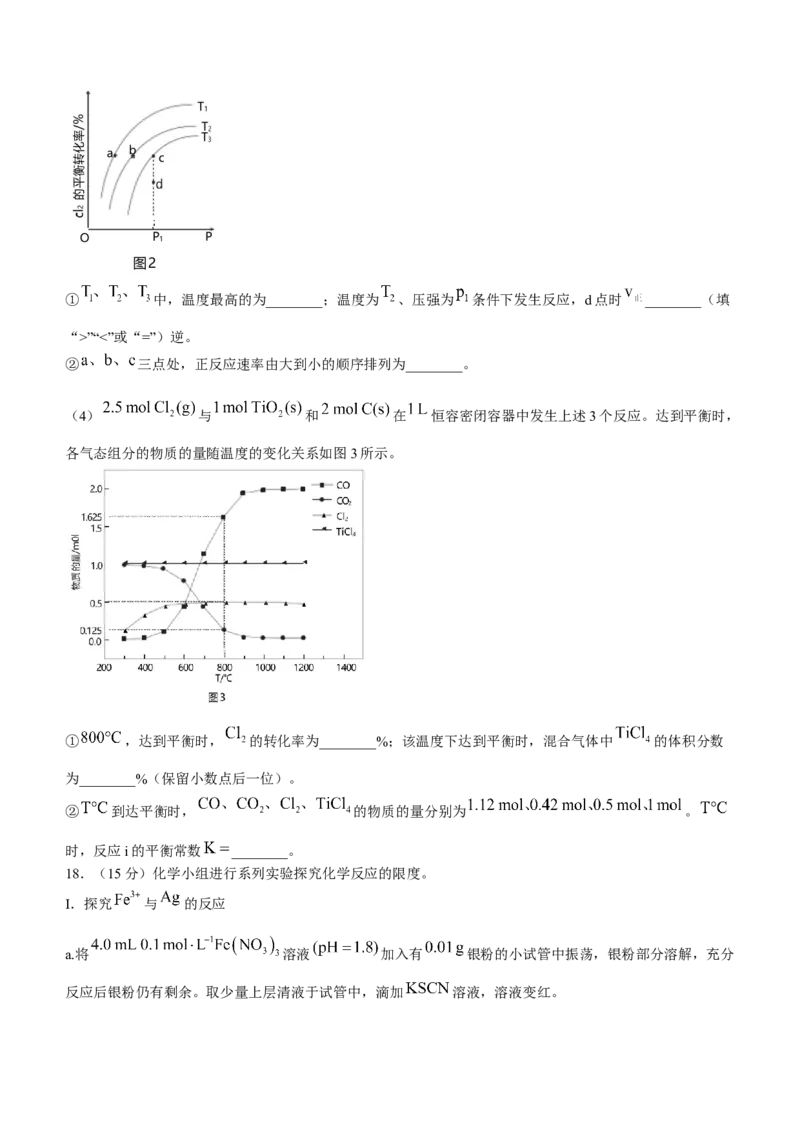
(2)工业上 加碳氯化的装置如图1所示,从下口通入 的原因是________。
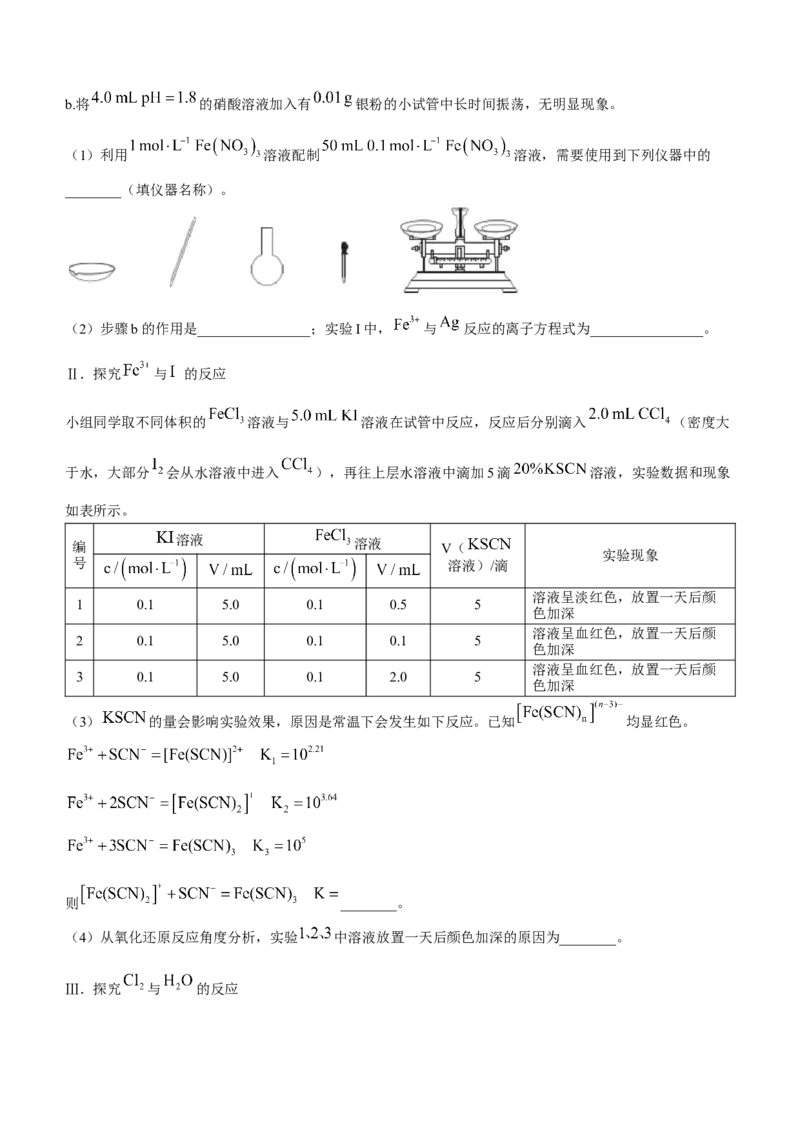
(3)往密闭容器中通入 和 ,仅发生反应:
。 的平衡转化率随温度、压强变化关系如图2所示。① 中,温度最高的为________;温度为 、压强为 条件下发生反应,d点时 ________(填
“>”“<”或“=”)逆。
② 三点处,正反应速率由大到小的顺序排列为________。
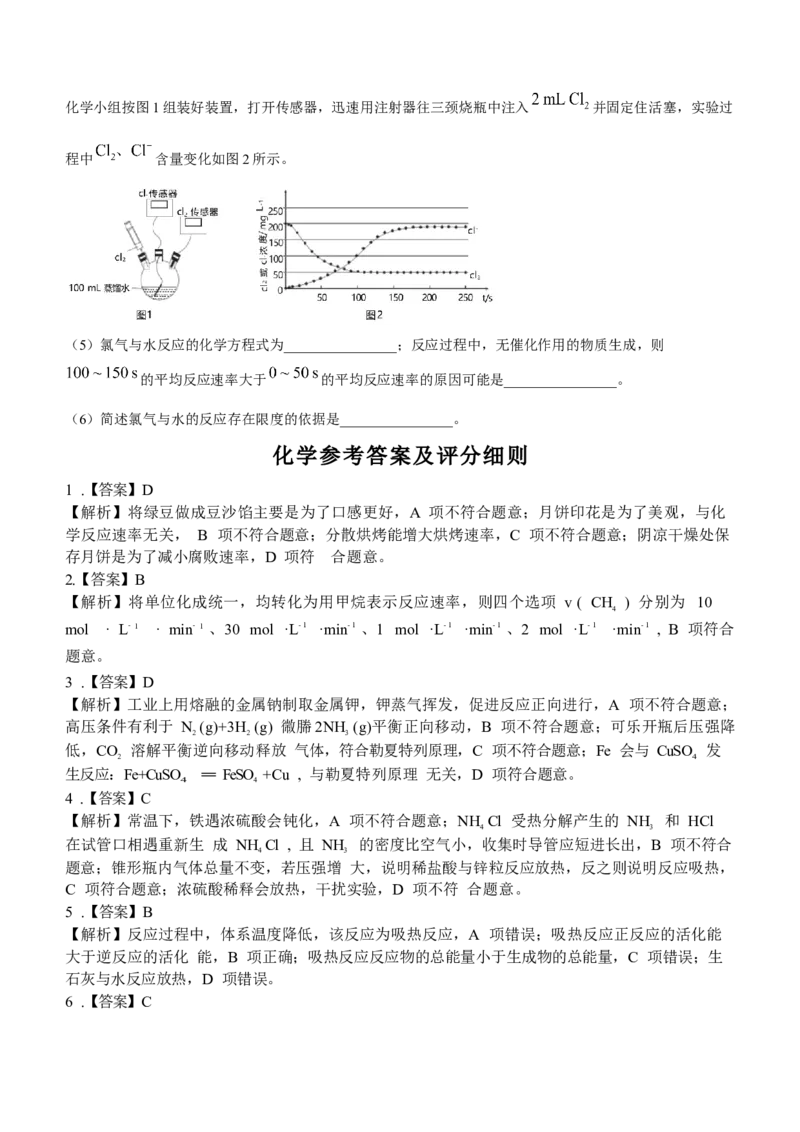
(4) 与 和 在 恒容密闭容器中发生上述3个反应。达到平衡时,
各气态组分的物质的量随温度的变化关系如图3所示。
① ,达到平衡时, 的转化率为________%;该温度下达到平衡时,混合气体中 的体积分数
为________%(保留小数点后一位)。
② 到达平衡时, 的物质的量分别为 。
时,反应i的平衡常数 ________。
18.(15分)化学小组进行系列实验探究化学反应的限度。
I.探究 与 的反应
a.将 溶液 加入有 银粉的小试管中振荡,银粉部分溶解,充分
反应后银粉仍有剩余。取少量上层清液于试管中,滴加 溶液,溶液变红。b.将 的硝酸溶液加入有 银粉的小试管中长时间振荡,无明显现象。
(1)利用 溶液配制 溶液,需要使用到下列仪器中的
________(填仪器名称)。
(2)步骤b的作用是________________;实验I中, 与 反应的离子方程式为________________。
Ⅱ.探究 与 的反应
小组同学取不同体积的 溶液与 溶液在试管中反应,反应后分别滴入 (密度大
于水,大部分 会从水溶液中进入 ),再往上层水溶液中滴加5滴 溶液,实验数据和现象
如表所示。
编 溶液 溶液 V(
实验现象
号 溶液)/滴
溶液呈淡红色,放置一天后颜
1 0.1 5.0 0.1 0.5 5
色加深
溶液呈血红色,放置一天后颜
2 0.1 5.0 0.1 0.1 5
色加深
溶液呈血红色,放置一天后颜
3 0.1 5.0 0.1 2.0 5
色加深
(3) 的量会影响实验效果,原因是常温下会发生如下反应。已知 均显红色。
则 ________。
(4)从氧化还原反应角度分析,实验 中溶液放置一天后颜色加深的原因为________。
Ⅲ.探究 与 的反应化学小组按图1组装好装置,打开传感器,迅速用注射器往三颈烧瓶中注入 并固定住活塞,实验过
程中 含量变化如图2所示。
(5)氯气与水反应的化学方程式为________________;反应过程中,无催化作用的物质生成,则
的平均反应速率大于 的平均反应速率的原因可能是________________。
(6)简述氯气与水的反应存在限度的依据是________________。
化学参考答案及评分细则
1 .【答案】D
【解析】将绿豆做成豆沙馅主要是为了口感更好,A 项不符合题意;月饼印花是为了美观,与化
学反应速率无关, B 项不符合题意;分散烘烤能增大烘烤速率,C 项不符合题意;阴凉干燥处保
存月饼是为了减小腐败速率,D 项符 合题意。
2.【答案】B
【解析】将单位化成统一,均转化为用甲烷表示反应速率,则四个选项 v ( CH ) 分别为 10
4
mol · L- 1 · min- 1 、30 mol ·L- 1 ·min- 1 、1 mol ·L- 1 ·min- 1 、2 mol ·L- 1 ·min- 1 , B 项符合
题意。
3 .【答案】D
【解析】工业上用熔融的金属钠制取金属钾,钾蒸气挥发,促进反应正向进行,A 项不符合题意;
高压条件有利于 N (g)+3H (g) 幑幐2NH (g)平衡正向移动,B 项不符合题意;可乐开瓶后压强降
2 2 3
低,CO 溶解平衡逆向移动释放 气体,符合勒夏特列原理,C 项不符合题意;Fe 会与 CuSO 发
2 4
生反应:Fe+CuSO = FeSO +Cu , 与勒夏特列原理 无关,D 项符合题意。
4 4
4 .【答案】C
【解析】常温下,铁遇浓硫酸会钝化,A 项不符合题意;NH Cl 受热分解产生的 NH 和 HCl
4 3
在试管口相遇重新生 成 NH Cl , 且 NH 的密度比空气小,收集时导管应短进长出,B 项不符合
4 3
题意;锥形瓶内气体总量不变,若压强增 大,说明稀盐酸与锌粒反应放热,反之则说明反应吸热,
C 项符合题意;浓硫酸稀释会放热,干扰实验,D 项不符 合题意。
5 .【答案】B
【解析】反应过程中,体系温度降低,该反应为吸热反应,A 项错误;吸热反应正反应的活化能
大于逆反应的活化 能,B 项正确;吸热反应反应物的总能量小于生成物的总能量,C 项错误;生
石灰与水反应放热,D 项错误。
6 .【答案】C【解析】该反应为可逆反应,不能进行到底,设充分反应后混合气体的物质的量为 n , 则 10
mol0 , i -C H (g)
1 2 3 1 4 10
能量更 低,更稳定,B 项正确;580 K 下到达平衡时,反应②的平衡常数 K= 10 , C 项错误;温度升高,反应
①②③的平衡 常数均增大,i -C H (g)的平衡转化率会增大,D 项错误。
4 10
13 .【答案】A
【解析】根据实验 1 、2 的数据可知 α= 2 , 根据 3 、4 的数据可知 β= 1 , A 项正确;其他条件不变,温度升高,
反应速 率加快,说明k 会随温度的升高而增大,B 项错误;其他条件不变,加入催化剂,反应速率加快,说明
k 会增大, C 项错误;其他条件不变,往容器中通入 He , 反应速率不改变,k 不发生改变,D 项错误。14 .【答案】D
【解析】Cl(g)参与了反应,改变了反应活化能,且最后又重新生成 Cl(g) , Cl(g) 为路径 Ⅱ 的催
化剂,A 项正确; 由图可知路径 Ⅰ逆反应的活化能为 e kJ ·mol- 1 , B 项正确;O (g)
3
+Cl(g)= O (g)+ClO(g)为放热过程,ΔH = - (d-b) kJ ·mol- 1 , C 项正确;Cl 的相对能量为 0
2 2 2
, Cl 的相对能量为(a-0) kJ ·mol- 1 , 故断裂 1 mol Cl—Cl 键时 吸收的能量为 2a kJ , D 项错误。
15 .【答案】(1)N (g)+O (g)= 2NO(g) ΔH= +180 . 5 kJ ·mol- 1(或其他合理答案,2 分,方程
2 2
式 1 分,焓变 1 分)
(2) ①CeSn(2 分)
②不是(2 分) 该反应为放热反应,温度升高,平衡转化率会下降,与图中 a 点后的趋势相反(2 分,合理表
述即可)
③B(2 分)
(3) ①> ( 1 分) < ( 1 分) ②BD(2 分,1 个 1 分,多选或错选不给分)
【解析】(1)N 与 O 反应生成 1 mol NO 需要吸收 90. 25 kJ 能量,则生成 2 mol NO 需要吸收
2 2
180. 5 kJ 能量,热 化学方程式为 N (g)+O (g) = 2NO(g) ΔH= +180 . 5 kJ ·mol- 1 。
2 2
(2) ①350 ℃ 时,t min 末,在 CeSn 催化作用下 NO 的转化率最高,反应速率最快,活化能最小。②2CO( g)
+ 2NO(g) 幑幐2CO (g)+N (g) 为放热反应,若 a 点处于平衡状态,则温度升高,NO 的转化率会下降,与图像
2 2
不 符,故 a 点不是处于平衡状态。③降低温度,反应速率减慢,A 项不符合题意;缩小容器的体积,平衡正向
移动 且反应速率加快,B 项符合题意;增大 NO 的浓度,NO 的平衡转化率下降,C 项不符合题意;使用高效
催化剂不 能提高 NO 的平衡转化率,D 项不符合题意。
(3) ①其他条件不变,压强增大,4NO(g)+4NH (g)+O (g) ==4N (g)+ 6H O(g) 平衡会逆向移动,NO 平衡转 化
3 2 2 2
率降低,NO 的含量增加,故 p >p ;根据图像信息可知,其他条件不变,温度升高,平衡时 NO 的体积分数增
1 2
大,则 NO 平衡转化率降低,故该反应为放热反应,ΔH<0 。②NO 和 NH 的投料比等于化学计量数之比,无论
3
反 应是否达到平衡状态,二者的转化率始终相等,A 项错误;反应未达到平衡状态时, 的值会发生改
变,当 的值不再改变时,可说明反应达到平衡状态,B 项正确;无论反应是否达到平衡,消耗 n mol
N 的同时 消耗 1 . 5n mol H O , C 项错误;该反应为气体分子数变化的反应,故容器内总压强不再改变时,
2 2
能说明反应达到 平衡状态,D 项正确。
16 .【答案】(1)检查装置气密性( 1 分,合理即可)
(2)2 . 0( 1 分,写 2 不扣分) H +(或反应物)浓度(2 分)
(3)溶液出现浑浊(2 分,类似表述均可)
(4)4( 1 分) 7( 1 分,顺序不限)
(5) (2 分,未化成最简式扣 1 分)(6)c(KMnO )越大,反应速率越大( 1 分),参与反应的 n(KMnO ) 增大不能抵消反应速率增大带
4 4
来的影响,总 反应时长减小( 1 分) (2 分,
物质错误、未配平不得分,未写 “↑ ”不扣分)
【解析】(1)加药品前必须进行的操作是检查装置气密性,确保装置气密性良好。
(2)根据控制变量的思维可知实验时,3 组实验溶液总体积需相同,故 a= 2 . 0;该组实验是探究反应物浓度对反
应速率的影响。
(3)反应生成了淡黄色的 S , 可以通过比较溶液出现浑浊所用的时间来简单判断反应速率的快慢。
(4)根据控制变量的思维可知实验 4 和实验 7 可探究温度对化学反应速率的影响。
(5) 。
(6)c(KMnO )小于 0. 01 mol ·L- 1 时,c(KMnO )越大,反应速率的增大程度大于 n(KMnO ) 增大程度,反
4 4 4
应时 长减小;c(KMnO )大于 0. 01 mol ·L- 1 时,c(KMnO ) 越大,反应速率的增大程度小于 n( KMnO )
4 4 4
增大程度,反 应时长增加;反应的离子方程式为 。
17 .【答案】(1) - 234 . 5(2 分,没写“-”号不给分)
(2)增大原料之间的接触面积( 1 分),加快反应速率,提高原料利用率( 1 分)
(3) ①T (2 分) >( 1 分)
3
②c>b>a(2 分,顺序正确即可)
(4) ①80(2 分) 30. 8(2 分)
②1 . 68(2 分)
【解析】(1)根据盖斯定律可知 ΔH = ( ΔH + ΔH ) = - 234 . 5 kJ ·mol- 1 。
1 2 3
(2)从下口通入 Cl 能增大氯气与 TiO 和焦炭的接触面积,能加快反应速率,提高原料利用率。
2 2
(3) ①TiO (s)+2Cl (g)+2CO(g) 幑幐TiCl (g)+2CO (g)为放热反应,其他条件相同,温度越高,Cl 的平衡转化
2 2 4 2 2
率越低,故温度最高的为 T ;d 点时,转化率小于平衡转化率,反应正向进行,v >v 。②温度越高、压强越大,
3 正 逆
反 应速率越快,故正反应速率:c>b>a 。
(4) ①800 ℃ , 到达平衡时,Cl 的转化率为 ;该温度下到达平衡时,混
2
合气体中 TiCl 的体积分数为 。②平衡时,c( Cl )
4 2
= 0. 5 mol · L- 1 、 c(TiCl ) = 1 mol · L- 1 、c ( CO ) = 0. 42 mol · L- 1 , 反 应 i 的 平
4 2
衡 常 数。
18 .【答案】(1)玻璃棒、胶头滴管(2 分,1 个 1 分)
(2)排除 在 pH = 1 . 8 时与银粉反应对实验的影响(2 分,类似表述即可) Fe3+ +Ag 幑幐Fe2+
+Ag+ (2 分,物 质错误、未配平不得分,“幑幐”写成“= ”扣 1 分)
(3)10 1 . 36 (2 分)
(4)部分 Fe2+ 被空气氧化为 Fe3+ (2 分,类似表述即可)
(5)Cl +H O 幑幐HCl+HClO(2 分,物质错误、未配平不得分,“幑幐 ”写成“= ”扣 1 分)
2 2
氯气与水的反应为 放热反应( 1 分,合理表述即可)
(6)200 s 后 Cl 和 Cl- 同时存在且含量不再发生改变(2 分,1 点 1 分)
2
【解析】(1)利用 1 mol ·L- 1 Fe(NO ) 溶液配制 50 mL 0. 1 mol · L- 1 Fe( NO ) 溶液,需使用量筒、烧
3 3 3 3
杯、玻璃 棒、50 mL 容量瓶、胶头滴管等仪器。
(2)0 . 1 mol ·L- 1 Fe(NO ) 溶液的 pH = 1 . 8 , 在酸性条件下具有强氧化性,可能会与银粉反应干扰实验;
3 3
实 验 a 中,银粉部分反应,最后 Fe3+ 和银粉均有剩余,说明发生了可逆反应:Fe3+ +Ag 幑幐Fe2+ +Ag+ 。
(3)根据盖斯定律可知[Fe(SCN) ] + +SCN- 幑幐Fe(SCN) 。
2 3
(4)溶液放置过程中,部分 Fe2+ 被空气中的 O 氧化为 Fe3+ , Fe3+ 与 SCN- 反应使溶液颜色加深。
2
(5)Cl 与 H O 发生可逆反应生成 HCl 和 HClO , 反应的化学方程式为 Cl +H O 幑幐HCl+HClO;氯气与水的
2 2 2 2
反 应为放热反应,温度升高,导致 100 ~ 150 s 的平均反应速率大于 0 ~ 50 s 的平均反应速率。