文档内容
高二10月月考化学试题
考试时间 75分钟 总分 100分
相对原子质量 H 1 C 12 Na 23 O 16
一、单选题(共14题,每题3分,共42分)
1.化学与生产、生活及社会发展密切相关,下列叙述正确的是( )
A.免洗洗手液的有效成分之一活性银离子能使病毒蛋白质变性
B.“酒曲”的酿酒工艺是利用催化剂使平衡正向移动的原理
C.华为5G手机麒麟9000芯片主要成分是二氧化硅
D.古法炼丹云:“丹砂(HgS)烧之成水银,积变(常温混合)又还原成丹砂”,二者为可逆反应
2.列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
选项 A B C D
强电解质 Fe NaCl
弱电解质 CO
2
非电解质 (蔗糖)
3.下列事实不能用勒夏特列原理解释的是 ( )
A.实验室收集氯气时,常用排饱和食盐水的方法
B.测量NO 的相对分子质量时应选择压强较低的环境更准确
2
C.工业合成氨适宜选择高温高压的反应条件
D.常温下,将 的醋酸溶液加水稀释到 ,测得其
4.下列说法正确的是( )
A.已知2K(s)+2HO(l)===2KOH(aq)+H(g) ΔH,2Na(s)+2HO(l)===2NaOH(aq)+H(g)
2 2 1 2 2
ΔH,则ΔH>ΔH
2 1 2
B.已知:金刚石(s)=石墨(s) ΔH<0,则该条件下石墨比金刚石稳定
C.已知中和热为57.3kJ•mol-1,则稀氨水与盐酸反应生成1mol水时放出的热量大于57.3kJ
D.已知:2C H(g)+6O(g)=4CO (g)+4HO(l) ΔH=-3200.8kJ•mol-1,则C H(g)的燃烧热
2 4 2 2 2 2 4ΔH=-3200.8kJ•mol-1
5. 为阿伏加德罗常数的值。下列说法正确的是 ( )
A. 溶于水,溶液中 的数目为
B.常温下, 的 溶液中氢离子数目为0.1N
A
C.若某溶液的 ,则由水电离出的氢离子数目为
D. 溶液中, 分子的数目为
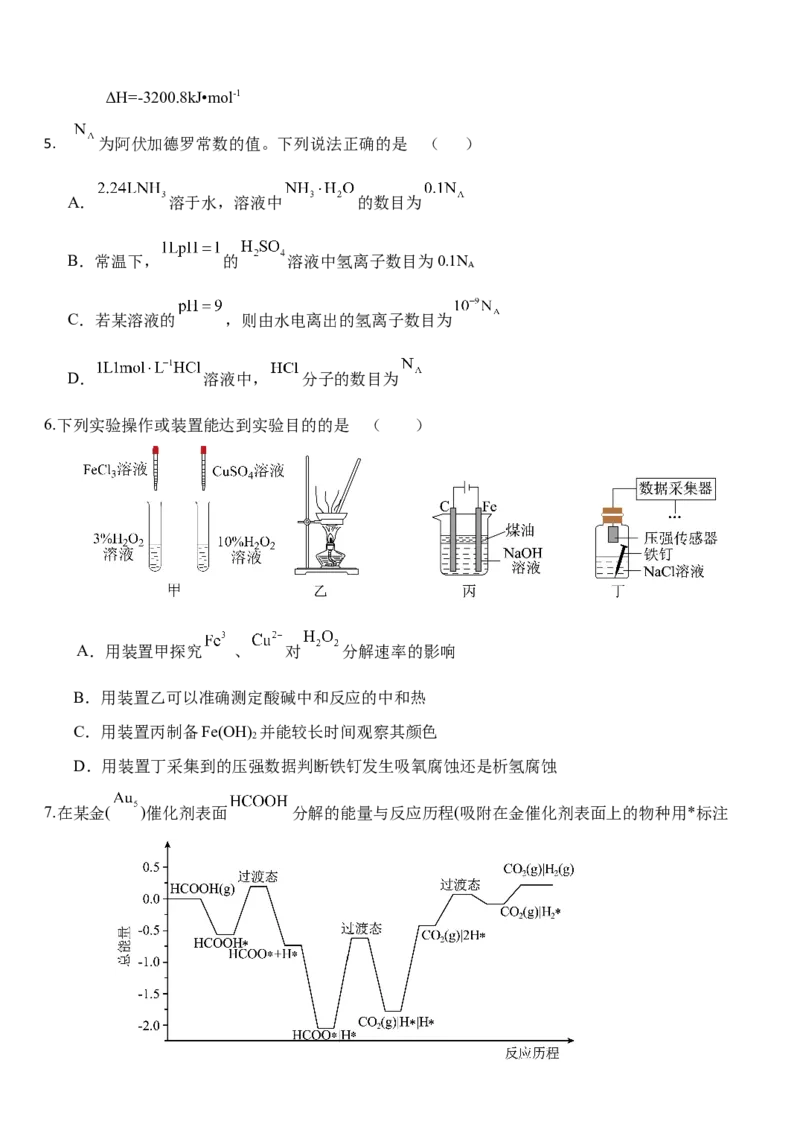
6.下列实验操作或装置能达到实验目的的是 ( )
A.用装置甲探究 、 对 分解速率的影响
B.用装置乙可以准确测定酸碱中和反应的中和热
C.用装置丙制备Fe(OH) 并能较长时间观察其颜色
2
D.用装置丁采集到的压强数据判断铁钉发生吸氧腐蚀还是析氢腐蚀
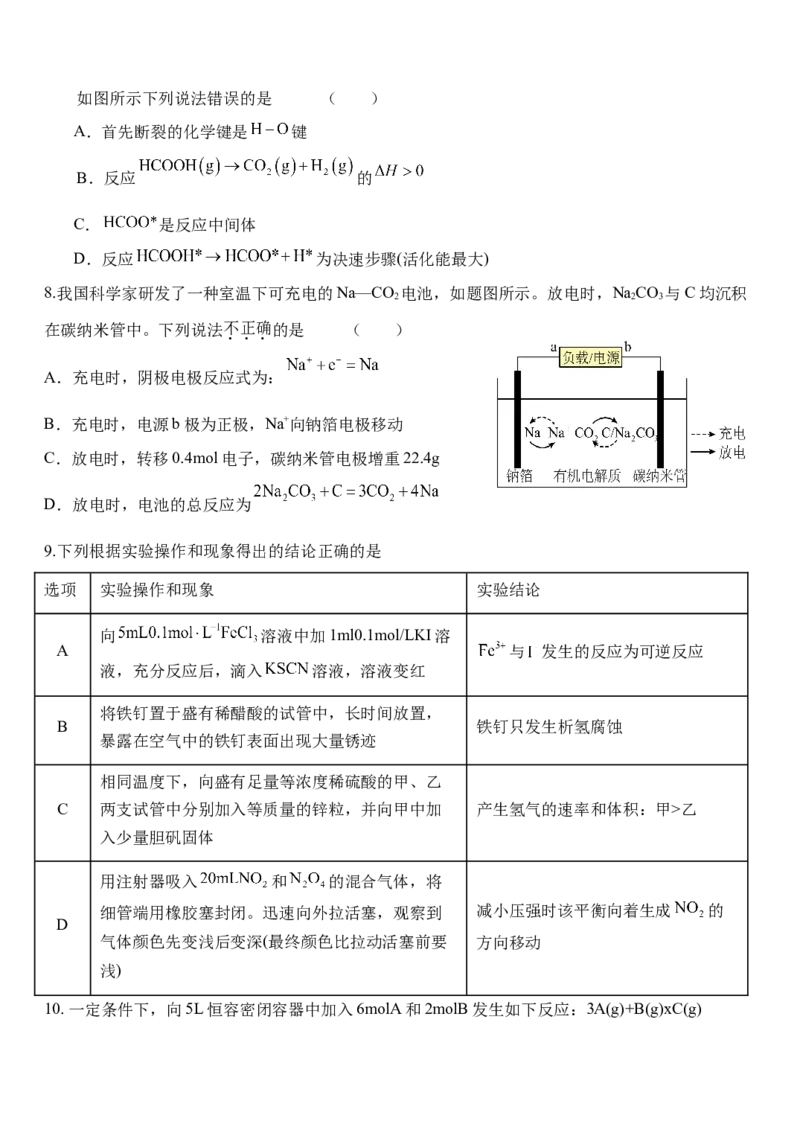
7.在某金( )催化剂表面 分解的能量与反应历程(吸附在金催化剂表面上的物种用*标注如图所示下列说法错误的是 ( )
A.首先断裂的化学键是 键
B.反应 的
C. 是反应中间体
D.反应 为决速步骤(活化能最大)
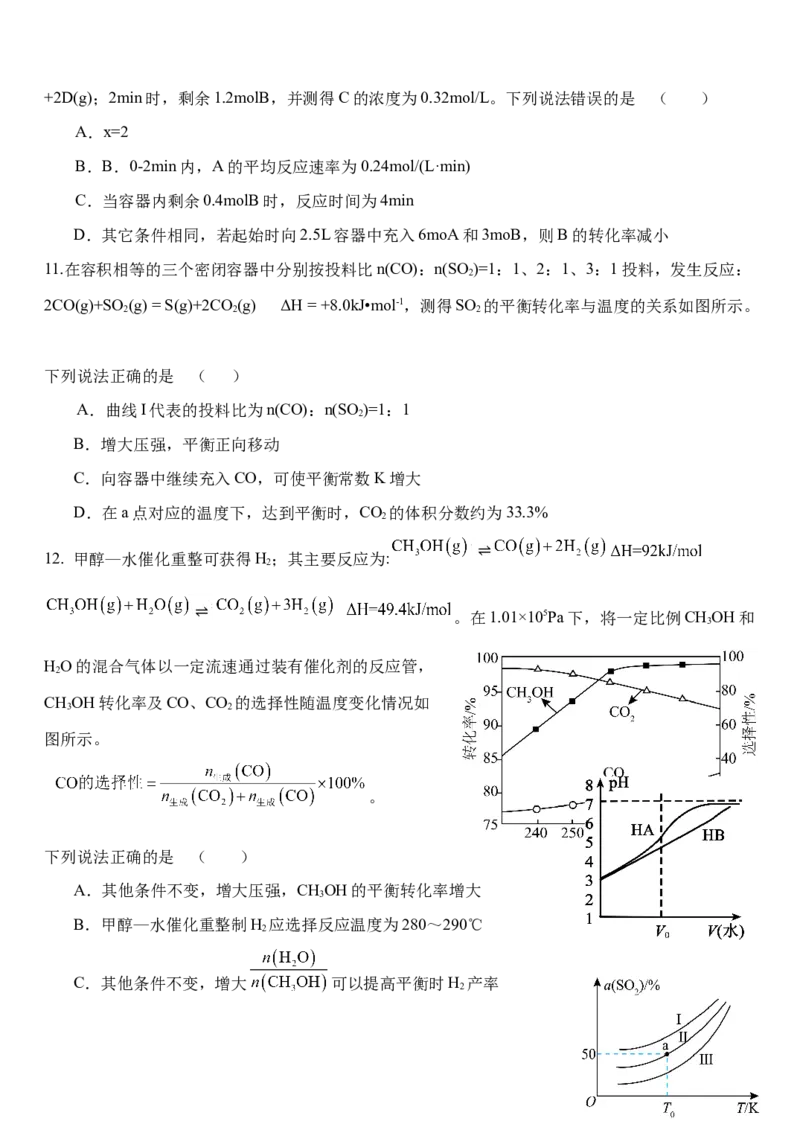
8.我国科学家研发了一种室温下可充电的Na—CO 电池,如题图所示。放电时,NaCO 与C均沉积
2 2 3
在碳纳米管中。下列说法不正确的是 ( )
A.充电时,阴极电极反应式为:
B.充电时,电源b极为正极,Na+向钠箔电极移动
C.放电时,转移0.4mol电子,碳纳米管电极增重22.4g
D.放电时,电池的总反应为
9.下列根据实验操作和现象得出的结论正确的是
选项 实验操作和现象 实验结论
向 溶液中加1ml0.1mol/LKI溶
A 与 发生的反应为可逆反应
液,充分反应后,滴入 溶液,溶液变红
将铁钉置于盛有稀醋酸的试管中,长时间放置,
B 铁钉只发生析氢腐蚀
暴露在空气中的铁钉表面出现大量锈迹
相同温度下,向盛有足量等浓度稀硫酸的甲、乙
C 两支试管中分别加入等质量的锌粒,并向甲中加 产生氢气的速率和体积:甲>乙
入少量胆矾固体
用注射器吸入 和 的混合气体,将
细管端用橡胶塞封闭。迅速向外拉活塞,观察到 减小压强时该平衡向着生成 的
D
气体颜色先变浅后变深(最终颜色比拉动活塞前要 方向移动
浅)
10.一定条件下,向5L恒容密闭容器中加入6molA和2molB发生如下反应:3A(g)+B(g)xC(g)+2D(g);2min时,剩余1.2molB,并测得C的浓度为0.32mol/L。下列说法错误的是 ( )
A.x=2
B.B.0-2min内,A的平均反应速率为0.24mol/(L·min)
C.当容器内剩余0.4molB时,反应时间为4min
D.其它条件相同,若起始时向2.5L容器中充入6moA和3moB,则B的转化率减小
11.在容积相等的三个密闭容器中分别按投料比n(CO):n(SO )=1:1、2:1、3:1投料,发生反应:
2
2CO(g)+SO (g) = S(g)+2CO (g) ΔH= +8.0kJ•mol-1,测得SO 的平衡转化率与温度的关系如图所示。
2 2 2
下列说法正确的是 ( )
A.曲线I代表的投料比为n(CO):n(SO )=1:1
2
B.增大压强,平衡正向移动
C.向容器中继续充入CO,可使平衡常数K增大
D.在a点对应的温度下,达到平衡时,CO 的体积分数约为33.3%
2
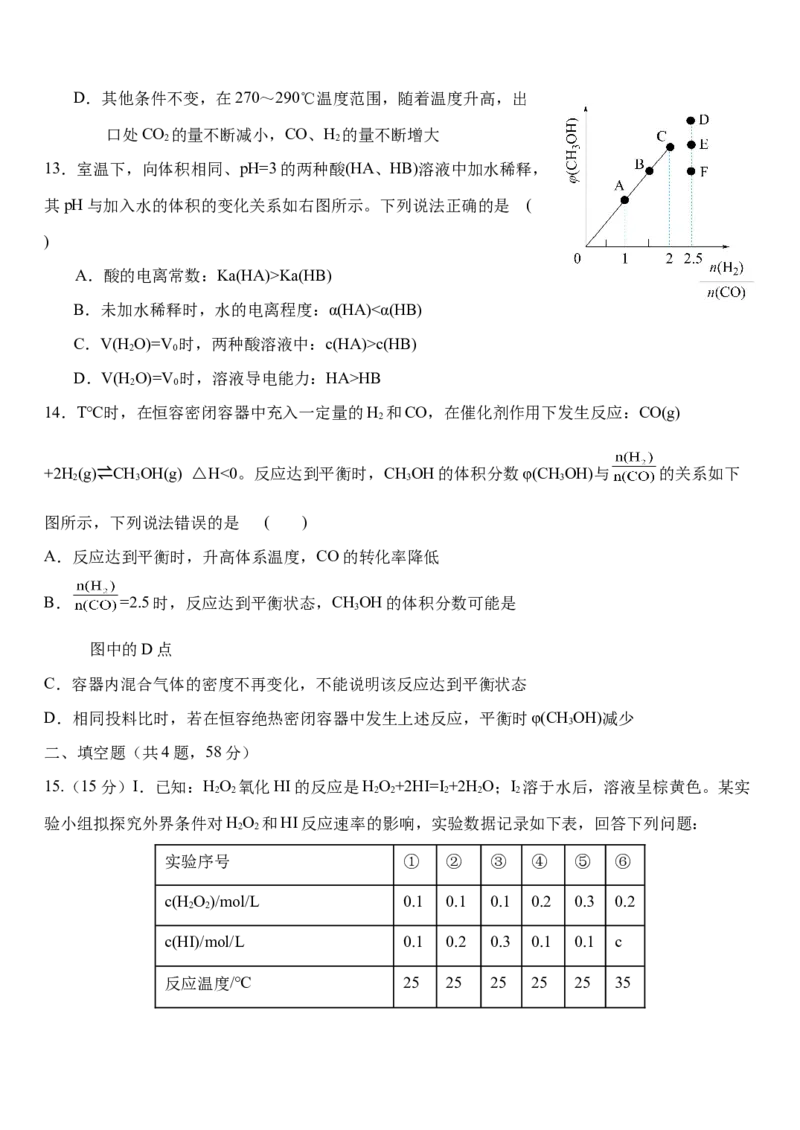
12. 甲醇—水催化重整可获得H;其主要反应为:
2
⇌
。在1.01×105Pa下,将一定比例CHOH和
3
⇌
HO的混合气体以一定流速通过装有催化剂的反应管,
2
CHOH转化率及CO、CO 的选择性随温度变化情况如
3 2
图所示。
。
下列说法正确的是 ( )
A.其他条件不变,增大压强,CHOH的平衡转化率增大
3
B.甲醇—水催化重整制H 应选择反应温度为280~290℃
2
C.其他条件不变,增大 可以提高平衡时H 产率
2D.其他条件不变,在270~290℃温度范围,随着温度升高,出
口处CO 的量不断减小,CO、H 的量不断增大
2 2
13.室温下,向体积相同、pH=3的两种酸(HA、HB)溶液中加水稀释,
其pH与加入水的体积的变化关系如右图所示。下列说法正确的是 (
)
A.酸的电离常数:Ka(HA)>Ka(HB)
B.未加水稀释时,水的电离程度:α(HA)<α(HB)
C.V(H O)=V 时,两种酸溶液中:c(HA)>c(HB)
2 0
D.V(H O)=V 时,溶液导电能力:HA>HB
2 0
14.T℃时,在恒容密闭容器中充入一定量的H 和CO,在催化剂作用下发生反应:CO(g)
2
+2H (g)⇌CH OH(g) △H<0。反应达到平衡时,CHOH的体积分数φ(CHOH)与 的关系如下
2 3 3 3
图所示,下列说法错误的是 ( )
A.反应达到平衡时,升高体系温度,CO的转化率降低
B. =2.5时,反应达到平衡状态,CHOH的体积分数可能是
3
图中的D点
C.容器内混合气体的密度不再变化,不能说明该反应达到平衡状态
D.相同投料比时,若在恒容绝热密闭容器中发生上述反应,平衡时φ(CHOH)减少
3
二、填空题(共4题,58分)
15.(15分)I.已知:HO 氧化HI的反应是HO+2HI=I +2H O;I 溶于水后,溶液呈棕黄色。某实
2 2 2 2 2 2 2
验小组拟探究外界条件对HO 和HI反应速率的影响,实验数据记录如下表,回答下列问题:
2 2
实验序号 ① ② ③ ④ ⑤ ⑥
c(HO)/mol/L 0.1 0.1 0.1 0.2 0.3 0.2
2 2
c(HI)/mol/L 0.1 0.2 0.3 0.1 0.1 c
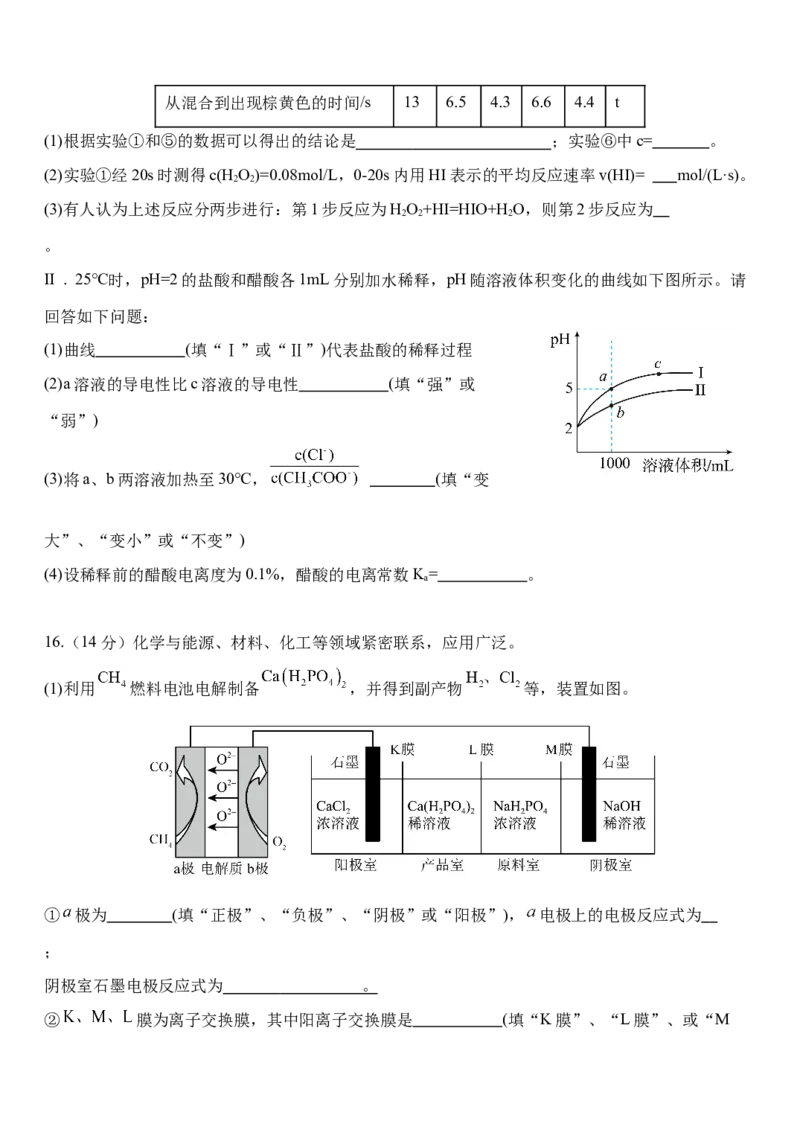
反应温度/℃ 25 25 25 25 25 35从混合到出现棕黄色的时间/s 13 6.5 4.3 6.6 4.4 t
(1)根据实验①和⑤的数据可以得出的结论是 ;实验⑥中c= 。
(2)实验①经20s时测得c(HO)=0.08mol/L,0-20s内用HI表示的平均反应速率v(HI)= mol/(L·s)。
2 2
(3)有人认为上述反应分两步进行:第1步反应为HO+HI=HIO+HO,则第2步反应为
2 2 2
。
II . 25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。请
回答如下问题:
(1)曲线 (填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程
(2)a溶液的导电性比c溶液的导电性 (填“强”或
“弱”)
(3)将a、b两溶液加热至30℃, (填“变
大”、“变小”或“不变”)
(4)设稀释前的醋酸电离度为0.1%,醋酸的电离常数K= 。
a
16.(14分)化学与能源、材料、化工等领域紧密联系,应用广泛。
(1)利用 燃料电池电解制备 ,并得到副产物 等,装置如图。
① 极为 (填“正极”、“负极”、“阴极”或“阳极”), 电极上的电极反应式为
;
阴极室石墨电极反应式为 。
② 膜为离子交换膜,其中阳离子交换膜是 (填“K膜”、“L膜”、或“M膜”)
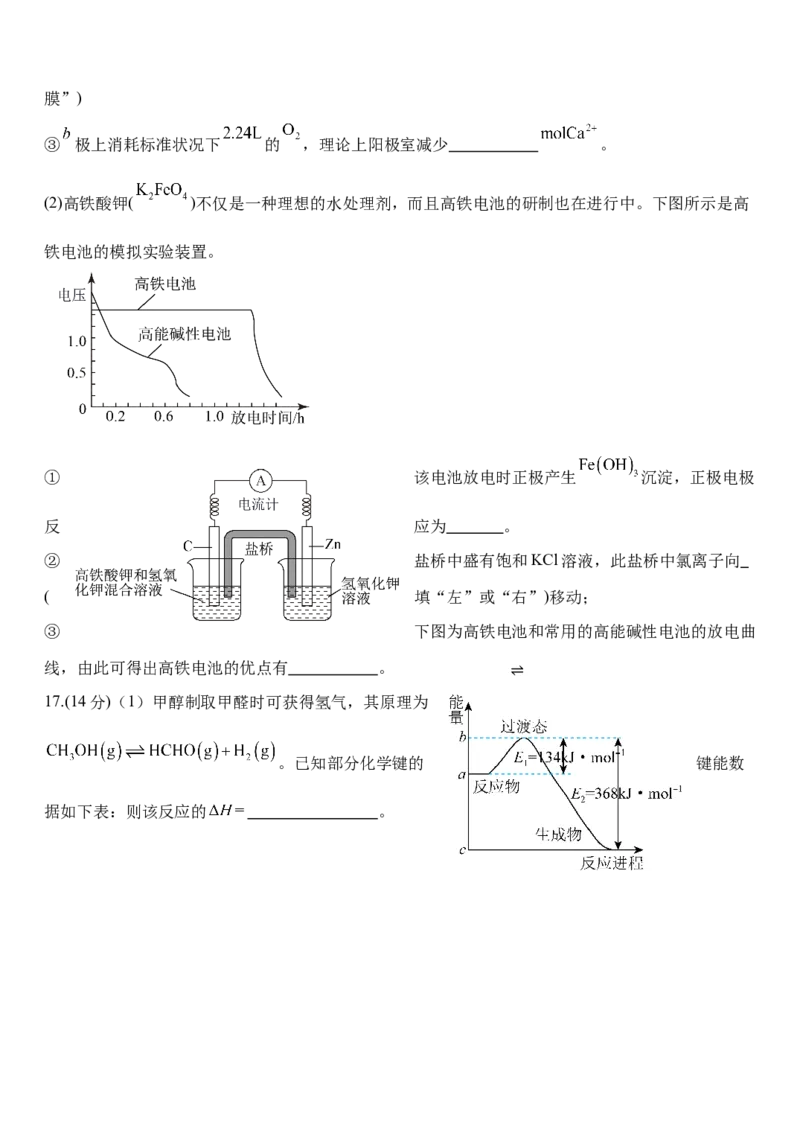
③ 极上消耗标准状况下 的 ,理论上阳极室减少 。
(2)高铁酸钾( )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高
铁电池的模拟实验装置。
① 该电池放电时正极产生 沉淀,正极电极
反 应为 。
② 盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
( 填“左”或“右”)移动;
③ 下图为高铁电池和常用的高能碱性电池的放电曲
线,由此可得出高铁电池的优点有 。
17.(14分)(1)甲醇制取甲醛时可获得氢气,其原理为
⇌
。已知部分化学键的 键能数
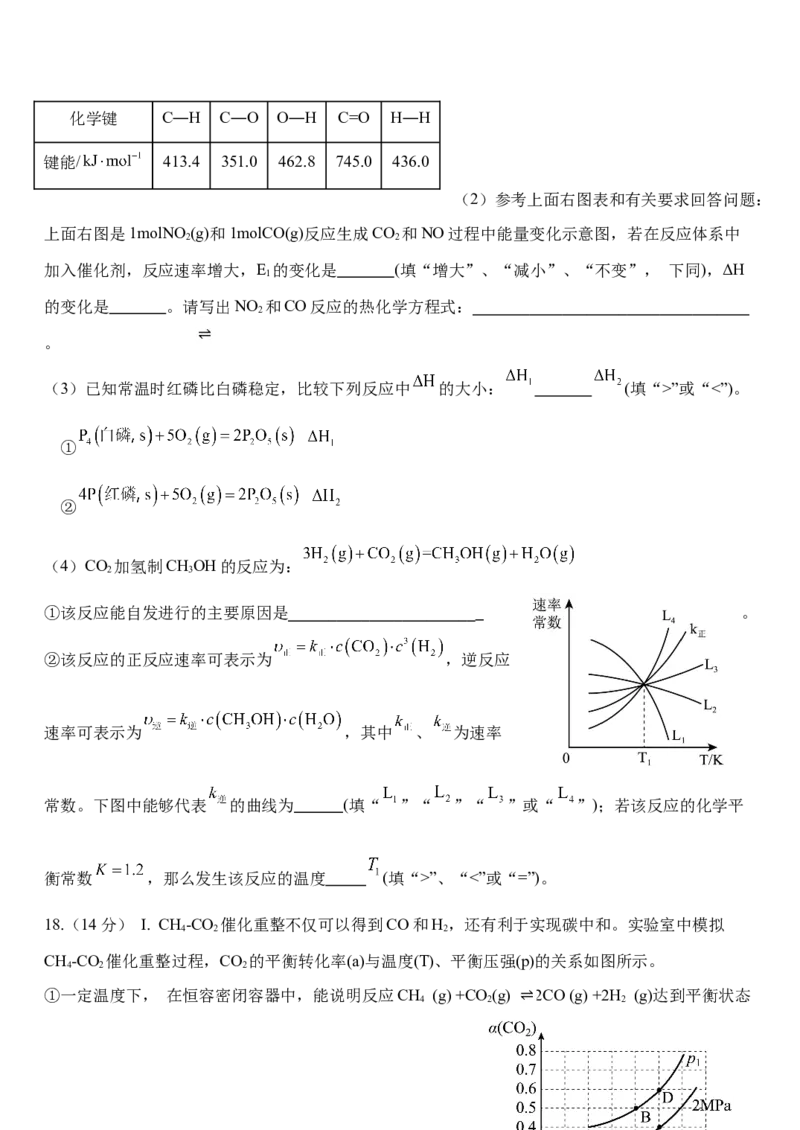
据如下表:则该反应的 。化学键 C―H C―O O―H C=O H―H
键能/ 413.4 351.0 462.8 745.0 436.0
(2)参考上面右图表和有关要求回答问题:
上面右图是1molNO (g)和1molCO(g)反应生成CO 和NO过程中能量变化示意图,若在反应体系中
2 2
加入催化剂,反应速率增大,E 的变化是 (填“增大”、“减小”、“不变”, 下同),ΔH
1
的变化是 。请写出NO 和CO反应的热化学方程式:
2
。
⇌
(3)已知常温时红磷比白磷稳定,比较下列反应中 的大小: (填“>”或“<”)。
①
②
(4)CO 加氢制CHOH的反应为:
2 3
①该反应能自发进行的主要原因是 。
②该反应的正反应速率可表示为 ,逆反应
速率可表示为 ,其中 、 为速率
常数。下图中能够代表 的曲线为 (填“ ”“ ”“ ”或“ ”);若该反应的化学平
衡常数 ,那么发生该反应的温度 (填“>”、“<”或“=”)。
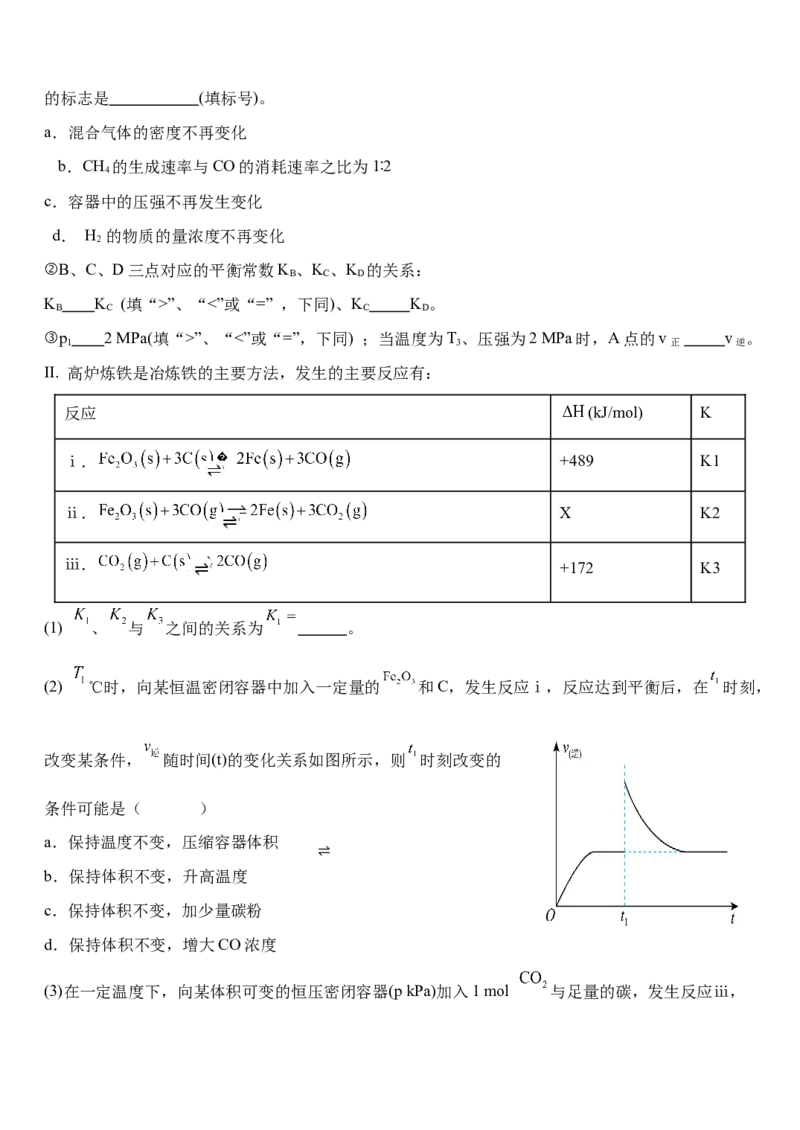
18.(14分) I. CH-CO 催化重整不仅可以得到CO和H,还有利于实现碳中和。实验室中模拟
4 2 2
CH-CO 催化重整过程,CO 的平衡转化率(a)与温度(T)、平衡压强(p)的关系如图所示。
4 2 2
①一定温度下, 在恒容密闭容器中,能说明反应CH (g) +CO (g) 2CO (g) +2H (g)达到平衡状态
4 2 2
⇌的标志是 (填标号)。
a.混合气体的密度不再变化
b.CH 的生成速率与CO的消耗速率之比为1∶2
4
c.容器中的压强不再发生变化
d. H 的物质的量浓度不再变化
2
②B、C、D三点对应的平衡常数K 、K 、K 的关系:
B C D
K K (填“>”、“<”或“=” ,下同)、K K 。
B C C D
③p 2 MPa(填“>”、“<”或“=”,下同) ;当温度为T、压强为2 MPa时,A点的v v 。
1 3 正 逆
II. 高炉炼铁是冶炼铁的主要方法,发生的主要反应有:
反应 (kJ/mol) K
ⅰ. +489 K1
ⅱ. X K2
ⅲ. +172 K3
(1) 、 与 之间的关系为 。
(2) ℃时,向某恒温密闭容器中加入一定量的 和C,发生反应ⅰ,反应达到平衡后,在 时刻,
改变某条件, 随时间(t)的变化关系如图所示,则 时刻改变的
条件可能是( )
a.保持温度不变,压缩容器体积
b.保持体积不变,升高温度
⇌
c.保持体积不变,加少量碳粉
d.保持体积不变,增大CO浓度
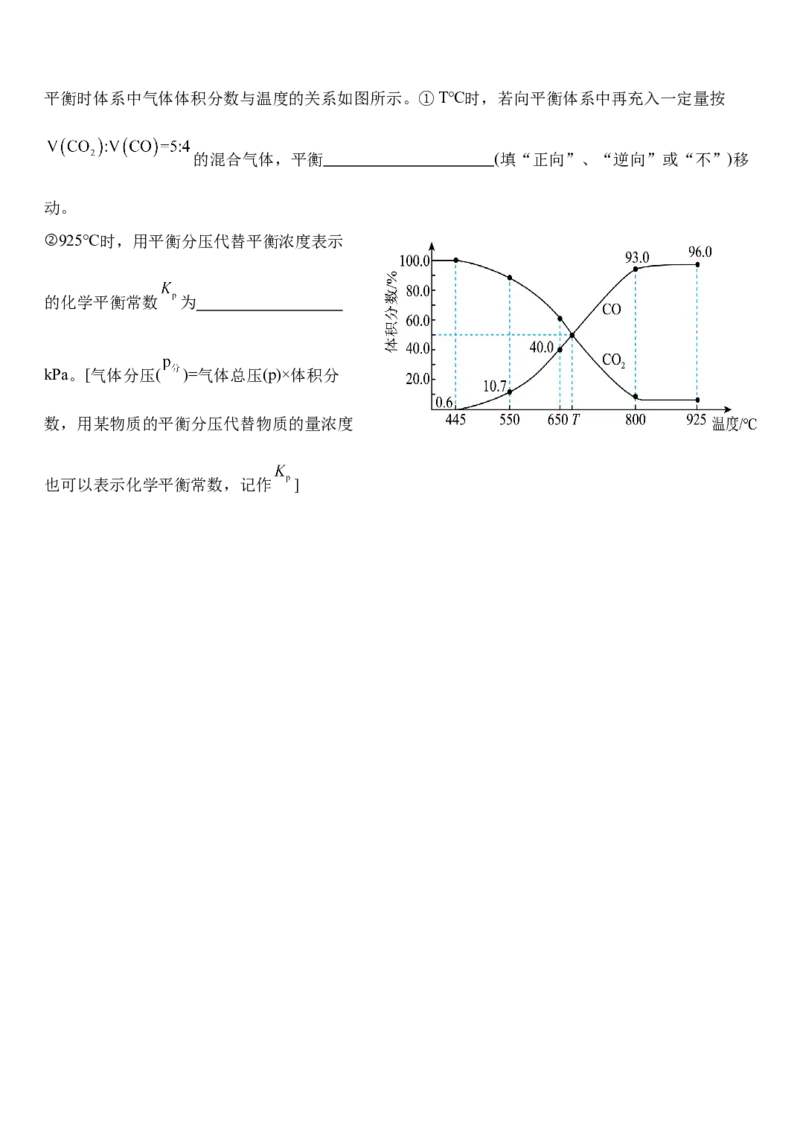
(3)在一定温度下,向某体积可变的恒压密闭容器(p kPa)加入1 mol 与足量的碳,发生反应ⅲ,平衡时体系中气体体积分数与温度的关系如图所示。①T℃时,若向平衡体系中再充入一定量按
的混合气体,平衡 (填“正向”、“逆向”或“不”)移
动。
②925℃时,用平衡分压代替平衡浓度表示
的化学平衡常数 为
kPa。[气体分压( )=气体总压(p)×体积分
数,用某物质的平衡分压代替物质的量浓度
也可以表示化学平衡常数,记作 ]题号 1 2 3 4 5 6 7 8 9 10
答案 A C C B B D D D D C
题号 11 12 13 14
答案 D C A B
15.(15分)
I.(1)相同条件下,过氧化氢的浓度越大反应速率越大 0.1
(2) 0.002 HI + HIO = I + H O
2 2
II. I 强 变小 10—3
16.(14分)(1)负极 CH + 4O2— —8e— == CO + 2H O
4 2 2
2H O + 2e—= H ↑ + 2OH—
2 2
K 膜 M膜 0.2 FeO 2—+ 4H O + 3e— == Fe(OH)3 + 5 OH—
4 2
右 电压稳定,放电时间长
17.(14分)(1)+46.2 kJ•mol-1
(2)减小 不变 CO(g)+NO (g) = NO(g)+CO (g) ΔH = —234 kJ•mol-1,
2 2
(3) < (4) ΔH<0 L4 <
18.(15分) I. cd < = < <
II. (1)K ×K 3 (2)ad 正向 23.04P
2 3