文档内容
2025 年上学期高二期中考试参考答案
化 学
一、选择题:本题包括 14 小题,每小题 3 分,共 42 分。每小题只有一项是符合
题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B A A D A B C B C D A C A
1. C 【解析】碳纤维属于新型无机非金属材料 ,A 项正确;化学变化前后元素种类和原
子个数不发生变化,而核反应涉及元素种类变化,因此核反应不属于化学变化,B 项正确;
直径为 2~20nm 的硅量子点没有形成分散系,故该硅量子点不是胶体,C 项错误。
2. B 【解析】H S 属于共价化合物,A 项错误; Br 的共价键是由两个 2p 轨道“头碰
2 2 中
头”重叠而成,称为 p-p σ键,B 项正确; NCl 中心 P 原子的价电子对数为 3+½(5-1×3)
3
=4,N 原子有 1 个孤电子对,NCl 的空间构型是三角锥形,C 项错误。
3
3. A 【解析】Al3+与氨水反应生成氢氧化铝沉淀,不可拆分,B 项错误;向 NaHSO 溶液
4
中逐滴加入 Ba(OH)
2
溶液至 SO
4
2-刚好沉淀完全:H+ +SO
4
2- + Ba2+ + OH - = BaSO
4
↓+ H
2
O,
C 项错误;石灰乳不可拆分,D 项错误。
4. A 【解析】配制一定物质的量浓度的溶液时,溶质要放在烧杯中溶解,不能直接放在
容量瓶中溶解,A 项错误;油污的主要成分是油脂,油脂在碱性条件下可以发生水解反应生
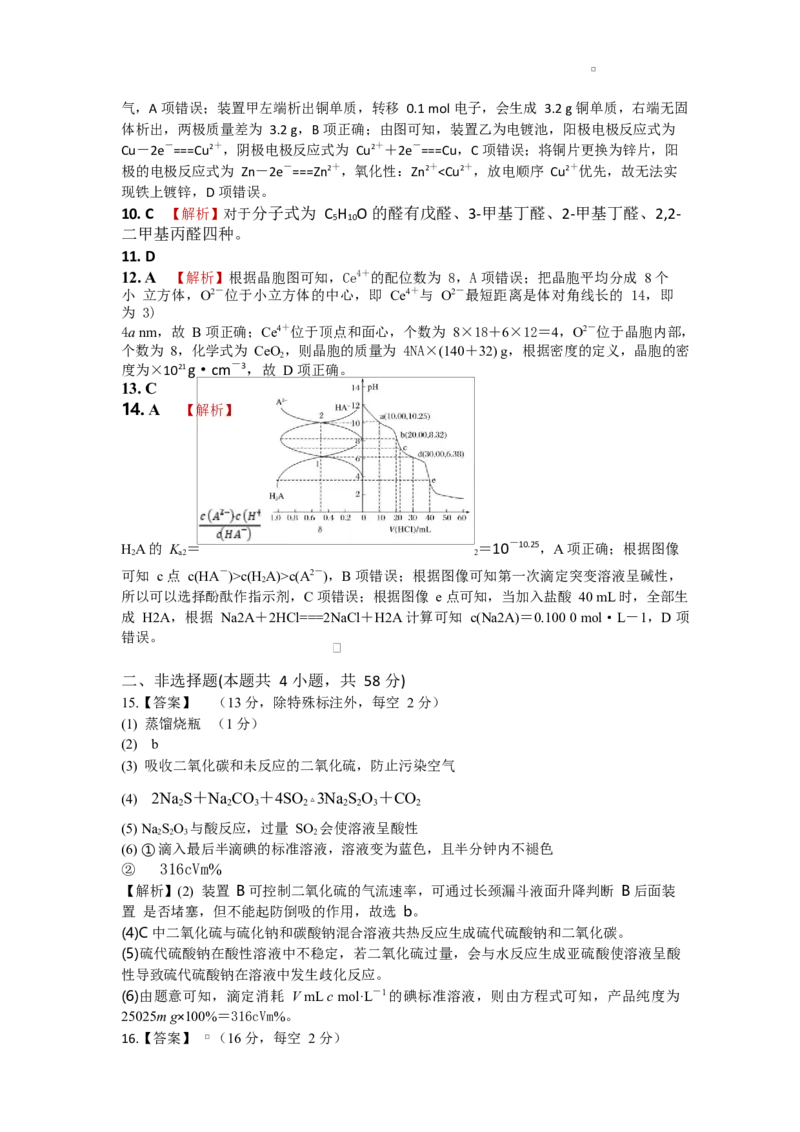
成可溶于水的甘油和高级脂肪酸盐,因此,铁钉放在 溶液中加热后可以除去其表面
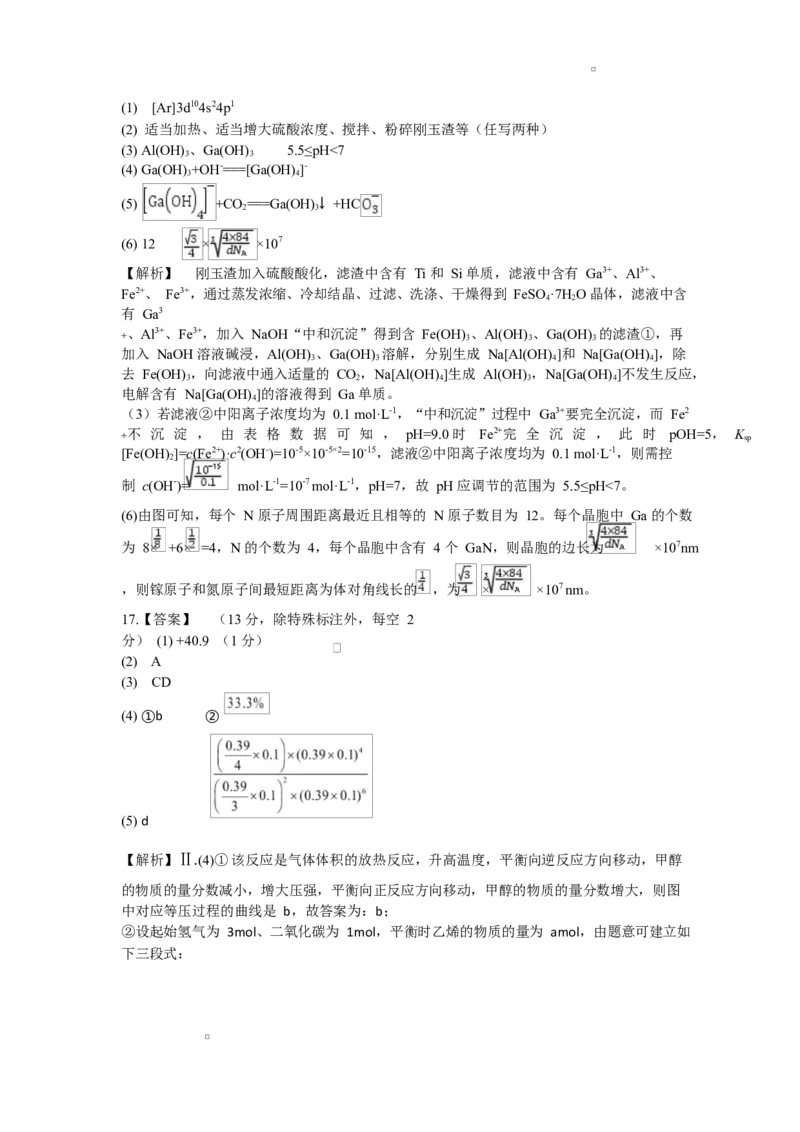
的油污,B 项正确;铁锈的主要成分是 ,其可溶于盐酸,因此,将铁钉放在
盐酸中可以除去其表面的铁锈,C 项正确;该装置为电解池,铁钉与电源负极相连作阴极,
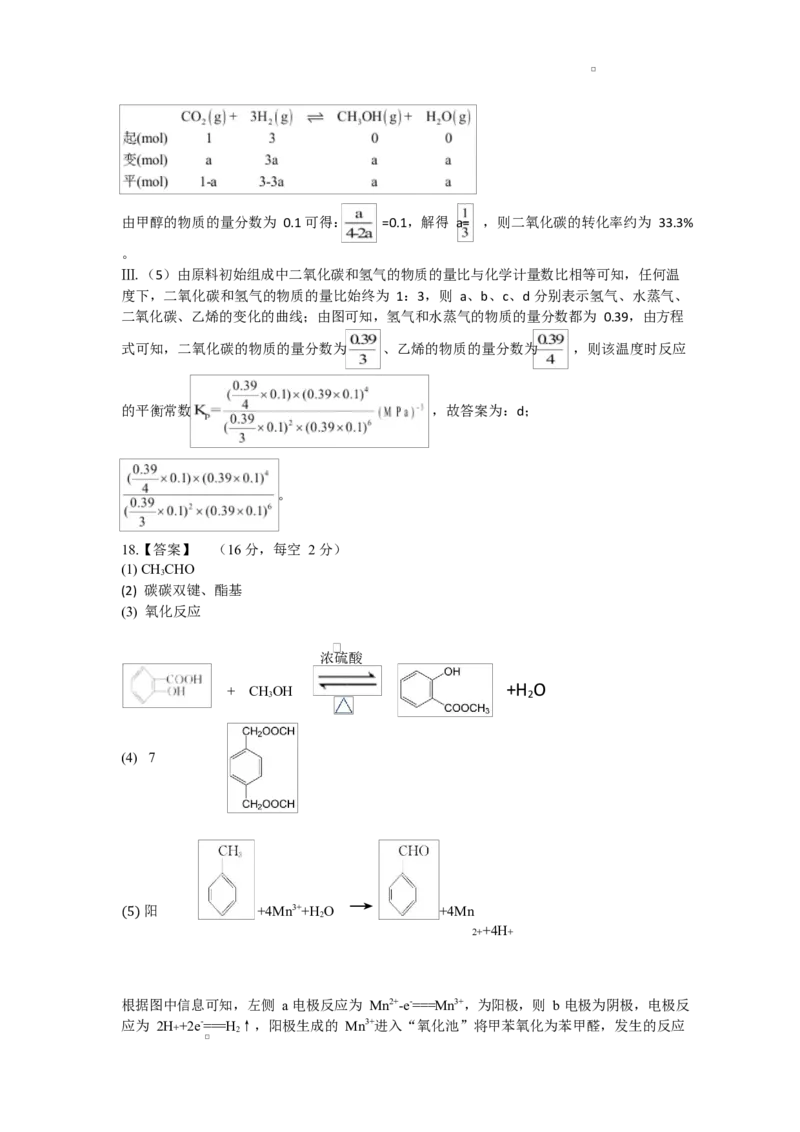
锌片与电源的正极相连作阳极,电解质溶液为 溶液,因此,该装置为电镀装置,可
以实现铁钉上镀锌,D 项正确。
5. D 【解析】 8.0g NH NO 的物质的量为 0.1mol,NH + 数目等于 0.1N ,A 项正
4 3 4 A
确; 生成 0.2mol HNO 时,0.5mol NH +被氧化,被氧化的 N 原子数为 0.5N ,B 项正
3 4 A
确;1L
pH=1 的 HNO
3
溶液中,电荷守恒 c(H+) = c(NO
3
-) + c(OH-),含 NO -数目小于 0.1N
A
;C 项正
3
确;生成 2.24L N (标准状况)时,转移的电子数为 0.375N , D 项错
2 A
误。 6. A
7. B 【解析】由四种基态原子的电子排布式可知,①是 S 元素,②是 P 元素,③是 N 元
素,④是 F 元素。第一电离能:S < P < N < F ,A 项错误;电负性: P < S < N < F,B 项正
确; 最高正化合价等于最外层电子数,但 F 无正价,C 项错误;同周期元素从左到右原子半
径依 次减小,电子层数越多原子半径越大,故原子半径: P > S > N > F,D 项错误。
8. C 【解析】据结构简式可知,该物质中含酯基、羟基、氨基、氯原子 4 种官能团,A
项错误;烃中只含 C、H 两种元素,该物质中含有 C、H、O、Cl 四种元素,不属于脂环烃,
B 项错误;该分子中含有苯环,属于芳香族化合物,C 项正确;该分子中的碳原子的杂化方
式有 sp2、sp3 两种,氮原子的杂化方式是 sp3,D 项错误。
9. B 【解析】由图可知,装置甲为电解池,右端石墨为阳极,氯离子发生氧化反应生成氯气,A 项错误;装置甲左端析出铜单质,转移 0.1 mol 电子,会生成 3.2 g 铜单质,右端无固
体析出,两极质量差为 3.2 g,B 项正确;由图可知,装置乙为电镀池,阳极电极反应式为
Cu-2e-===Cu2+,阴极电极反应式为 Cu2++2e-===Cu,C 项错误;将铜片更换为锌片,阳
极的电极反应式为 Zn-2e-===Zn2+,氧化性:Zn2+c(H A)>c(A2-),B 项错误;根据图像可知第一次滴定突变溶液呈碱性,
2
所以可以选择酚酞作指示剂,C 项错误;根据图像 e 点可知,当加入盐酸 40 mL 时,全部生
成 H2A,根据 Na2A+2HCl===2NaCl+H2A 计算可知 c(Na2A)=0.100 0 mol·L-1,D 项
错误。
二、非选择题(本题共 4 小题,共 58 分)
15.【答案】 (13 分,除特殊标注外,每空 2 分)
(1) 蒸馏烧瓶 (1 分)
(2) b
(3) 吸收二氧化碳和未反应的二氧化硫,防止污染空气
(4) 2Na S+Na CO +4SO 3Na S O +CO
2 2 3 2△ 2 2 3 2
(5) Na SO 与酸反应,过量 SO 会使溶液呈酸性
2 2 3 2
(6) ①滴入最后半滴碘的标准溶液,溶液变为蓝色,且半分钟内不褪色
② 316cVm%
【解析】(2) 装置 B 可控制二氧化硫的气流速率,可通过长颈漏斗液面升降判断 B 后面装
置 是否堵塞,但不能起防倒吸的作用,故选 b。
(4)C 中二氧化硫与硫化钠和碳酸钠混合溶液共热反应生成硫代硫酸钠和二氧化碳。
(5)硫代硫酸钠在酸性溶液中不稳定,若二氧化硫过量,会与水反应生成亚硫酸使溶液呈酸
性导致硫代硫酸钠在溶液中发生歧化反应。
(6)由题意可知,滴定消耗 V mL c mol·L-1 的碘标准溶液,则由方程式可知,产品纯度为
25025m g×100%=316cVm%。
16.【答案】 (16 分,每空 2 分)(1) [Ar]3d104s24p1
(2) 适当加热、适当增大硫酸浓度、搅拌、粉碎刚玉渣等(任写两种)
(3) Al(OH) 、Ga(OH) 5.5≤pH<7
3 3
(4) Ga(OH) +OH-===[Ga(OH)]-
3 4
(5) +CO ===Ga(OH)↓ +HC
2 3
(6) 12 × ×107
【解析】 刚玉渣加入硫酸酸化,滤渣中含有 Ti 和 Si 单质,滤液中含有 Ga3+、Al3+、
Fe2+、 Fe3+,通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到 FeSO ·7H O 晶体,滤液中含
4 2
有 Ga3
+ 、Al3+、Fe3+,加入 NaOH“中和沉淀”得到含 Fe(OH) 3 、Al(OH) 3 、Ga(OH) 3 的滤渣①,再
加入 NaOH 溶液碱浸,Al(OH) 、Ga(OH) 溶解,分别生成 Na[Al(OH)]和 Na[Ga(OH) ],除
3 3 4 4
去 Fe(OH) ,向滤液中通入适量的 CO,Na[Al(OH)]生成 Al(OH) ,Na[Ga(OH) ]不发生反应,
3 2 4 3 4
电解含有 Na[Ga(OH) ]的溶液得到 Ga 单质。
4
(3)若滤液②中阳离子浓度均为 0.1 mol·L-1,“中和沉淀”过程中 Ga3+要完全沉淀,而 Fe2
+ 不 沉 淀 , 由 表 格 数 据 可 知 , pH=9.0 时 Fe2+完 全 沉 淀 , 此 时 pOH=5, K sp
[Fe(OH) ]=c(Fe2+)·c2(OH-)=10-5×10-5×2=10-15,滤液②中阳离子浓度均为 0.1 mol·L-1,则需控
2
制 c(OH-)= mol·L-1=10-7 mol·L-1,pH=7,故 pH 应调节的范围为 5.5≤pH<7。
(6)由图可知,每个 N 原子周围距离最近且相等的 N 原子数目为 12。每个晶胞中 Ga 的个数
为 8× +6× =4,N 的个数为 4,每个晶胞中含有 4 个 GaN,则晶胞的边长为 ×107nm
,则镓原子和氮原子间最短距离为体对角线长的 ,为 × ×107 nm。
17.【答案】 (13 分,除特殊标注外,每空 2
分) (1) +40.9 (1 分)
(2) A
(3) CD
(4) ①b ②
(5) d
【解析】Ⅱ.(4)①该反应是气体体积的放热反应,升高温度,平衡向逆反应方向移动,甲醇
的物质的量分数减小,增大压强,平衡向正反应方向移动,甲醇的物质的量分数增大,则图
中对应等压过程的曲线是 b,故答案为:b;
②设起始氢气为 3mol、二氧化碳为 1mol,平衡时乙烯的物质的量为 amol,由题意可建立如
下三段式:由甲醇的物质的量分数为 0.1 可得: =0.1,解得 a= ,则二氧化碳的转化率约为 33.3%
。
Ⅲ.(5)由原料初始组成中二氧化碳和氢气的物质的量比与化学计量数比相等可知,任何温
度下,二氧化碳和氢气的物质的量比始终为 1:3,则 a、b、c、d 分别表示氢气、水蒸气、
二氧化碳、乙烯的变化的曲线;由图可知,氢气和水蒸气的物质的量分数都为 0.39,由方程
式可知,二氧化碳的物质的量分数为 、乙烯的物质的量分数为 ,则该温度时反应
的平衡常数 ,故答案为:d;
。
18.【答案】 (16 分,每空 2 分)
(1) CH CHO
3
(2) 碳碳双键、酯基
(3) 氧化反应
浓硫酸
+ CHOH +H O
3 2
(4) 7
→
阳 +4Mn3++H O +4Mn
2
2++4H+
(5)
根据图中信息可知,左侧 a 电极反应为 Mn2+-e-===Mn3+,为阳极,则 b 电极为阴极,电极反
应为 2H++2e-===H
2
↑,阳极生成的 Mn3+进入“氧化池”将甲苯氧化为苯甲醛,发生的反应→
为 +4Mn3++H O +4Mn
2
2++4H+ 。