文档内容
2024 年秋季学期高二年级校联体第二次联考
化 学
(试卷总分100分,考试时间75分钟)
注意事项:
1.答题前,务必将自己的姓名、班级、准考证号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其它答案标号。
3.答非选择题时,必须使用0.5毫米黑色签字笔,将答案书写在答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上答题无效。
可能用到相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Cr-52
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求。
1.劳动创造美好生活,下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 帮厨活动:将食物放在冰箱里保存 降低温度可以减小化学反应速率
B 实践活动:用泡沫灭火剂进行消防演习 灭火剂溶液中Al3+和HCO 发生双水解
3
C 家务劳动:用活性炭去除房间内甲醛 活性炭具有较强还原性
D 学农活动:野炊时将煤炭碾碎使用 增大煤炭与空气接触面积,加快燃烧
2.下列变化或操作过程放热的是
A.FeCl 水解 B.CH COOH电离 C.CaCO 溶解至平衡 D.稀释浓硫酸
3 3 3
3.解释下列事实的方程式不正确的是
A.酚酞遇醋酸钠溶液变红:CH COO-+H O CH COOH+OH-
3 2 3
B.溶有CO 的雨水pH约为5.6:H O+CO H CO 2H++CO2-
2 2 2 2 3 3
C.纯碱溶液处理锅炉中的水垢:CaSO (s)+CO2(aq) CaCO (s)+SO2(aq)
4 3 3 4
D.甲烷的燃烧热为890kJmol1:CH
4
(g)+2O
2
(g)===CO
2
(g)+2H
2
O(l) ΔH=-890.3kJ/mol
4.以下生活除垢或除渍中,其原理不属于盐类水解的是
A.醋酸除水垢 B.明矾净水 C.NH Cl溶液除锈 D.热碱除油污
4
5.室温下,下列各组离子在指定溶液中一定能大量共存的是
A.由水电离产生的c(OH-)为11013的溶液中:Mg2、Cu2、CO2、NO
3 3
B.pH12的溶液中:Na、NH、CO2、MnO
4 3 4
C.加甲基橙呈红色的溶液中:NO、Cl、HCO 、Na
3 3
D.c(H+)/c(OH-)=109的溶液中:NH、Cl、Al3、SO2
4 4
高二 化学 第 1 页 共 6 页6.工业制备硫酸的生产过程及相关信息如下。下列有关说法不正确的是
不同压强下接触室中SO 的平衡转化率/%
温度/℃ 2
1MPa 10MPa
450 99.2 99.7
550 94.9 97.7
工艺流程
A.冷却分离后的SO 和O 可循环利用
2 2
B.2SO (g)+O (g)2SO (g)的正反应为放热反应
2 2 3
C.寻找并使用合适的催化剂可以提高反应速率
D.实际生产中,SO 的催化氧化应采用温度450C,压强10Mpa
2
7.在一定温度下,当过量Mg(OH) 固体在水溶液中达到平衡:Mg(OH) (s) Mg2+(aq)+2OH-(aq),
2 2
要使Mg(OH) 固体减少而c(Mg2+)不变,可采取的措施是
2
A.加MgCl 固体 B.加HCl气体 C.加少量水 D.加NaOH固体
2
8.N O 和 CO 是环境污染性气体,可在 Pt O+表面转化为无害气体,其反应为:
2 2
N O(g)+CO(g)===CO (g)+N (g) ΔH,有关化学反应的物质变化过程如图1所示,能量变化
2 2 2
过程如图2所示,下列说法正确的是
A.由图1可知ΔH=ΔH +ΔH
1 2
B.由图1可知Pt O+作催化剂,可使反应的焓变减小
2
C.由图2可知正反应的活化能小于逆反应的活化能,所以ΔH=ΔE -ΔE
2 1
D.由图2可知该反应过程中只涉及极性键的断裂和生成
9.N 是阿伏加德罗常数的值,下列说法正确的是
A
A.0.5molL-1 FeCl 溶液中,含有Cl-的数目为1.5N
3 A
B.常温下,1LpH=13的Ba(OH) 溶液中,含有OH-的数目为0.1N
2 A
C.1L0.1mol/L的NH NO 溶液中含有NH的数目为0.1N
4 3 4 A
D.1molN (g)和3molH (g)在密闭容器中充分反应后,生成NH (g)的数目为2N
2 2 3 A
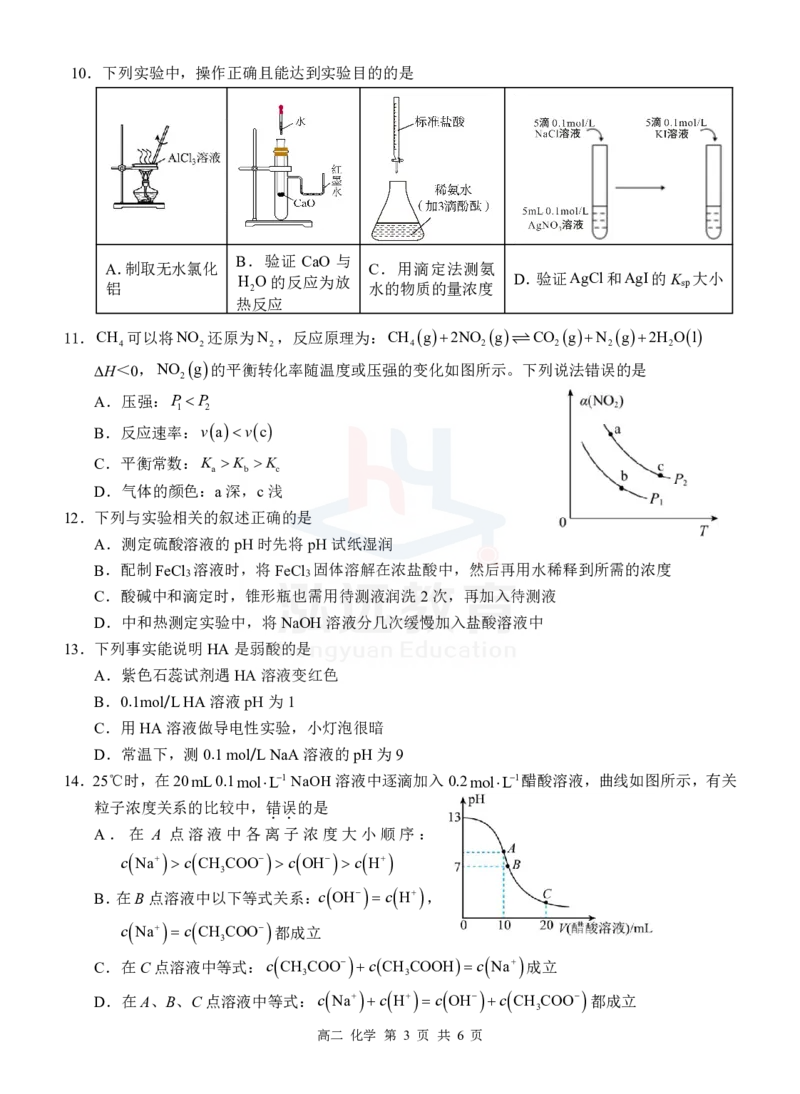
高二 化学 第 2 页 共 6 页10.下列实验中,操作正确且能达到实验目的的是
B.验证 CaO 与
A.制取无水氯化 C.用滴定法测氨
铝 H 2 O的反应为放 水的物质的量浓度 D.验证AgCl和AgI的K sp 大小
热反应
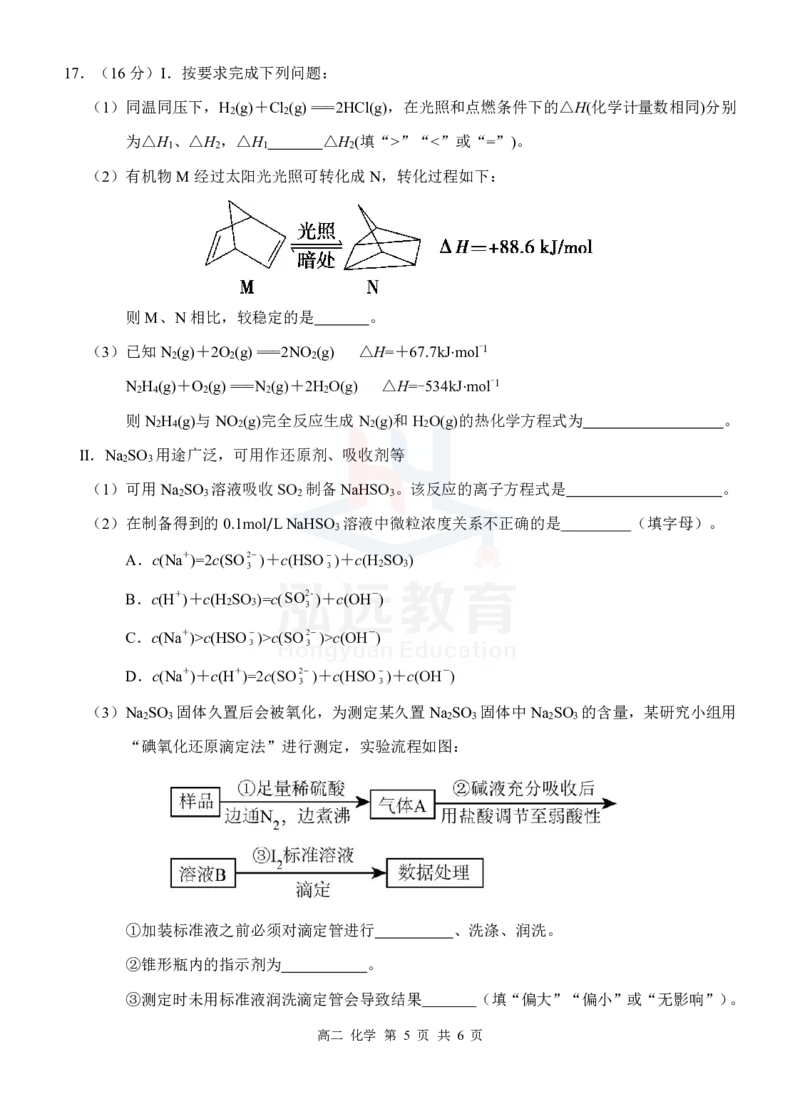
11.CH 可以将NO 还原为N ,反应原理为:CH g2NO g CO gN g2H Ol
4 2 2 4 2 2 2 2
∆H<0,NO g的平衡转化率随温度或压强的变化如图所示。下列说法错误的是
2
A.压强:P P
1 2
B.反应速率:vavc
C.平衡常数:K K K
a b c
D.气体的颜色:a深,c浅
12.下列与实验相关的叙述正确的是
A.测定硫酸溶液的pH时先将pH试纸湿润
B.配制FeCl 溶液时,将FeCl 固体溶解在浓盐酸中,然后再用水稀释到所需的浓度
3 3
C.酸碱中和滴定时,锥形瓶也需用待测液润洗2次,再加入待测液
D.中和热测定实验中,将NaOH溶液分几次缓慢加入盐酸溶液中
13.下列事实能说明HA是弱酸的是
A.紫色石蕊试剂遇HA溶液变红色
B.0.1mol/LHA溶液pH为1
C.用HA溶液做导电性实验,小灯泡很暗
D.常温下,测0.1mol/LNaA溶液的pH为9
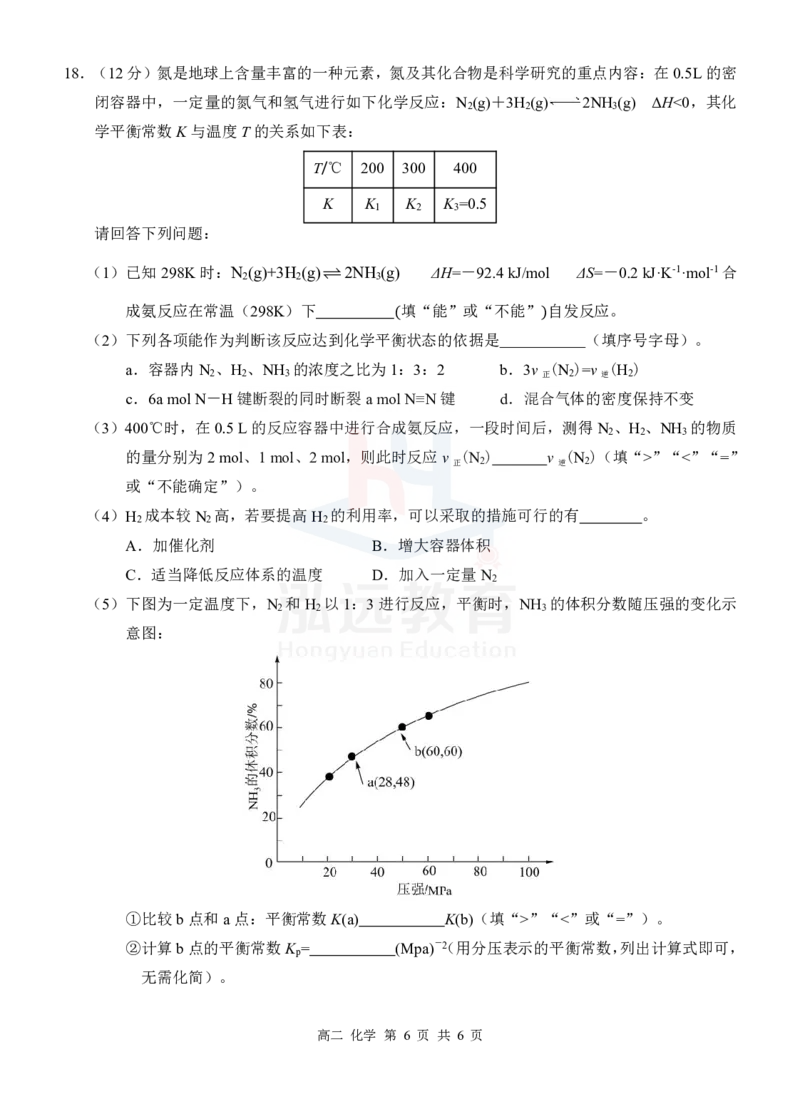
14.25℃时,在20mL0.1molL1 NaOH溶液中逐滴加入0.2molL1醋酸溶液,曲线如图所示,有关
粒子浓度关系的比较中,错误的是
..
A.在 A 点溶液中各离子浓度大小顺序:
c
Na
c
CH
COO
c
OH
c
H
3
B.在B点溶液中以下等式关系:c
OH
c
H
,
c
Na
c
CH
COO
都成立
3
C.在C点溶液中等式:c CH COO cCH COOHc Na 成立
3 3
D.在A、B、C点溶液中等式:c
Na
c
H
c
OH
c
CH
COO
都成立
3
高二 化学 第 3 页 共 6 页二、非选择题:本题共4小题,共58分。
15.(14分)现有下列化合物①NaCl、②NaOH、③HCl、④NH Cl、⑤CH COONa、⑥CH COOH、
4 3 3
⑦NH ·H O、⑧FeCl 回答问题:
3 2 3
(1)上述化合物中属于强电解质的是 (填序号);⑧FeCl 水溶液蒸干灼烧
3
得到的物质是 (填化学式)。
(2)物质的量浓度均为0.1mol·L-1的①NaCl、④NH Cl、⑤CH COONa三种稀溶液,按pH由
4 3
大到小的顺序为 (填序号)。
(3)常温下,pH=10 的CH COONa水溶液中,水电离出来的 c(OH-)为 mol/L,在 pH=3
3
的CH COOH溶液中水电离出来的 c(H+)为 mol/L。
3
(4)室温下,pH=3的盐酸与pH=11的氨水溶液等体积混合后pH 7(填“>”“<”或“=”)。
(5)已知水中存在如下平衡:H O+H O H O++OH- ΔH>0,现欲使平衡向右移动,且所得
2 2 3
溶液显酸性,选择的方法是 。
A.向水中加入 NaHSO 固体 B.向水中加入 Na CO 固体
4 2 3
C.加热至 100℃ D.向水中加入 (NH ) SO 固体
4 2 4
16.(16 分)二草酸合铜酸钾是一种重要的化工原料,微溶于冷水、酒精,可溶于热水。已知
CuO2KHC O K CuC O H O , 实 验 室 制 备 二 草 酸 合 铜 酸 钾 晶 体
2 4 2 2 4 2 2
K CuC O 2H O 可采用下列步骤:
2 2 4 2 2
回答下列问题:
(1)CuSO 溶于水所得溶液显 (填“酸性”“碱性”或“中性”)。
4
(2)在常温下,CuSO 溶液与氢氧化钠溶液反应生成氢氧化铜,当所得溶液的pH7时,则溶
4
液中c Cu2 (已知该温度下K CuOH 2.21020)。
sp
2
(3)过滤时用到的玻璃仪器有漏斗、 。
(4)操作④后得到的晶体需用少量酒精洗涤,其目的是 。
(5)已知在25℃时,草酸(H C O )的K =5.6×10-2,K =1.5×10-4,K (CaC O )=4.0×10-8,
2 2 4 a1 a2 sp 2 4
回答下列问题。
①写出草酸在水中的第一步电离的方程式 。
②25℃时,KHC O 溶液的 pH 7(选填“>”“<”或“=”),请说明原
2 4
因: 。
③已知反应:Ca2++2HC O CaC O ↓+H C O ,该反应的平衡常数K= (列
2 4 2 4 2 2 4
出计算式即可,无需化简)。
高二 化学 第 4 页 共 6 页17.(16分)I.按要求完成下列问题:
(1)同温同压下,H (g)+Cl (g)===2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别
2 2
为△H 、△H ,△H △H (填“>”“<”或“=”)。
1 2 1 2
(2)有机物M经过太阳光光照可转化成N,转化过程如下:
则M、N相比,较稳定的是 。
(3)已知N (g)+2O (g)===2NO (g) △H=+67.7kJ·mol-1
2 2 2
N H (g)+O (g)===N (g)+2H O(g) △H=-534kJ·mol-1
2 4 2 2 2
则N H (g)与NO (g)完全反应生成N (g)和H O(g)的热化学方程式为 。
2 4 2 2 2
II.Na SO 用途广泛,可用作还原剂、吸收剂等
2 3
(1)可用Na SO 溶液吸收SO 制备NaHSO 。该反应的离子方程式是 。
2 3 2 3
(2)在制备得到的0.1mol/LNaHSO 溶液中微粒浓度关系不正确的是 (填字母)。
3
A.c(Na+)=2c(SO2)+c(HSO)+c(H SO )
3 3 2 3
B.c(H+)+c(H SO )=c(SO2-)+c(OH-)
2 3 3
C.c(Na+)>c(HSO)>c(SO2)>c(OH-)
3 3
D.c(Na+)+c(H+)=2c(SO2)+c(HSO)+c(OH-)
3 3
(3)Na SO 固体久置后会被氧化,为测定某久置Na SO 固体中Na SO 的含量,某研究小组用
2 3 2 3 2 3
“碘氧化还原滴定法”进行测定,实验流程如图:
①加装标准液之前必须对滴定管进行 、洗涤、润洗。
②锥形瓶内的指示剂为 。
③测定时未用标准液润洗滴定管会导致结果 (填“偏大”“偏小”或“无影响”)。
高二 化学 第 5 页 共 6 页18.(12分)氮是地球上含量丰富的一种元素,氮及其化合物是科学研究的重点内容:在0.5L的密
闭容器中,一定量的氮气和氢气进行如下化学反应:N (g)+3H (g) 2NH (g) ΔH<0,其化
2 2 3
学平衡常数K与温度T的关系如下表:
T/℃ 200 300 400
K K K K =0.5
1 2 3
请回答下列问题:
(1)已知298K时:N
2
(g)+3H
2
(g)2NH
3
(g) ΔH=-92.4kJ/mol ΔS=-0.2kJ·K-1·mol-1合
成氨反应在常温(298K)下 填“能”或“不能” 自发反应。
(2)下列各项能作为判断该反应达到化学平衡
(
状态的依据是
)
(填序号字母)。
a.容器内N 、H 、NH 的浓度之比为1:3:2 b.3v (N )=v (H )
2 2 3 正 2 逆 2
c.6amolN-H键断裂的同时断裂amolN≡N键 d.混合气体的密度保持不变
(3)400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N 、H 、NH 的物质
2 2 3
的量分别为2mol、1mol、2mol,则此时反应v (N ) v (N )(填“>”“<”“=”
正 2 逆 2
或“不能确定”)。
(4)H 成本较N 高,若要提高H 的利用率,可以采取的措施可行的有 。
2 2 2
A.加催化剂 B.增大容器体积
C.适当降低反应体系的温度 D.加入一定量N
2
(5)下图为一定温度下,N 和H 以1:3进行反应,平衡时,NH 的体积分数随压强的变化示
2 2 3
意图:
①比较b点和a点:平衡常数K(a) K(b)(填“>”“<”或“=”)。
②计算b点的平衡常数K = (Mpa)-(2 用分压表示的平衡常数,列出计算式即可,
p
无需化简)。
高二 化学 第 6 页 共 6 页