文档内容
2024-2025 学年度高三上学 12 月考试(A)
化学试卷
考试范围:必修1,必修2,选必1第1章第2章,选必2
考试时间75分钟,满分100分
可能用到的相对原子质量:H-1 O-16 Cl-35.5 Cu-64 Ni-59
一.选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.在第33届巴黎奥运会上,科技与体育双向奔赴。下列说法正确的是
A.中国制造的场地自行车主要成分是碳纤维,为有机高分子材料
B.空气净化系统捕获的PM10.0、PM2.5颗粒物,均为胶体
C.奥运会场馆的硅酸盐水泥、普通玻璃均为无机非金属材料
D.足球内胆装芯片,芯片的主要成分晶体硅是分子晶体
【答案】C
【解析】碳纤维是无机非金属材料,A错误;PM10.0、PM2.5颗粒物是分散质,它分布在空气中形
成胶体,B错误;硅酸盐水泥、普通玻璃均为无机非金属材料,C正确;晶体硅是共价晶体,D错误。
2.下列化学用语或图示表达不正确的是
A.NH 的电子式为:
3
B.中子数为1的氢原子:H
C.HCHO分子的空间结构模型为
D.乙烯分子中π键的形成过程:
【答案】A
【解析】NH 是共价化合物,N、H原子间共用1对电子对,N原子最外层电子数为8,其电子式为
3
,A错误;中子数为1的氢原子,其质量数为2,表示为H,B正确;HCHO是平面结构的
分子,含有C=O键和C—H键,且原子半径:C>O>H,其空间结构模型为 ,C正确;
乙烯分子中的π键是C原子的2p轨道以“肩并肩”的方式重叠形成的,其形成过程为
,D正确。
3.近年来我国科技在各个领域都有重大进展。下列说法错误的是
A.“中国天眼”的射电板所用铝合金具有较强的抗腐蚀性
B.“华龙一号”核电海外投产,其反应堆中含有 的与 互为同素异形体
C.“深海一号”从深海中开采的石油和天然气都属于混合物
D.用磷酸钠钡钴盐实现零下273.056 ℃制冷,其晶体属于离子晶体
1
学科网(北京)股份有限公司【答案】B
【解析】铝合金具有较强的抗腐蚀性,A正确; 与 互为同位素,B错误;石油和天然气都
是混合物,C正确;磷酸钠钡钴盐由金属阳离子和酸根离子构成,为离子晶体,D正确。
4.下列有关说法中错误的是
A.硝酸钾属于盐,是复合肥料
B.SO 和NO 具有氧化性和还原性
2 2
C.工业上用海水为原料制得饱和食盐水,再通电电解可以制备氯气
D.用铜和浓硫酸反应制取CuSO 符合绿色化学理念
4
【答案】D
【解析】硝酸钾中含有酸根和金属阳离子,属于盐类物质,含有氮和钾两种营养元素,能够为植物
提供必要的养分,是复合肥料,A正确;SO 和NO 中的N、S元素均为中间价态,SO 和NO 均具
2 2 2 2
有氧化性和还原性,B正确;海水中含有大量Cl−,用海水为原料制得饱和食盐水,再通电电解制得
氯气,C正确;绿色化学的核心原则是减少或消除化学过程中对环境的负面影响,提高原料的利用率,
减少废物排放,用铜和浓硫酸反应制取CuSO 会生成有毒气体二氧化硫,这是一种大气污染物,对
4
环境和人体健康有害,不符合绿色化学理念,D错误。
5.“稀土之父”徐光宪先生提出了稀土串级萃取理论,促进了中国从稀土资源大国向高纯稀土生产大国
的飞跃,稀土串级萃取理论其基本操作是利用有机络合剂把稀土离子从水相富集到有机相再进行分
离。分离时可用的玻璃装置是
A. B. C. D. 【答案】A
【解析】利用有机络合剂把稀土离子从水相富集到有机相是萃取,使用的仪器是分液漏斗和烧杯,
选A。
6.一种农业常用肥料的结构如图所示。其中X、Y、Z、W为核电荷数依次增大的前20号主族元素,且
位于不同周期,该物质的水溶液显酸性。下列说法正确的是
A.该化合物的焰色反应呈黄色
B.Z的简单气态氢化物的热稳定性比Y的强
C.Y与其他三种元素均可形成两种或两种以上的二元化合物
D.该物质的水溶液中:c(X ZY)>c(XZY)
3 4
【答案】C
【解析】X、Y、Z、W为核电荷数依次增大的前20号主族元素,且位于不同的周期,则它们分别为
2
学科网(北京)股份有限公司第一、二、三和四周期,而W可形成一价阳离子,为K元素,根据结构图,可推出X、Y、Z分别
是H、O、P元素。该化合物含有K元素,焰色反应是紫色,A错误;非金属性O>N>P,故PH 的热
3
稳定性比HO的要差,B错误;O元素与其它三种元素可形成:HO、HO;KO、KO、KO ;
2 2 2 2 2 2 2 2
PO、PO 至少两种二元化合物,C正确;KH PO 溶液中,HPO PO HPO+H+,
2 5 4 10 2 4 2 既能电离也能水解,H2
HPO+H O HPO +OH−,溶液显酸性,电离程度大于水解程度,故c(HPO)>c(H PO ),D错误。
2 2 3 4 3 4
7.结构决定性质,性质反映结构。下列对物质性质的解释错误的是
选项 性质 解释
某些金属灼烧时有特征
A 核外电子受热吸收能量跃迁至较高能级
焰色
B I 易溶于CCl I 和CCl 均为非极性分子,相似相溶
2 4 2 4
氢键具有方向性,冰中水分子的空间利用
C 冰的密度比水小
率小
晶体中粒子在微观空间里呈现周期性的有
D 晶体具有自范性
序排列
A.A B.B C.C D.D
【答案】A
【解析】焰色试验是电子从高能到低能释放能量所发出的光波,不是从低能级跃迁至较高能级时吸
收光,A错误;I 和CCl 是非极性分子,根据相似相溶原理可知碘易溶于四氯化碳,B正确;冰中氢
2 4
键具有方向性和饱和性,每个水分子能与4个水分子形成4个氢键,降低了水分子的空间利用率,导
致冰的密度小于水,C正确;晶体的自范性是指:在适宜的条件下,晶体能够自发地呈现封闭的规则
和凸面体外形的性质,晶体的自范性是晶体中粒子微观空间里呈现周期性的有序排列的宏观表象,D
正确。
8.POCl 是一种重要的化工原料,常温下呈液态,在潮湿的空气中可发生反应
3
POCl +3H O=HPO +3HCl。N 为阿伏加德罗常数的值,下列说法正确的是
3 2 3 4 A
A.标准状况下,22.4 L POCl 中含有的分子数目为N
3 A
B.1 mol固态冰中含有的σ键数目为2 N
A
C.1 L 0.1 mol·L−1 HSO 溶液中含有的H+数目为0.2 N
2 3 A
D.常温下,7.3 g HCl中含有的电子数目为1.6 N
A
【答案】B
【解析】标准状况下22.4 L气体的物质的量是1 mol,而POCl 常温下呈液态,无法进行相关计算,
3
A错误;HO中包含2个O-Hσ键,冰即水的固态,故1 mol冰中含2 molσ键,即2 N 个,B正确;
2 A
HSO 为中强酸,其电离是分步进行,且每步电离都是部分进行,故0.1 mol HSO 溶液中H+数目小
2 3 2 3
于0.2 N ,C错误;1 mol HCl所含电子数为18 mol,7.3 g的HCl的物质的量为0.2 mol,故所含电
A
子为数3.6 mol即3.6 N ,D错误;
A
3
学科网(北京)股份有限公司9.室温下,为探究纳米铁去除水样中SeO的影响因素,测得不同条件下SeO浓度随时间变化关系如下图。
实验序号 水样体积/mL 纳米铁质量/mg 水样初始pH
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.实验①中,0~2小时内平均反应速率v(SeO)=2.0 mol·L−1·h−1
B.实验③中,反应的离子方程式为:2Fe2++SeO+8H+=2Fe3++Se+4H O
2
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始pH越小,SeO的去除效果越好
【答案】C
【解析】实验①中,0~2小时内平均反应速率v(SeO)=(5.0×10−5−1.0×10−5) mol·L−1÷2h=2.0×10−5
mol·L−1·h−1,A错误;实验③中水样初始pH=8,溶液显弱碱性,发生反应的离子方程式中不能用
H+配电荷守恒,B错误;综合分析实验①和②可知,在相同时间内,实验①中SeO浓度的变化量大,
因此,其他条件相同时,适当增加纳米铁质量可加快反应速率,C正确;综合分析实验③和②可知,
在相同时间内,实验②中SeO浓度的变化量大,因此,其他条件相同时,适当减小初始pH,SeO的
去除效果越好,但是当初始pH太小时,H+浓度太大,纳米铁与H+反应速率加快,会导致与SeO反
应的纳米铁减少,因此,当初始pH越小时SeO的去除效果不一定越好,D错误。
10.室温下,下列实验探究方案能达到探究目的的是
探究方案 探究目的
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN
A 食品脱氧剂样品中有无 价铁
溶液,观察溶液颜色变化
向淀粉溶液中加适量20%硫酸溶液,加热,冷却后加 淀粉溶液在稀硫酸和加热条件
B
NaOH溶液至碱性,再加少量碘水,观察溶液颜色变化 下是否水解
C 向浓HNO 中插入红热的炭,观察生成气体的颜色 炭可与浓HNO 反应生成NO
3 3 2
4
学科网(北京)股份有限公司分别向Mg(OH) 和Al(OH) 沉淀中滴加足量的NaOH溶
2 3
D 比较镁和铝的金属性
液,观察沉淀是否溶解
A.A B.B C.C D.D
【答案】D
【解析】由于该反应2Fe3++Fe=3Fe2+,若铁过量则溶液中可能不存在Fe3+,而无法使KSCN显色检测
Fe3+,A不符合题意;I 与NaOH反应而无法与淀粉显色,从而无法确定淀粉水解情况,若要检验淀
2
粉发生水解,应向淀粉溶液中加适量20%硫酸溶液,加热,冷却后加NaOH溶液至碱性后再加少量
新制的氢氧化铜,可观察到砖红色沉淀,若要检验淀粉是否已经水解完全,应该在冷却的酸性的水
解液中直接碘水,B不符合题意;浓HNO 受热会分解产生NO ,从而无法确定炭与浓HNO 是否发
3 2 3
生反应产生NO ,C不符合题意;金属元素最高价氧化物的水化物碱性越强,金属性越强;分别向
2
Mg(OH) 和Al(OH) 沉淀中滴加足量的 溶液,观察沉淀是否溶解:Mg(OH) 沉淀不溶于氢氧
2 3 2
化钠溶液,Al(OH) 沉淀溶于氢氧化钠溶液,说明Al(OH) 是两性氢氧化物,则碱性:Mg(OH) >
3 3 2
Al(OH) ,说明金属性:镁>铝,D符合题意。
3
11.硫酸是重要化工原料,工业生产制取硫酸的原理示意图如下。
下列说法不正确的是
A.I的化学方程式:3FeS+8O =====Fe O+6SO
2 2 3 4 2
B.Ⅱ中的反应条件都是为了提高SO 平衡转化率
2
C.将黄铁矿换成硫黄可以减少废渣的产生
D.生产过程中产生的尾气可用碱液吸收
【答案】B
【解析】反应I是黄铁矿和空气中的O 在加热条件下发生反应,生成SO 和Fe O,化学方程式:
2 2 3 4
3FeS+8O =====Fe O+6SO ,A正确;反应Ⅱ条件要兼顾平衡转化率和反应速率,还要考虑生产成
2 2 3 4 2
本,如Ⅱ中“常压、催化剂”不是为了提高SO 平衡转化率,B错误;将黄铁矿换成硫黄,则不再产
2
生Fe O,即可以减少废渣产生,C正确;硫酸工业产生的尾气为SO 、SO ,可以用碱液吸收,D正
3 4 2 3
确。
12.可采用Deacon催化氧化法将工业副产物HCl制成Cl,实现氯资源的再利用。反应的热化学方程式:
2
4HCl(g)+O (g) 2Cl(g)+2H O(g) ΔH=−114.4 kJ·mol−1。下图所示为该法的一种催化机理。
2 2 2
5
学科网(北京)股份有限公司下列说法不正确的是
A.Y为反应物HCl,W为生成物HO
2
B.反应制得1 mol Cl ,须投入2 mol CuO
2
C.升高反应温度,HCl被O 氧化制Cl 的反应平衡常数减小
2 2
D.图中转化涉及的反应中有两个属于氧化还原反应
【答案】B
【解析】由该反应的热化学方程式可知,该反应涉及的主要物质有HCl、O、CuO、Cl、HO;CuO
2 2 2
与Y反应生成Cu(OH)Cl,则Y为HCl;Cu(OH)Cl分解生成W和Cu OCl ,则W为HO;CuCl 分解
2 2 2 2
为X和CuCl,则X为Cl;CuCl和Z反应生成Cu OCl ,则Z为O;综上所述,X、Y、Z、W依次
2 2 2 2
是Cl、HCl、O、HO。由分析可知,Y为反应物HCl,W为生成物HO,A正确; 在反应中
2 2 2 2
作催化剂,会不断循环,适量即可,B错误;总反应为放热反应,其他条件一定,升温平衡逆向移动,
平衡常数减小,C正确;图中涉及的两个氧化还原反应是CuCl →CuCl和CuCl→Cu OCl ,D正确。
2 2 2
13.一种控制分子是否发光的“分子开关”工作原理如图所示。
下列说法不正确的是
A.分子P中的O均为sp2杂化
B.分子P转化为超分子Q时,N与H+形成配位键
C.增大溶液pH并除去Na+,可使超分子Q转变为分子P
D.推测分子P可以增大NaCl在有机溶剂中的溶解度
【答案】A
【解析】分子P中的O均形成2个σ键、有两对孤电子对,O的价层电子对数为4,O都采取sp3杂
化,A错误;N上有孤电子对,H+有空轨道,故分子P转化为超分子Q时,N与H+形成配位键,B
正确;分子P+Na++H+ 超分子Q,增大溶液pH并除去Na+,消耗H+,H+和Na+的浓度减小,反
应逆向进行,超分子Q转变为分子P,C正确;分子P为有机物、易溶于有机溶剂,分子P能与
Na+形成超分子,可以增大NaCl在有机溶剂中的溶解度,D正确。
14.部分含Mg或Al或Fe物质的分类与相应化合价关系如图。下列推断合理的是
6
学科网(北京)股份有限公司A.若a在沸水中可生成e,则a→f的反应一定是化合反应
B.加热c的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系
C.若b和d均能与同一物质反应生成c,则组成a的元素一定位于周期表p区
B.在g→f→e→d转化过程中,一定存在物质颜色的变化
【答案】D
【解析】若a在沸水中可生成e,此时a为Mg,e为Mg(OH) ,即f为镁盐,a→f的反应有多种,可
2
能为Mg+2HCl=MgCl +H ↑,该反应属于置换反应,可能为Mg+Cl MgCl ,该反应属于化合反应,
2 2 2 2
综上a→f的反应不一定是化合反应,A错误;由题意得,此时能产生丁达尔效应的红棕色分散系为
Fe(OH) 胶体,c应为铁盐,加热铁盐的饱和溶液,也有可能直接得到Fe(OH) 沉淀,B错误;假设b
3 3
为Al O,即d为Al(OH) ,c为铝盐,Al O、Al(OH) 与稀盐酸反应均生成铝盐,此时组成a的元素
2 3 3 2 3 3
为Al,位于周期表p区;假设b为Fe O,即d为Fe(OH) ,c为铁盐,Fe O、Fe(OH) 与稀盐酸反应
2 3 3 2 3 3
均生成铁盐,此时组成a的元素为Fe,位于周期表d区,C错误;FeO是黑色,转化为Fe2+是浅绿色,
f能转化为e,此时e为白色沉淀Fe(OH) ,e转化为d,d为红褐色沉淀Fe(OH) ,说明在g→f→e→d
2 3
转化过程中,一定存在物质颜色的变化,D正确。
15.某同学为测定Cu和Cu O混合粉末中Cu的含量。将31.2 g Cu和Cu O混合粉末加入500 mL 4
2 2
mol·L−1的稀硝酸中,得到NO气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的
是
A.反应后有固体剩余
B.反应后的溶液中c(Cu2+)=0.8 mol·L−1
C.Cu单质在混合粉末中的质量分数约为35.2%
D.在反应后的溶液中加入足量铁粉,可置换出28.8 g Cu
【答案】D
【解析】Cu与稀硝酸反应的化学方程式为3Cu+8HNO (稀) 3Cu(NO ) +2NO↑+4HO,Cu O与稀
3 3 2 2 2
硝酸反应的化学方程式为3Cu O+14HNO (稀) 6Cu(NO ) +2NO↑+7HO,根据方程式,利用NO气
2 3 3 2 2
体是0.2 mol,可以判断硝酸过量,不会有固体剩余,A错误;设混合粉末中 和Cu O的物质的量
2
分别为x mol、y mol,依题意可得64x+144y=31.2,(2x+2y)/3=0.2,联立解得x=0.15,y=0.15,
c(Cu2+)=(x+2y)/0.5=0.9 mol·L−1,B错误;Cu单质在混合粉末中的质量分数为
64×0.15÷31.2×100%≈30.8%,C错误;可置换出铜的质量为64×(0.15+0.15×2)=28.8 g,D正确。
二.非选择题:本题共4小题,共55分。
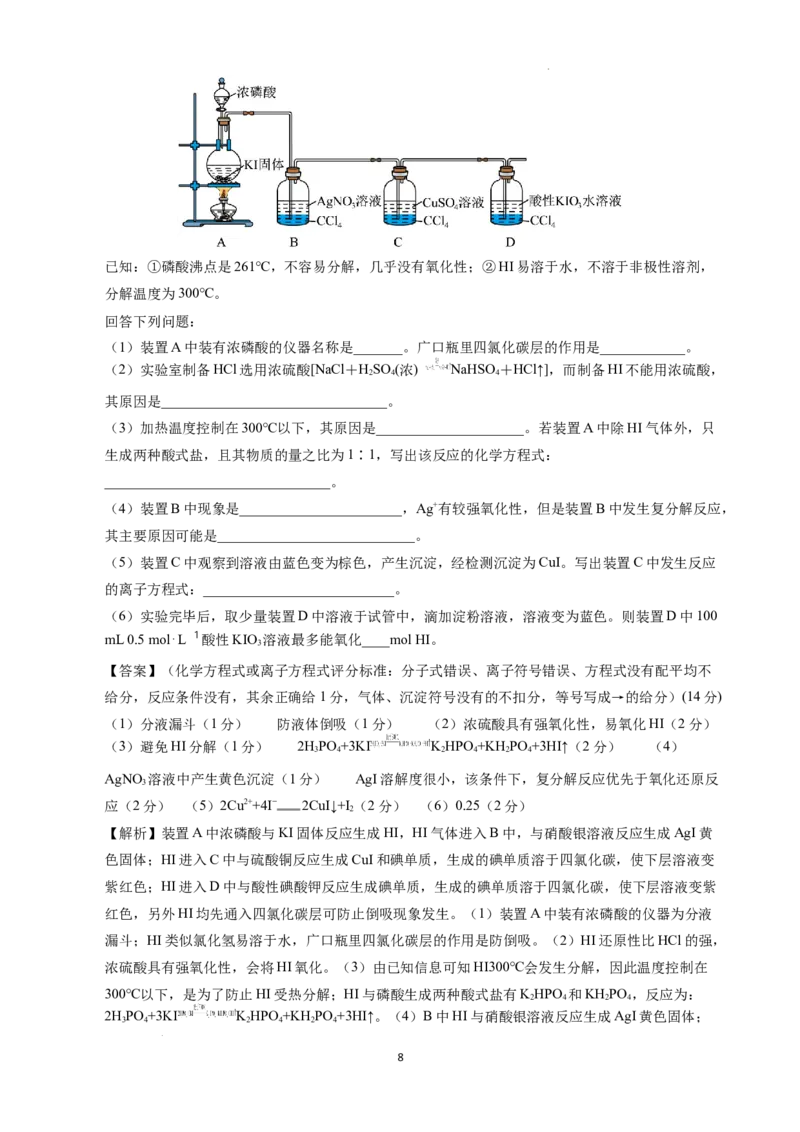
16.(14分) 某课外兴趣小组设计实验探究氢碘酸(HI)的制备及其性质,有关装置如图所示。
7
学科网(北京)股份有限公司已知:①磷酸沸点是261℃,不容易分解,几乎没有氧化性;②HI易溶于水,不溶于非极性溶剂,
分解温度为300℃。
回答下列问题:
(1)装置A中装有浓磷酸的仪器名称是_______。广口瓶里四氯化碳层的作用是____________。
(2)实验室制备HCl选用浓硫酸[NaCl+HSO (浓) NaHSO+HCl↑],而制备HI不能用浓硫酸,
2 4 4
其原因是________________________________。
(3)加热温度控制在300℃以下,其原因是_____________________。若装置A中除HI气体外,只
生成两种酸式盐,且其物质的量之比为1∶1,写出该反应的化学方程式:
________________________________。
(4)装置B中现象是_______________________,Ag+有较强氧化性,但是装置B中发生复分解反应,
其主要原因可能是____________________________。
(5)装置C中观察到溶液由蓝色变为棕色,产生沉淀,经检测沉淀为CuI。写出装置C中发生反应
的离子方程式:___________________________。
(6)实验完毕后,取少量装置D中溶液于试管中,滴加淀粉溶液,溶液变为蓝色。则装置D中100
mL 0.5 mol⋅L 酸性KIO 溶液最多能氧化____mol HI。
3
【答案】(化学方程式或离子方程式评分标准:分子式错误、离子符号错误、方程式没有配平均不
给分,反应条件没有,其余正确给1分,气体、沉淀符号没有的不扣分,等号写成→的给分)(14分)
(1)分液漏斗(1分) 防液体倒吸(1分) (2)浓硫酸具有强氧化性,易氧化HI(2分)
(3)避免HI分解(1分) 2HPO +3KI KHPO +KHPO +3HI↑(2分) (4)
3 4 2 4 2 4
AgNO 溶液中产生黄色沉淀(1分) AgI溶解度很小,该条件下,复分解反应优先于氧化还原反
3
应(2分) (5)2Cu2++4I− 2CuI↓+I (2分) (6)0.25(2分)
2
【解析】装置A中浓磷酸与KI固体反应生成HI,HI气体进入B中,与硝酸银溶液反应生成AgI黄
色固体;HI进入C中与硫酸铜反应生成CuI和碘单质,生成的碘单质溶于四氯化碳,使下层溶液变
紫红色;HI进入D中与酸性碘酸钾反应生成碘单质,生成的碘单质溶于四氯化碳,使下层溶液变紫
红色,另外HI均先通入四氯化碳层可防止倒吸现象发生。(1)装置A中装有浓磷酸的仪器为分液
漏斗;HI类似氯化氢易溶于水,广口瓶里四氯化碳层的作用是防倒吸。(2)HI还原性比HCl的强,
浓硫酸具有强氧化性,会将HI氧化。(3)由已知信息可知HI300℃会发生分解,因此温度控制在
300℃以下,是为了防止HI受热分解;HI与磷酸生成两种酸式盐有KHPO 和KH PO ,反应为:
2 4 2 4
2HPO +3KI KHPO +KHPO +3HI↑。(4)B中HI与硝酸银溶液反应生成AgI黄色固体;
3 4 2 4 2 4
8
学科网(北京)股份有限公司AgI溶解度小,复分解反应优先于氧化还原反应。(5)硫酸铜与HI发生氧化还原反应生成CuI、I
2
和HSO ,离子方程式为:2Cu2++4I− 2CuI↓+I。(6)n(KIO )=0.5 mol·L−1×0.1 L=0.05 mol,5I−
2 4 2 3
+IO+6H+ 3I+3H O,n(HI)=0.25 mol。
2 2
17.(13分)氮和氯是重要的非金属元素,研究它们的性质对生产、生活和科研有重要意义。
(1)氮的单质常用作保护气(如填充灯泡、焊接保护等),原因是___________。
(2)化工厂用浓氨水检验输送Cl 的管道时,有漏气的地方有白烟生成,发生反应的化学方程式为
2
___________。
(3)①实验室中浓HNO 盛放在棕色试剂瓶中,请用化学方程式说明其原因___________。
3
②实验室中用足量的浓HSO 和Cu充分反应,发生反应的氧化剂和还原剂的物质的量之比是
2 4
___________。
③上面两个反应都有污染性气体生成,下列哪些试剂在处理两种污染性气体中均可以使用
___________(填标号)。
a.HO b.NaOH c.NaHSO d.NaCO
2 3 2 3
(4)自来水安全问题关系民生。我国开始用ClO 替代Cl 对自来水消毒,优点之一是
2 2
______________________,可用NaClO 在酸性条件下制得ClO ,同时得到中性钠盐,发生反应的离
2 2
子方程式是_________________________。
【答案】(13分)(1)N 的化学性质稳定(1分) (2)8NH +3Cl N+6NHCl(2分)
2 3 2 2 4
(3)①4HNO=====4NO ↑+O ↑+2H O(2分) ②1∶1(2分) ③bd(2分,选1个正确给
3 2 2 2
1分,但只要有错误,该小题0分) (4)消毒效率高,避免生成有机氯化物对人体有害(1分,
答出一点即可) 5ClO+6H+ 4ClO ↑+Cl−+2H O(2分)
2 2
【解析】(1)氮的单质常用作保护气(如填充灯泡、焊接保护等),原因是氮气分子中两个氮原子均
满足8电子稳定结构,并且氮氮键的键能特别大,因此N 的化学性质很稳定。(2)用浓氨水检验输
2
送Cl 的管道时,有漏气的地方有白烟生成,即生成了氯化铵,化学方程式为8NH +3Cl
2 3 2
N+6NHCl。(3)①浓硝酸见光易分解,化学方程式为4HNO=====4NO ↑+O ↑+2H O,因此需要盛
2 4 3 2 2 2
放在棕色试剂瓶中;②实验室中足量的浓HSO 和Cu充分反应,生成硫酸铜、二氧化硫和水,Cu化
2 4
合价由0价升高到+2价,做还原剂,浓HSO 中的S由+6价降低到+4价,做氧化剂,根据转移电子
2 4
守恒可知,氧化剂和还原剂的物质的量之比为1∶1;③上面两个反应分别生成NO 、SO 两种污染性
2 2
气体;a.NO 与水反应会生成硝酸和NO,NO还是污染性气体,a不选;b.两种气体均能被氢氧化
2
钠溶液吸收,b选;c.SO 不能和NaHSO 溶液反应,c不选;d.碳酸钠溶液呈碱性,可以吸收
2 3
NO 、SO 两种污染性气体,d选;选bd;(4)自来水安全问题关系民生。我国开始用二氧化氯替代
2 2
氯气对自来水消毒,优点之一是消毒效率更高,避免生成有机氯化物对人体有害;可用亚氯酸钠在
酸性条件下制得二氧化氯,同时得到中性钠盐NaCl,发生反应的离子方程式是5ClO+6H+
4ClO ↑+Cl−+2H O。
2 2
18.(14分)化石燃料的燃烧会排放大量的CO、CO,综合利用CO、CO可以减缓温室效应,保护环
2 2
境。回答下列问题:
(1)各化学键的键能如下:
9
学科网(北京)股份有限公司化学键 H-H C≡O C=O H-O C-O C-H
键能(kJ/mol) 436 1072 803 465 326 413
已知反应:CO(g)+H(g) CO(g)+HO(g),该反应_______(填“吸热”或“放热”)反应。
2 2 2
(2)T 温度时,在容积为1 L的恒容密闭容器中发生反应CO(g)+3H(g) CHOH(g)+H O(g)。不同
1 2 2 3 2
时刻测得容器中n(H )、n(CO)、n(CHOH)如下表:
2 2 3
时间/min 0 1 2 3 5 6 7
n(H )/mol 3.0 1.5 0.9 0.6 0.6
2
n(CO)/mol 0.5 0.4 0.2 0.2
2
n(CHOH)/mol 0 0.6 0.7 1.0
3
①表格中的个别数据有误,有误的数据是______(填第几行第几列)。第7 min时
c(CO)_____mol/L。
2
②0~2 min内该反应的v(H O)=______ mol·L-1·s-1。
2
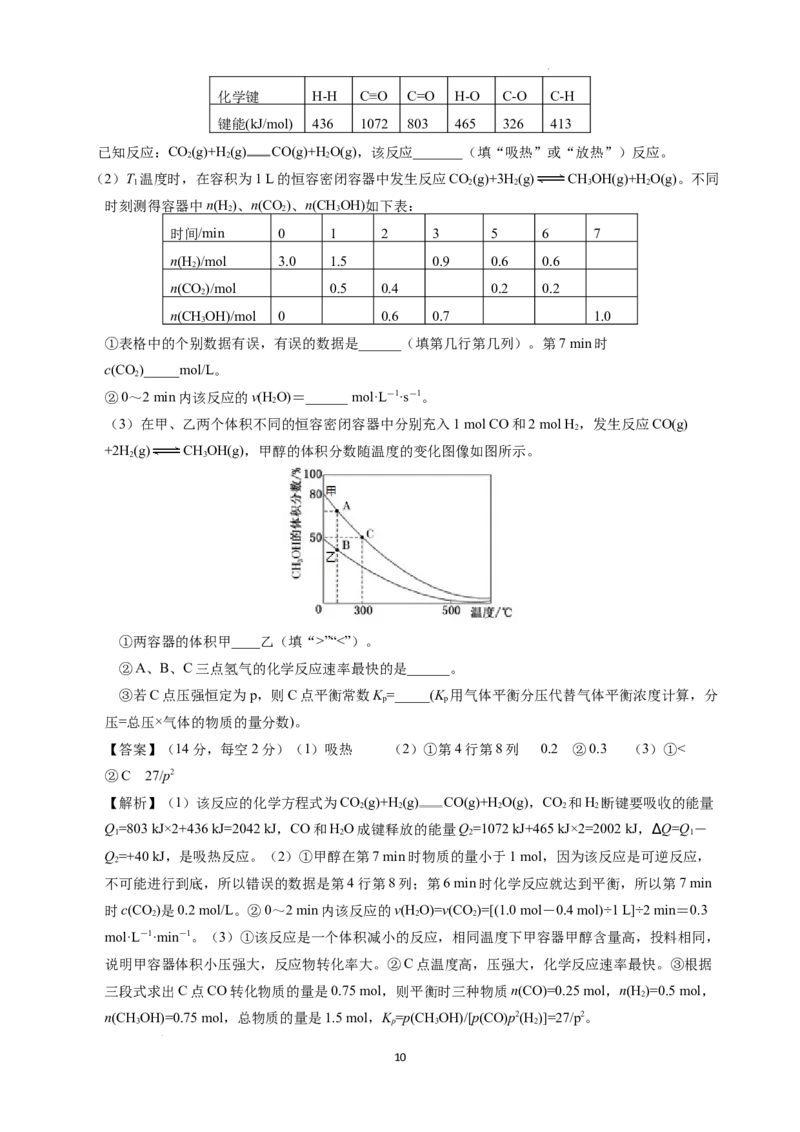
(3)在甲、乙两个体积不同的恒容密闭容器中分别充入1 mol CO和2 mol H ,发生反应CO(g)
2
+2H (g) CHOH(g),甲醇的体积分数随温度的变化图像如图所示。
2 3
①两容器的体积甲____乙(填“>”“<”)。
②A、B、C三点氢气的化学反应速率最快的是______。
③若C点压强恒定为p,则C点平衡常数K =_____(K 用气体平衡分压代替气体平衡浓度计算,分
p p
压=总压×气体的物质的量分数)。
【答案】(14分,每空2分)(1)吸热 (2)①第4行第8列 0.2 ②0.3 (3)①<
②C 27/p2
【解析】(1)该反应的化学方程式为CO(g)+H(g) CO(g)+HO(g),CO 和H 断键要吸收的能量
2 2 2 2 2
Q=803 kJ×2+436 kJ=2042 kJ,CO和HO成键释放的能量Q=1072 kJ+465 kJ×2=2002 kJ,∆Q=Q-
1 2 2 1
Q=+40 kJ,是吸热反应。(2)①甲醇在第7 min时物质的量小于1 mol,因为该反应是可逆反应,
2
不可能进行到底,所以错误的数据是第4行第8列;第6 min时化学反应就达到平衡,所以第7 min
时c(CO)是0.2 mol/L。②0~2 min内该反应的v(H O)=v(CO)=[(1.0 mol-0.4 mol)÷1 L]÷2 min=0.3
2 2 2
mol·L-1·min-1。(3)①该反应是一个体积减小的反应,相同温度下甲容器甲醇含量高,投料相同,
说明甲容器体积小压强大,反应物转化率大。②C点温度高,压强大,化学反应速率最快。③根据
三段式求出C点CO转化物质的量是0.75 mol,则平衡时三种物质n(CO)=0.25 mol,n(H )=0.5 mol,
2
n(CHOH)=0.75 mol,总物质的量是1.5 mol,K =p(CHOH)/[p(CO)p2(H )]=27/p2。
3 p 3 2
10
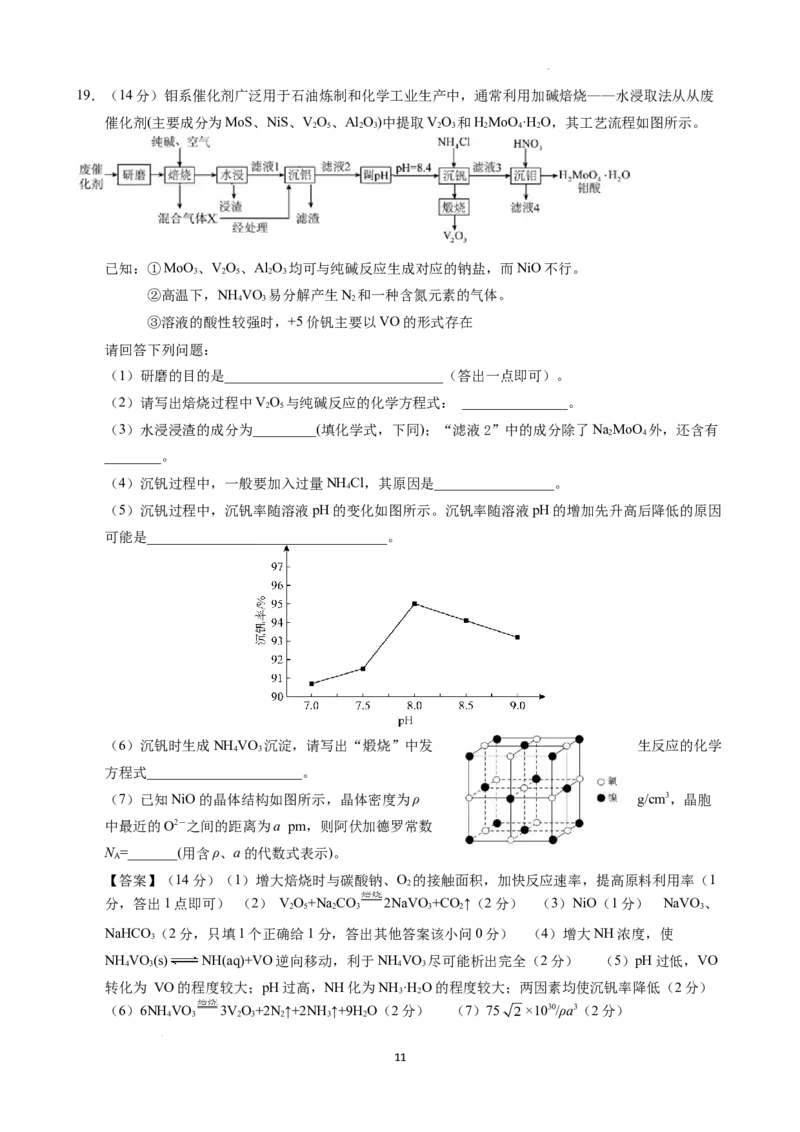
学科网(北京)股份有限公司19.(14分)钼系催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从从废
催化剂(主要成分为MoS、NiS、VO、Al O)中提取VO 和HMoO ·H O,其工艺流程如图所示。
2 5 2 3 2 3 2 4 2
已知:①MoO 、VO、Al O 均可与纯碱反应生成对应的钠盐,而NiO不行。
3 2 5 2 3
②高温下,NH VO 易分解产生N 和一种含氮元素的气体。
4 3 2
③溶液的酸性较强时,+5价钒主要以VO的形式存在
请回答下列问题:
(1)研磨的目的是_______________________________(答出一点即可)。
(2)请写出焙烧过程中VO 与纯碱反应的化学方程式: _______________。
2 5
(3)水浸浸渣的成分为_________(填化学式,下同);“滤液2”中的成分除了NaMoO 外,还含有
2 4
________。
(4)沉钒过程中,一般要加入过量NH Cl,其原因是_________________。
4
(5)沉钒过程中,沉钒率随溶液pH的变化如图所示。沉钒率随溶液pH的增加先升高后降低的原因
可能是__________________________________。
(6)沉钒时生成NH VO 沉淀,请写出“煅烧”中发 生反应的化学
4 3
方程式______________________。
(7)已知NiO 的晶体结构如图所示,晶体密度为ρ g/cm3,晶胞
中最近的O2-之间的距离为a pm,则阿伏加德罗常数
N =_______(用含ρ、a的代数式表示)。
A
【答案】(14分)(1)增大焙烧时与碳酸钠、O 的接触面积,加快反应速率,提高原料利用率(1
2
分,答出1点即可) (2) VO+Na CO 2NaVO +CO ↑(2分) (3)NiO(1分) NaVO 、
2 5 2 3 3 2 3
NaHCO (2分,只填1个正确给1分,答出其他答案该小问0分) (4)增大NH浓度,使
3
NH VO (s) NH(aq)+VO逆向移动,利于NH VO 尽可能析出完全(2分) (5)pH过低,VO
4 3 4 3
转化为 VO的程度较大;pH过高,NH化为NH ·H O的程度较大;两因素均使沉钒率降低(2分)
3 2
(6)6NH VO 3VO+2N ↑+2NH↑+9H O(2分) (7)75 ×1030/ρa3(2分)
4 3 2 3 2 3 2
11
学科网(北京)股份有限公司【解析】(1)“研磨”的目的为增大焙烧时与碳酸钠、O 的接触面积,加快反应速率,提高原料利
2
用率。(2)硫化物焙烧时生成氧化物和二氧化硫,而NiO不能与碳酸钠反应;VO 可与纯碱反应生
2 5
成对应的钠盐,VO+Na CO 2NaVO +CO ↑。(3)由于NiO不能与碳酸钠反应,故“水浸”时
2 5 2 3 3 2
以“浸渣”的形式沉淀出来,而MoO 、VO、Al O 与纯碱反应生成NaMoO 、NaVO 和NaAlO ,
3 2 5 2 3 2 4 3 2
沉铝通入CO 生成沉淀Al(OH) 和NaHCO ,故“浸渣”的成分为NiO;“滤液2”中的成分除了
2 3 3
NaMoO 外,还含有NaVO 、NaHCO 。(4)“沉钒”的目的是将VO完全转化为NH VO 沉淀析出,
2 4 3 3 4 3
加入过量NH Cl的目的是利用同离子效应,促进NH VO 尽可能析出完全,所以加入过量的NH Cl,
4 4 3 4
会增大NH浓度,使NH VO (s) NH(aq)+VO逆向移动,有利于NH VO 尽可能析出完全。(5)
4 3 4 3
由已知③在水溶液中存在:VO+2H+ VO+H O,pH过低,该平衡正向移动,VO转化为VO的程
2
度较大;pH过高,NH转化为NH ·H O的程度较大;两因素均使沉钒率降低。(6)由信息和流程可
3 2
知,NH VO 沉淀煅烧时分解产生VO 和两种气体,根据氧化还原反应原理可知,其中一种气体为氮
4 3 2 3
气,另外一种只能是氨气,故反应的化学方程式为6NH VO 3VO+2N ↑+2NH↑+9H O。(7)晶
4 3 2 3 2 3 2
胞中Ni2+位于顶点和面心,一个晶胞中Ni2+数目为8×1/8+6×1/2=4,O2-原子位于晶胞内部1个、棱心
12个,一个晶胞中O2-数目为1+12×1/4=4,则晶胞质量为(4×59+4×16)÷N =300/N g;晶胞中最近的
A A
O2-之间的距离为面对角线长度的二分之一为a pm,则晶胞边长为 a pm,则晶胞体积为( a
pm)3=2 a3×10-30cm3,根据密度为ρ=m/V=(300/N g)/(2 a3×10-30cm3)=75 /(a3×10-30 N ) g/cm3,
A A
则N =75 ×1030/ρa3 mol-1。
A
12
学科网(北京)股份有限公司