文档内容
{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}{#{QQABTQQEggggApAAAAhCUwHICkIQkACAAYgOhEAIIAAASBFABCA=}#}2024~2025 学年高三(25 届)二模化学科试卷
参考答案
1 B【解析】A选项,低温石英具有手性,被广泛用作压电材料,如制作石英手表(选择
性必修2第82页第一段,2023年7月第6次印刷),故正确;B选项,碳酸钠可用
作食用碱,其结晶水合物有Na CO ·H O、Na CO ·7H O和Na CO ·10H O三种(必
2 3 2 2 3 2 2 3 2
修1第39页第一段和脚注,2022年6月第3次印刷)。故B错误;C选项,“含有苯
环的蛋白质均能发生这个反应。皮肤、指甲不慎沾上浓硝酸会出现黄色就是由此造
成的”(选择性必修3第117页显色反应第一段中间,2023年7月第6次印刷),故
C正确;D选项,低密度聚乙烯柔软,用于食品包装袋等薄膜制品(选择性必修3
第138页最后第一段,2023年7月第6次印刷)。故D正确。
2 D 【解析】A选项,Na O 与水反应生成NaOH的同时有放出O ,Na O 中氧为-1价,
2 2 2 2 2
属于过氧化物不是碱性氧化物,故A错误;B选项,电离出的阳离子全部是H+的化
合物才是酸性氧化物,NaHSO 属于盐,故B错误;C选项,分散系的分类是按照分
4
散质粒子直径大小为标准进行分类的,故C错误;D选项,并非所有的无氧酸都是
二元化合物,如HCN,故D正确。
3 A【解析】A选项,侯氏制碱法是在饱和氯化钠溶液中先通入足量氨气,再通入足量
CO 。利用碳酸氢钠的溶解度较低而获得碳酸氢钠晶体后加热分解制得碳酸钠,故A
2
错误;B选项,青蒿素分子中有氧原子,是烃的衍生物,故B正确;C选项,稀土
元素是镧系元素以及钇和钪,共17种金属元素,故C正确;D选项,胺是NH 分子
3
中H原子被烃基取代的一类有机物,有碱性,能与酸反应。故D正确。
4 D【解析】A选项,CO 的分子空间结构为直线形,SO 、NO 的分子空间结构为V形,
2 2 2
故A错误;B选项,四氯化碳的电子式中氯原子周围的孤电子对丢失,故B错误;C
选项,邻羟基苯甲醛分子内氢键在羟基氢与羰基氧之间,故C错误;D选项,B原
子最外层3个电子,分别位于1个2s轨道和1个2p轨道中,故D正确。
5 C【解析】A选项,乙醇能取代不能加成,乙醛能加成,α-H也能发生取代如碘仿反
应(高中未学相关性质),故A不符合题意;B选项,乙烷和乙酸均能发生取代反应
而不能发生加成反应,故B不符合题意;C选项,烯丙醇和油酸均含有碳碳双键,
能发生加成反应,烯丙醇中羟基和油酸中羧基均能发生取代反应(如酯化),故C符
合题意;D选项,聚丙烯分子中不存在碳碳双键,不能发生加成反应,故D不符合
题意。
6 A【解析】A选项,焰色试验是电子跃迁现象,属于物理变化;电解质溶液的导电的过
程是电解过程,属于化学变化。故A正确;B选项,酸性KMnO 溶液可以氧化Cl
4
-,无论是否含有FeCl ,酸性KMnO 溶液都会褪色。故B错误;C选项,氧化剂
2 4
在反应中得到电子,发生还原反应,故C错误;D选项,人体内没有纤维素水解酶,
纤维素不能在人体内水解,故D错误。7 B【解析】A选项,NH NO 、C H NH NO 均为离子晶体,C H NH+离子半大于NH+,
4 3 2 5 3 3 2 5 3 4
故熔点低,NH 为分子晶体,常温下为气体,熔点更低,故A正确;B选项,
3
[Cu(NH ) ]SO 是离子化合物,易溶于极性溶剂,因此在强极性溶剂水中溶解性大于
3 4 4
在弱极性溶剂乙醇中。故B错误;C选项,取代基的吸电子能力越大,羧酸的酸性
越强。吸电子能力-CF >-ClCH ,而甲基是推电子基,使羧酸酸性减弱。故C正
3 2
确;D选项,同周期第一电离能随原子序数递增,波动性递增,其中N大于O,故
D正确。
8 D【解析】短周期元素W的原子核外s电子总数与p电子总数相同且与Y形成双键可
确定W为O,根据化合物的结构,可确定X为H,Y为C,Z为N。A选项,第一
电离能:N>O>C>H,故A错误;B选项,Y与W形成的化合物为CO 或CO,
2
晶体都是分子晶体。Z与W形成的化合物为NO ,晶体也都是分子晶体。故B错误;
x
C选项,W的氢化物可能是H O或H O ,常温下为液态。Y的氢化物为烃,常温下
2 2 2
固态、液态、气态都有可能。故C错误;D选项,化合物具有平面结构且Y、Z均
形成3个σ键则均为sp2杂化。故D正确。
9 C【解析】A选项,碳酸氢根与铝离子发生彻底双水解,故A错误;B选项,在较强酸
性溶液中Fe2+与NO-发生氧化还原反应,故B错误;C选项,甲基橙显红色的溶液
3
为酸性,酸性溶液中四种离子均可大量存在,故C正确;D选项,该溶液可能为强
酸性,也可能为强碱性。若为强碱性,则NH+不大量存在,故D错误;
4
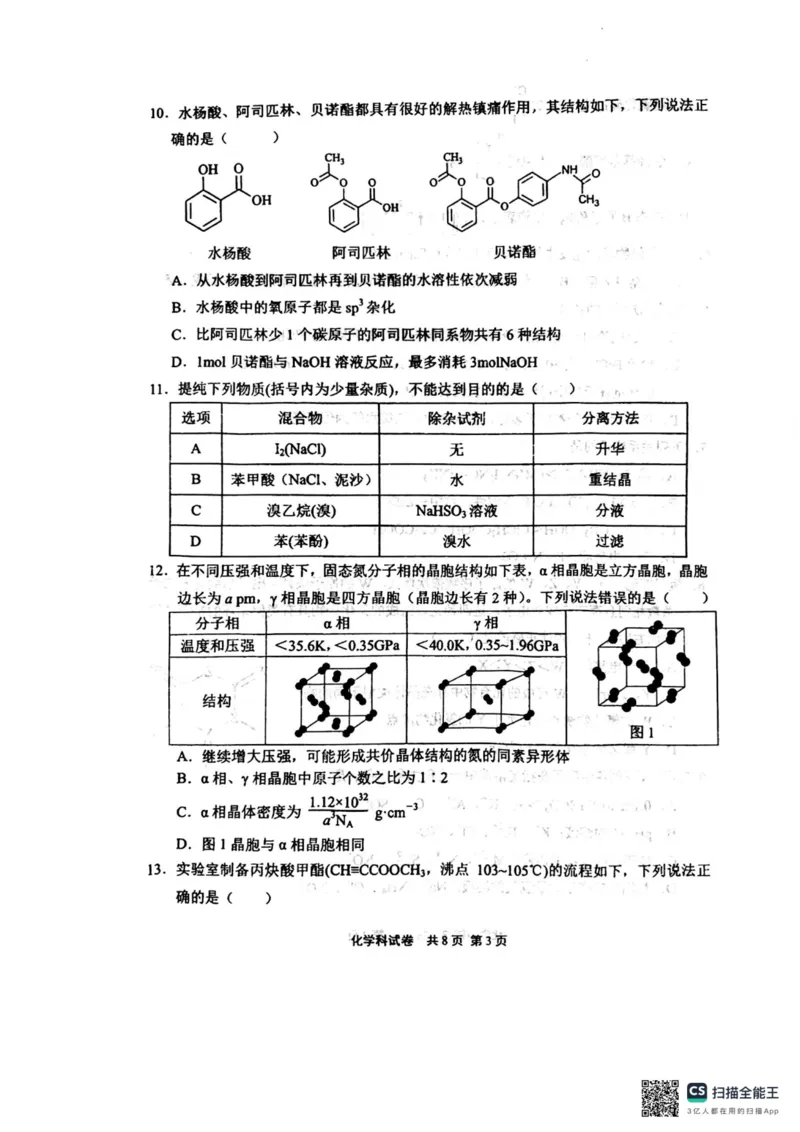
10 A【解析】A选项,从水杨酸到阿司匹林再到贝诺酯,分子中的亲水基数目递减,憎
水基数目递增。脂溶性增强水溶性降低,故A正确;根据杂化理论,原子杂化只涉
及中心原子,即端位原子不杂化。水杨酸中羧基中羰基氧原子为端位原子,不杂化。
其余两个氧原子是sp3杂化。B错误。比阿司匹林少1个碳原子的阿司匹林同系物具
HCOO COOH
备一个羧基和一个甲酸苯酚酯,即甲酰水杨酸,其结构只有三种: 、
HCOO COOH
、HCOO COOH。C错误。1mol贝诺酯分子中含有2mol个酚
酯,消耗4molNaOH,1mol酰胺基,消耗1molNaOH,共计54molNaOH。D错误。
11 D【解析】A选项,NaCl难升华而I 易升华,故A正确;B选项,苯甲酸中混有
2
NaCl、泥沙杂质用水加热溶解、趁热过滤、冷却结晶、过滤、洗涤、干燥获得纯净
苯甲酸,该过程为重结晶,故B正确;C选项,溴可氧化NaHSO ,自身被还原为Br
3
-,进入水层,溴乙烷不溶于水。故C正确;D选项,苯酚与溴水反应生成三溴苯酚
溶解在苯中,通过过滤不能提纯,同时引入新的杂质溴。故D错误。
12 B【解析】在通常状况下,N 分子内部以极强的共价键结合,分子间以较弱的范德华
2
作用力结合。随着压强的不断增大,分子间距离不断被压缩。固体分子中分子间距
逐渐接近于原子尺寸级别,且不同分子中相邻原子之间的相互作用逐渐增强。当分
子间相互作用与分子内部的原子间共价作用相当时,分子内部原有的共价键会被破
坏发生断裂,从而使得双原子分子结构发生解离,转变为原子相,A项正确;α相晶胞中平均含有4个分子,γ相晶胞中平均含有2个分子,此时原子个数之比=分子个
4×28 1.12×1032
数之比=2:1,B项错误;α相晶体密度= = g·cm-3,C项
(a×1010)3×NA a3NA
正确;将α相晶胞向右平移半个晶胞即为图1,D项正确。
13 C【解析】A选项,丙炔酸甲酯的沸点为103~105℃,蒸馏时不能用水浴。故A错误;B
选项,操作1为有机相用无水硫酸钠除水,除去水后硫酸钠为固态晶体,用过滤分
离,故B错误;C选项,经食盐水洗涤后的有机相含有少量丙炔酸和硫酸等酸性杂
质,碳酸钠除去酸性杂质,故C正确;D选项,酯化反应药品添加顺序为醇、浓硫
酸、有机酸。故D错误。
14 A【解析】A选项,硫化氢为弱电解质,离子方程式应保留,故A正确;B选项,CuS
为还原剂,故B错误;C选项,物质的量之比为4:1,故C错误;D选项,未言明
为标矿,气体体积不可知。故D错误。
15 B【解析】A选项,分析Q的结构特征可以发现,该高聚物中含有氨基(-NH ),具有
2
碱性,故A正确;B选项,分析M的结构可以发现,M的含氧官能团有醛基
(-CHO)、酯基(-COO-)和醚键(-O-)三种,故B错误;C选项,通过机理图可
以看出,Q分子与M分子之间通过相互作用形成更大分子团,正是超分子的自组装
特征,故C正确;D选项,通过机理图可以发现自愈合过程是Q分子的氨基
(-NH )和M分子的醛基(-CHO)之间形成亚胺(-C=N-)的过程,是氨基先与
2
羰基加成后再脱水形成的。故D正确。
16(16分)
⑴ ① ABC (2分,有错不得分,每少一个扣1分)
② 2:1 1s22s22p6 (各2分)
⑵ ① B(1分) ② N H (HSO ) (2分)
2 6 4 2
⑶ ① sp2 (1分)
② 6 3 (各1分)
③ 当H+浓度高时,邻二氮菲中的N优先与H+形成配位键,导致与Fe2+配位能
力减弱;当OH-浓度高时,OH-与Fe2+反应,影响Fe2+与邻二氮菲配位 (2分,酸性强原
因1分,碱性强原因1分)
④ 4(2分)
17(12分)
⑴ BC(2分,有错不得分,漏选得1分)
⑵ ① 硫氰化钾(1分,写化学式不得分)
② FeCl +3H O⇌Fe(OH) +3HCl或4 Fe(OH) +O +2H O=4Fe(OH) (2分)
3 2 3 2 2 2 3
⑶ ① 铜粉过量(1分)
② Fe3+氧化性强于Cu2+,Fe3+过量时,Cu不与Cu2+反应(2分)
⑷ ① SO +2Cu2++2Cl-+2H O=2CuCl↓+SO2-+4H+(2分)
2 2 4
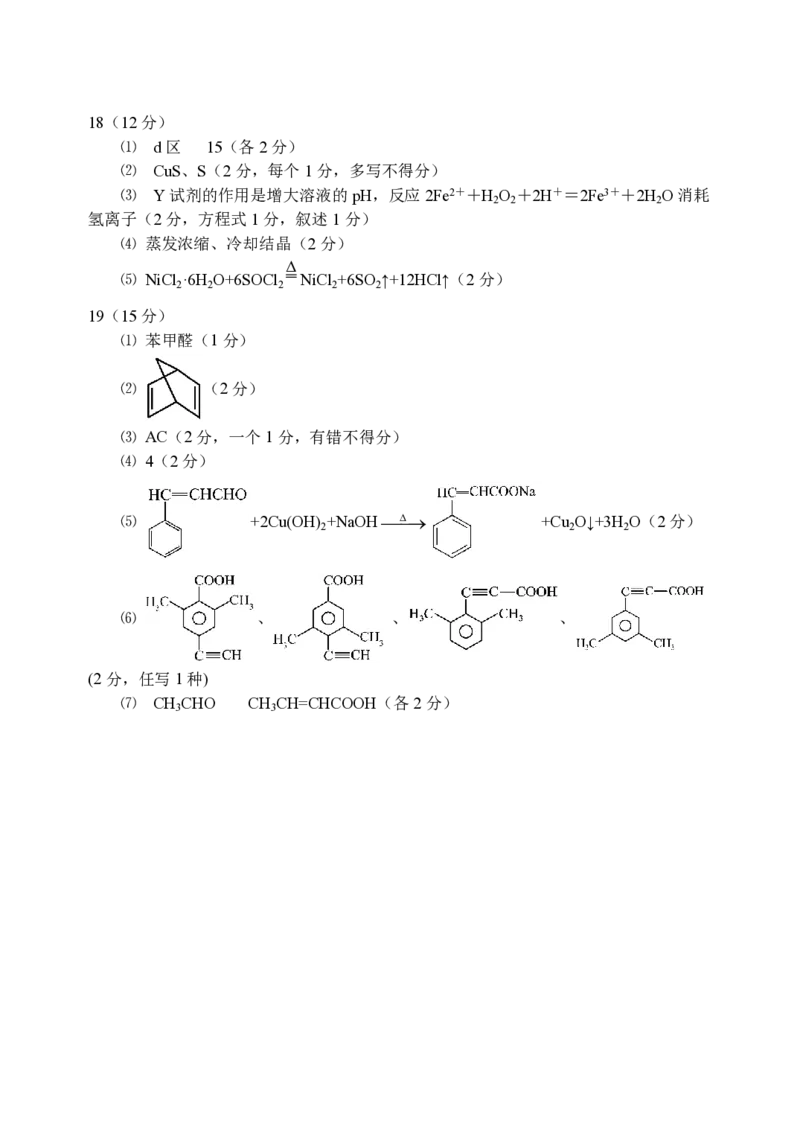
② 快速过滤,防止氯化亚铜被氧化(2分)18(12分)
⑴ d区 15(各2分)
⑵ CuS、S(2分,每个1分,多写不得分)
⑶ Y试剂的作用是增大溶液的pH,反应2Fe2++H O +2H+=2Fe3++2H O消耗
2 2 2
氢离子(2分,方程式1分,叙述1分)
⑷ 蒸发浓缩、冷却结晶(2分)
Δ
⑸ NiCl ·6H O+6SOCl NiCl +6SO ↑+12HCl↑(2分)
2 2 2 2 2
19(15分)
⑴ 苯甲醛(1分)
⑵ (2分)
⑶ AC(2分,一个1分,有错不得分)
⑷ 4(2分)
⑸ +2Cu(OH) +NaOH +Cu O↓+3H O(2分)
2 2 2
⑹ 、 、 、
(2分,任写1种)
⑺ CH CHO CH CH=CHCOOH(各2分)
3 3