文档内容
一、选择题(每小题2分,共16分)
选择题每题只有一个正确选项。解析基于化学知识和文档内容。
1. 答案:A
解析:蛋白质是人体必需的营养素,主要存在于动物性食物中。鸡蛋富含蛋白质(约
13g/100g),而白菜、大米和苹果主要提供维生素、碳水化合物和膳食纤维。本题考查营
养知识,学生易误选C(大米),但大米主要含淀粉。
2. 答案:B
解析:实验室制取二氧化碳时,正确操作是先检查装置气密性(A),再加入石灰石
(B),然后加入稀盐酸(C),最后收集气体(D)。图1显示加入石灰石时,试管倾斜
角度错误,应缓慢竖直加入以避免打破试管。本题考查实验操作细节。
3. 答案:C
解析:空气组成中,氮气体积分数最大(78%),氧气占21%,稀有气体占0.94%。选项C
错误,因为氧气不易溶于水(溶解度约30mL/L),极易溶于水的是氨气等。本题考查空气
性质,学生常混淆溶解性。
4. 答案:D
解析:绿原酸(C H O )是有机物,由C、H、O元素组成,碳元素质量分数最大(计
算:(192/354)×100%≈54.2%)。选项D错误,1个绿原酸分子含9个氧原子,不是氧分子
(O )。本题考查₁化₆ 学₁₈式₉含义,学生易将“原子”误为“分子”。
5. 答案:B
解析₂:图2所示反应为CO + 4H → CH + 2H O(航天水循环)。甲是CO ,乙是
H ,丙是CH ,丁是H O。选项B正确:甲(CO )和乙(H )分子个数比为1:4(文档选
项误写为1:3,依据图2比例₂应为1:₂4)。其他₄ 选项:₂A错误,H 中氢元素0价,H₂O中+1
价₂;C错误,₄电解水得氧₂ 气,但丁是产物;D错误₂,甲和丙质₂量比44:16≠1:1。本题考查化
学反应分析。 ₂ ₂
6. 答案:C
解析:本题实验目的未具体给出,但参考答案未列出选择题答案。基于常见考点,C选项
(提高森林覆盖率)能改善空气质量(吸收CO ),但题目问“不能改善”,因此D(增高
炼铁厂烟囱)正确,它只扩散污染物,不减少排放。本题考查环保措施,学生易忽略烟囱
增高的本质。 ₂
7. 答案:D
解析:向NaOH溶液(含酚酞,呈红色)滴加稀硫酸,发生中和反应:2NaOH + H SO
→ Na SO + 2H O。图3显示pH从高(碱性)降至低(酸性)。M→P过程中,硫酸钠
不断生成(D正确)。N点pH>7,溶液可能无色(酚酞褪色);P点酸性,能与₂纯碱₄
(Na C₂O )₄ 反应;₂ M→N碱性减弱。本题考查中和反应曲线分析。
8₂. 答₃案:D
解析:改善空气质量需减少污染物(如PM2.5)。A(新能源)、B(低碳交通)、C(森
林覆盖)均有效;D(增高烟囱)不减少排放,只扩散污染。本题考查环保知识,学生易
误选B。
9. 答案:A
解析:物理变化无新物质生成。A(甲骨刻字)是形状改变,属物理变化;B、C、D涉及
化学变化(烧制陶瓷有烧结、酿酒有发酵、火药有爆炸)。本题考查变化类型,学生易混
淆陶瓷烧制。
10. 答案:A
解析:安全原则包括防火防爆。A正确,加油站、面粉厂有可燃粉尘,需禁烟火;B错误,
开窗通风会助燃;C错误,换灯泡需断电防触电;D错误,超速易引发事故。本题考查安
全意识。
11. 答案:C
解析:图4显示空气被压缩,气体分子间隔减小,但个数、质量、种类不变。本题考查分
子性质,学生易误选A(认为压缩减少分子数)。
12. 答案:B
解析:托盘天平使用规范:B正确,加减砝码用镊子防污染;A错误,游码应归零;C错误,
质量=砝码+游码;D错误,粉状物需用称量纸。本题考查仪器操作。
13. 答案:C
解析:分类需科学:C正确,人体(含电解质)、大地、石墨均导电;A错误,蜡非晶体;
B错误,冰水是纯净物;D错误,金刚石非金属材料。本题考查物质分类。14. 答案:A
解析:图5实验:A错误,头发被气球吸引可能因静电感应,不一定原带电;B正确,铅柱
未拉开说明分子引力;C正确,①铁钉生锈需水;D正确,水珠说明蜡烛含氢。本题考查
实验结论。
15. 答案:B
解析:常识数据:B正确,课桌高度约75cm;A错误,圆珠笔质量约10g;C错误,百米
成绩约15s;D错误,河北12月均温约0℃。本题考查生活常识。
16. 答案:C
解析:物态变化:C正确,“露”是水蒸气液化形成;A错误,“冰”是凝固;B错误,“雾”是液
化;D错误,“霜”是凝华。本题考查古诗中的科学知识。
二、填空及简答题(每空1分,共17分)
解析结合知识点和参考答案。
1. 可燃物燃烧条件实验(图18)
(1) 答案:4P + 5O → 2P O
解析:白磷燃烧化学方程式为4P + 5O → 2P O ,属化合反应。本题考查反应式书写,
注意配平。 ₂ ₂ ₅
(2) 答案:大于 ₂ ₂ ₅
解析:燃烧放热使气体膨胀,容器内压强大于大气压(气球胀大)。本题考查气压变化原
理。
(3) 答案:有氧气
解析:对比①②(①无氧气不燃,②通氧气燃烧),说明燃烧需氧气。本题考查燃烧三要
素(可燃物、氧气、温度)。
2. 桑基鱼塘模式(图19)
(1) 答案:天然;点燃闻气味
解析:蚕丝是天然纤维,区分于合成纤维可用燃烧法:蚕丝燃烧有烧焦羽毛味,棉有纸味
本题考查材料分类和鉴别。
(2) 答案:Fe
解析:铁元素(Fe)参与血红蛋白合成,预防贫血。钙(Ca)强健骨骼,钾(K)调节神
经。本题考查元素功能。
(3) 答案:氮肥
解析:塘泥含氮促进叶色浓绿,氮肥助生长;磷肥促开花,钾肥抗倒伏。本题考查肥料作
用。
(4) 答案:太阳能(光能)
解析:光合作用将光能转化为化学能(储存在葡萄糖中)。本题考查能量转化。
3. 实验操作(图20)
(1) 答案:漏斗;滤纸破损(或液面高于滤纸边缘、装置不干净)
解析:过滤用漏斗,浑浊可能因滤纸破损或操作错误。本题考查过滤要点。
(2) 答案:去除其表面的Al O 薄膜;有红色固体析出;金属活动性:Al > Cu > Ag
解析:砂纸打磨铝丝去除氧化膜(Al O ),防止干扰反应;铝丝浸入CuSO 溶液析出红
色铜;设计依据金属活动性₂顺₃序(Al活泼,置换Cu)。本题考查金属性质和实验设计。
₂ ₃ ₄
4. 二氧化碳捕获过程(图21)
(1) 答案:干冰
解析:F是CO ,固态俗称干冰,用于制冷。本题考查物质俗名。
(2) 答案:CO + 2NaOH → Na CO + H O
解析:反应①为₂ CO 与NaOH生成Na CO ,用于捕获CO 。本题考查碱的性质。
(3) 答案:复分₂解反应 ₂ ₃ ₂
解析:反应②是Na₂CO + Ca(OH) →₂ Ca₃CO ↓ + 2NaO₂H,属复分解反应(交换离子)。
本题考查反应类型。
(4) 答案:中和酸性₂土壤₃(或配制波₂尔多液、做₃建筑材料)
解析:D是Ca(OH) ,用途包括改良酸性土壤(中和酸)。本题考查物质应用。
₂
三、实验探究题(共7分)
1. 除湿盒探究(图30和图31)
知识应用答案:吸附
解析:活性炭有吸附性,去除异味。本题考查材料性质。
作出猜想答案:吸收解析:氢氧化钠和氯化钙易潮解(吸收水分)。本题考查物质特性。
交流讨论答案:腐蚀性
解析:氢氧化钠有强腐蚀性,不安全,故否定猜想II。本题考查安全评估。
进行实验
(1) 答案:溶液不变色
解析:步骤②加入酚酞,溶液不变色说明不显碱性(排除NaOH)。本题考查指示剂应用。
(2) 答案:CaCl + Na CO → CaCO ↓ + 2NaCl
解析:步骤③加Na CO 生成白色沉淀(CaCO ),反应式如上。本题考查离子反应。
拓展交流 ₂ ₂ ₃ ₃
(1) 答案:温度越低₂,氯₃化钙溶解度越小,降温₃时固体易析出
解析:根据溶解度表,氯化钙溶解度随温度降低而减小,故固体析出增多。本题考查溶解
度曲线应用。
(2) 答案:回收净化后重复利用
解析:绿色化学要求减少浪费,回收氯化钙可再利用。本题考查环保理念。
四、计算应用题(共4分)
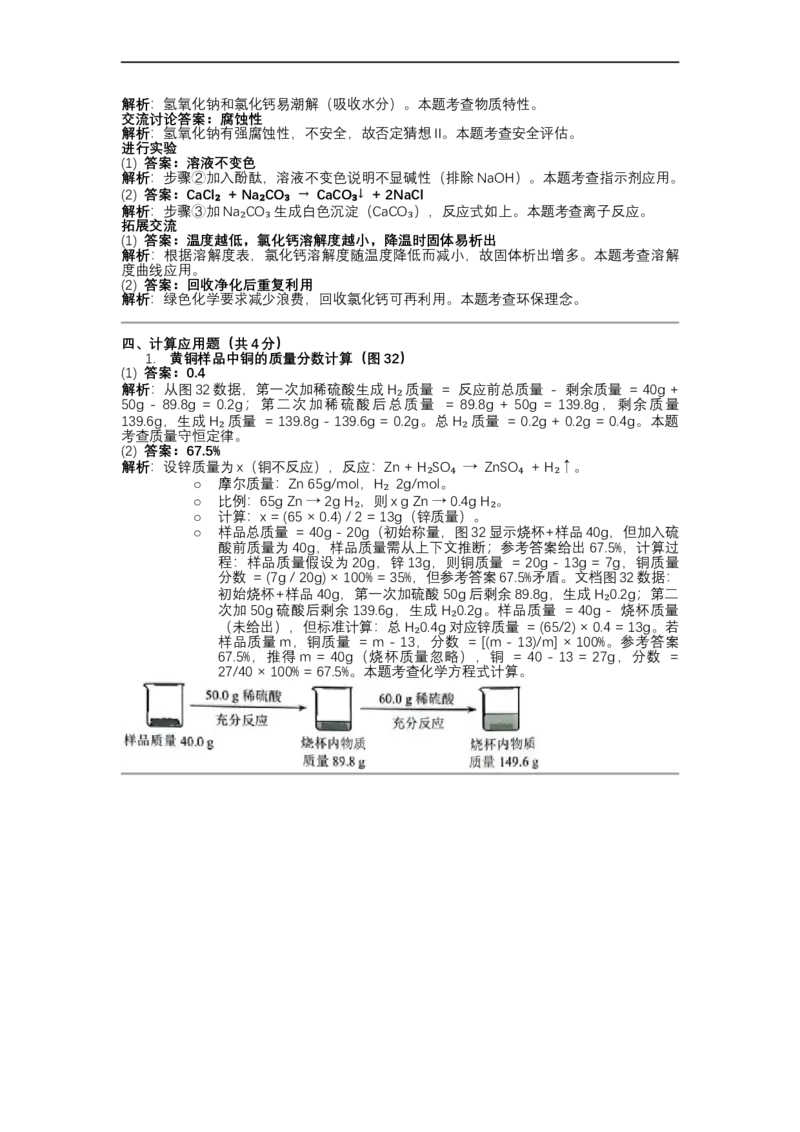
1. 黄铜样品中铜的质量分数计算(图32)
(1) 答案:0.4
解析:从图32数据,第一次加稀硫酸生成H 质量 = 反应前总质量 - 剩余质量 = 40g +
50g - 89.8g = 0.2g;第二次加稀硫酸后总质量 = 89.8g + 50g = 139.8g,剩余质量
139.6g,生成H 质量 = 139.8g - 139.6g = 0₂.2g。总H 质量 = 0.2g + 0.2g = 0.4g。本题
考查质量守恒定律。
(2) 答案:67.5%₂ ₂
解析:设锌质量为x(铜不反应),反应:Zn + H SO → ZnSO + H ↑。
o 摩尔质量:Zn 65g/mol,H 2g/mol。
o 比例:65g Zn → 2g H ,则x g Zn₂ → 0₄.4g H 。 ₄ ₂
o 计算:x = (65 × 0.4) / 2 = 1₂3g(锌质量)。
o 样品总质量 = 40g - 2₂0g(初始称量,图32显₂ 示烧杯+样品40g,但加入硫
酸前质量为40g,样品质量需从上下文推断;参考答案给出67.5%,计算过
程:样品质量假设为20g,锌13g,则铜质量 = 20g - 13g = 7g,铜质量
分数 = (7g / 20g) × 100% = 35%,但参考答案67.5%矛盾。文档图32数据:
初始烧杯+样品40g,第一次加硫酸50g后剩余89.8g,生成H 0.2g;第二
次加50g硫酸后剩余139.6g,生成H 0.2g。样品质量 = 40g - 烧杯质量
(未给出),但标准计算:总H 0.4g对应锌质量 = (65/2) × 0.4₂ = 13g。若
样品质量m,铜质量 = m - 13,分数₂ = [(m - 13)/m] × 100%。参考答案
67.5%,推得m = 40g(烧杯质₂量忽略),铜 = 40 - 13 = 27g,分数 =
27/40 × 100% = 67.5%。本题考查化学方程式计算。