文档内容
浙江省杭州市2018年中考化学真题试题
1.南京理工大学胡炳成团队用新方法制得了NaN·3HO.该化合物中含有N-等微粒。已知N
5 2 5
为7号元素,则下列有关说法正确的是
A. N-是一种单质 B.1个N-带1个单位的正电荷
5 5
C.1个N-中共含有35个质子 D.1个N-中共含有35个电子
5 5
2.一种用软锰矿(主要成分是MnO)制备KMnO 的工艺中主要涉及下列反应:
2 4
①2MnO+O+ 4KOH △ 2 K MnO+ 2HO
2 2 2 4 2
②2KMnO+2H2O==2KMnO+2KOH+H↑
2 4 4 2
下列有关说法正确的是
A. KMnO 中锰元素显十7价 B. KMnO 属于盐类物质
2 4 4
C.反应②属于复分解反应 D.该制法中KMnO 是主要原料
2 4
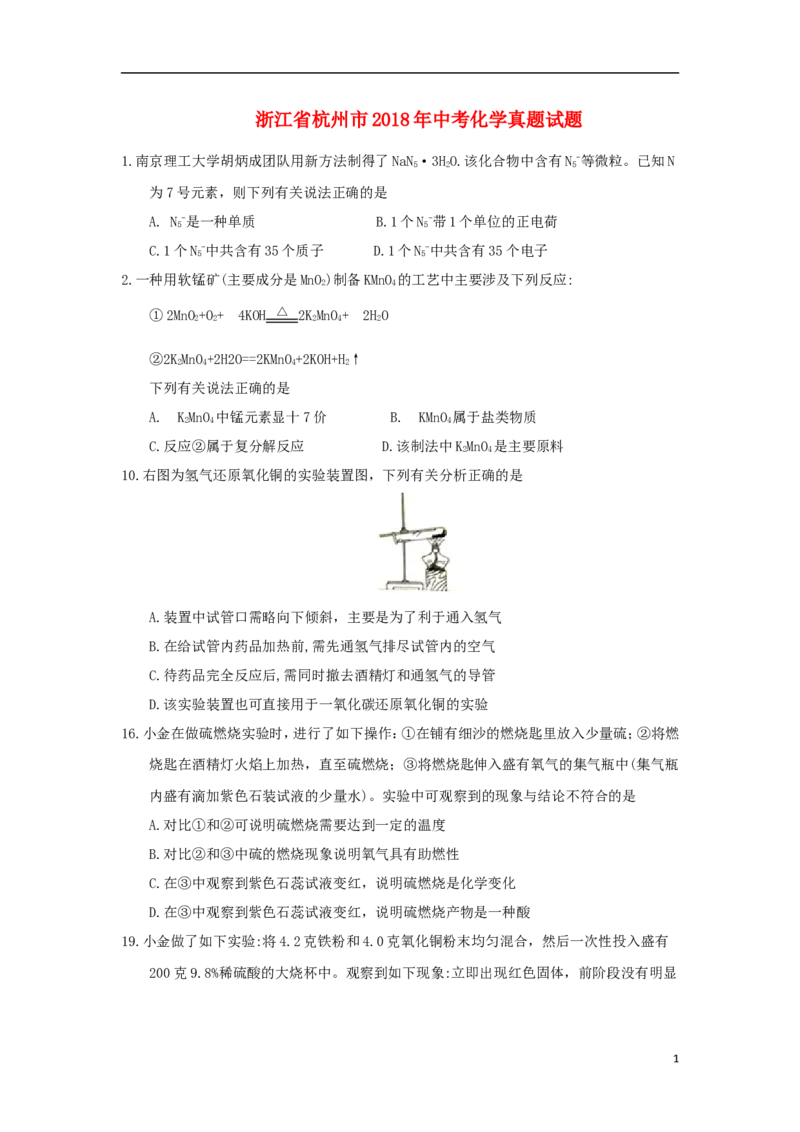
10.右图为氢气还原氧化铜的实验装置图,下列有关分析正确的是
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
16.小金在做硫燃烧实验时,进行了如下操作:①在铺有细沙的燃烧匙里放入少量硫;②将燃
烧匙在酒精灯火焰上加热,直至硫燃烧;③将燃烧匙伸入盛有氧气的集气瓶中(集气瓶
内盛有滴加紫色石装试液的少量水)。实验中可观察到的现象与结论不符合的是
A.对比①和②可说明硫燃烧需要达到一定的温度
B.对比②和③中硫的燃烧现象说明氧气具有助燃性
C.在③中观察到紫色石蕊试液变红,说明硫燃烧是化学变化
D.在③中观察到紫色石蕊试液变红,说明硫燃烧产物是一种酸
19.小金做了如下实验:将4.2克铁粉和4.0克氧化铜粉末均匀混合,然后一次性投入盛有
200克9.8%稀硫酸的大烧杯中。观察到如下现象:立即出现红色固体,前阶段没有明显
1的气泡产生,后阶段产生大量无色气泡,充分反应后上层清液是浅绿色。由此小金作出
下列判断,其中不合理的是
A.“立即出现红色固体”是由于很快发生了如下转化:CuO CuSO4 Cu
B.“产生大量无色气泡”是由于发生了如下反应:Fe+ HSO=FeSO+H↑
2 4 4 2
C.该实验条件下,硫酸铜比稀硫酸更容易跟铁粉发生反应
D.在不同浓度的硫酸铜和稀疏酸的混合溶液中投入铁粉,都是硫酸铜先跟铁粉反应
23.(4分)某化工厂利用含有1% -2%BaCO 的废料制取BaCl(废料中其他物质不溶于水和稀
3 2
盐酸、且不与稀盐酸反应)。其部分流程如下:
滤渣必须经过充分洗涤,确保其中Ba2+含最达到规定标准才能作为固体度弃物处理,检
验Ba2+的试剂可用______,洗涤滤渣的主要目的是________。
24.(4分)CO 的转化和利用是一个热门的研究课题。回答下列相关问题:
2
(1)2016年我国科研人员研制出一种“可呼吸CO”的电池,放电时该电池“吸收
2
CO ”,充电时该电池“放出CO”。放电时,金属钠和CO 发生置换反应生成一种非金属
,2 2 2
单质和一种常见的盐,写出此反应的化学方程式_________。
(2)2018年5月,某杂志介绍了我国的项研究成果:在一种新催化剂作用下可实现二氧
化碳高效转化为甲醇,相关反应如图所示,参加反应的甲和乙的分子个数之比为
_________。
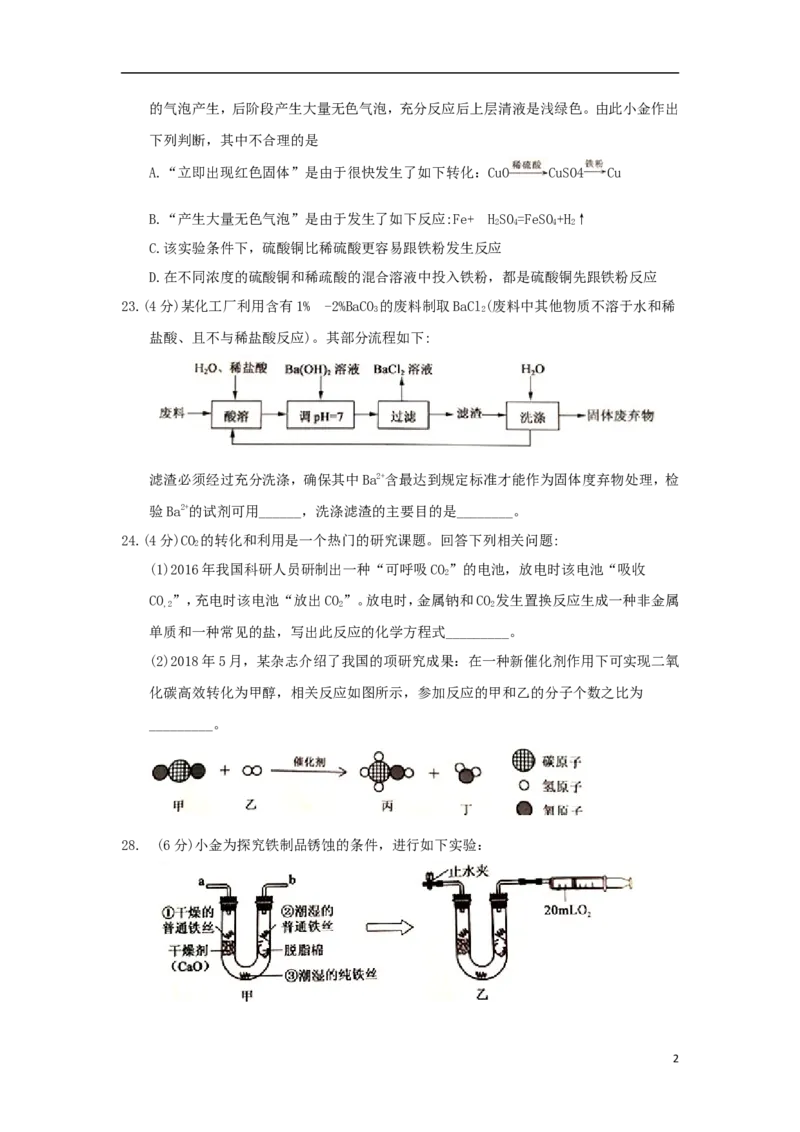
28. (6分)小金为探究铁制品锈蚀的条件,进行如下实验:
2步骤1:利用图甲所示装置,将干燥的O 从导管a通入U形管(装置气密性良好.药品如
2
图所示);待U形管内充满O 后,在导管b处连接一活塞推至底部的注射器收集20mLO
2 2
后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 现象
①干燥的普通铁丝 没有明显变化
②潮湿的普通铁丝 较多红褐色锈斑
③潮湿的纯铁丝 没有明显变化
(1)步骤1中,检查U形管内是否已充满O 的方法是_______。
2
(2)铁制品锈蚀的条件之一是需要 O,在此实验中能支持此条件的证据是_____。
2
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是________。
29.(8分)碱式碳酸锌[Zn(OH)(CO)]是制备功能材料ZnO的原料,其化学反应表达式为:
x y 3 z
Zn(OH)(CO) ZnO+CO↑+HO(x、y、z为正整数)。小金设计了图甲所示装置对碱式
x y 3 z 2 2
碳酸锌的组成进行探究(装置气密性良好,药品足量,实验操作正确):
(1)图甲中装置B的作用是___________。
(2)查阅资料发现在不同温度条件下充分加热等质量的碱式碳酸锌样品,剩余固体的质
量与加热温度的关系如图乙所示。实验中加热时,热分解装置的温度至少要达到
______℃(选填“200”、“300”或“100”)。
(3)部分实验步骤为:“……加热前先通人N 排尽装置内的空气,关闭通入N 的活塞,
2 2
……控制一定温度下加热……”。实验过程中可根据_____现象判断碱式碳酸锌样品已
完
36.(4分)用“盐酸——硫化钡法”生产BaCl 会放出有毒气体HS(其水溶液有酸性),可用
2 2
NaOH吸收HS制取NaS进行处理。下表为HS回收工艺的各项生产成本:
2 2 2
表 HS回收工艺的各项生产成本
2
项目 单价(元/吨)
NaOH 2500
3NaS 5000
2
辅助费用(以处理1吨HS计) 1114
2
(1)工业处理尾气需考虑经济效益和社会效益,根据上述资料分析,单从经济效益考虑
这种处理HS的方法是______(选填“盈利”或“亏损”)的。
2
(2)若某化工厂每天要处理10吨HS,需消耗NaOH多少吨? (写出计算过程,结果保留
2
1位小数)
4参考答案
1C 2B 10B 16D 19D
23.(4分)稀硫酸 防止固体废弃物中可溶性钡盐对环境的污染
24. (4分)(1)4Na+3CO2=2Na2CO3+C (2)1:3
28. (6分)
(1)将带火量的木条放置在b导管口.若木条复燃,则证明U形管内已充满O
2
(2)观察到注射器活塞向左移动(或注射器内O 体积减少)
2
(3)水分和金属的内部结构
29. (8分)
(1)吸收反应生成的CO;(2)300
2
(3)一段时间.A装置中的长导管管口不再有气泡冒出;(4)5:6:2
36.(4分)
(1)盈利
(2)23.5吨
5