文档内容
2021年江苏省徐州市中考化学试卷
一.选择题(每小题2分,共20分。每小题只有一个正确选项)
1.(2分)(2021•徐州)下列说法与“珍爱地球,人与自然和谐共生”的理念不相符的
是( )
A.要积极开发利用氢能、太阳能等新能源
B.对生活垃圾要分类,以便回收再利用
C.工业废水、生活污水排入水体不会引起污染
D.固定利用CO 有利于实现“碳中和”
2
2.(2分)(2021•徐州)学习化学要科学使用化学符号。下列叙述正确的是( )
A.氯化镁(MgCl )中含有1个Cl元素
2
B.微粒H、H+的质子数相同但电子数不同
C.空气、地壳中含量最多的元素都是N
D.铝表面致密氧化膜的化学式是3O2Al
3.(2分)(2021•徐州)学习化学要正确认识物质的组成结构和变化。下列说法正确的
是( )
A.钢铁制品锈蚀、CO 制汽水的过程都没有包含化学变化
2
B.陶瓷、有机玻璃都是用途非常广泛的无机非金属材料
C.金刚石和石墨这两种物质中碳原子的排列方式是不同的
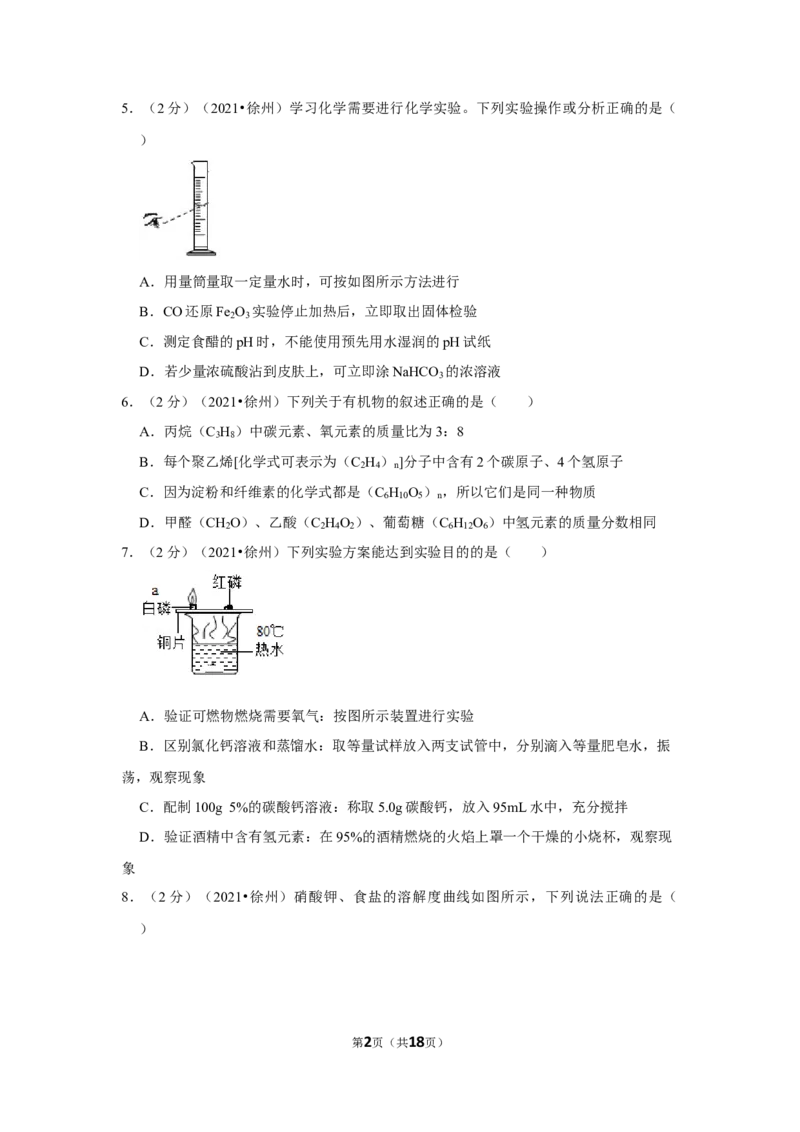
D.如图所示,从蜡烛火焰中引出的“白烟”属于纯净物
4.(2分)(2021•徐州)已知H S是一种生命体系信号分子,它在O 中燃烧的化学方程
2 2
式是2H S+3O 2X+2H O。下列说法正确的是( )
2 2 2
A.该反应过程中放出热量
B.H S中硫元素的化合价是﹣1
2
C.该反应体现O 的可燃性
2
D.大量X进入空气不会引起酸雨
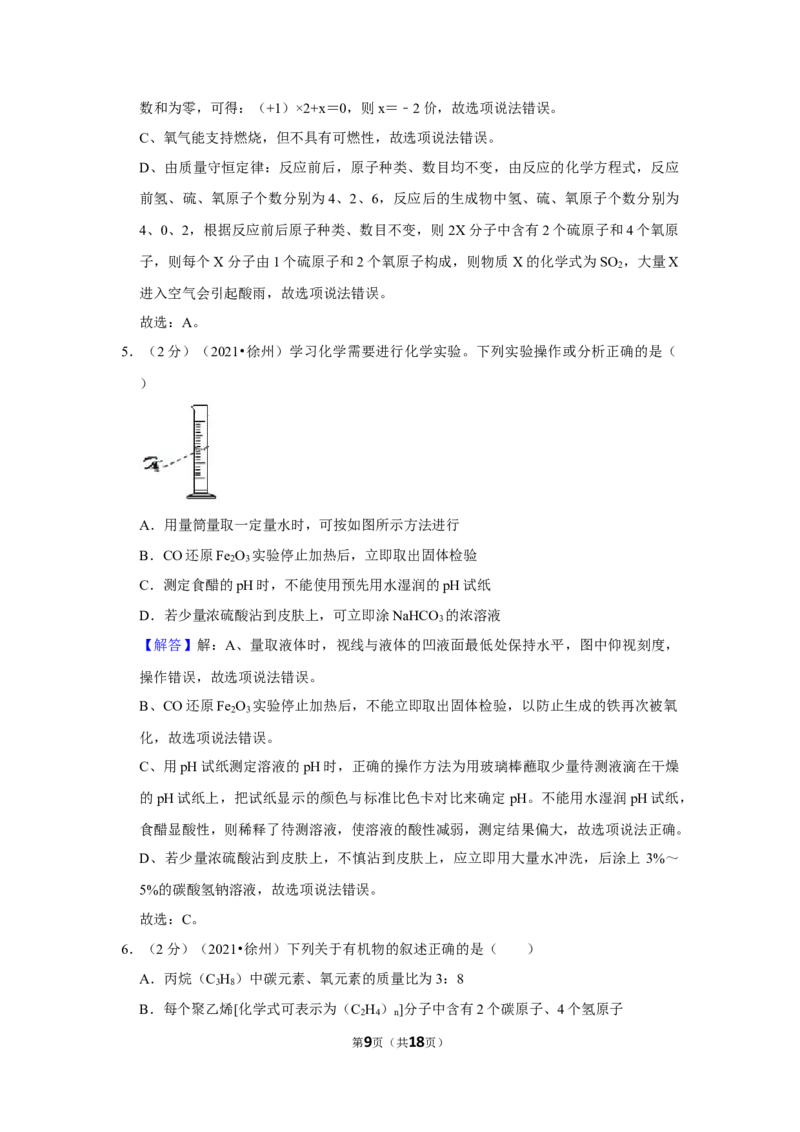
第1页(共18页)5.(2分)(2021•徐州)学习化学需要进行化学实验。下列实验操作或分析正确的是(
)
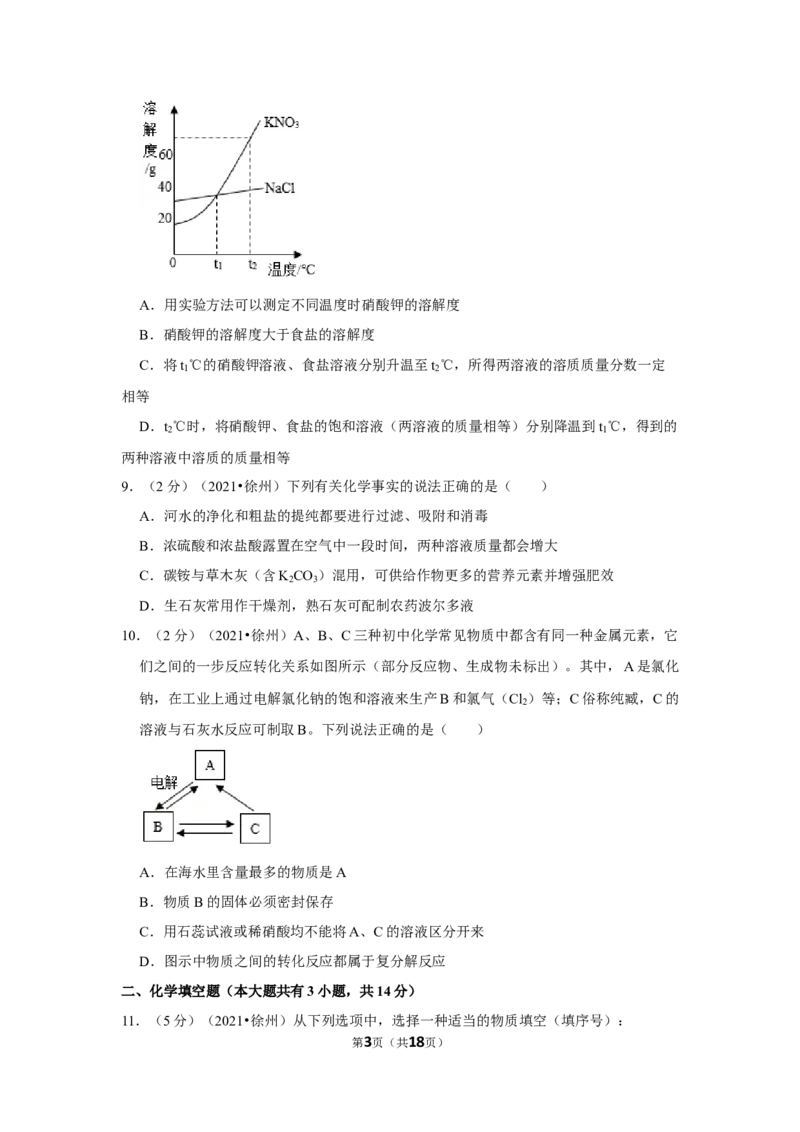
A.用量筒量取一定量水时,可按如图所示方法进行
B.CO还原Fe O 实验停止加热后,立即取出固体检验
2 3
C.测定食醋的pH时,不能使用预先用水湿润的pH试纸
D.若少量浓硫酸沾到皮肤上,可立即涂NaHCO 的浓溶液
3
6.(2分)(2021•徐州)下列关于有机物的叙述正确的是( )
A.丙烷(C H )中碳元素、氧元素的质量比为3:8
3 8
B.每个聚乙烯[化学式可表示为(C H ) ]分子中含有2个碳原子、4个氢原子
2 4 n
C.因为淀粉和纤维素的化学式都是(C H O ) ,所以它们是同一种物质
6 10 5 n
D.甲醛(CH O)、乙酸(C H O )、葡萄糖(C H O )中氢元素的质量分数相同
2 2 4 2 6 12 6
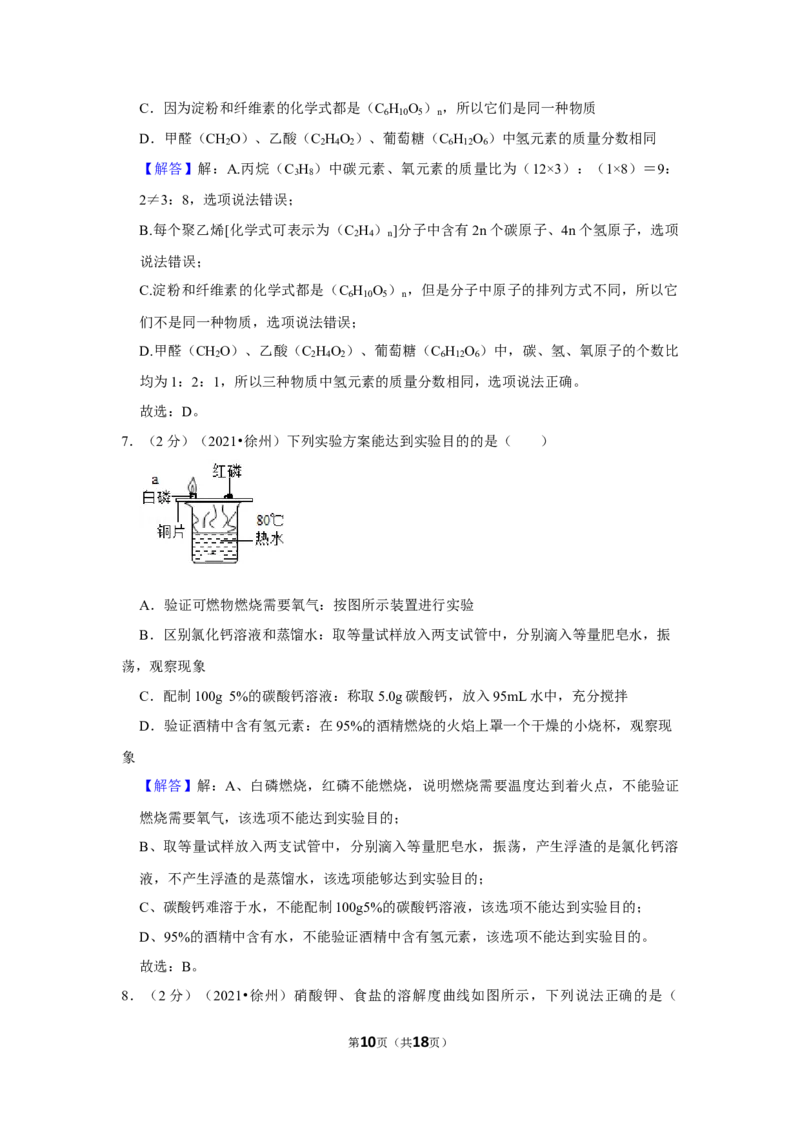
7.(2分)(2021•徐州)下列实验方案能达到实验目的的是( )
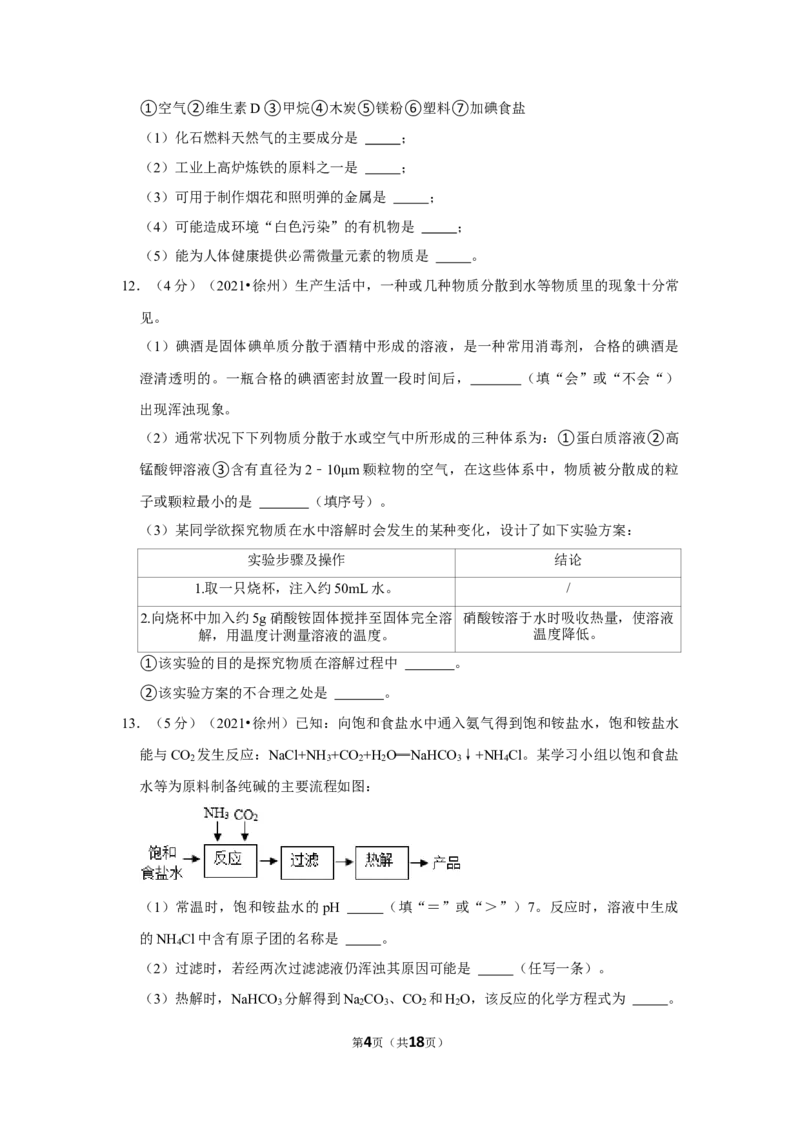
A.验证可燃物燃烧需要氧气:按图所示装置进行实验
B.区别氯化钙溶液和蒸馏水:取等量试样放入两支试管中,分别滴入等量肥皂水,振
荡,观察现象
C.配制100g 5%的碳酸钙溶液:称取5.0g碳酸钙,放入95mL水中,充分搅拌
D.验证酒精中含有氢元素:在95%的酒精燃烧的火焰上罩一个干燥的小烧杯,观察现
象
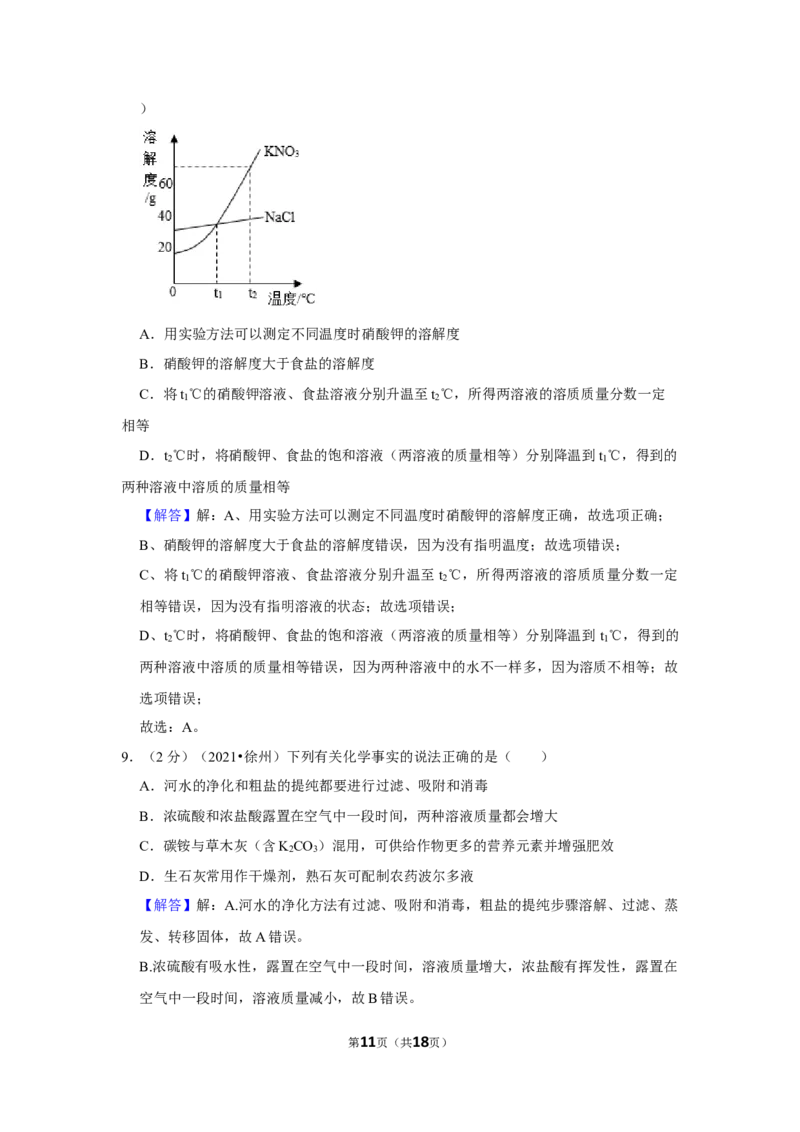
8.(2分)(2021•徐州)硝酸钾、食盐的溶解度曲线如图所示,下列说法正确的是(
)
第2页(共18页)A.用实验方法可以测定不同温度时硝酸钾的溶解度
B.硝酸钾的溶解度大于食盐的溶解度
C.将t ℃的硝酸钾溶液、食盐溶液分别升温至t ℃,所得两溶液的溶质质量分数一定
1 2
相等
D.t ℃时,将硝酸钾、食盐的饱和溶液(两溶液的质量相等)分别降温到t ℃,得到的
2 1
两种溶液中溶质的质量相等
9.(2分)(2021•徐州)下列有关化学事实的说法正确的是( )
A.河水的净化和粗盐的提纯都要进行过滤、吸附和消毒
B.浓硫酸和浓盐酸露置在空气中一段时间,两种溶液质量都会增大
C.碳铵与草木灰(含K CO )混用,可供给作物更多的营养元素并增强肥效
2 3
D.生石灰常用作干燥剂,熟石灰可配制农药波尔多液
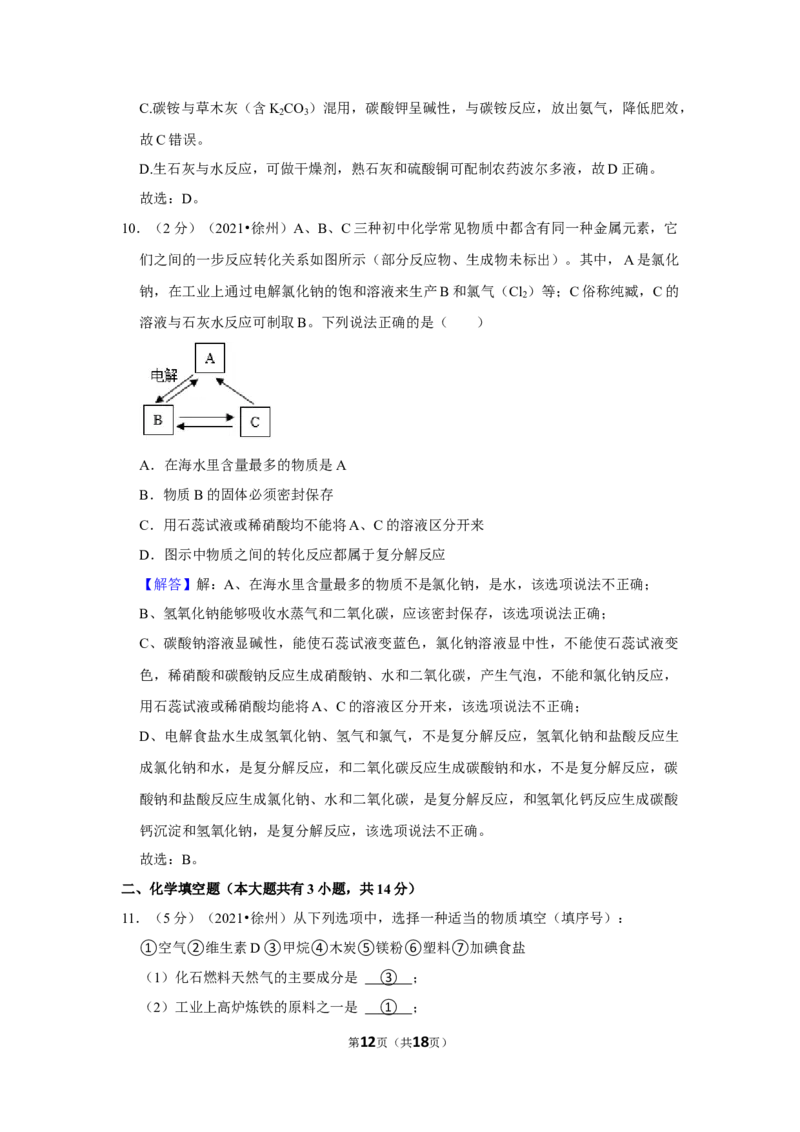
10.(2分)(2021•徐州)A、B、C三种初中化学常见物质中都含有同一种金属元素,它
们之间的一步反应转化关系如图所示(部分反应物、生成物未标出)。其中,A是氯化
钠,在工业上通过电解氯化钠的饱和溶液来生产B和氯气(Cl )等;C俗称纯臧,C的
2
溶液与石灰水反应可制取B。下列说法正确的是( )
A.在海水里含量最多的物质是A
B.物质B的固体必须密封保存
C.用石蕊试液或稀硝酸均不能将A、C的溶液区分开来
D.图示中物质之间的转化反应都属于复分解反应
二、化学填空题(本大题共有3小题,共14分)
11.(5分)(2021•徐州)从下列选项中,选择一种适当的物质填空(填序号):
第3页(共18页)①空气②维生素D③甲烷④木炭⑤镁粉⑥塑料⑦加碘食盐
(1)化石燃料天然气的主要成分是 ;
(2)工业上高炉炼铁的原料之一是 ;
(3)可用于制作烟花和照明弹的金属是 ;
(4)可能造成环境“白色污染”的有机物是 ;
(5)能为人体健康提供必需微量元素的物质是 。
12.(4分)(2021•徐州)生产生活中,一种或几种物质分散到水等物质里的现象十分常
见。
(1)碘酒是固体碘单质分散于酒精中形成的溶液,是一种常用消毒剂,合格的碘酒是
澄清透明的。一瓶合格的碘酒密封放置一段时间后, (填“会”或“不会“)
出现浑浊现象。
(2)通常状况下下列物质分散于水或空气中所形成的三种体系为:①蛋白质溶液②高
锰酸钾溶液③含有直径为2﹣10 m颗粒物的空气,在这些体系中,物质被分散成的粒
子或颗粒最小的是 (填序μ号)。
(3)某同学欲探究物质在水中溶解时会发生的某种变化,设计了如下实验方案:
实验步骤及操作 结论
1.取一只烧杯,注入约50mL水。 /
2.向烧杯中加入约5g硝酸铵固体搅拌至固体完全溶 硝酸铵溶于水时吸收热量,使溶液
解,用温度计测量溶液的温度。 温度降低。
①该实验的目的是探究物质在溶解过程中 。
②该实验方案的不合理之处是 。
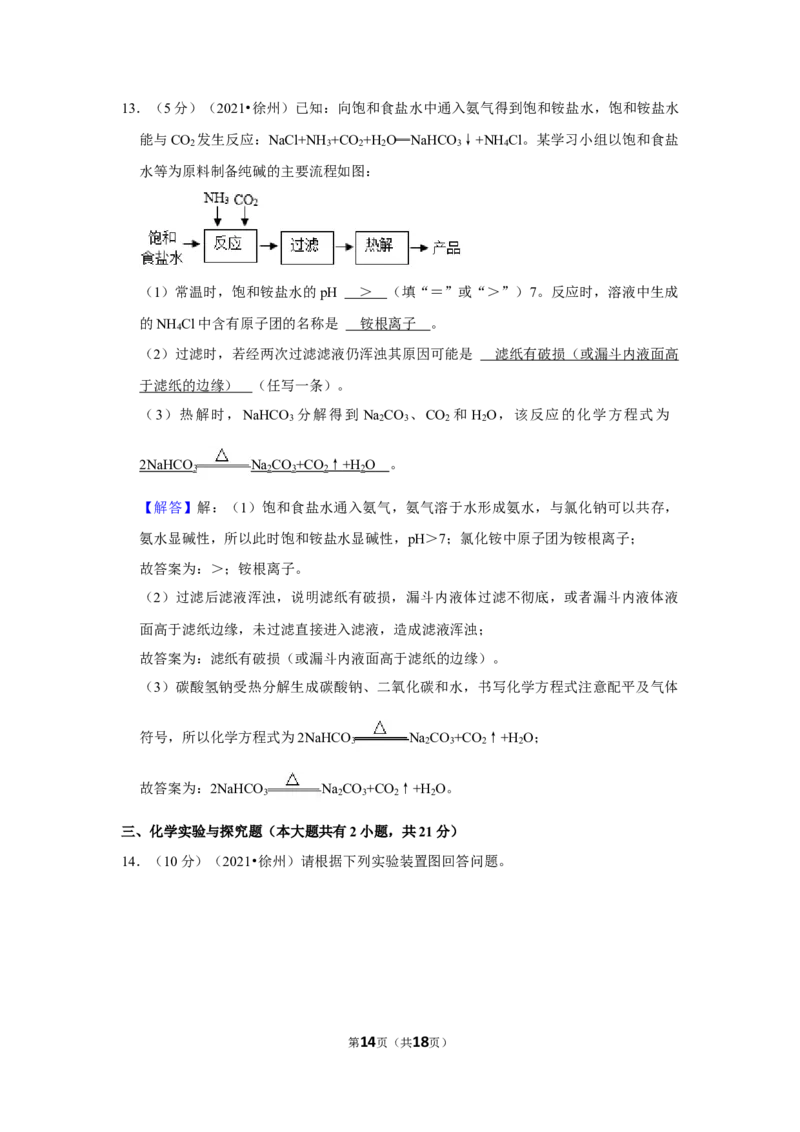
13.(5分)(2021•徐州)已知:向饱和食盐水中通入氨气得到饱和铵盐水,饱和铵盐水
能与CO 发生反应:NaCl+NH +CO +H O═NaHCO ↓+NH Cl。某学习小组以饱和食盐
2 3 2 2 3 4
水等为原料制备纯碱的主要流程如图:
(1)常温时,饱和铵盐水的pH (填“=”或“>”)7。反应时,溶液中生成
的NH Cl中含有原子团的名称是 。
4
(2)过滤时,若经两次过滤滤液仍浑浊其原因可能是 (任写一条)。
(3)热解时,NaHCO 分解得到Na CO 、CO 和H O,该反应的化学方程式为 。
3 2 3 2 2
第4页(共18页)三、化学实验与探究题(本大题共有2小题,共21分)
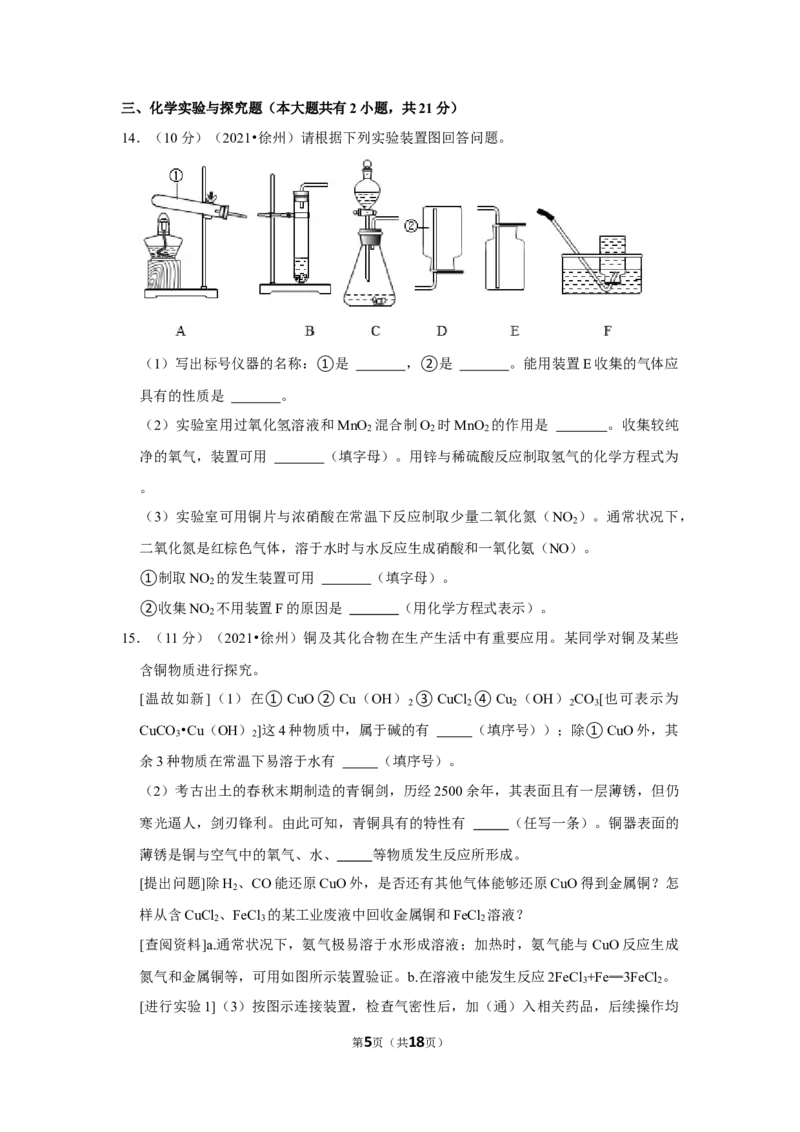
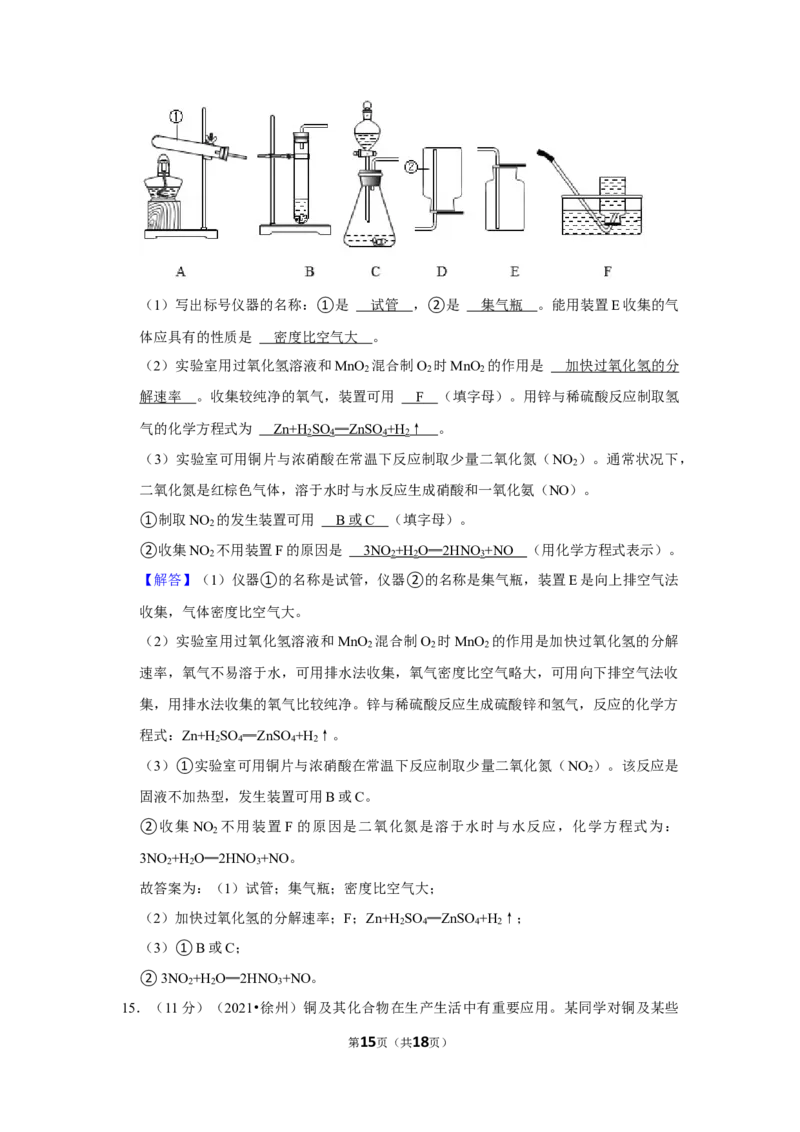
14.(10分)(2021•徐州)请根据下列实验装置图回答问题。
(1)写出标号仪器的名称:①是 ,②是 。能用装置E收集的气体应
具有的性质是 。
(2)实验室用过氧化氢溶液和MnO 混合制O 时MnO 的作用是 。收集较纯
2 2 2
净的氧气,装置可用 (填字母)。用锌与稀硫酸反应制取氢气的化学方程式为
。
(3)实验室可用铜片与浓硝酸在常温下反应制取少量二氧化氮(NO )。通常状况下,
2
二氧化氮是红棕色气体,溶于水时与水反应生成硝酸和一氧化氨(NO)。
①制取NO 的发生装置可用 (填字母)。
2
②收集NO 不用装置F的原因是 (用化学方程式表示)。
2
15.(11分)(2021•徐州)铜及其化合物在生产生活中有重要应用。某同学对铜及某些
含铜物质进行探究。
[温故如新](1)在①CuO②Cu(OH) ③CuCl ④Cu (OH) CO [也可表示为
2 2 2 2 3
CuCO •Cu(OH) ]这4种物质中,属于碱的有 (填序号));除①CuO外,其
3 2
余3种物质在常温下易溶于水有 (填序号)。
(2)考古出土的春秋末期制造的青铜剑,历经2500余年,其表面且有一层薄锈,但仍
寒光逼人,剑刃锋利。由此可知,青铜具有的特性有 (任写一条)。铜器表面的
薄锈是铜与空气中的氧气、水、 等物质发生反应所形成。
[提出问题]除H 、CO能还原CuO外,是否还有其他气体能够还原CuO得到金属铜?怎
2
样从含CuCl 、FeCl 的某工业废液中回收金属铜和FeCl 溶液?
2 3 2
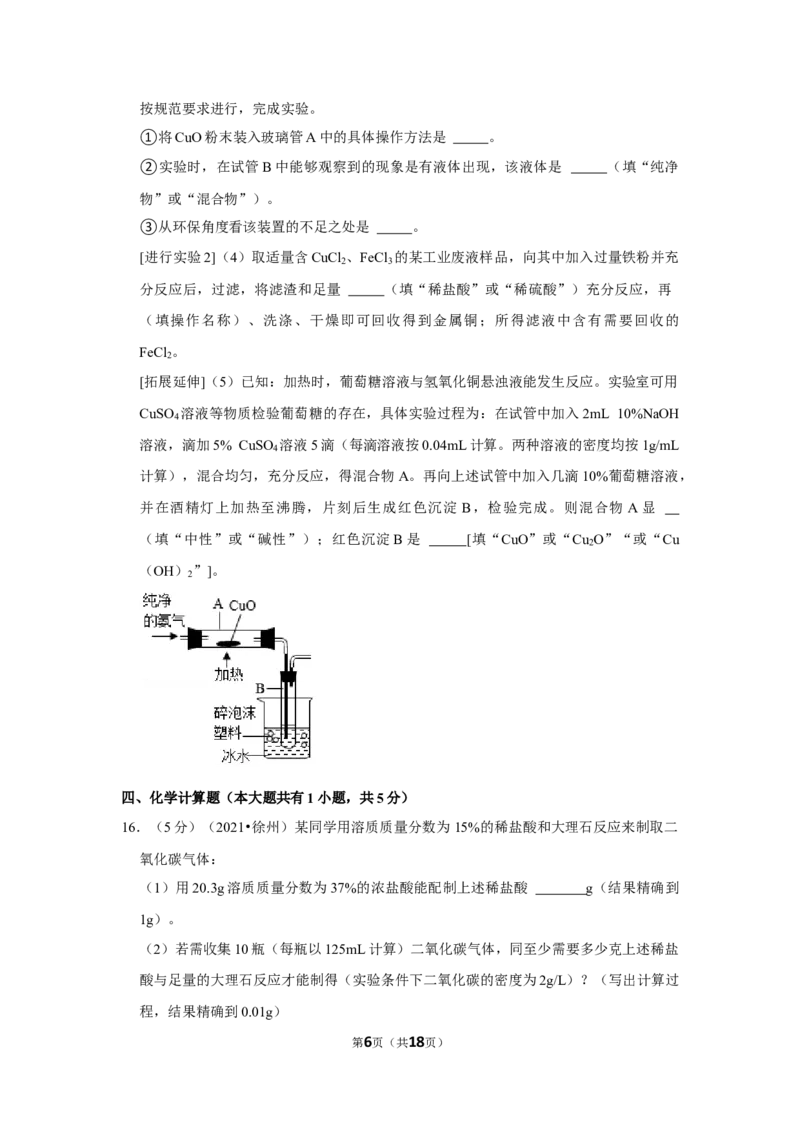
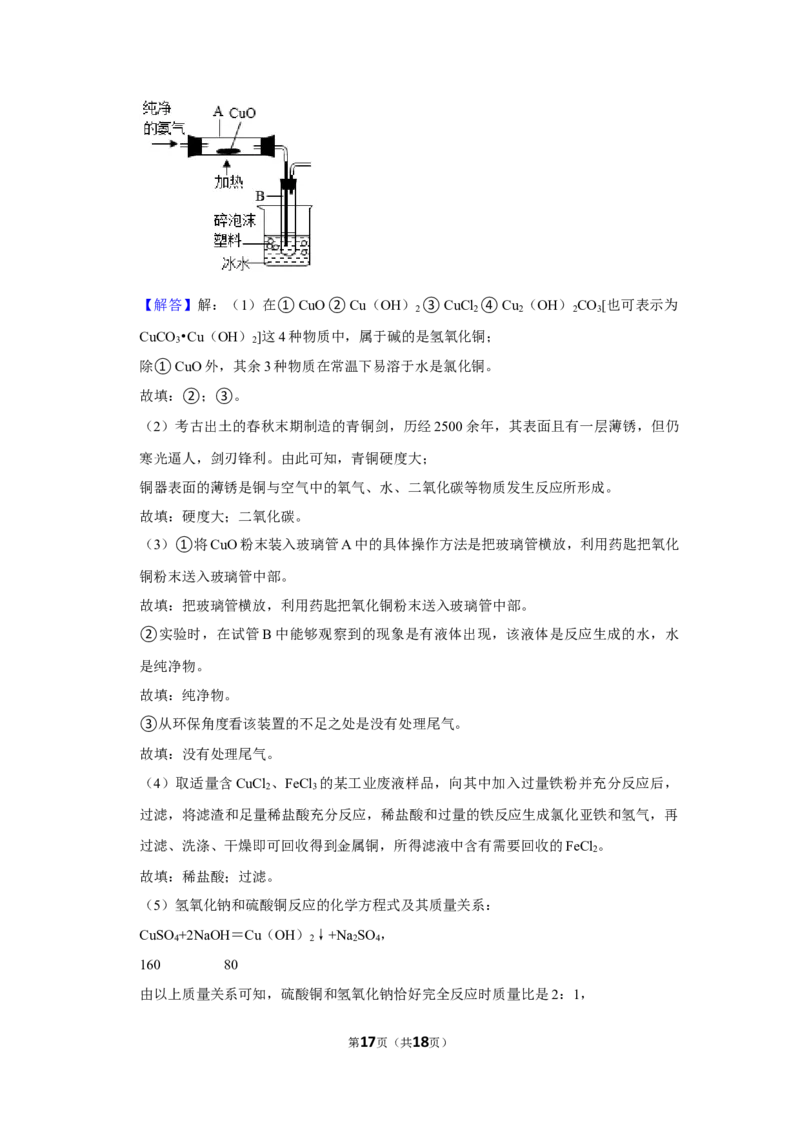
[查阅资料]a.通常状况下,氨气极易溶于水形成溶液;加热时,氨气能与 CuO反应生成
氮气和金属铜等,可用如图所示装置验证。b.在溶液中能发生反应2FeCl +Fe═3FeCl 。
3 2
[进行实验1](3)按图示连接装置,检查气密性后,加(通)入相关药品,后续操作均
第5页(共18页)按规范要求进行,完成实验。
①将CuO粉末装入玻璃管A中的具体操作方法是 。
②实验时,在试管B中能够观察到的现象是有液体出现,该液体是 (填“纯净
物”或“混合物”)。
③从环保角度看该装置的不足之处是 。
[进行实验2](4)取适量含CuCl 、FeCl 的某工业废液样品,向其中加入过量铁粉并充
2 3
分反应后,过滤,将滤渣和足量 (填“稀盐酸”或“稀硫酸”)充分反应,再
(填操作名称)、洗涤、干燥即可回收得到金属铜;所得滤液中含有需要回收的
FeCl 。
2
[拓展延伸](5)已知:加热时,葡萄糖溶液与氢氧化铜悬浊液能发生反应。实验室可用
CuSO 溶液等物质检验葡萄糖的存在,具体实验过程为:在试管中加入2mL 10%NaOH
4
溶液,滴加5% CuSO 溶液5滴(每滴溶液按0.04mL计算。两种溶液的密度均按1g/mL
4
计算),混合均匀,充分反应,得混合物A。再向上述试管中加入几滴10%葡萄糖溶液,
并在酒精灯上加热至沸腾,片刻后生成红色沉淀 B,检验完成。则混合物 A显
(填“中性”或“碱性”);红色沉淀B是 [填“CuO”或“Cu O”“或“Cu
2
(OH) ”]。
2
四、化学计算题(本大题共有1小题,共5分)
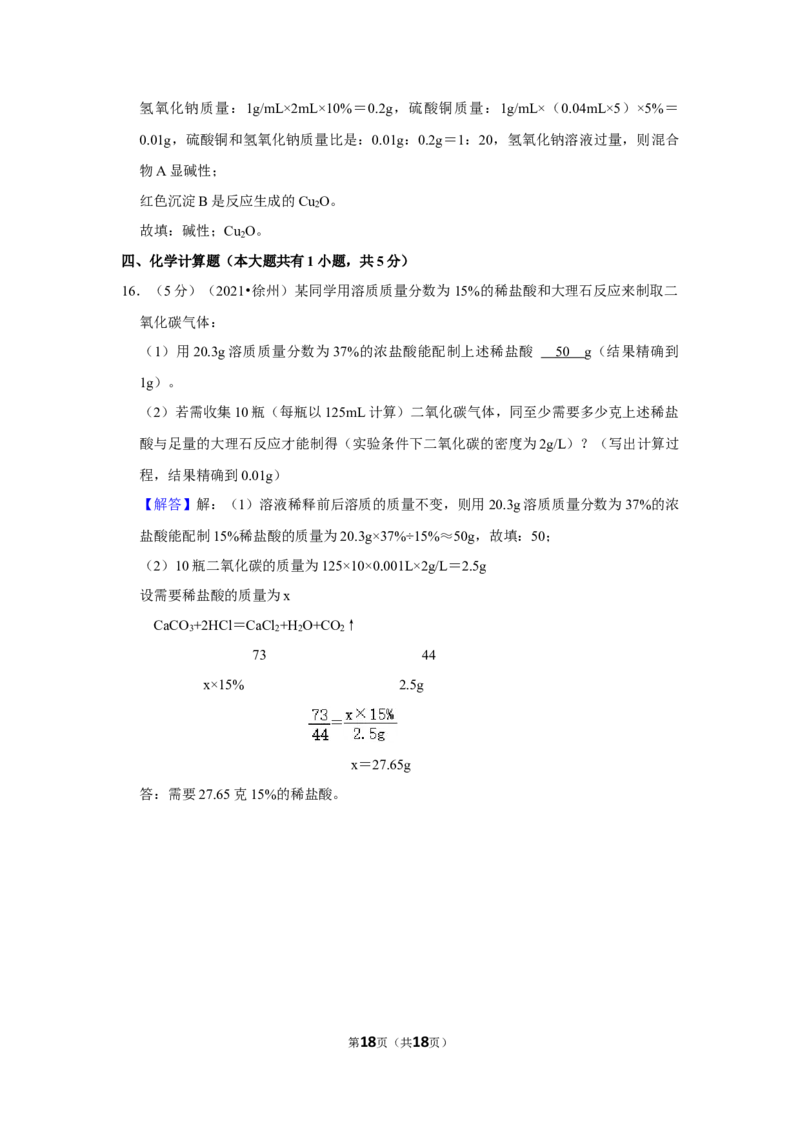
16.(5分)(2021•徐州)某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二
氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸 g(结果精确到
1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,同至少需要多少克上述稀盐
酸与足量的大理石反应才能制得(实验条件下二氧化碳的密度为2g/L)?(写出计算过
程,结果精确到0.01g)
第6页(共18页)2021年江苏省徐州市中考化学试卷
参考答案与试题解析
一.选择题(每小题2分,共20分。每小题只有一个正确选项)
1.(2分)(2021•徐州)下列说法与“珍爱地球,人与自然和谐共生”的理念不相符的
是( )
A.要积极开发利用氢能、太阳能等新能源
B.对生活垃圾要分类,以便回收再利用
C.工业废水、生活污水排入水体不会引起污染
D.固定利用CO 有利于实现“碳中和”
2
【解答】解:A、要积极开发利用氢能、太阳能等新能源,能减少空气污染,与“珍爱
地球,人与自然和谐共生”的理念相符,故选项错误。
B、对生活垃圾要分类,有利于节约资源、减少污染,与“珍爱地球,人与自然和谐共
生”的理念相符,故选项错误。
C、工业废水、生活污水排入水体,会引起水体污染,与“珍爱地球,人与自然和谐共
生”的理念不相符,故选项正确。
D、固定利用CO ,有利于减缓温室效应,实现“碳中和”,与“珍爱地球,人与自然
2
和谐共生”的理念相符,故选项错误。
故选:C。
2.(2分)(2021•徐州)学习化学要科学使用化学符号。下列叙述正确的是( )
A.氯化镁(MgCl )中含有1个Cl元素
2
B.微粒H、H+的质子数相同但电子数不同
C.空气、地壳中含量最多的元素都是N
D.铝表面致密氧化膜的化学式是3O2Al
【解答】解:A、元素只讲种类,不讲个数,故选项说法错误。
B、氢原子失去1个电子形成氢离子,微粒H、H+的质子数相同但电子数不同,故选项
说法正确。
C、空气中含量最多的气体是氮气,氮气是由氮元素组成的,所以空气中含量最多的元
素是氮元素,地壳中含量最多的元素是氧元素,故选项说法错误。
D、铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一
第7页(共18页)步被氧化,氧化铝的化学式为Al O ,故选项说法错误。
2 3
故选:B。
3.(2分)(2021•徐州)学习化学要正确认识物质的组成结构和变化。下列说法正确的
是( )
A.钢铁制品锈蚀、CO 制汽水的过程都没有包含化学变化
2
B.陶瓷、有机玻璃都是用途非常广泛的无机非金属材料
C.金刚石和石墨这两种物质中碳原子的排列方式是不同的
D.如图所示,从蜡烛火焰中引出的“白烟”属于纯净物
【解答】解:A、钢铁制品锈蚀,铁与氧气、水反应生成铁锈,CO 制汽水的过程,二
2
氧化碳与水反应生成碳酸,都包含化学变化,故选项说法错误。
B、陶瓷是用瓷土烧制而成的,属于无机非金属材料;有机玻璃是化学合成的一种塑料,
外观颇似玻璃,属于合成材料,故选项说法错误。
C、金刚石和石墨这两种物质中碳原子的排列方式是不同的,它们的物理性质有很大差
异,故选项说法正确。
D、从蜡烛火焰中引出的“白烟”,是石蜡蒸气凝成的石蜡固体,石蜡是一种烃类混合
物,主要成分是固体烷烃,故选项说法错误。
故选:C。
4.(2分)(2021•徐州)已知H S是一种生命体系信号分子,它在O 中燃烧的化学方程
2 2
式是2H S+3O 2X+2H O。下列说法正确的是( )
2 2 2
A.该反应过程中放出热量
B.H S中硫元素的化合价是﹣1
2
C.该反应体现O 的可燃性
2
D.大量X进入空气不会引起酸雨
【解答】解:A、由题意,H S能在O 中燃烧,该反应过程中放出热量,故选项说法正
2 2
确。
B、在化合物中氢元素显+1价,设硫元素的化合价是x,根据在化合物中正负化合价代
第8页(共18页)数和为零,可得:(+1)×2+x=0,则x=﹣2价,故选项说法错误。
C、氧气能支持燃烧,但不具有可燃性,故选项说法错误。
D、由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应
前氢、硫、氧原子个数分别为4、2、6,反应后的生成物中氢、硫、氧原子个数分别为
4、0、2,根据反应前后原子种类、数目不变,则2X分子中含有2个硫原子和4个氧原
子,则每个X分子由1个硫原子和2个氧原子构成,则物质X的化学式为SO ,大量X
2
进入空气会引起酸雨,故选项说法错误。
故选:A。
5.(2分)(2021•徐州)学习化学需要进行化学实验。下列实验操作或分析正确的是(
)
A.用量筒量取一定量水时,可按如图所示方法进行
B.CO还原Fe O 实验停止加热后,立即取出固体检验
2 3
C.测定食醋的pH时,不能使用预先用水湿润的pH试纸
D.若少量浓硫酸沾到皮肤上,可立即涂NaHCO 的浓溶液
3
【解答】解:A、量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度,
操作错误,故选项说法错误。
B、CO还原Fe O 实验停止加热后,不能立即取出固体检验,以防止生成的铁再次被氧
2 3
化,故选项说法错误。
C、用pH试纸测定溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥
的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH。不能用水湿润pH试纸,
食醋显酸性,则稀释了待测溶液,使溶液的酸性减弱,测定结果偏大,故选项说法正确。
D、若少量浓硫酸沾到皮肤上,不慎沾到皮肤上,应立即用大量水冲洗,后涂上 3%~
5%的碳酸氢钠溶液,故选项说法错误。
故选:C。
6.(2分)(2021•徐州)下列关于有机物的叙述正确的是( )
A.丙烷(C H )中碳元素、氧元素的质量比为3:8
3 8
B.每个聚乙烯[化学式可表示为(C H ) ]分子中含有2个碳原子、4个氢原子
2 4 n
第9页(共18页)C.因为淀粉和纤维素的化学式都是(C H O ) ,所以它们是同一种物质
6 10 5 n
D.甲醛(CH O)、乙酸(C H O )、葡萄糖(C H O )中氢元素的质量分数相同
2 2 4 2 6 12 6
【解答】解:A.丙烷(C H )中碳元素、氧元素的质量比为(12×3):(1×8)=9:
3 8
2≠3:8,选项说法错误;
B.每个聚乙烯[化学式可表示为(C H ) ]分子中含有2n个碳原子、4n个氢原子,选项
2 4 n
说法错误;
C.淀粉和纤维素的化学式都是(C H O ) ,但是分子中原子的排列方式不同,所以它
6 10 5 n
们不是同一种物质,选项说法错误;
D.甲醛(CH O)、乙酸(C H O )、葡萄糖(C H O )中,碳、氢、氧原子的个数比
2 2 4 2 6 12 6
均为1:2:1,所以三种物质中氢元素的质量分数相同,选项说法正确。
故选:D。
7.(2分)(2021•徐州)下列实验方案能达到实验目的的是( )
A.验证可燃物燃烧需要氧气:按图所示装置进行实验
B.区别氯化钙溶液和蒸馏水:取等量试样放入两支试管中,分别滴入等量肥皂水,振
荡,观察现象
C.配制100g 5%的碳酸钙溶液:称取5.0g碳酸钙,放入95mL水中,充分搅拌
D.验证酒精中含有氢元素:在95%的酒精燃烧的火焰上罩一个干燥的小烧杯,观察现
象
【解答】解:A、白磷燃烧,红磷不能燃烧,说明燃烧需要温度达到着火点,不能验证
燃烧需要氧气,该选项不能达到实验目的;
B、取等量试样放入两支试管中,分别滴入等量肥皂水,振荡,产生浮渣的是氯化钙溶
液,不产生浮渣的是蒸馏水,该选项能够达到实验目的;
C、碳酸钙难溶于水,不能配制100g5%的碳酸钙溶液,该选项不能达到实验目的;
D、95%的酒精中含有水,不能验证酒精中含有氢元素,该选项不能达到实验目的。
故选:B。
8.(2分)(2021•徐州)硝酸钾、食盐的溶解度曲线如图所示,下列说法正确的是(
第10页(共18页))
A.用实验方法可以测定不同温度时硝酸钾的溶解度
B.硝酸钾的溶解度大于食盐的溶解度
C.将t ℃的硝酸钾溶液、食盐溶液分别升温至t ℃,所得两溶液的溶质质量分数一定
1 2
相等
D.t ℃时,将硝酸钾、食盐的饱和溶液(两溶液的质量相等)分别降温到t ℃,得到的
2 1
两种溶液中溶质的质量相等
【解答】解:A、用实验方法可以测定不同温度时硝酸钾的溶解度正确,故选项正确;
B、硝酸钾的溶解度大于食盐的溶解度错误,因为没有指明温度;故选项错误;
C、将t ℃的硝酸钾溶液、食盐溶液分别升温至 t ℃,所得两溶液的溶质质量分数一定
1 2
相等错误,因为没有指明溶液的状态;故选项错误;
D、t ℃时,将硝酸钾、食盐的饱和溶液(两溶液的质量相等)分别降温到 t ℃,得到的
2 1
两种溶液中溶质的质量相等错误,因为两种溶液中的水不一样多,因为溶质不相等;故
选项错误;
故选:A。
9.(2分)(2021•徐州)下列有关化学事实的说法正确的是( )
A.河水的净化和粗盐的提纯都要进行过滤、吸附和消毒
B.浓硫酸和浓盐酸露置在空气中一段时间,两种溶液质量都会增大
C.碳铵与草木灰(含K CO )混用,可供给作物更多的营养元素并增强肥效
2 3
D.生石灰常用作干燥剂,熟石灰可配制农药波尔多液
【解答】解:A.河水的净化方法有过滤、吸附和消毒,粗盐的提纯步骤溶解、过滤、蒸
发、转移固体,故A错误。
B.浓硫酸有吸水性,露置在空气中一段时间,溶液质量增大,浓盐酸有挥发性,露置在
空气中一段时间,溶液质量减小,故B错误。
第11页(共18页)C.碳铵与草木灰(含K CO )混用,碳酸钾呈碱性,与碳铵反应,放出氨气,降低肥效,
2 3
故C错误。
D.生石灰与水反应,可做干燥剂,熟石灰和硫酸铜可配制农药波尔多液,故D正确。
故选:D。
10.(2分)(2021•徐州)A、B、C三种初中化学常见物质中都含有同一种金属元素,它
们之间的一步反应转化关系如图所示(部分反应物、生成物未标出)。其中,A是氯化
钠,在工业上通过电解氯化钠的饱和溶液来生产B和氯气(Cl )等;C俗称纯臧,C的
2
溶液与石灰水反应可制取B。下列说法正确的是( )
A.在海水里含量最多的物质是A
B.物质B的固体必须密封保存
C.用石蕊试液或稀硝酸均不能将A、C的溶液区分开来
D.图示中物质之间的转化反应都属于复分解反应
【解答】解:A、在海水里含量最多的物质不是氯化钠,是水,该选项说法不正确;
B、氢氧化钠能够吸收水蒸气和二氧化碳,应该密封保存,该选项说法正确;
C、碳酸钠溶液显碱性,能使石蕊试液变蓝色,氯化钠溶液显中性,不能使石蕊试液变
色,稀硝酸和碳酸钠反应生成硝酸钠、水和二氧化碳,产生气泡,不能和氯化钠反应,
用石蕊试液或稀硝酸均能将A、C的溶液区分开来,该选项说法不正确;
D、电解食盐水生成氢氧化钠、氢气和氯气,不是复分解反应,氢氧化钠和盐酸反应生
成氯化钠和水,是复分解反应,和二氧化碳反应生成碳酸钠和水,不是复分解反应,碳
酸钠和盐酸反应生成氯化钠、水和二氧化碳,是复分解反应,和氢氧化钙反应生成碳酸
钙沉淀和氢氧化钠,是复分解反应,该选项说法不正确。
故选:B。
二、化学填空题(本大题共有3小题,共14分)
11.(5分)(2021•徐州)从下列选项中,选择一种适当的物质填空(填序号):
①空气②维生素D③甲烷④木炭⑤镁粉⑥塑料⑦加碘食盐
(1)化石燃料天然气的主要成分是 ③ ;
(2)工业上高炉炼铁的原料之一是 ① ;
第12页(共18页)(3)可用于制作烟花和照明弹的金属是 ⑤ ;
(4)可能造成环境“白色污染”的有机物是 ⑥ ;
(5)能为人体健康提供必需微量元素的物质是 ⑦ 。
【解答】解:(1)化石燃料天然气的主要成分是甲烷;故填:③;
(2)空气是工业上高炉炼铁的原料之一;故填:①;
(3)镁粉燃烧时会发出耀眼的白光,所以镁粉是可用于制作烟花和照明弹的金属;故
填:⑤;
(4)塑料是一种有机物,在自然界中很难降解,可能造成“白色污染”;故填:⑥;
(5)加碘食盐中含有碘元素,碘元素是人体必需微量元素;故填:⑦。
12.(4分)(2021•徐州)生产生活中,一种或几种物质分散到水等物质里的现象十分常
见。
(1)碘酒是固体碘单质分散于酒精中形成的溶液,是一种常用消毒剂,合格的碘酒是
澄清透明的。一瓶合格的碘酒密封放置一段时间后, 不会 (填“会”或“不会“)
出现浑浊现象。
(2)通常状况下下列物质分散于水或空气中所形成的三种体系为:①蛋白质溶液②高
锰酸钾溶液③含有直径为2﹣10 m颗粒物的空气,在这些体系中,物质被分散成的粒
子或颗粒最小的是 ② (填序μ号)。
(3)某同学欲探究物质在水中溶解时会发生的某种变化,设计了如下实验方案:
实验步骤及操作 结论
1.取一只烧杯,注入约50mL水。 /
2.向烧杯中加入约5g硝酸铵固体搅拌至固体完全溶 硝酸铵溶于水时吸收热量,使溶液
解,用温度计测量溶液的温度。 温度降低。
①该实验的目的是探究物质在溶解过程中 溶液温度的变化情况 。
②该实验方案的不合理之处是 没有设计一个对比实验 。
【解答】解:(1)溶液具有均一性和稳定性,所以一瓶合格的碘酒密封放置一段时间
后,不会出现浑浊现象;故填:不会;
(2)在溶液中,溶质是以分子或离子的形式存在,溶剂是以分子的性质存在,所以在
这些体系中,物质被分散成的粒子或颗粒最小的是②;故填:②;
(3)①由实验过程可知,该实验的目的是探究物质在溶解过程中溶液温度的变化情况;
故填:溶液温度的变化情况;
②该实验方案的不合理之处是没有设计一个对比实验;故填:没有设计一个对比实验。
第13页(共18页)13.(5分)(2021•徐州)已知:向饱和食盐水中通入氨气得到饱和铵盐水,饱和铵盐水
能与CO 发生反应:NaCl+NH +CO +H O═NaHCO ↓+NH Cl。某学习小组以饱和食盐
2 3 2 2 3 4
水等为原料制备纯碱的主要流程如图:
(1)常温时,饱和铵盐水的pH > (填“=”或“>”)7。反应时,溶液中生成
的NH Cl中含有原子团的名称是 铵根离子 。
4
(2)过滤时,若经两次过滤滤液仍浑浊其原因可能是 滤纸有破损(或漏斗内液面高
于滤纸的边缘) (任写一条)。
(3)热解时,NaHCO 分解得到 Na CO 、CO 和 H O,该反应的化学方程式为
3 2 3 2 2
2NaHCO Na CO +CO ↑ +H O 。
3 2 3 2 2
【解答】解:(1)饱和食盐水通入氨气,氨气溶于水形成氨水,与氯化钠可以共存,
氨水显碱性,所以此时饱和铵盐水显碱性,pH>7;氯化铵中原子团为铵根离子;
故答案为:>;铵根离子。
(2)过滤后滤液浑浊,说明滤纸有破损,漏斗内液体过滤不彻底,或者漏斗内液体液
面高于滤纸边缘,未过滤直接进入滤液,造成滤液浑浊;
故答案为:滤纸有破损(或漏斗内液面高于滤纸的边缘)。
(3)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,书写化学方程式注意配平及气体
符号,所以化学方程式为2NaHCO Na CO +CO ↑+H O;
3 2 3 2 2
故答案为:2NaHCO Na CO +CO ↑+H O。
3 2 3 2 2
三、化学实验与探究题(本大题共有2小题,共21分)
14.(10分)(2021•徐州)请根据下列实验装置图回答问题。
第14页(共18页)(1)写出标号仪器的名称:①是 试管 ,②是 集气瓶 。能用装置E收集的气
体应具有的性质是 密度比空气大 。
(2)实验室用过氧化氢溶液和MnO 混合制O 时MnO 的作用是 加快过氧化氢的分
2 2 2
解速率 。收集较纯净的氧气,装置可用 F (填字母)。用锌与稀硫酸反应制取氢
气的化学方程式为 Zn+H SO ═ ZnSO +H ↑ 。
2 4 4 2
(3)实验室可用铜片与浓硝酸在常温下反应制取少量二氧化氮(NO )。通常状况下,
2
二氧化氮是红棕色气体,溶于水时与水反应生成硝酸和一氧化氨(NO)。
①制取NO 的发生装置可用 B 或 C (填字母)。
2
②收集NO 不用装置F的原因是 3NO +H O ═ 2HNO +NO (用化学方程式表示)。
2 2 2 3
【解答】(1)仪器①的名称是试管,仪器②的名称是集气瓶,装置E是向上排空气法
收集,气体密度比空气大。
(2)实验室用过氧化氢溶液和MnO 混合制O 时MnO 的作用是加快过氧化氢的分解
2 2 2
速率,氧气不易溶于水,可用排水法收集,氧气密度比空气略大,可用向下排空气法收
集,用排水法收集的氧气比较纯净。锌与稀硫酸反应生成硫酸锌和氢气,反应的化学方
程式:Zn+H SO ═ZnSO +H ↑。
2 4 4 2
(3)①实验室可用铜片与浓硝酸在常温下反应制取少量二氧化氮(NO )。该反应是
2
固液不加热型,发生装置可用B或C。
②收集NO 不用装置 F的原因是二氧化氮是溶于水时与水反应,化学方程式为:
2
3NO +H O═2HNO +NO。
2 2 3
故答案为:(1)试管;集气瓶;密度比空气大;
(2)加快过氧化氢的分解速率;F;Zn+H SO ═ZnSO +H ↑;
2 4 4 2
(3)①B或C;
②3NO +H O═2HNO +NO。
2 2 3
15.(11分)(2021•徐州)铜及其化合物在生产生活中有重要应用。某同学对铜及某些
第15页(共18页)含铜物质进行探究。
[温故如新](1)在①CuO②Cu(OH) ③CuCl ④Cu (OH) CO [也可表示为
2 2 2 2 3
CuCO •Cu(OH) ]这4种物质中,属于碱的有 ② (填序号));除①CuO外,
3 2
其余3种物质在常温下易溶于水有 ③ (填序号)。
(2)考古出土的春秋末期制造的青铜剑,历经2500余年,其表面且有一层薄锈,但仍
寒光逼人,剑刃锋利。由此可知,青铜具有的特性有 硬度大 (任写一条)。铜器
表面的薄锈是铜与空气中的氧气、水、 二氧化碳 等物质发生反应所形成。
[提出问题]除H 、CO能还原CuO外,是否还有其他气体能够还原CuO得到金属铜?怎
2
样从含CuCl 、FeCl 的某工业废液中回收金属铜和FeCl 溶液?
2 3 2
[查阅资料]a.通常状况下,氨气极易溶于水形成溶液;加热时,氨气能与 CuO反应生成
氮气和金属铜等,可用如图所示装置验证。b.在溶液中能发生反应2FeCl +Fe═3FeCl 。
3 2
[进行实验1](3)按图示连接装置,检查气密性后,加(通)入相关药品,后续操作均
按规范要求进行,完成实验。
①将CuO粉末装入玻璃管A中的具体操作方法是 把玻璃管横放,利用药匙把氧化铜
粉末送入玻璃管中部 。
②实验时,在试管B中能够观察到的现象是有液体出现,该液体是 纯净物 (填
“纯净物”或“混合物”)。
③从环保角度看该装置的不足之处是 没有处理尾气 。
[进行实验2](4)取适量含CuCl 、FeCl 的某工业废液样品,向其中加入过量铁粉并充
2 3
分反应后,过滤,将滤渣和足量 稀盐酸 (填“稀盐酸”或“稀硫酸”)充分反应,
再 过滤 (填操作名称)、洗涤、干燥即可回收得到金属铜;所得滤液中含有需要
回收的FeCl 。
2
[拓展延伸](5)已知:加热时,葡萄糖溶液与氢氧化铜悬浊液能发生反应。实验室可用
CuSO 溶液等物质检验葡萄糖的存在,具体实验过程为:在试管中加入2mL 10%NaOH
4
溶液,滴加5% CuSO 溶液5滴(每滴溶液按0.04mL计算。两种溶液的密度均按1g/mL
4
计算),混合均匀,充分反应,得混合物A。再向上述试管中加入几滴10%葡萄糖溶液,
并在酒精灯上加热至沸腾,片刻后生成红色沉淀B,检验完成。则混合物A显 碱性
(填“中性”或“碱性”);红色沉淀 B是 C u O [填“CuO”或“Cu O”“或
2 2
“Cu(OH) ”]。
2
第16页(共18页)【解答】解:(1)在①CuO②Cu(OH) ③CuCl ④Cu (OH) CO [也可表示为
2 2 2 2 3
CuCO •Cu(OH) ]这4种物质中,属于碱的是氢氧化铜;
3 2
除①CuO外,其余3种物质在常温下易溶于水是氯化铜。
故填:②;③。
(2)考古出土的春秋末期制造的青铜剑,历经2500余年,其表面且有一层薄锈,但仍
寒光逼人,剑刃锋利。由此可知,青铜硬度大;
铜器表面的薄锈是铜与空气中的氧气、水、二氧化碳等物质发生反应所形成。
故填:硬度大;二氧化碳。
(3)①将CuO粉末装入玻璃管A中的具体操作方法是把玻璃管横放,利用药匙把氧化
铜粉末送入玻璃管中部。
故填:把玻璃管横放,利用药匙把氧化铜粉末送入玻璃管中部。
②实验时,在试管B中能够观察到的现象是有液体出现,该液体是反应生成的水,水
是纯净物。
故填:纯净物。
③从环保角度看该装置的不足之处是没有处理尾气。
故填:没有处理尾气。
(4)取适量含CuCl 、FeCl 的某工业废液样品,向其中加入过量铁粉并充分反应后,
2 3
过滤,将滤渣和足量稀盐酸充分反应,稀盐酸和过量的铁反应生成氯化亚铁和氢气,再
过滤、洗涤、干燥即可回收得到金属铜,所得滤液中含有需要回收的FeCl 。
2
故填:稀盐酸;过滤。
(5)氢氧化钠和硫酸铜反应的化学方程式及其质量关系:
CuSO +2NaOH=Cu(OH) ↓+Na SO ,
4 2 2 4
160 80
由以上质量关系可知,硫酸铜和氢氧化钠恰好完全反应时质量比是2:1,
第17页(共18页)氢氧化钠质量:1g/mL×2mL×10%=0.2g,硫酸铜质量:1g/mL×(0.04mL×5)×5%=
0.01g,硫酸铜和氢氧化钠质量比是:0.01g:0.2g=1:20,氢氧化钠溶液过量,则混合
物A显碱性;
红色沉淀B是反应生成的Cu O。
2
故填:碱性;Cu O。
2
四、化学计算题(本大题共有1小题,共5分)
16.(5分)(2021•徐州)某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二
氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸 50 g(结果精确到
1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,同至少需要多少克上述稀盐
酸与足量的大理石反应才能制得(实验条件下二氧化碳的密度为2g/L)?(写出计算过
程,结果精确到0.01g)
【解答】解:(1)溶液稀释前后溶质的质量不变,则用20.3g溶质质量分数为37%的浓
盐酸能配制15%稀盐酸的质量为20.3g×37%÷15%≈50g,故填:50;
(2)10瓶二氧化碳的质量为125×10×0.001L×2g/L=2.5g
设需要稀盐酸的质量为x
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
73 44
x×15% 2.5g
=
x=27.65g
答:需要27.65克15%的稀盐酸。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2021/7/24 14:03:46;用户:刘康;邮箱:sjhzxyh15@xyh.com;学号:37802005
第18页(共18页)