文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 01 物质的性质与应用
目 录
01 挑战中考题·查知识漏洞
命题点一 氧气的性质与用途
命题点二 水的性质和应用
命题点三 氢气的性质与氢能的优缺点
命题点四 金属的性质及用途
命题点五 碳单质的性质及用途
命题点六 酸的性质及用途
命题点七 碱的特性和用途
命题点八 盐的特性和用途
命题点九 生石灰
02 回顾教材·补知识漏洞
03 知识通关演练
命题点一 氧气的性质与用途
1.(2023•长沙)2023年5月30日神舟十六号载人飞船顺利发射,将三名航天员成功送入空间站。下列能
供给航天员呼吸的气体是( )
A.氧气 B.氮气 C.二氧化硫 D.氦气
2.(2023•德州)如图是硫粉分别在空气和氧气里燃烧的实验。下列说法正确的是( )
A.硫在氧气里燃烧发出微弱的淡蓝色火焰
B.集气瓶中放入水主要是防止集气瓶底炸裂
C.硫燃烧的剧烈程度主要与氧气的浓度有关
D.硫燃烧的化学方程式是2S+3O 2SO
2 3
命题点二 水的性质和应用
3.(2023•德阳)饮用矿泉水可分为碳酸水、硅酸水、锶水等几大类,此外还有含锌、锶、碘、硒等的矿
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
泉水。下列相关说法正确的是( )
A.矿泉水中含有的“锌、锶、碘、硒”是指单质
B.取50mL矿泉水与50mL酒精混合后,总体积为100mL
C.锶原子的结构示意图为 ,故锶原子在化学反应中易失去最外层电子
D.长期饮用纯净水替代矿泉水更有利于身体健康
4.(2023•成都)溶解氧一般指溶解于水中的氧气。用实验装置测定河水、喷泉水及自来水的溶解氧数据
如图。下列相关分析正确的是( )
A.a为自来水,b为喷泉水
B.空气中氧气含量不影响溶解氧的含量
C.自然界里河水中溶解氧的含量不发生改变
D.管材选择可能会影响自来水输送中溶解氧的含量
命题点三 氢气的性质与氢能的优缺点
5.(2023•长沙)液氢已应用于航天等领域。目前在生活生产中大量使用氢能源还存在一定困难,原因是
( )
A.氢气本身无毒
B.氢气制取成本高和贮存困难
C.氢气燃烧放出的热量多
D.氢气燃烧产物不污染空气
6.(2023•苏州)氢能是一种清洁能源,氢气的生产和储存是科学研究的重要方向。
目前制氢的方法主要有化石能源制氢和电解水制氢。由化石能源(煤、天然气)制得的H 中含有CO,利
2
用液氮的低温可将CO液化分离,从而获得纯净的氢气。电解水法制氢的能量转化如图所示,氚可用于核
能发电,氚是一种原子核中有1个质子和2个中子的原子。
氢气的储存有物理储氢和化学储氢。物理储氢包括加压储氢和吸附储氢。用物理方法将石墨进行剥离,得
到的石墨烯可用于常温吸附氢气。锂氮化合物Li N可用于化学储氢。
x
(1)下列有关氢能的说法不正确的是 。
A.氢气的燃烧产物无污染,所以氢能是一种清洁能源
B.利用太阳能发电并电解水制氢可实现二氧化碳零排放
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.现阶段氢能已经能完全替代化石能源
(2)利用液氮的低温能将H 与CO分离,说明氢气的沸点比CO的沸点 。
2
(3)①氚属于 元素的一种原子。
②下列示意图能表示氚原子的是 (填序号)。
(4)①将氢气压缩进储氢瓶过程中,发生改变的是 (从微观角度解释)。
②石墨烯是一种 (填“单质”或“化合物”)。
③化合物Li N中质量比m(Li):m(N)=3:2,则x= 。
x
命题点四 金属的性质及用途
7.(2023•牡丹江)下列物质的性质和用途对应关系错误的是( )
A.铜的导电性好——作导线
B.氧气支持燃烧——作燃料
C.金刚石硬度大——作钻探机钻头
D.氮气的化学性质不活泼——作保护气
8.(2023•东区)金属M与硝酸银溶液反应的化学方程式为:2AgNO +M═2Ag+M(NO ) 。下列说法正
3 3 2
确的是( )
A.该反应属于化合反应
B.金属M可能是铝
C.若M是铜,则反应后溶液质量变小
D.反应前后相比较,M的化合价降低
命题点五 碳单质的性质及用途
9.(2023•东区)下列有关碳和碳的化合物说法中,错误的是( )
A.金刚石、石墨都是由碳元素组成的单质
B.常温下,碳的化学性质很活泼
C.二氧化碳和一氧化碳的分子构成不同
D.金刚石硬度大,可用于裁切玻璃
10.(2023•扬州)下列物质性质和用途对应关系正确的是( )
A.活性炭有吸附性,可用作除味剂
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.铝有导热性,可用于制电线
C.石墨有导电性,可用作润滑剂
D.盐酸有挥发性,可用于除铁锈
11.(2023•临沂)化学来源于生活,服务于社会。请根据所学化学知识回答下列问题:
(1)天然气的主要成分是甲烷,其化学式为 。
(2)家用净水机常用活性炭除去水中的异味,这是利用活性炭的 。
(3)高锰酸钾(KMnO )在生活中常用作消毒剂,高锰酸钾中锰元素的化合价为 。
4
(4)氢燃料电池汽车基本实现碳的“零排放”。写出氢气燃烧的化学方程式
。
命题点六 酸的性质及用途
12.(2023•郴州)下列关于硫酸的说法错误的是( )
A.浓硫酸有强烈的腐蚀性
B.稀释浓硫酸时,应将水注入浓硫酸中,并用玻璃棒搅拌
C.稀硫酸可用来除铁锈
D.浓硫酸有吸水性,可作干燥剂
命题点七 碱的特性和用途
13.(2023•深圳)有关NaOH说法错误的是( )
A.NaOH固体溶解时放出热量
B.NaOH包装箱上张贴的标识是
C.NaOH是所有气体的干燥剂
D.NaOH应密封保存
14.(2023•广安)性质决定用途,用途反映性质。下列物质的用途与性质对应不正确的是( )
A.用熟石灰改良酸性土壤——熟石灰可与酸性物质反应
B.用CO冶炼金属——CO具有可燃性
C.用洗涤剂清洗餐具上的油渍——洗涤剂有乳化功能
D.用稀盐酸除铁锈——盐酸可与Fe O 反应
2 3
命题点八 盐的特性和用途
15.(2023•济南)已知某溶液X是稀盐酸和Ca(OH) 溶液两者之一,甲、乙、丙是NaNO 溶液、
2 3
K CO 溶液、FeCl 溶液中的各一种。取三等份溶液X,分别向其中滴入适量的甲、乙、丙三种溶液,产生
2 3 3
的实验现象如下表所示。则依据实验现象做出的下列推断中,合理的是( )
所加溶液 甲 乙 丙
实验现象 产生白色沉淀 产生红褐色沉淀 无明显现象
A.甲是K CO 溶液 B.乙是NaNO 溶液
2 3 3
C.丙是FeCl 溶液 D.溶液X是稀盐酸
3
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
16.(2023•盘锦)下列日常生活中的物质与其用途不对应的是( )
A.Na CO ——配制生理盐水
2 3
B.NaCl——用作调味品
C.CaCO ——用作补钙剂
3
D.NaHCO ——焙制糕点
3
命题点九 生石灰
17.(2023•江西)《天工开物》中记载:“凡石灰经火焚炼为用”。“石灰”主要成分为氧化钙,下列说
法错误的是( )
A.“石灰”与石灰石成分相同
B.“石灰”含有钙、氧元素
C.“石灰”与水反应会放热
D.“石灰”可用作干燥剂
18.(2023•南充)下列图像能正确反映其对应关系的是( )
A. 表示常温下,向pH=3的某溶液中加水稀释
B. 表示向一定质量氢氧化钙的饱和溶液中加入少量氧化钙固体
C. 表示向质量和质量分数都相同的盐酸中分别加入锌和铁
D. 表示向一定质量的氧化镁固体中逐渐加入稀盐酸
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
一、氧气的性质与用途
1、氧气的物理性质:
(1)色、味、态:通常情况下,是无色无味的气体
(2)密度:标准状况下,密度略大于空气(可用向上排空法收集)
(3)溶解性:氧气不易溶于水(可用排水法收集)
(4)三态变化:降温后,氧气可以变为淡蓝色的液体,甚至淡蓝色雪花状固体。(物理变化)
2、氧气的化学性质:(很活泼)具有助燃性(支持燃烧)和氧化性。
3、氧气的用途
(1)支持燃烧;例如,日常生活中,我们用到的燃烧;冶金工业上,在炼钢过程中吹以高纯度氧气,和
其中的碳及磷、硫、硅等起氧化反应,这不但降低了钢的含碳量,还有利于清除磷、硫、硅等杂质;国防
工业上,液氧是现代火箭最好的助燃剂,在超音速飞机中也需要液氧作氧化剂,可燃物质浸渍液氧后具有
强烈的爆炸性,可制作液氧炸药;还有,在金属切割及焊接等方面也有着广泛的用途。
(2)是供给呼吸;例如,在潜水作业、登山运动、高空飞行、宇宙航行、医疗抢救等缺氧、低氧或无氧
环境中,供给氧气,以维持人或动物等正常的呼吸。
二、水的性质和应用
1、水的物理性质:纯净的水是无色、无味、无形的透明液体,在101kPa时,水的凝固点是0℃,沸点是
100℃,4℃时相对密度最大1g/cm3;水结冰时体积膨胀,所以冰的密度小于水的密度,能浮在水面上,还
有,水能够溶解很多种物质,是最常用的溶剂。
2、水的化学性质:a.在通电的条件下,能够分解成氢气和氧气;b.水能够与二氧化碳等非金属氧化物反
应,生成碳酸等相应的酸;c.水能够与氧化钙等金属氧化物反应,生成氢氧化钙等相应的碱;d.水能够与
氧气、铁等金属发生反应,使金属锈蚀;e.水与二氧化碳被绿色植物利用,能够进行光合作用,合成有机
物(主要是淀粉),该反应的化学方程式为:6CO+6H O C H O+6O ;f.水能够跟较活泼金属
2 2 6 12 6 2
或碳反应(即氧化性),使氢被还原成氢气;例如,2Na+2HO=2NaOH+H ↑,Mg+2HO=Mg(OH)
2 2 2
+H ↑,C+H O高温¯CO+H,等等。
2 2 2 2
3、水的应用:水的应用是非常的广泛,它是人及一切生物生存所必需的,可以说,没有水就没有生命,
水在日常生活中的应用,都比较熟悉,就不多说了;农业上用水在浇灌农作物,使之进行光合作用等;工
业上用水作原料、制冷或洗涤等;化学实验中常用水作反应物、制冷、溶解物质、稀释浓溶液、洗涤仪
器、灭火或用排水法收集气体等等。
三、氢气的性质与氢能的优缺点
1、氢气物理性质:氢气是一种无色、无味、无臭的气体,是世界上最轻的气体,难溶于水,且在标准温
度和压力下,氢气是一种气态物质。
2、氢气化学性质:氢气是一种极易燃烧的气体,燃点只有574℃,在空气中的体积分数为4%-75%时都能
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
燃烧,同时产生水并放出大量的热量。氢气还具有还原性,可在许多化学工业领域作为原料,例如:合成
氨就是用氢气和氮气为原料。
3、氢气的用途:
(1)氢气可以用作还原剂、合成氨、合成甲醇、合成盐酸的原料等,是石油化工、电子工业、冶金工业
等行业中重要的工业原料和气体。
(2)氢气可以用作高能燃料,被广泛应用于航天领域。
(3)氢气对中枢神经系统疾病、脑血管病、神经退行性疾病、肝脏病等有一定的治疗作用。
四、金属的性质及用途
1、金属物理性质:
(1)常温下为固体(特殊:汞为液体),有金属光泽,密度较大,熔点较高。
(2)大多数金属呈银白色,特殊:铜紫红色,金金黄色,铁粉黑色(铁片为银白色)。
(3)大多数金属具有优良的导电性、导热性,有延展性(延:拉成丝;展:压成片)。
2、金属的化学性质
(1)大多数金属可与氧气的反应
金属 在空气中 在氧气中
镁 常温下逐渐变暗,表面形成氧化 点燃,剧烈燃烧,发出耀眼的白光,生成白
膜。点燃,剧烈燃烧,发出耀眼的 色的固体
白光,生成白色的固体。 2Mg + O 点燃 2MgO
2
铝 常温下表面变暗,生成一种致密的 点燃,剧烈燃烧,发出耀眼的白光,生成白
氧化膜 色的固体4Al + 3O 点燃 2Al O
2 2 3
铁 持续加热变红 点燃,剧烈燃烧,火星四射,生成黑色的固
体3Fe + 2O 点燃 Fe O
2 3 4
铜 加热,生成黑色物质;在潮湿的空 紫红色的铜丝加热后变黑2Cu + O 加热
2
气中,生成铜绿而被腐蚀 2CuO
银、 即使在高温时也不与氧气发生反应
金
(2)金属 + 酸 → 盐 + H ↑(置换反应)
2
反应条件:金属活动性排在H前
注意:实验前用砂纸打磨金属,除去镁、铁等金属表面的氧化膜,便于金属与酸接触反应。
+稀盐酸
镁 锌 铁
+稀硫酸
固体逐渐溶解,无色溶液
固体逐渐溶解,产生 固体逐渐溶解,产生较
现象 变为浅绿色,产生少量气
大量气泡 多气泡
泡
Mg+2HCl = MgCl +H ↑ Zn+2HCl = ZnCl +H ↑ Fe+ 2HCl = FeCl + H ↑
2 2 2 2 2 2
方程式 Mg+HSO =
2 4
Zn+H SO = ZnSO+H ↑ Fe+H SO =FeSO +H ↑
2 4 4 2 2 4 4 2
MgSO +H ↑
4 2
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
根据金属与酸混合时是否有氢气产生将金属分为两类:活泼金属和不活泼金属:通过金属与酸能否反应或
与酸反应的剧烈程度判断金属的活动性。镁>锌>铁>铜(不反应)
铁与稀盐酸和稀硫酸反应生成的铁的化合物中,铁化合价为+2价。有Fe2+的溶液为浅绿色
(3)金属与金属化合物的反应
金属+盐→新盐+新金属 (置换反应)
反应条件:参加反应的金属活动性必须强于盐中金属的活动性(K、Ca、Na除外),且盐必须可溶
现象的描述重点:金属表面生成固体的颜色,溶液颜色的变化。
实验 铁钉+硫酸铜溶液 铝丝+硫酸铜溶液 铜丝+硝酸银溶液
铁表面有红色固体 铝表面有红色固体产生, 铜表面有银白色固体产
现象 产生,溶液由蓝色 溶液由蓝色逐渐变为无 生,溶液由无色逐渐变
逐渐变为浅绿色。 色。 为蓝色。
Fe+CuSO 2Al+3CuSO =Al(SO ) Cu+2AgNO
4 4 2 4 3 3
化学方程式
=Cu+FeSO +3Cu =2Ag+Cu(NO)
4 3 2
活动性比较 铁>铜 铝>铜 铜>银
*通过金属与金属化合物溶液是否反应判断金属的活动性。
总结:比较金属活动性的方法:
3、金属的用途:(性质和用途要对应)
物质的性质在很大程度上决定了物质的用途,另外还需要考虑价格、资源、是否美观、使用是否便利以及
是否容易回收和对环境的影响等多种因素。
(1)性质决定用途
铜、铝具有导电性→电线;钨熔点高→灯丝;铬硬度大→做镀层金属;铁硬度大→菜刀、镰刀、锤子等;
(2)生活中应用的金属
干电池外皮→锌/锰;“银粉”→铝;水银温度计→汞;“锡箔”纸→铝或锡;保温瓶内胆→银
五、碳单质的性质及用途
1、碳单质的物理性质比较
石墨C 金刚石C C
60
碳单质
碳原子构成 碳原子构成 C 分子构成
60
微观结构
深灰色的有金属光泽不透明 无色透明的、正八面体形状的
物理性质
的细鳞片状固体,耐高温, 固体。天然存在的最硬的物
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质地较软,有滑腻感,有良 质。
好的导电性
作电极或电刷、石墨炸弹、 制装饰品(钻石)、制钻头、切割 用于超导、催化、材料
用途 制铅笔芯、做坩埚,作机械 大理石、玻璃 科学等领域
高温润滑剂
金刚石和石墨物理性质差异大的原因:碳原子的排列方式不
性质差异
同
2、碳的化学性质:碳的几种单质物理性质各异,而化学性质却相似。
(1)常温下化学性质不活泼(原因:碳原子的最外层电子数为4,不易得失)
用途:用炭黑制成的墨书写绘画,档案用碳素墨水书写,木质电线杆埋入地下部分烤焦增强耐腐蚀性。
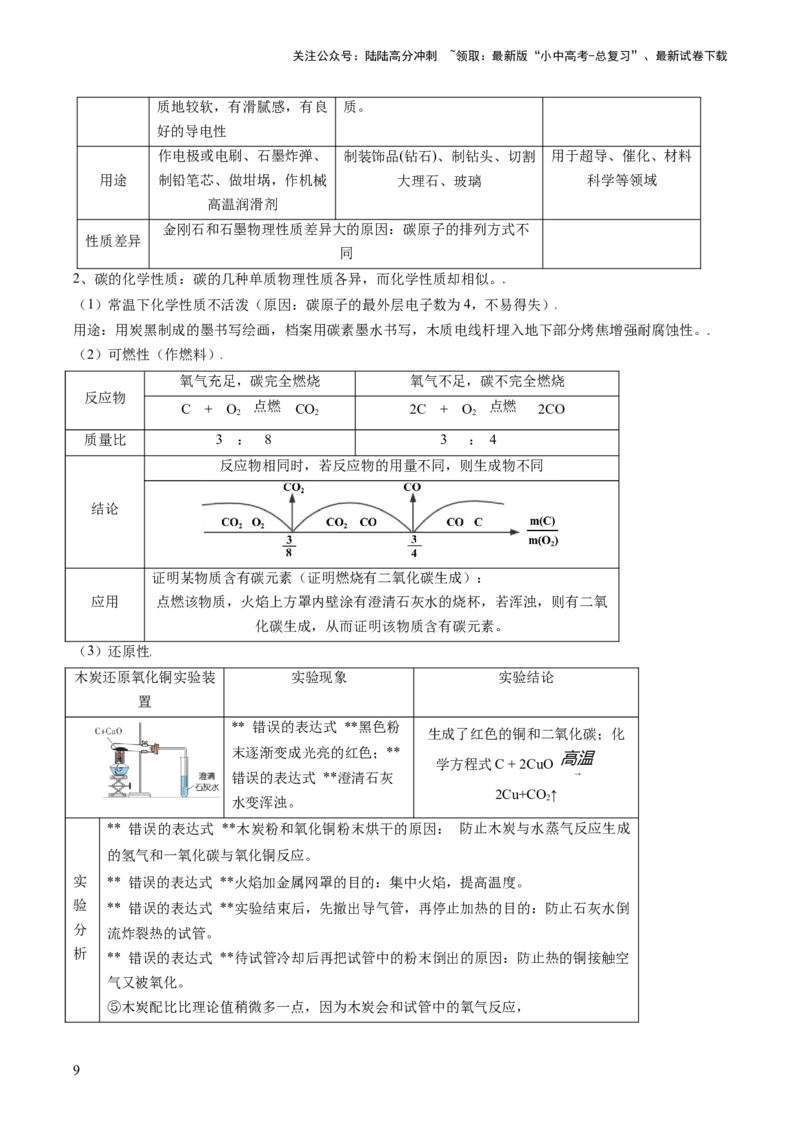
(2)可燃性(作燃料)
氧气充足,碳完全燃烧 氧气不足,碳不完全燃烧
反应物
C + O 点燃 CO 2C + O 点燃 2CO
2 2 2
质量比 3 : 8 3 : 4
反应物相同时,若反应物的用量不同,则生成物不同
结论
证明某物质含有碳元素(证明燃烧有二氧化碳生成):
应用 点燃该物质,火焰上方罩内壁涂有澄清石灰水的烧杯,若浑浊,则有二氧
化碳生成,从而证明该物质含有碳元素。
(3)还原性
木炭还原氧化铜实验装 实验现象 实验结论
置
** 错误的表达式 **黑色粉
生成了红色的铜和二氧化碳;化
末逐渐变成光亮的红色;**
高温
学方程式C + 2CuO
错误的表达式 **澄清石灰 →
2Cu+CO ↑
水变浑浊。 2
** 错误的表达式 **木炭粉和氧化铜粉末烘干的原因: 防止木炭与水蒸气反应生成
的氢气和一氧化碳与氧化铜反应。
实 ** 错误的表达式 **火焰加金属网罩的目的:集中火焰,提高温度。
验 ** 错误的表达式 **实验结束后,先撤出导气管,再停止加热的目的:防止石灰水倒
分 流炸裂热的试管。
析
** 错误的表达式 **待试管冷却后再把试管中的粉末倒出的原因:防止热的铜接触空
气又被氧化。
⑤木炭配比比理论值稍微多一点,因为木炭会和试管中的氧气反应,
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3、不同种类的碳的用途
(1)木炭和活性炭:有疏松多孔结构,具有吸附性,可吸附色素、异味等。
①木 炭:用于除去食品和工业产品里的色素,作冰箱去味剂等。
②活性炭:活性炭的吸附性比木炭强。用于防毒面具滤毒罐中过滤毒气,制糖工业中白糖脱色,用于净水
器、冰箱除味剂,环保活性炭包等。
(2)焦 炭:用于冶炼金属。
(3)炭 黑:制造黑色染料,油墨,油漆等,添加到橡胶里做补强剂,增强耐磨性。(碳和炭的区别:
“碳”是元素名称,并不指具体某种物质;“炭”表示由碳元素组成的具体物质)。
六、酸的性质及用途
1、盐酸和硫酸物理性质及用途比较
硫酸 HSO 盐酸 HCl
2 4
纯净的硫酸是无色、无味、黏稠的油状液体, 纯净的盐酸是无色的液体、有刺激性气味的液
物理性 不易挥发;浓硫酸有很强的腐蚀性,溶于水放 体;浓盐酸具有挥发性,会发出的氯化氢气体
质 出大量的热,有吸水性,打开瓶塞瓶口无明显 与空气中的水蒸气结合形成盐酸小液滴,打开
现象。 瓶塞瓶口有白雾出现。
浓度和 常用浓盐酸1.19g/cm3 (37%~38%)(氯化
常用浓硫酸1.84g/cm3 (98%)
密度 氢气体溶于水形成,一定是混合物)
特性 吸水性、脱水性、腐蚀性 挥发性和腐蚀性都很强
重要化工原料。用于生产化肥、农药、火药、
重要化工产品。用于金属表面除锈、制造药物
染料以及冶炼金属、精炼石油和金属除锈等。
用途 (如盐酸麻黄素、氯化锌)等;人体胃液中有
浓硫酸有吸水性,在实验室中常用它做干燥
盐酸,可帮助消化。
剂。
保存方
密封保存 密封保存
法
敞放在空气中的变化(物理变化)
性质 溶质质量 溶剂质量 溶液质量 溶质质量分数 保存
浓盐酸 挥发性 减小 不变 减小 减小 密封
浓硫酸 吸水性 不变 增大 增大 减小 密封
2、浓硫酸腐蚀性
(1)具有脱水性(化学性质);它能夺取纸张、木材、布料、皮肤(都由含碳、氢、氧等元素的化合物
组成)里的水分,生成黑色的炭。
(2)危险处理:不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶
液。
稀硫酸沾在衣服上,水分蒸发后会变成浓硫酸,也要进行处理。
3、酸的化学性质
(1)与酸碱指示剂反应显色:紫色石蕊溶液变红;无色酚酞不变色。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
使用点滴板进行实验优点:操作简单、节约药品、便于对照、效果较好。
(2)与活泼金属反应(不包括浓硫酸和硝酸):金属+酸→盐+氢气(置换反应)
①铁和酸反应:Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑
【现象】铁表面有气泡产生;溶液由无色逐渐变为浅绿色(Fe2+的盐溶液呈浅绿色)
②锌和酸反应:Zn+2HCl = ZnCl +H↑ Zn+HSO = ZnSO+H↑
2 2 2 4 4 2
现象:固体逐渐溶解,产生气泡
(3)与金属氧化物反应:金属氧化物+酸→盐+水(复分解反应)
①氧化铁和酸反应:Fe O+6HCl = 2FeCl +3HO Fe2O3+3H2SO4 = Fe2(SO4)3+3H2O
2 3 3 2
现象:红色固体逐渐溶解,溶液由无色变为黄色。
②氧化铜和酸反应:CuO+2HCl = CuCl +HO CuO+HSO = CuSO4+H O
2 2 2 4 2
现象:黑色固体逐渐溶解,溶液由无色变为蓝色。
(4)与碱反应(中和反应):酸+碱→盐+水
①HCl与NaOH反应:HCl+NaOH = NaCl+HO
2
②H SO 与Ca(OH) 反应:HSO +Ca(OH) = CaSO+2HO
2 4 2 2 4 2 4 2
(5)与某些盐反应:酸+盐→新盐+新酸(复分解反应)
①HCl与CaCO 反应:2HCl+CaCO = CaCl +HO+CO↑
3 3 2 2 2
现象:固体逐渐溶解,产生气泡
②除硫酸钡以外的钡盐都能与硫酸反应:BaCl2+H2SO4=BaSO4↓+ 2HCl(注意:HCl 是稀盐酸,不写↑)
③HSO 与NaCO 反应:HSO +NaCO = Na SO +HO+CO↑
2 4 2 3 2 4 2 3 2 4 2 2
现象:产生大量气泡
④硝酸银能与盐酸反应:AgNO3+HCl=HNO3+AgCl↓
七、碱的特性和用途
1、氢氧化钠和氢氧化钙的特性和用途
碱 氢氧化钠(NaOH) 氢氧化钙(Ca(OH) )
2
俗称 烧碱、火碱、苛性钠 消石灰、熟石灰
工业制法 NaCO+Ca(OH) =2NaOH+CaCO ↓ CaO+H O=Ca(OH)
2 3 2 3 2 2
白色块状固体,具有强腐蚀性,如果不慎将氢氧化钠
白色粉末状固体较强腐蚀性微溶于
溶液沾到皮肤上,先用大量水冲洗,再涂上硼酸溶
物理性质 水,溶于水时放热不明显,溶解度
液;易溶于水,溶于水时放出大量的热;氢氧化钠固
随温度升高而减小。
体易吸水而潮解,可做干燥剂。
鉴别 通入CO,产生白色沉淀的为氢氧化钙
2
用于制取肥皂、石油、造纸、纺织和印染工业氢氧化做建筑材料、涂树木上防冻伤和防
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
虫卵改良酸性土壤和河流、配制波
钠能与油脂反应,所以可以除油污,实验室做某些气
用途 尔多液,在实验室中检验二氧化
体的干燥剂。
碳。
2、碱的化学性质
(1)与酸碱指示剂反应显色:碱溶液(四大强碱的溶液、氨水)能使指示剂变色;使紫色石蕊溶液变
蓝,使无色酚酞溶液变红。由于弱碱不溶于水,所以弱碱不能使指示剂变色。
(2)与某些非金属氧化物反应:非金属氧化物+碱→盐+水
反应发生的条件:A.碱是四大强碱; B.非金属氧化物是二氧化碳、二氧化硫、三氧化硫
2NaOH+CO = Na CO+H O(用氢氧化钠溶液吸收二氧化碳)
2 2 3 2
2NaOH+SO = Na SO +H O(用氢氧化钠溶液吸收二氧化硫)
2 2 3 2
2NaOH+SO = Na SO +H O
3 2 4 2
Ca(OH) +CO = CaCO↓+ H O(检验二氧化碳;石灰墙“出汗”)
2 2 3 2
(3)碱+酸→盐+水(复分解反应、中和反应)
6HCl+Fe(OH) = FeCl +3HO 现象:红褐色固体消失,溶液变为黄色
3 3 2
2HCl+Cu(OH) = CuCl +2HO 现象:蓝色固体消失,溶液变为蓝色
2 2 2
(4)碱+盐 → 新碱+新盐(复分解反应)
反应发生的条件:A.反应物能溶于水(包括氢氧化钙,不包括其他微溶于水的物质); B.新碱是氨水;
C.若新碱不是氨水,新碱和新盐中至少有一个沉淀。D.铵盐一定能与四大强碱反应。
新碱是沉淀:
蓝色沉淀:2NaOH+CuSO =Na SO +Cu(OH) ↓
4 2 4 2
红褐色沉淀:3NaOH+FeCl =3NaCl+Fe(OH) ↓
3 3
白色沉淀:2NaOH+MgSO =Na SO +Mg(OH) ↓
4 2 4 2
新盐是沉淀:
Ba(OH) +Na SO =BaSO ↓+2NaOH Ca(OH) +Na CO=CaCO ↓+2NaOH
2 2 4 4 2 2 3 3
蓝白沉淀:Ba(OH) +CuSO=BaSO ↓+ Cu(OH) ↓
2 4 4 2
红白沉淀:3Ba(OH) +Fe (SO )=3BaSO ↓+ 2Fe(OH) ↓
2 2 4 3 4 3
波尔多液(注:波尔多液不是溶液):Ca(OH) +CuSO=CaSO +Cu(OH) ↓
2 4 4 2
八、盐的特性和用途
1、盐的化学性质主要有如下几点
(1)与某些金属反应:盐+金属→另一种盐+另一种金属(置换反应)
反应条件:盐必须可溶;金属单质(K、Ca、Na除外)的活泼性要大于盐中金属的活泼性。
列:CuSO +Fe = FeSO +Cu
4 4
现象:有红色固体析出,溶液由蓝色变为浅绿色;
2AgNO+Cu = Cu(NO)+2Ag
3 3 2
现象:有银白色物体析出,溶液由无色变为蓝色;
(2)与酸反应:盐+酸→另一种盐+另一种酸(复分解反应)
反应条件:有沉淀、气体生成。 HCl+AgNO = AgCl↓+2HNO
3 3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
现象:有白色沉淀生成 HSO +BaCl = BaSO↓+2HCl
2 4 2 4
现象:有白色沉淀生成 NaCO+2HCl = 2NaCl+HO+CO↑
2 3 2 2
现象:有气泡产生
(3)与碱反应:盐+碱→新盐+新碱(复分解反应)
反应条件:反应物均溶于水,生成物有沉淀。
NaCO+Ca(OH) = CaCO↓+2NaOH
2 3 2 3
现象:有白色沉淀生成
2NaOH+CuSO = Cu(OH) ↓+NaSO
4 2 2 4
现象:有蓝色沉淀生成,溶液由蓝色变为无色
(4)与某些盐反应:盐+盐→一种新盐+另一种新盐(复分解反应)
反应条件:反应物均溶于水,生成物有沉淀
NaCO+CaCl = CaCO↓+2NaCl
2 3 2 3
现象:有白色沉淀生成
NaSO +BaCl = BaSO↓+2NaCl
2 4 2 4
现象:有白色沉淀生成
2、常用盐的用途
(1)氯化钠(俗称食盐)经常用来做调味品、防腐剂、融雪剂(降低雪的熔点),农业上常用一定质量
分数的氯化钠溶液来选种,医疗上还用氯化钠来制生理盐水(0.9% 氯化钠溶液),工业上还常用来制取
氯气、烧碱等;
(2)碳酸钠(俗称纯碱、苏打)广泛应用于生产玻璃、造纸、纺织、洗涤剂等,还常用于食品工业等;
(3)碳酸氢钠,(俗称小苏打)是焙制糕点所常用的发酵粉的主要成分之一;在医疗上,它是治疗胃酸
过多症的一种药剂;它还被用于生产汽水、干粉灭火器等;
(4)碳酸钙(石灰石、大理石的主要成分)大量用于建筑业;天安门前的华表、人民大会堂的许多柱子
就是用大理石做的;它还可被用作补钙剂等。
九、生石灰
1、生石灰的主要成分是氧化钙(CaO);是工业上制取二氧化碳的副产物.它的性质是白色晶体或粉末,
具有腐蚀性,易溶于酸,难溶于水,但具有吸水性,能与水剧烈反应放出大量的热,生成白色固体(即氢
氧化钙,俗称熟石灰;反应的化学方程式是CaO+H O=Ca(OH))。
2 2
2、它的用途主要是用于消毒,改良水质,实验室里和食品包装中常用做干燥剂。
1.(2024•重庆二模)金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是(
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
)
A.硬度很大、熔点很高 B.是银白色的固体
C.易与酸反应产生氢气 D.能够导电、能够导热
2.(2024•鼎城区一模)有一种“即热即食型食品”适合外出旅游时使用,其内层用铝箔包装食品,外层
则是包装两种化学物质。使用预留在外的开关,使两种物质发生化学反应,此时便可以对食品进行加热,
这两种化学物质最适合的选择是( )
A.熟石灰与水 B.生石灰与水
C.食盐与水 D.浓硫酸与水
3.(2024•章丘区二模)已知某溶液X是(NH ) CO 溶液和(NH ) SO 溶液两者之一,又知甲、乙、
4 2 3 4 2 4
丙三种试剂分别是稀盐酸、NaOH溶液、Ba(NO ) 溶液三种溶液中的各一种。取三等份溶液X,分别向
3 2
其中加入适量的甲、乙、丙三种试剂,产生的现象如下表所示。则依据实验现象做出的下列推断中,合理
的是( )
加入试剂 甲 乙 丙
实验现象 产生白色沉淀 无明显现象 产生有刺激性气味的气体
A.溶液X是(NH ) CO 溶液
4 2 3
B.溶液X是(NH ) SO 溶液
4 2 4
C.乙是硝酸钡溶液
D.上表中产生气体能使无色酚酞试液变蓝
4.(2024•晋中模拟)对“嫦娥五号”取回样品的分析表明,月壤中的金属氧化物和水分可以被有效提取
出来,用于制备氧气。下列对于制得的氧气用途分析正确的是( )
A.可用于供给航天员呼吸
B.可用于电气设备灭火消防
C.可用作火箭发动机的燃烧剂
D.可用作太空种植蔬菜光合作用的原料
5.(2024•荣昌区校级一模)美国洛斯﹣阿拉莫斯国家实验室的研究人员日前用普通水制造出了一种新型
的固体物质.科学家们介绍说,这种新型固体物质的分子中仅包含有一个氢原子和一个氧原子.下列说法
正确的是( )
A.该固体物质和水是同种物质
B.该固体物质属于一种新型化合物
C.该固体物质中氢元素与氧元素的质量比为1:1
D.由普通水制成该固体物质后,分子停止运动
6.(2024•无锡一模)下列碳单质的用途与其化学性质有关的是( )
A.用石墨粉末作锁的润滑剂
B.用碳素笔书写档案材料
C.用活性炭作冰箱除味剂
D.用金刚石切割玻璃
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
7.(2024•广东模拟)下列有关溶质质量分数为98%的浓硫酸的性质说法不正确的是( )
A.浓硫酸是无色、油状的液体
B.浓硫酸的密度大于水的密度
C.浓硫酸因具有很强的脱水性而被装入干燥管中使用
D.装有浓硫酸的试剂瓶敞开放置在空气中,质量分数会变小
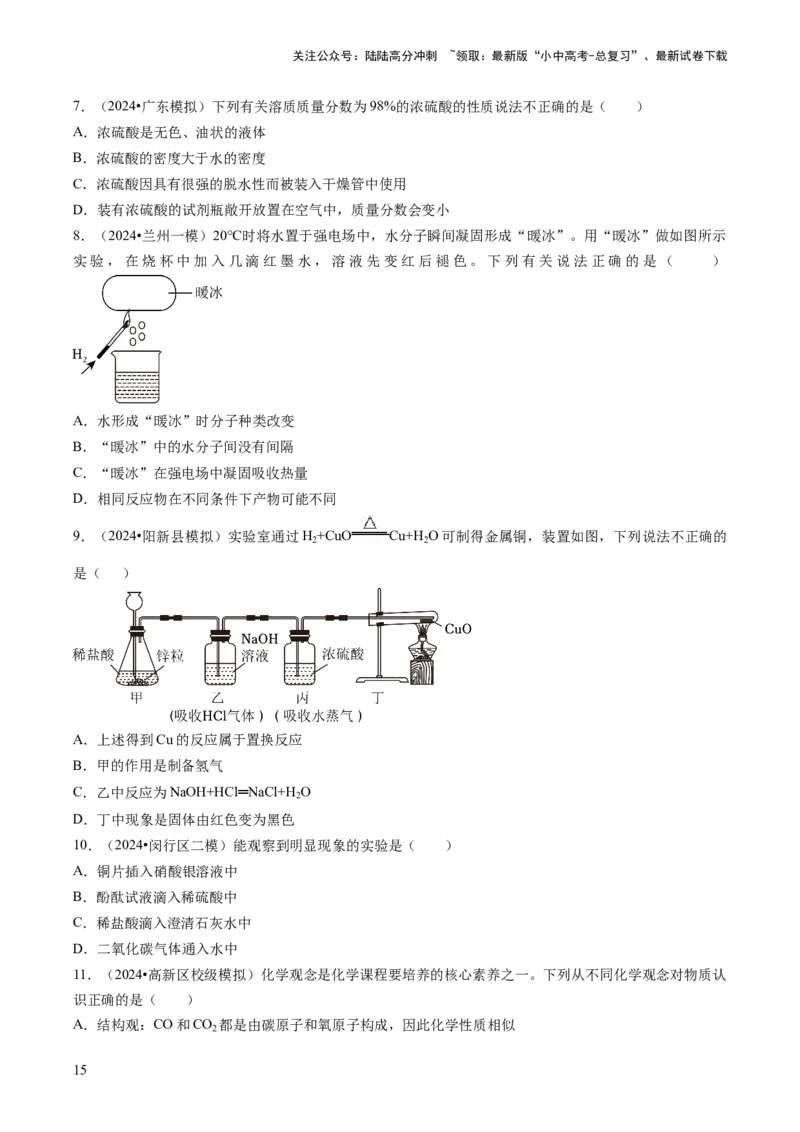
8.(2024•兰州一模)20℃时将水置于强电场中,水分子瞬间凝固形成“暖冰”。用“暖冰”做如图所示
实验,在烧杯中加入几滴红墨水,溶液先变红后褪色。下列有关说法正确的是( )
A.水形成“暖冰”时分子种类改变
B.“暖冰”中的水分子间没有间隔
C.“暖冰”在强电场中凝固吸收热量
D.相同反应物在不同条件下产物可能不同
9.(2024•阳新县模拟)实验室通过H +CuO Cu+H O可制得金属铜,装置如图,下列说法不正确的
2 2
是( )
A.上述得到Cu的反应属于置换反应
B.甲的作用是制备氢气
C.乙中反应为NaOH+HCl═NaCl+H O
2
D.丁中现象是固体由红色变为黑色
10.(2024•闵行区二模)能观察到明显现象的实验是( )
A.铜片插入硝酸银溶液中
B.酚酞试液滴入稀硫酸中
C.稀盐酸滴入澄清石灰水中
D.二氧化碳气体通入水中
11.(2024•高新区校级模拟)化学观念是化学课程要培养的核心素养之一。下列从不同化学观念对物质认
识正确的是( )
A.结构观:CO和CO 都是由碳原子和氧原子构成,因此化学性质相似
2
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.元素观:生铁和钢均含有铁元素、碳元素,因此性能完全相同
C.守恒观:化学反应前后元素质量不变,因此6g镁与6g氧气反应生成12g氧化镁
D.微粒观:酸溶液中的阳离子都是氢离子,因此酸具有相似的化学性质
12.(2024•东昌府区一模)以下是摘录小艾同学记录的部分实验现象,其中有错误的是( )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.向石灰水中滴加紫色石蕊试液,溶液变成蓝色
C.将浓盐酸敞口一天后测其酸碱度,发现pH的数值变小了
D.将生锈的铁钉放入足量稀盐酸中,开始溶液变黄,一段时间后,铁钉表面有气泡生成
13.(2024•锡山区模拟)mgCaCO 煅烧一段时间,冷却,称得剩余固体的质量为21.2g,向剩余固体中加
3
入足量的稀HCl,充分反应,将所得溶液蒸干,得到33.3gCaCl ,下列说法不正确的是( )
2
A.m=30
B.剩余固体中CaCO 、CaO的质量比为25:14
3
C.向剩余固体中加入稀HCl时,会有气泡产生
D.煅烧前后的固体分别与足量稀HCl反应,两者消耗HCl的质量相等
14.(2024•武威一模)化学源于生活,生活中很多现象蕴含着化学知识,请你填空:
(1)下列物质中,能够使紫色石蕊溶液变为红色的是 (填字母序号)。
A.石灰水 B.白醋 C.稀盐酸 D.蒸馏水
(2)浓硫酸能使木条变黑,是因为浓硫酸有 性,浓硫酸敞口放置空气中,溶液质量将
(填“增大”或“减小”)。
(3)某食盐中“碘”主要以碘酸钾(KIO )的形式加入,其中碘元素的化合价为 价。
3
(4)新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号 。
(5)共享单车支架常用铝合金,铝合金硬度比纯铝 (填“大”或“小”)。
15.(2024•越秀区校级一模)截至2023年12月,广州地铁运营线路共16条,运营里程653公里,位列
中国第三名。
(1)列车车厢顶部用石墨做电弓是利用石墨具有良好的 性。
(2)列车车厢用到了大量的铝合金材料,铝制品具有较好的抗腐蚀性能是因为
。
(3)列车车厢表面刷漆是为了防止金属生锈,铁锈中主要成分是Fe O ,可用盐酸除铁锈,其反应的化学
2 3
方程式是 。
(4)列车钢轨采用铝和氧化铁在高温下反应生成铁和氧化铝,实现无缝焊接,该反应的化学方程式为
。
16.(2024•沈丘县一模)合金是重要的金属材料。
(1)如图能表示锡铅合金的是 (填“a”“b”或“c”)。
(2)铝具有较好的抗腐蚀性能,原因是铝在空气中能形成一层致密的 (填化学式)薄膜。
(3)镁与氢气在300℃和高压条件下,能发生化合反应生成氢化镁(MgH ),反应的化学方程式为
2
。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
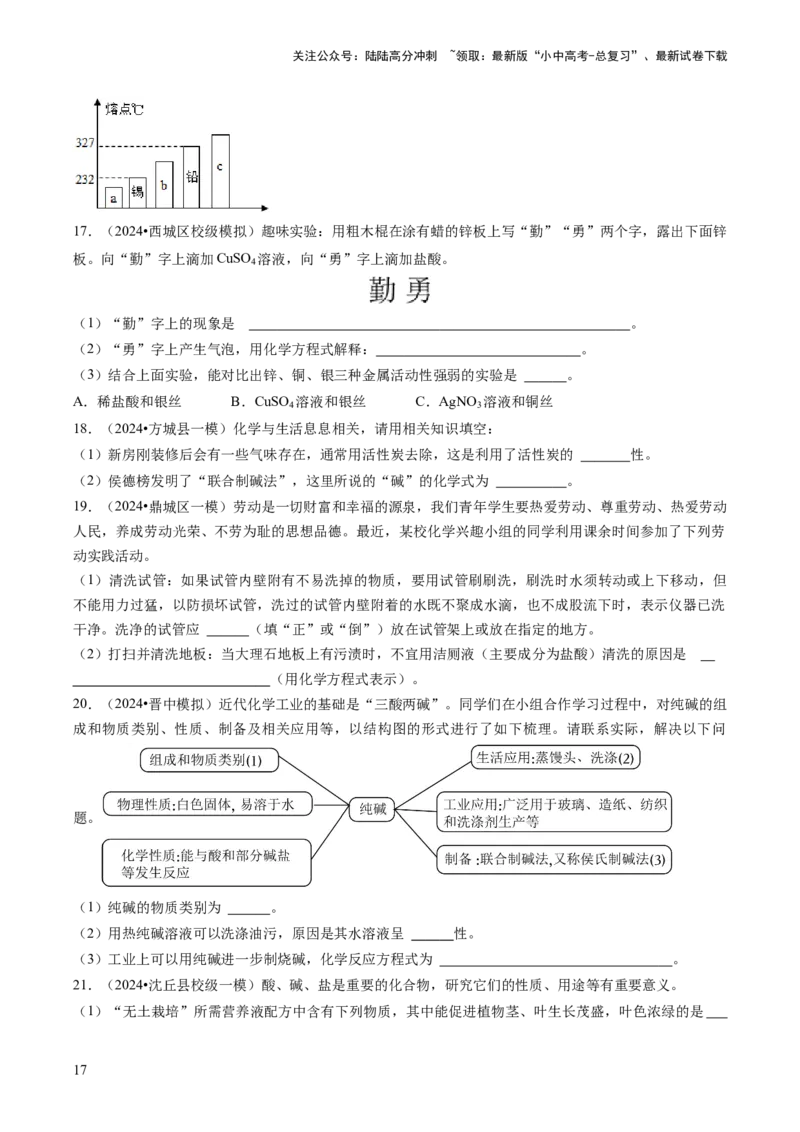
17.(2024•西城区校级模拟)趣味实验:用粗木棍在涂有蜡的锌板上写“勤”“勇”两个字,露出下面锌
板。向“勤”字上滴加CuSO 溶液,向“勇”字上滴加盐酸。
4
(1)“勤”字上的现象是 。
(2)“勇”字上产生气泡,用化学方程式解释: 。
(3)结合上面实验,能对比出锌、铜、银三种金属活动性强弱的实验是 。
A.稀盐酸和银丝 B.CuSO 溶液和银丝 C.AgNO 溶液和铜丝
4 3
18.(2024•方城县一模)化学与生活息息相关,请用相关知识填空:
(1)新房刚装修后会有一些气味存在,通常用活性炭去除,这是利用了活性炭的 性。
(2)侯德榜发明了“联合制碱法”,这里所说的“碱”的化学式为 。
19.(2024•鼎城区一模)劳动是一切财富和幸福的源泉,我们青年学生要热爱劳动、尊重劳动、热爱劳动
人民,养成劳动光荣、不劳为耻的思想品德。最近,某校化学兴趣小组的同学利用课余时间参加了下列劳
动实践活动。
(1)清洗试管:如果试管内壁附有不易洗掉的物质,要用试管刷刷洗,刷洗时水须转动或上下移动,但
不能用力过猛,以防损坏试管,洗过的试管内壁附着的水既不聚成水滴,也不成股流下时,表示仪器已洗
干净。洗净的试管应 (填“正”或“倒”)放在试管架上或放在指定的地方。
(2)打扫并清洗地板:当大理石地板上有污渍时,不宜用洁厕液(主要成分为盐酸)清洗的原因是
(用化学方程式表示)。
20.(2024•晋中模拟)近代化学工业的基础是“三酸两碱”。同学们在小组合作学习过程中,对纯碱的组
成和物质类别、性质、制备及相关应用等,以结构图的形式进行了如下梳理。请联系实际,解决以下问
题。
(1)纯碱的物质类别为 。
(2)用热纯碱溶液可以洗涤油污,原因是其水溶液呈 性。
(3)工业上可以用纯碱进一步制烧碱,化学反应方程式为 。
21.(2024•沈丘县校级一模)酸、碱、盐是重要的化合物,研究它们的性质、用途等有重要意义。
(1)“无土栽培”所需营养液配方中含有下列物质,其中能促进植物茎、叶生长茂盛,叶色浓绿的是
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(填字母)。
a.CO(NH ) b.K SO c.KH PO d.MgSO
2 2 2 4 2 4 4
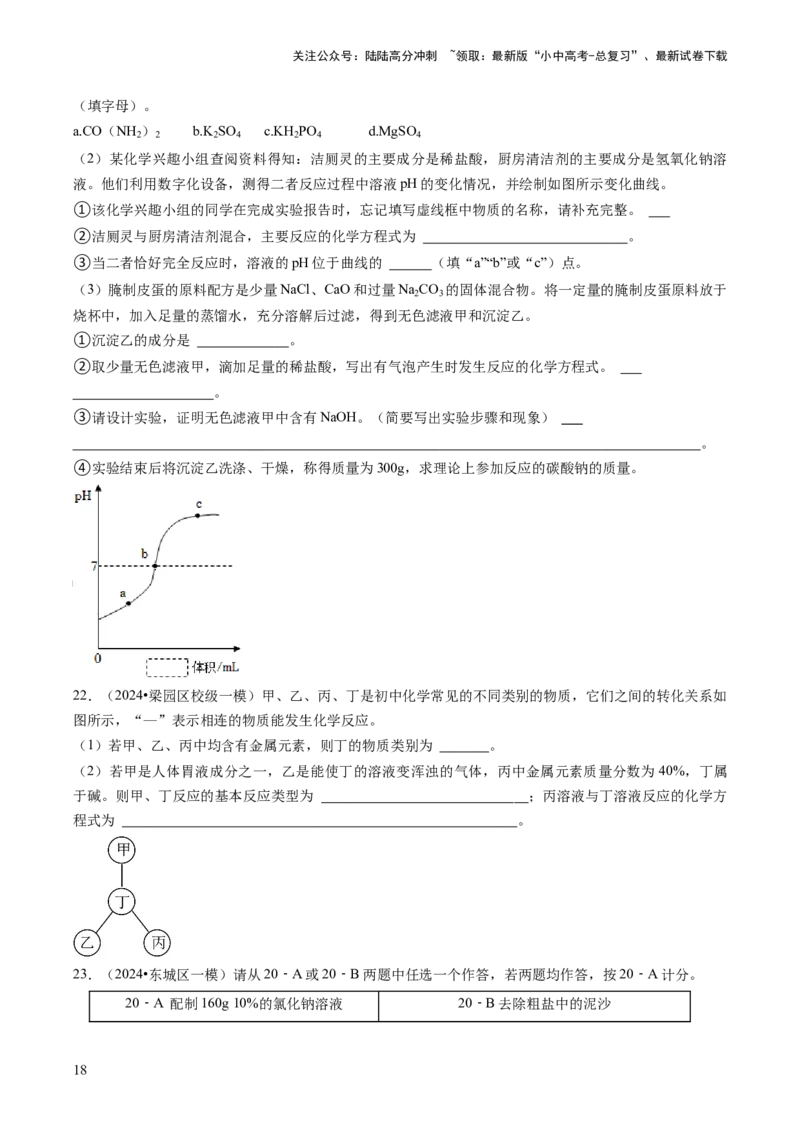
(2)某化学兴趣小组查阅资料得知:洁厕灵的主要成分是稀盐酸,厨房清洁剂的主要成分是氢氧化钠溶
液。他们利用数字化设备,测得二者反应过程中溶液pH的变化情况,并绘制如图所示变化曲线。
①该化学兴趣小组的同学在完成实验报告时,忘记填写虚线框中物质的名称,请补充完整。
②洁厕灵与厨房清洁剂混合,主要反应的化学方程式为 。
③当二者恰好完全反应时,溶液的pH位于曲线的 (填“a”“b”或“c”)点。
(3)腌制皮蛋的原料配方是少量NaCl、CaO和过量Na CO 的固体混合物。将一定量的腌制皮蛋原料放于
2 3
烧杯中,加入足量的蒸馏水,充分溶解后过滤,得到无色滤液甲和沉淀乙。
①沉淀乙的成分是 。
②取少量无色滤液甲,滴加足量的稀盐酸,写出有气泡产生时发生反应的化学方程式。
。
③请设计实验,证明无色滤液甲中含有NaOH。(简要写出实验步骤和现象)
。
④实验结束后将沉淀乙洗涤、干燥,称得质量为300g,求理论上参加反应的碳酸钠的质量。
22.(2024•梁园区校级一模)甲、乙、丙、丁是初中化学常见的不同类别的物质,它们之间的转化关系如
图所示,“—”表示相连的物质能发生化学反应。
(1)若甲、乙、丙中均含有金属元素,则丁的物质类别为 。
(2)若甲是人体胃液成分之一,乙是能使丁的溶液变浑浊的气体,丙中金属元素质量分数为40%,丁属
于碱。则甲、丁反应的基本反应类型为 ;丙溶液与丁溶液反应的化学方
程式为 。
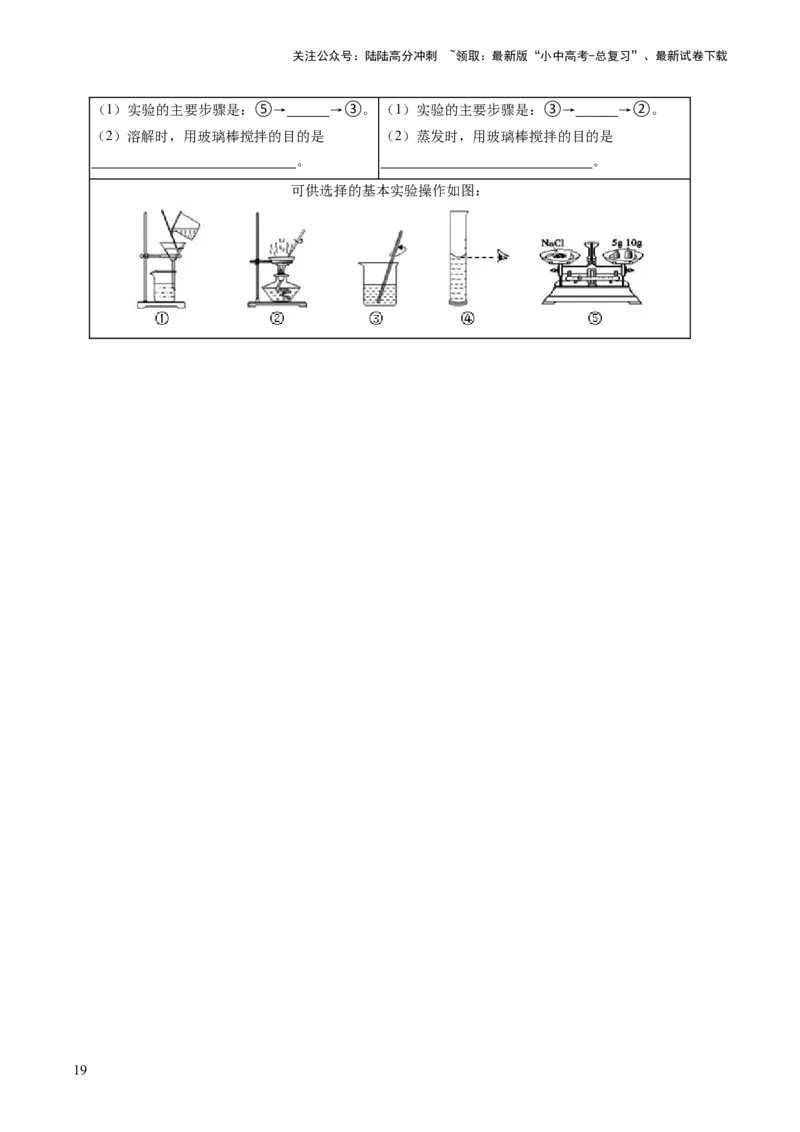
23.(2024•东城区一模)请从20﹣A或20﹣B两题中任选一个作答,若两题均作答,按20﹣A计分。
20﹣A 配制160g 10%的氯化钠溶液 20﹣B去除粗盐中的泥沙
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)实验的主要步骤是:⑤→ →③。 (1)实验的主要步骤是:③→ →②。
(2)溶解时,用玻璃棒搅拌的目的是 (2)蒸发时,用玻璃棒搅拌的目的是
。 。
可供选择的基本实验操作如图:
19