文档内容
2007 年江苏高考化学真题及答案
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28
S 32 Cl 35.5 K 39 Ca 40 Fe 56 Cu 64 Br 80
一、单项选择题:本题包括8小题,每小题4分。共计32分。每小题只有一个选项符合题意。
1.据估计,地球上的绿色植物通过光合作用每年能结合来自CO 中的碳1500亿吨和来自水中
2
的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:
光能
CO
2
+ H
2
O + 微量元素(P、N等)
叶绿素
(蛋白质、碳水化台物、脂肪等)+O
2
下列说法不正确的是
A.某些无机物通过光合作用可转化为有机物
B.碳水化合物就是碳和水组成的化合物
C.叶绿素是光合作用的催化剂
D.增加植被,保护环境是人类生存的需要
2. 下列叙述正确的是
A.聚丙烯的结构简式为: ComCH-CH-CHCom
bin 2 2 2bin
B.石英的化学式为:CaSiO
3
C.在CS、PCl 中各原子最外层均能达到8电子的稳定结构
2 3
D.Ar原子的结构示意图为
3.三聚氰酸[CN(OH)]可用于消除汽车尾气中的NO。其反应原理为:
3 3 3 2
CN(OH) ==== 3HNCO; 8HNCO+6NO ==== 7N+8CO+4HO
3 3 3 2 2 2 2
下列说法正确的是
A.CN(OH) 与HNCO为同一物质 B.HNCO是一种很强的氧化剂
3 3 3
C.1 molNO 在反应中转移的电子为4mol D.反应中NO 是还原剂
2 2
4.下列说法正确的是
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
5.下列有关实验的说法正确的是
A.除去铁粉中混有的少量铝粉。可加人过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备Fe(OH) 胶体,通常是将Fe(OH) 固体溶于热水中
3 3
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO2-
3
6. 向存在大量Na+、Cl-的溶液中通入足量的NH 后,该溶液中还可能大量存在的离子组是
3
A.K+、Br-、CO2-
3
B.Al3+、H+、MnO-
4
C.NH+、Fe3+、SO2-
4 4
D.Ag+、Cu2+、NO-
3
7.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原 能 量
理是
CHOH(g)+HO(g)
①CHOH(g)+HO(g)=CO(g)+3H(g); △H= + 49.0 kJ·mol-1 反应物的总 3 2
3 2 2 2
能量
②CHOH(g)+O(g)=CO(g)+2H(g); △H=-192.9 kJ·mol-1
3 2 2 2
下列说法正确的是 ΔH
A.CHOH的燃烧热为192.9 kJ·mol-1
3
B.反应①中的能量变化如右图所示 生成物的总
C.CHOH转变成H 的过程一定要吸收能量 能量
3 2 CO(g)+3H(g)
2 2
D.根据②推知反应:CHOH(l)+O(g)=CO(g)+2H(g)的△H>-
3 2 2 2
反应过程192.9kJ·mol-1
8.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.2.24LCO 中含有的原子数为0.3 ×6.02×1023
2
B.0.1L3 mol·L-1的NHNO 溶液中含有的NH+数目为0.3 ×6.02×1023
4 3 4
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D.4.5 SiO 晶体中含有的硅氧键数目为0.3 ×6.02×1023
2
二、不定项选择题:本题包括8小题.每小题4分。共计32分。每小题有一个或两个选项符合题意。若
正确答案只包括一个选项,多选时该题为0分;若正确答案包括两个选项,只选一个且正确的
得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.下列离子方程式书写正确的是
A.过量的SO 通入NaOH溶液中:SO+2OH-=SO2-+HO
2 2 3 2
B.Fe(NO) 溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I
3 3 2
C.NaNO 溶液中加入酸性KMnO 溶液:2MnO-+5NO-+6H+=2Mn2++5NO-+3HO
2 4 4 2 3 2
D.NaHCO 溶液中加入过量的Ba(OH) 溶液:2HCO-+Ba2++2OH-=BaCO↓+2HO+CO2-
3 2 3 3 2 3
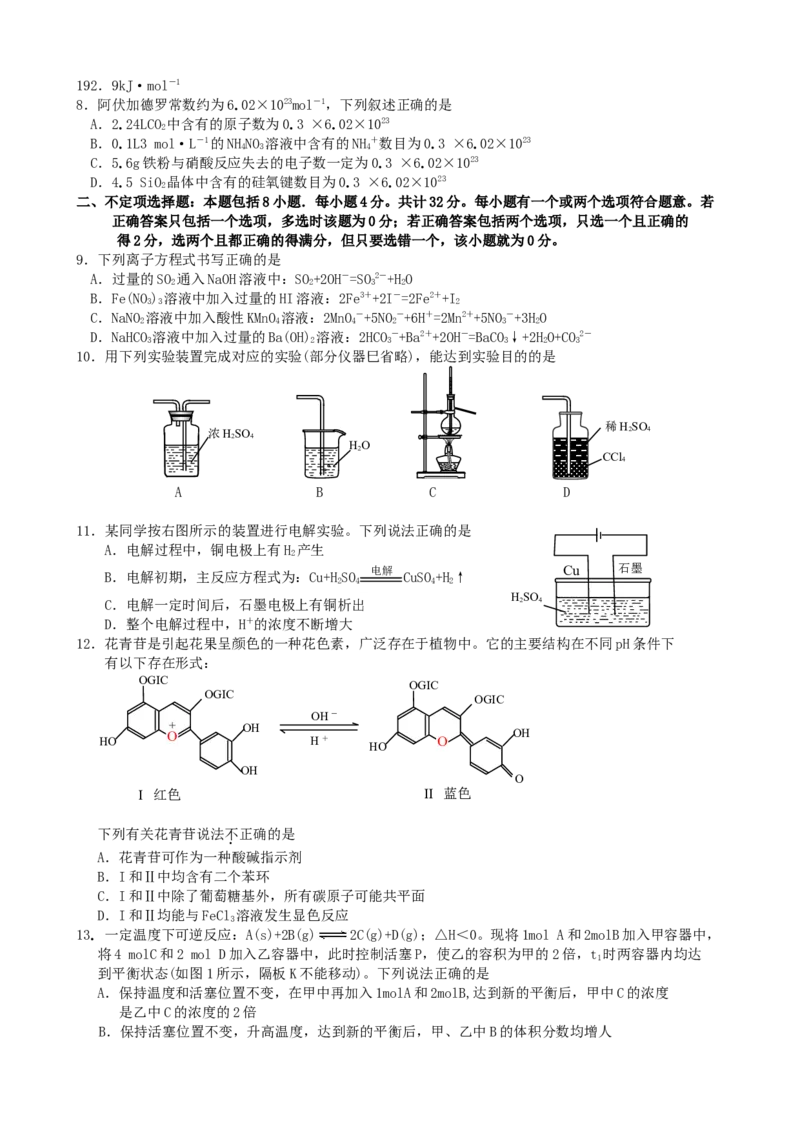
10.用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
稀HSO
浓HSO 2 4
2 4
HO
2
CCl
4
A B C D
11.某同学按右图所示的装置进行电解实验。下列说法正确的是
A.电解过程中,铜电极上有H 产生
2
电解 Cu 石墨
B.电解初期,主反应方程式为:Cu+HSO CuSO+H↑
2 4 4 2
HSO
C.电解一定时间后,石墨电极上有铜析出 2 4
D.整个电解过程中,H+的浓度不断增大
12.花青苷是引起花果呈颜色的一种花色素,广泛存在于植物中。它的主要结构在不同pH条件下
有以下存在形式:
OGIC
OGIC
OGIC
OGIC
OH-
+ OH
O OH
HO H+ O
HO
OH
O
I 红色 II 蓝色
下列有关花青苷说法不正确的是
A.花青苷可作为一种酸碱指示剂
B.I和Ⅱ中均含有二个苯环
C.I和Ⅱ中除了葡萄糖基外,所有碳原子可能共平面
D.I和Ⅱ均能与FeCl 溶液发生显色反应
3
13. 一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,
将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t 时两容器内均达
1
到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度
是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增人C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数
是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t 时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速
2
率变化情况分别如图2和图3所示(t 前的反应速率变化已省略)
1
K
P
甲 乙
1 2 3 活塞
4
图1
14.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同
(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X,则Y元素形成的单质一定是Y
2 2
D.若Y的最高正价为+m,则X的最高正价一定为+m
15.下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.l mol·L-1CuSO·(NH)SO·6HO的溶液中:c(SO2-)>c(NH+))>c(Cu2+)>c(H+)>c(OH-)
4 4 2 4 2 4 4
C.0.1 mol·L-1NaHCO 溶液中: c(Na+)+c(H+)+c(HCO)=c(HCO-)+c(CO2-)+c(OH-)
3 2 3 3 3
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)
16.某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部
投入50mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
下列说法正确的是
A.若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
B.若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-)
三、本题包括2小题.共计22分。
17.(10分)实验室常利用甲醛法测定(NH)SO 样品中氮的质量分数,其反应原理为:
4 2 4
4NH++6HCHO=3H++6HO+(CH)NH+ [滴定时,1 mol(CH)NH+与 l mol H+相当],
4 2 2 6 4 2 6 4
然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置
5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由 色变成 色。
V率速
甲容器
V正=V逆 V正=V逆
tt 11 t 2 时间 t
V率速
乙容器
V正=V逆
V正
V正=V逆
V逆
t 1 t 2 时间 t
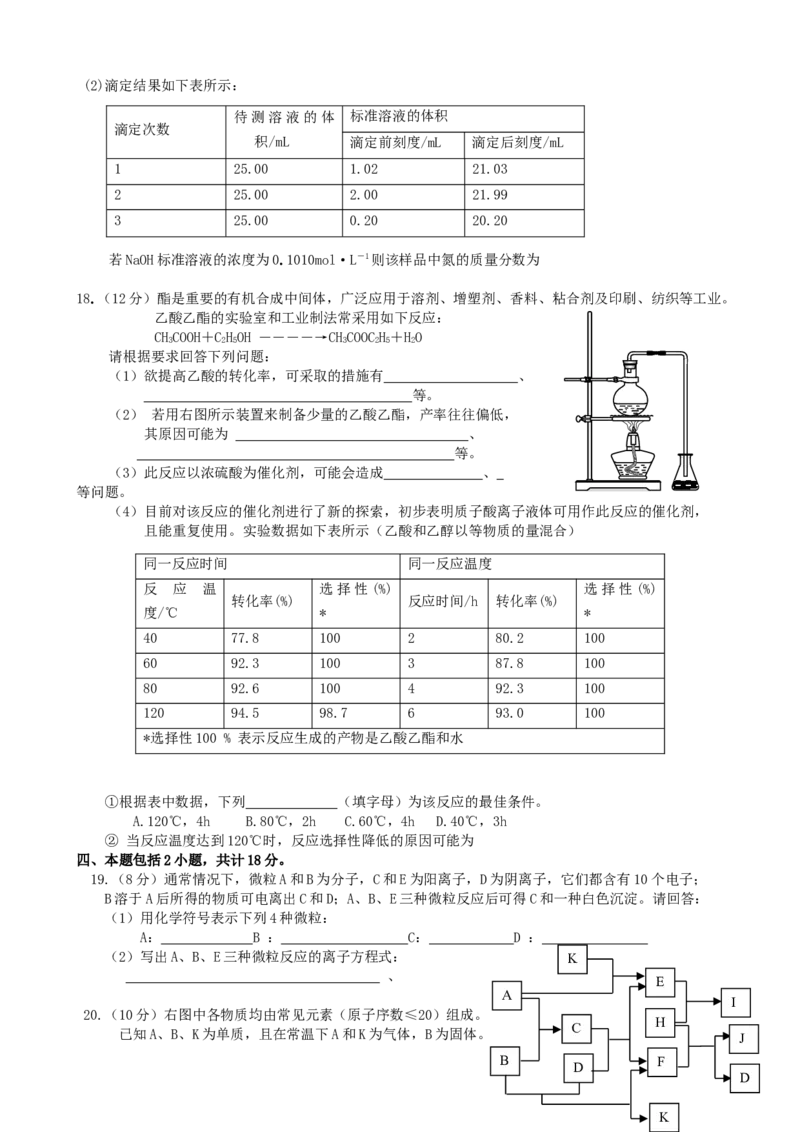
图2 图3(2)滴定结果如下表所示:
待测溶液的体 标准溶液的体积
滴定次数
积/mL 滴定前刻度/mL 滴定后刻度/mL
1 25.00 1.02 21.03
2 25.00 2.00 21.99
3 25.00 0.20 20.20
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为
18.(12分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。
乙酸乙酯的实验室和工业制法常采用如下反应:
CHCOOH+CHOH ――――→CHCOOCH+HO
3 2 5 3 2 5 2
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有 、
等。
(2) 若用右图所示装置来制备少量的乙酸乙酯,产率往往偏低,
其原因可能为 、
等。
(3)此反应以浓硫酸为催化剂,可能会造成 、
等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,
且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
同一反应时间 同一反应温度
反 应 温 选择性(%) 选择性(%)
转化率(%) 反应时间/h 转化率(%)
度/℃ * *
40 77.8 100 2 80.2 100
60 92.3 100 3 87.8 100
80 92.6 100 4 92.3 100
120 94.5 98.7 6 93.0 100
*选择性100 % 表示反应生成的产物是乙酸乙酯和水
①根据表中数据,下列 (填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
② 当反应温度达到120℃时,反应选择性降低的原因可能为
四、本题包括2小题,共计18分。
19.(8分)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;
B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A: B : C: D :
(2)写出A、B、E三种微粒反应的离子方程式: K
、
E
A
I
20.(10分)右图中各物质均由常见元素(原子序数≤20)组成。
H
C
已知A、B、K为单质,且在常温下A和K为气体,B为固体。
J
B F
D
D
KD为常见的无色液体。I是一种常用的化肥,在其水溶液中滴
加AgNO 溶液有不溶于稀HNO 的白色沉淀产生。J是一种实验
3 3
室常用的干燥剂。它们的相互转化关系如右图所示
(图中反应条件未列出)。请回答下列问题:
(1)I的化学式为 ; J的电子式为
(2)反应①的化学方程式为
(3)F的水溶液与氯气反应的离子方程式为
五、本题包括1小题,共计10分。
21.(10分)工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N、O 外,还含有SO、微量的SO
2 2 2 3
和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO 转化为有用
2
的副产品。请按要求回答下列问题:(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生
的两个氧化还原反应的化学方程式: 、
。
(2)在尾气与氨水反应所得到的高浓度溶液中,按一定比例加入氨水或碳酸氢铵,此时溶液的温度
会自行降低,并析出晶体。
①导致溶液温度降低的原因可能是 ;
②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质
量为134,则其化学式为 ;
③生产中往往需要向溶液中加入适量的对苯二酚或对苯二胺等物质,其目的是
(3)能用于测定硫酸尾气中SO 含量的是 。(填字母)
2
A.NaOH溶液、酚酞试液 B.KMnO 溶液、稀HSO
4 2 4
C.碘水、淀粉溶液 D.氨水、酚酞试液
六、本题包括2小题,共计18分。
22. (8分)肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中。
工业上可通过下列反应制备:
-CHO+CHCHO――――→-CH=CHCHO+HO
3 2
A B
(1)请推测B侧链上可能发生反应的类型: (任填两种)
(2)请写出两分子乙醛在上述条件下反应的化学方程式:
(3)请写出同时满足括号内条件下的所有同分异构体的结构简式:
(①分子中不含羰基和羟基 ②是苯的对二取代物 ③除苯环外,不含其他环状结构。)
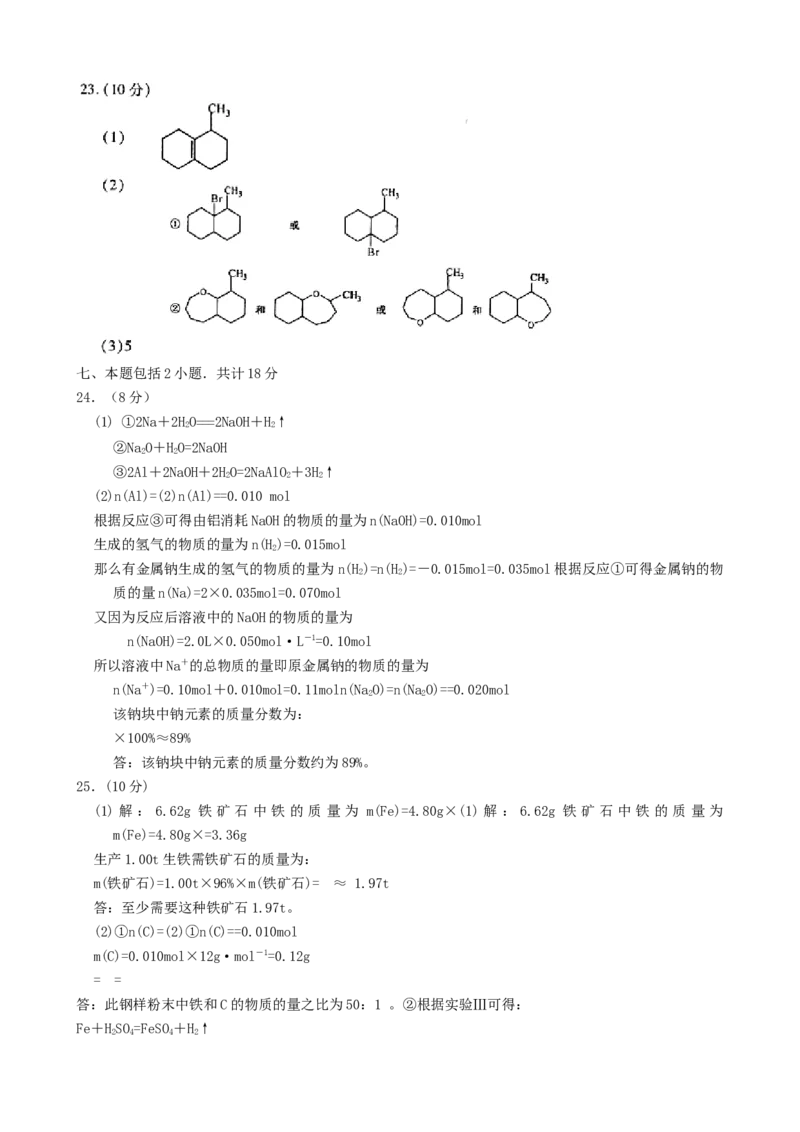
23.(10分)物质A(C H )是一种不饱和烃,它广泛存在于自然界中,也是重要的有机合成
11 18
中间体之一。某化学实验小组从A经反应①到⑤完成了环醚F的合成工作:
――――→B――――→C――――→D―――――→E―――――→F
该小组经过上述反应,最终除得到F 外,还得到它的同分异构体,
1
其中B、C、D、E、F、分别代表一种或多种物质。已知:
R 1 R 3 ①O R 1 R 3
C= C= + C=
R 2 C R 4 ②Zn3/H 2 O R 2 O R 4 O
(R、R、R、R 为烃基或H)
1 2 3 4请完成:
(1)写出由A制备环醚F 的合成路线中C的结构简式: 。
1
(2)①写出B的一种结构简式:
②写出由该B出发经过上述反应得到的F 的同分异构体的结构简式: 。
1
(3)该小组完成由A到F的合成工作中,最多可得到 种环醚化合物。
七、本题包括2小题.共计18分。
24.(8分)在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除氧化膜、并用针刺
一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器
中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内
溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050mol·L-1
(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块中钠元素的质量分数。
25.(10分)钢铁工业是国家工业的基础。2006年我国粗钢产量突破4亿吨,居世界首位。
某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工
艺流程有了全面的感性认识。请您对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62 g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH 溶液,
充分反应后,过滤、洗涤、灼烧得4.80g FeO。现以该铁矿石为原料炼铁,若生产过程中铁
2 3
元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?
(保留两位小数)
(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO 气体224mL(标准状况)。
2
① 计算此钢样粉术中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末 分别加到100mL相通浓度的HSO 溶液中,充分反 应后,
2 4
测得的实验数据如下表所示:
实验序号 Ⅰ Ⅱ Ⅲ
加入钢样粉末的质量/g 2.812 5.624 8.436
生成气体的体积/L(标准状况) 1.120 2.240 2.800
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?
(用含m的代数式表示)参考答案
一、单项选择题:本题包括8小题,每小题4分。共计32分。
1.B 2.C 3.C 4.B 5.A 6.A 7.D 8.D
二、不定项选择题:本题包括8小题.每小题4分。共计32分。
9.C 10.D 11.BC 12.B 13.BD 14.A 15.CD 16.AD
三、本题包括2小题.共计22分。
17.(10分)(1)①偏高 ②无影响 ③ B ④ 无 粉红(或浅红) (2) 18.85%
18.(12)分(1)增大乙醇的浓度 移去生成物
(2)原料来不及反应就蒸出 温度过高发生了副反应 冷凝效果不好,部分产物挥发了(任填两种)
(3)产生大量酸性废液(或造成环境污染) 部分原料炭化 催化剂重复使用困难 催化效果不理想 (任填
两种)
(4)①C ②乙醇脱水生成了乙醚
四、本题包括2小题,共计18分
19.(8分)
(1)HO NH NH+ OH-
2 3 4
(2)Al3++3NH+3HO===Al(OH)↓+3NH+
3 2 3 4
Mg2++2NH+2HO===Mg(OH)↓+2NH+
3 2 2 4
20.(10分)
(1)HCl 氯化钙 电子式
N 4
(2)CaN+6HO===3Ca(OH)+2NH↑
3 2 2 2 3
(3)3Cl+2OH-===ClO-+Cl-+HO
2 2
五、本题包括1小题,共计10分
21.(10分)(1)2HSO+O===2HSO 2(NH)SO+O===2(NH)SO
2 3 2 2 4 4 2 3 2 4 2 4
2NHHSO+O===2NHHSO(任填两个)
4 3 2 4 4
(2)①反应吸热 ②(NH)SO·HO③防止亚硫酸铵被氧化
4 2 3 2
(3)BC
六、本题包括2小题,共计18分
22.(8分)
(1)加成反应 氧化反应 还原反应
(2)2CHCHO CHCH=CHCHO+HO
3 3 2
NaOH
Δ
(3)HC-O- -C≡CH ,HC- -O-C≡CH
3 3七、本题包括2小题.共计18分
24.(8分)
(1) ①2Na+2HO===2NaOH+H↑
2 2
②NaO+HO=2NaOH
2 2
③2Al+2NaOH+2HO=2NaAlO+3H↑
2 2 2
(2)n(Al)=(2)n(Al)==0.010 mol
根据反应③可得由铝消耗NaOH的物质的量为n(NaOH)=0.010mol
生成的氢气的物质的量为n(H)=0.015mol
2
那么有金属钠生成的氢气的物质的量为n(H)=n(H)=-0.015mol=0.035mol根据反应①可得金属钠的物
2 2
质的量n(Na)=2×0.035mol=0.070mol
又因为反应后溶液中的NaOH的物质的量为
n(NaOH)=2.0L×0.050mol·L-1=0.10mol
所以溶液中Na+的总物质的量即原金属钠的物质的量为
n(Na+)=0.10mol+0.010mol=0.11moln(NaO)=n(NaO)==0.020mol
2 2
该钠块中钠元素的质量分数为:
×100%≈89%
答:该钠块中钠元素的质量分数约为89%。
25.(10分)
(1) 解 : 6.62g 铁 矿 石 中 铁 的 质 量 为 m(Fe)=4.80g×(1) 解 : 6.62g 铁 矿 石 中 铁 的 质 量 为
m(Fe)=4.80g×=3.36g
生产1.00t生铁需铁矿石的质量为:
m(铁矿石)=1.00t×96%×m(铁矿石)= ≈ 1.97t
答:至少需要这种铁矿石1.97t。
(2)①n(C)=(2)①n(C)==0.010mol
m(C)=0.010mol×12g·mol-1=0.12g
= =
答:此钢样粉末中铁和C的物质的量之比为50:1 。②根据实验Ⅲ可得:
Fe+HSO=FeSO+H↑
2 4 4 21mol 22.4L
n(HSO) 2.800L
2 4
n(HSO)=1.125mol
2 4
c(HSO)=c(HSO)==1.25mol·L-1
2 4 2 4
答:硫酸溶液的物质的量浓度为1.25mol·L-1。
③当钢样粉末中的铁未全部溶解时(m>1.406g),剩余的固体质量为:
(5.624g+m g)-0.125mol×56g·mol-1=(m-1.376)g
当钢样粉末中的铁全部溶解时(m≤1.406g),剩余的固体质量为:
(5.624+m)g×
答:当铁未完全溶解时,剩余固体的质量为(m-1.376)g;
当铁完全溶解时,剩余固体质量为(5.624+m)g×