文档内容
2012 年普通高等学校招生全国统一考试理
科综合能力测试(山东卷)
化学试题
(1)气体A中的大气污染物可选用下列试剂中的______吸收。
a.浓HSO b.稀HNO c.NaOH溶液 d.氨水
2 4 3
第Ⅰ卷(必做,共88分) (2)用稀HSO 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在______(填离子符号),
2 4
相对原子质量:O 16 Na 23 S 32 Ca 40 Pb 207 检验溶液中还存在Fe2+的方法是______(注明试剂、现象)。
一、选择题(本题包括15小题,每小题只有一个选项符合题意) (3)由泡铜冶炼粗铜的化学反应方程式为____________________________。
7.下列与化学概念有关的说法正确的是( ) (4)以CuSO 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
4
A.化合反应均为氧化还原反应 ______。
B.金属氧化物均为碱性氧化物 a.电能全部转化为化学能
C.催化剂能改变可逆反应达到平衡的时间 b.粗铜接电源正极,发生氧化反应
D.石油是混合物,其分馏产品汽油为纯净物 c.溶液中Cu2+向阳极移动
8.下列与含氯化合物有关的说法正确的是( ) d.利用阳极泥可回收Ag、Pt、Au等金属
A.HClO是弱酸,所以NaClO是弱电解质 (5)利用反应2Cu+O +2HSO ===2CuSO +2HO可制备CuSO ,若将该反应设计为原电池,其正极电极反应
2 2 4 4 2 4
B.向沸水中逐滴加入少量饱和FeCl 溶液,可制得Fe(OH) 胶体 式为________________。
3 3
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 29.(16分)偏二甲肼与NO 是常用的火箭推进剂,二者发生如下化学反应:
2 4
D.电解NaCl溶液得到22.4 L H
2
(标准状况),理论上需要转移N
A
个电子(N
A
表示阿伏加德罗常数) (CH
3
)
2
NNH
2
(l)+2N
2
O
4
(l)===2CO
2
(g)+3N
2
(g)+4H
2
O(g) (Ⅰ)
9.下列关于原子结构、元素性质的说法正确的是( ) (1)反应(Ⅰ)中氧化剂是______。
A.非金属元素组成的化合物中只含共价键 (2)火箭残骸中常现红棕色气体,原因为:NO(g) 2NO (g) (Ⅱ)
2 4 2
B.ⅠA族金属元素是同周期中金属性最强的元素 当温度升高时,气体颜色变深,则反应(Ⅱ)为______(填“吸热”或“放热”)反应。
C.同种元素的原子均有相同的质子数和中子数
(3)一定温度下,反应(Ⅱ)的焓变为 H。现将1 mol N O 充入一恒压密闭容器中,下列示意图正确且能说明反
2 4
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
应达到平衡状态的是______。
10.下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO 溶液褪色
4
B.甲烷和Cl 的反应与乙烯和Br 的反应属于同一类型的反应
2 2
C.葡萄糖、果糖的分子式均为C H O,二者互为同分异构体
6 12 6
D.乙醇、乙酸均能与Na反应放出H,二者分子中官能团相同
2
11.下列实验操作正确的是( )
A.中和滴定实验时,用待测液润洗锥形瓶
B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”),
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 反应3 s后NO 的物质的量为0.6 mol,则0~3 s内的平均反应速率v(N O)=______ mol/(L·s)-1。
2 2 4
D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 (4)NO 可用氨水吸收生成 NH NO 。25 ℃时,将 a mol NH NO 溶于水,溶液显酸性,原因是
2 4 3 4 3
12.下列由相关实验现象所推出的结论正确的是( ) ________________(用离子方程式表示)。向该溶液滴加b L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡
A.Cl、SO 均能使品红溶液褪色,说明二者均有氧化性 将______(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为______mol·L-1。(NH ·H O的电离平衡常数取K =
2 2 3 2 b
B.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有 2×10-5 mol·L-1)
3 2
30.(14分)实验室采用MgCl 、AlCl 的混合溶液与过量氨水反应制备MgAlO,主要流程如下:
C.Fe与稀HNO、稀HSO 反应均有气泡产生,说明Fe与两种酸均发生置换反应 2 3 2 4
3 2 4
D.分别充满HCl、NH 的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
3
13.下列与金属腐蚀有关的说法正确的是( )
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入______(填“A”或“B”),再滴加另一反应物。
(2)如下图所示,过滤操作中的一处错误是______________________。
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,CuZn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,ZnMnO 干电池自放电腐蚀主要是由MnO 的氧化作用引起的
2 2
(3)判断流程中沉淀是否洗净所用的试剂是______。高温焙烧时,用于盛放固体的仪器名称是______。
第Ⅱ卷(必做120分+选做32分,共152分)
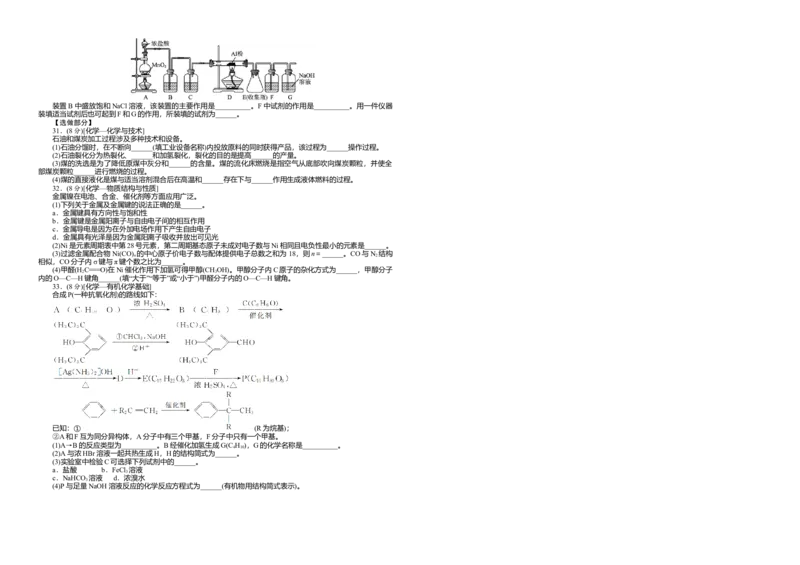
(4)无水AlCl (183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
【必做部分】 3
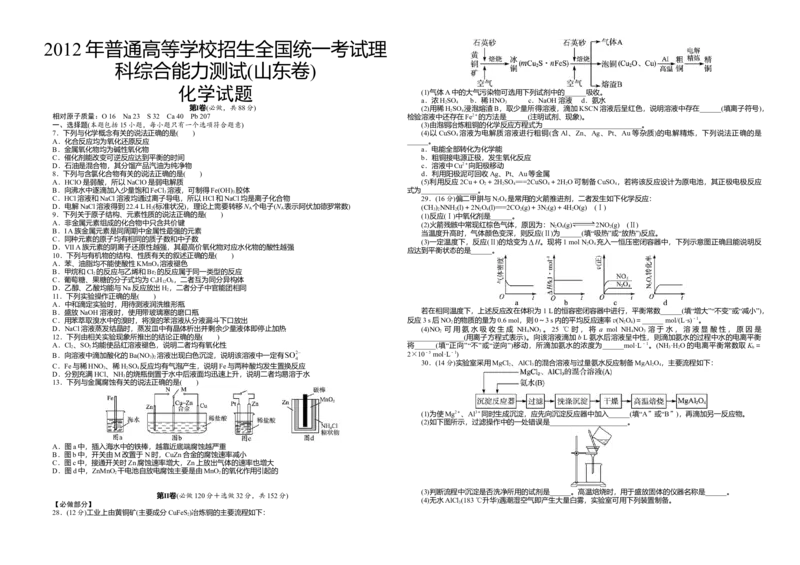
28.(12分)工业上由黄铜矿(主要成分CuFeS)冶炼铜的主要流程如下:
2装置B中盛放饱和NaCl溶液,该装置的主要作用是__________。F中试剂的作用是__________。用一件仪器
装填适当试剂后也可起到F和G的作用,所装填的试剂为______。
【选做部分】
31.(8分)[化学—化学与技术]
石油和煤炭加工过程涉及多种技术和设备。
(1)石油分馏时,在不断向______(填工业设备名称)内投放原料的同时获得产品,该过程为______操作过程。
(2)石油裂化分为热裂化、______和加氢裂化,裂化的目的是提高______的产量。
(3)煤的洗选是为了降低原煤中灰分和______的含量。煤的流化床燃烧是指空气从底部吹向煤炭颗粒,并使全
部煤炭颗粒______进行燃烧的过程。
(4)煤的直接液化是煤与适当溶剂混合后在高温和______存在下与______作用生成液体燃料的过程。
32.(8分)[化学—物质结构与性质]
金属镍在电池、合金、催化剂等方面应用广泛。
(1)下列关于金属及金属键的说法正确的是______。
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是______。
(3)过滤金属配合物Ni(CO) 的中心原子价电子数与配体提供电子总数之和为18,则n=______。CO与N 结构
n 2
相似,CO分子内σ键与π键个数之比为______。
(4)甲醛(H C===O)在Ni催化作用下加氢可得甲醇(CHOH)。甲醇分子内C原子的杂化方式为______,甲醇分子
2 3
内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
33.(8分)[化学—有机化学基础]
合成P(一种抗氧化剂)的路线如下:
已知:① (R为烷基);
②A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基。
(1)A→B的反应类型为__________。B经催化加氢生成G(C H ),G的化学名称是__________。
4 10
(2)A与浓HBr溶液一起共热生成H,H的结构简式为______。
(3)实验室中检验C可选择下列试剂中的______。
a.盐酸 b.FeCl 溶液
3
c.NaHCO 溶液 d.浓溴水
3
(4)P与足量NaOH溶液反应的化学反应方程式为______(有机物用结构简式表示)。