文档内容
2018年全国统一高考化学试卷(新课标Ⅱ)
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项
中,只有一项是符合题目要求的。
1.(6分)化学与生活密切相关,下列说法错误的是( )
A.碳酸钠可用于去除餐具的油污
B.漂白粉可用于生活用水的消毒
C.氢氧化铝可用于中和过多胃酸
D.碳酸钡可用于胃肠X射线造影检查
2.(6分)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关
(如图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
3.(6分)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
在光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
( )A. B.
C. D.
4.(6分)W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可
生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子
最外层的电子数与W的电子总数相同,下列叙述正确的是( )
A.X与其他三种元素均可形成两种或两种以上的二元化合物
B.Y与其他三种元素分别形成的化合物中只含有离子键
C.四种元素的简单离子具有相同的电子层结构
D.W的氧化物对应的水化物均为强酸
5.(6分)N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温常压下,124gP 中所含P一P键数目为4N
4 A
B.100 mL 1mol•L﹣1FeCl 溶液中所含Fe3+的数目为0.1N
3 A
C.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2N
A
D.密闭容器中,2 mol SO 和1molO 催化反应后分子总数为2N
2 2 A
6.(6分)我国科学家研发了一种室温下“可呼吸”的 Na﹣CO 二次电池,将
2
NaClO 溶于有机溶剂作为电解液。钠和负载碳纳米管的镍网分别作为电极材
4
料,电池的总反应为:3CO +4Na 2Na CO +C,下列说法错误的是( )
2 2 3
⇌A.放电时,ClO ﹣向负极移动
4
B.充电时释放CO ,放电时吸收CO
2 2
C.放电时,正极反应为:3CO +4e﹣═2CO 2﹣+C
2 3
D.充电时,正极反应为:Na++e﹣═Na
7.(6分)下列实验过程可以达到实验目的是( )
编号 实验目的 实验过程
A 配制 0.4000mol•L﹣1的 称取 4.0g固体 NaOH于烧杯中,加入少量蒸
NaOH溶液 馏水溶解,转移至250mL容量瓶中定容
B 探究维生素C的还原性 向盛有2mL黄色氯化铁溶液的试管中滴加浓
的维生素C溶液,观察颜色变化
C 制取并纯化氢气 向稀盐酸中加入锌粒,将生成的气体依次通
过NaOH溶液、浓硫酸和KMnO 溶液
4
D 探究浓度对反应速率 向 2 支盛有 5mL 不同浓度 NaHSO 溶液的试
3
的影响 管中同时加入 2mL5%H O 溶液,观察实验
2 2
现象
A.A B.B C.C D.D
二、非选择题:每个试题考生必须作答。
8.(14 分)我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿
(ZnS,含有SiO 和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如
2
图所示:相关金属离子[c (Mn+)=0.1mol•L﹣1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Fe3+ Fe2+ Zn2+ Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为 。
(2)滤渣1的主要成分除SiO 外还有 ;氧化除杂工序中ZnO的作用是
2
,若不通入氧气,其后果是 。
(3)溶液中的Cd2+用锌粉除去,还原除杂工序中反应的离子方程式为 。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为 ;沉积锌后的
电解液可返回 工序继续使用。
9.(14分)CH ﹣CO 的催化重整不仅可以得到合成气(CO和H ),还对温
4 2 2
室气体的减排具有重要意义。回答下列问题:
(1)CH ﹣CO 催化重整反应为:CH (g)+CO (g)═2CO(g)+2H
4 2 4 2 2
(g)。
已知:C(s)+2H (g)═CH (g)△H=﹣75kJ•mol﹣1
2 4
C(s)+O (g)=CO (g)△H=﹣394kJ•mol﹣1
2 2
C(s)+ (g)=CO(g)△H=﹣111kJ•mol﹣1
该催化重整反应的△H= kJ•mol﹣1.有利于提高CH 平衡转化率的条件是
4
(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
某温度下,在体积为2L的容器中加入2mol CH 、1molCO 以及催化剂进行重整
4 2
反应,达到平衡时CO 的转化率是50%,其平衡常数为 mol2•L﹣2。
2
(2)反中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳碳量减少。相关数据如下表:
积碳反应 消碳反应
CH (g)═C(s)+2H CO (g)+C(s)═2CO
4 2 2
(g) (g)
△H/(kJ•mol﹣1) 75 172
活化能/ 催化剂X 33 91
(kJ•mol﹣ 催化剂Y 43 72
1)
①由上表判断,催化剂X Y(填“优于或劣于”),理由是 。在
反应进料气组成,压强及反应时间相同的情况下,某催化剂表面的积碳量随
温度的变化关系如右图1所示。升高温度时,下列关于积碳反应,消碳反应
的平衡常数(K)和速率(v)的叙述正确的是 (填标号)。
A.K 、K 均增加
积 消
B.V 减小、V 增加
积 消
C.K 减小、K 增加
积 消
D.V 增加的倍数比V 增加的倍数大
消 积
图1 图2
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为 v=k•p(CH )•[p
4
(CO )]﹣0.5(k为速率常数)。在p(CH )一定时,不同p(CO )下积碳
2 4 2
量随时间的变化趋势如图2所示,则P (CO )、P (CO )、P (CO )从
a 2 b 2 c 2
大到小的顺序为 。
10.(15分)K [Fe(C O ) ]•3H O(三草酸合铁酸钾)为亮绿色晶体,可用
3 2 4 3 2
于晒制蓝图,回答下列问题:
(1)晒制蓝图时,用K [Fe(C O ) ]•3H O作感光剂,以K Fe[(CN) ]溶
3 2 4 3 2 3 6液为显色剂。其光解反应的化学方程式为 2K [Fe(C O ) ]
3 2 4 3
2FeC O +3K C O +2CO ↑;显色反应的化学方程式为 。
2 4 2 2 4 2
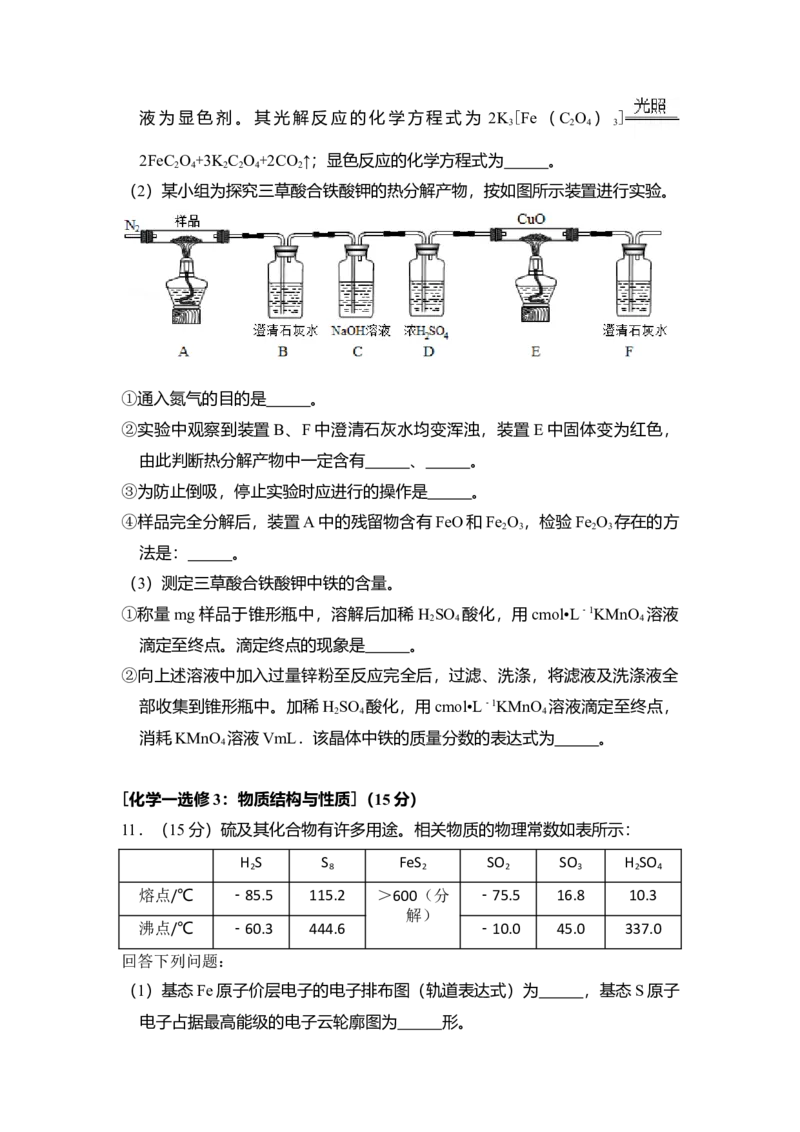
(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。
①通入氮气的目的是 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,
由此判断热分解产物中一定含有 、 。
③为防止倒吸,停止实验时应进行的操作是 。
④样品完全分解后,装置A中的残留物含有FeO和Fe O ,检验Fe O 存在的方
2 3 2 3
法是: 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀 H SO 酸化,用cmol•L﹣1KMnO 溶液
2 4 4
滴定至终点。滴定终点的现象是 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全
部收集到锥形瓶中。加稀H SO 酸化,用cmol•L﹣1KMnO 溶液滴定至终点,
2 4 4
消耗KMnO 溶液VmL.该晶体中铁的质量分数的表达式为 。
4
[化学一选修3:物质结构与性质](15分)
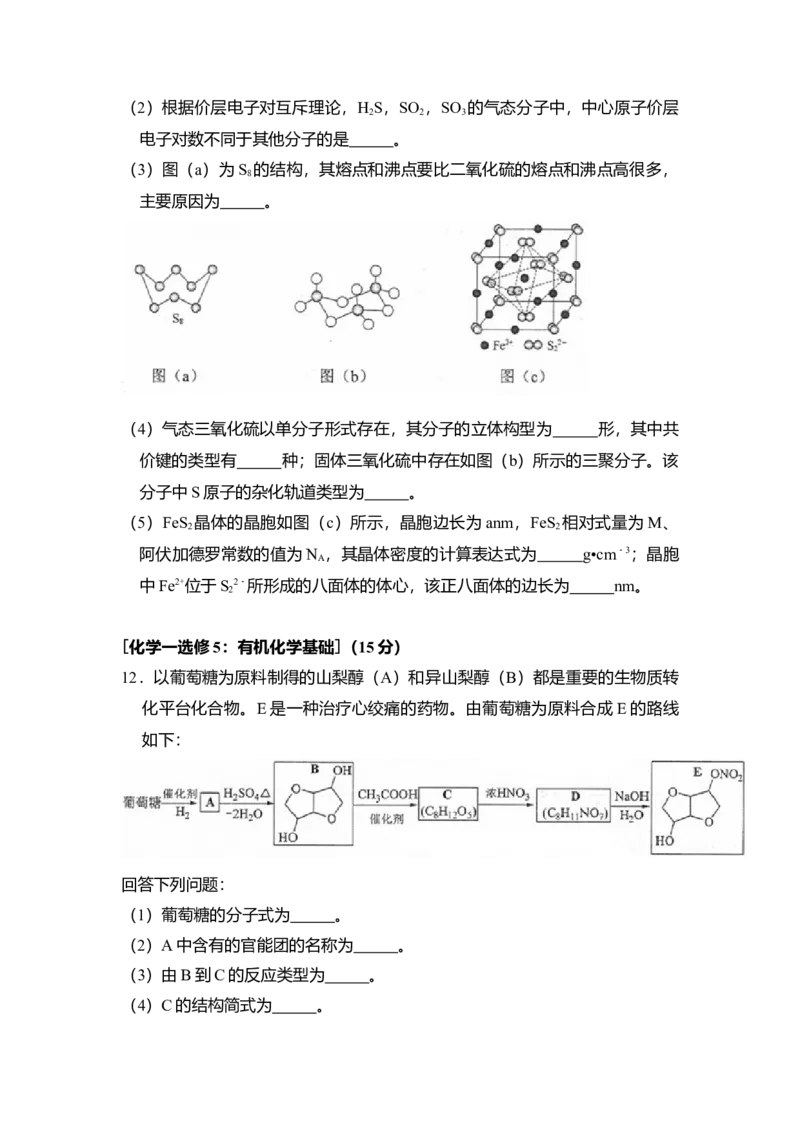
11.(15分)硫及其化合物有许多用途。相关物质的物理常数如表所示:
H S S FeS SO SO H SO
2 8 2 2 3 2 4
熔点/℃ ﹣85.5 115.2 >600(分 ﹣75.5 16.8 10.3
解)
沸点/℃ ﹣60.3 444.6 ﹣10.0 45.0 337.0
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为 ,基态S原子
电子占据最高能级的电子云轮廓图为 形。(2)根据价层电子对互斥理论,H S,SO ,SO 的气态分子中,中心原子价层
2 2 3
电子对数不同于其他分子的是 。
(3)图(a)为S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,
8
主要原因为 。
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为 形,其中共
价键的类型有 种;固体三氧化硫中存在如图(b)所示的三聚分子。该
分子中S原子的杂化轨道类型为 。
(5)FeS 晶体的晶胞如图(c)所示,晶胞边长为anm,FeS 相对式量为M、
2 2
阿伏加德罗常数的值为N ,其晶体密度的计算表达式为 g•cm﹣3;晶胞
A
中Fe2+位于S 2﹣所形成的八面体的体心,该正八面体的边长为 nm。
2
[化学一选修5:有机化学基础](15分)
12.以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转
化平台化合物。E是一种治疗心绞痛的药物。由葡萄糖为原料合成 E的路线
如下:
回答下列问题:
(1)葡萄糖的分子式为 。
(2)A中含有的官能团的名称为 。
(3)由B到C的反应类型为 。
(4)C的结构简式为 。(5)由D到E的反应方程式为 。
(6)F是B的同分异构体,7.30g的F与足量饱和碳酸氢钠反应可释放出2.24L
二氧化碳(标准状况),F的可能结构共有 种(不考虑立体异构);
其中核磁共振氢谱为三组峰,峰面积比为3:1:1的结构简式为 。