文档内容
山东省 2020 年普通高中学业水平等级考试
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净
后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Fe 56
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
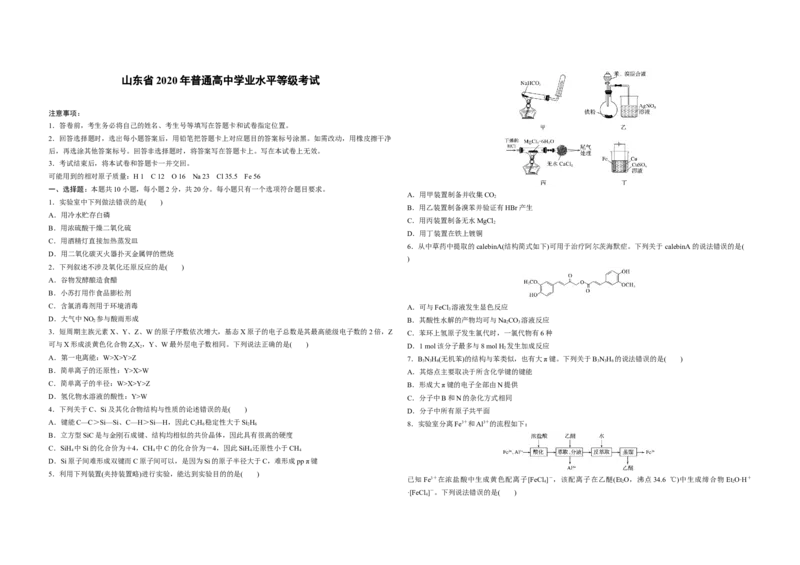
A.用甲装置制备并收集CO
2
1.实验室中下列做法错误的是( )
B.用乙装置制备溴苯并验证有HBr产生
A.用冷水贮存白磷
C.用丙装置制备无水MgCl
2
B.用浓硫酸干燥二氧化硫
D.用丁装置在铁上镀铜
C.用酒精灯直接加热蒸发皿
6.从中草药中提取的calebinA(结构简式如下)可用于治疗阿尔茨海默症。下列关于calebinA的说法错误的是(
D.用二氧化碳灭火器扑灭金属钾的燃烧
)
2.下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒 A.可与FeCl 溶液发生显色反应
3
D.大气中NO 2 参与酸雨形成 B.其酸性水解的产物均可与Na 2 CO 3 溶液反应
3.短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高能级电子数的2倍,Z C.苯环上氢原子发生氯代时,一氯代物有6种
可与X形成淡黄色化合物Z 2 X 2 ,Y、W最外层电子数相同。下列说法正确的是( ) D.1 mol该分子最多与8 mol H 2 发生加成反应
A.第一电离能:W>X>Y>Z 7.B NH(无机苯)的结构与苯类似,也有大π键。下列关于B NH 的说法错误的是( )
3 3 6 3 3 6
B.简单离子的还原性:Y>X>W A.其熔点主要取决于所含化学键的键能
C.简单离子的半径:W>X>Y>Z B.形成大π键的电子全部由N提供
D.氢化物水溶液的酸性:Y>W C.分子中B和N的杂化方式相同
4.下列关于C、Si及其化合物结构与性质的论述错误的是( ) D.分子中所有原子共平面
A.键能C—C>Si—Si、C—H>Si—H,因此C
2
H
6
稳定性大于Si
2
H
6
8.实验室分离Fe3+和Al3+的流程如下:
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于CH
4 4 4 4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成pp π键
5.利用下列装置(夹持装置略)进行实验,能达到实验目的的是( )
已知Fe3+在浓盐酸中生成黄色配离子[FeCl ]-,该配离子在乙醚(Et O,沸点34.6 ℃)中生成缔合物EtO·H+
4 2 2
·[FeCl ]-。下列说法错误的是( )
4A.萃取振荡时,分液漏斗下口应倾斜向下 出
B.分液时,应先将下层液体由分液漏斗下口放出 配制用于检验醛基的氢氧化铜 向试管中加入2 mL 10% NaOH溶液,再滴加数
D
C.分液后水相为无色,说明已达到分离目的 悬浊液 滴2% CuSO 溶液,振荡
4
D.蒸馏时选用直形冷凝管
9.以菱镁矿(主要成分为MgCO ,含少量SiO、Fe O 和Al O)为原料制备高纯镁砂的工艺流程如下: 12.α氰基丙烯酸异丁酯可用作医用胶,其结构简式如下。下列关于α氰基丙烯酸异丁酯的说法错误的是( )
3 2 2 3 2 3
已知浸出时产生的废渣中有SO ,Fe(OH) 和Al(OH) 。下列说法错误的是( ) A.其分子式为C H NO
2 3 3 8 11 2
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO B.分子中的碳原子有3种杂化方式
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行 C.分子中可能共平面的碳原子最多为6个
C.流程中可循环使用的物质有NH 、NH Cl D.其任一含苯环的同分异构体中至少有4种不同化学环境的氢原子
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同 13.采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,
sp
10.微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。 下列说法错误的是( )
现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含CHCOO-的溶液为例)。下列说法错
3
误的是( )
A.阳极反应为2HO-4e-===4H++O↑
2 2
B.电解一段时间后,阳极室的pH未变
A.负极反应为CHCOO-+2HO-8e-===2CO↑+7H+ C.电解过程中,H+由a极区向b极区迁移
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
14.1,3丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3丁二烯生成碳正离子( );第二步Br-
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
进攻碳正离子完成1,2加成或1,4加成。反应进程中的能量变化如下图所示。已知在0 ℃和40 ℃时,1,2加成产
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,
物与1,4加成产物的比例分别为70∶30和15∶85。下列说法正确的是( )
选对但不全的得2分,有选错的得0分。
11.下列操作不能达到实验目的的是( )
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与NaHCO 混合产生的气体直接通入苯
3
B 证明酸性:碳酸>苯酚
酚钠溶液
A.1,4加成产物比1,2加成产物稳定
C 除去碱式滴定管胶管内的气泡 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排
B.与0 ℃相比,40 ℃时1,3丁二烯的转化率增大C.从0 ℃升至40 ℃,1,2加成正反应速率增大,1,4加成正反应速率减小 (5)碳化过程中发生反应的离子方程式为______________________。
D.从0 ℃升至40 ℃,1,2加成正反应速率的增大程度小于其逆反应速率的增大程度 17.(12分)CdSnAs 是一种高迁移率的新型热电材料,回答下列问题:
2
15.25 ℃时,某混合溶液中c(CH COOH)+c(CH COO-)=0.1 mol·L-1,lg c(CH COOH)、lg c(CHCOO-)、 (1)Sn为ⅣA族元素,单质 Sn与干燥Cl 反应生成SnCl 。常温常压下SnCl 为无色液体,SnCl 空间构型为
3 3 3 3 2 4 4 4
lg c(H+)和lg c(OH-)随pH变化的关系如下图所示。K 为CHCOOH的电离常数,下列说法正确的是( ) ____________,其固体的晶体类型为____________。
a 3
(2)NH 、PH 、AsH 的沸点由高到低的顺序为____________(填化学式,下同),还原性由强到弱的顺序为
3 3 3
____________,键角由大到小的顺序为____________。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 Cd2+配
合物的结构如图所示,1 mol该配合物中通过螯合作用形成的配位键有________ mol,该螯合物中N的杂化方式
有__________种。
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,pH=-lg K
a
0.1c(H+)
C.该体系中,c(CHCOOH)= mol·L-1
3 K +c(H+)
a
D.pH由7到14的变化过程中,CHCOO-的水解程度始终增大
3
三、非选择题:本题共5小题,共60分
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系
16.(12分)用软锰矿(主要成分为MnO ,含少量Fe O、Al O)和BaS制备高纯MnCO 的工艺流程如下:
2 3 4 2 3 3 CdSnAs 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
2
坐标
x y z
原子
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0.125
已知:MnO 是一种两性氧化物;25 ℃时相关物质的K 见下表。
2 sp
物质 Fe(OH) Fe(OH) Al(OH) Mn(OH)
2 3 3 2
K 1×10-16.3 1×10-38.6 1×10-32.3 1×10-12.7
sp
回答下列问题:
(1)软锰矿预先粉碎的目的是__________________________,MnO 与BaS溶液反应转化为MnO的化学方程式为
一个晶胞中有________个Sn,找出距离Cd(0,0,0)最近的Sn________(用分数坐标表示)。CdSnAs
2
晶体中与单个
2
________________________________。
Sn键合的As有__________个。
(2)保持BaS投料量不变,随MnO 与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH) 的量达到最 18.(12分)探究CH 3 OH合成反应化学平衡的影响因素,有利于提高 CH 3 OH的产率。以CO 2 、H 2 为原料合成
2 2
大值后会减小,减小的原因是______________________。 CH 3 OH涉及的主要反应如下:
(3)滤液Ⅰ可循环使用,应当将其导入到________操作中(填操作单元的名称)。 Ⅰ.CO 2 (g)+3H 2 (g) CH 3 OH(g)+H 2 O(g)
(4)净化时需先加入的试剂 X 为________(填化学式),再使用氨水调溶液的 pH,则 pH 的理论最小值为 ΔH 1 =-49.5 kJ·mol-1
________(当溶液中某离子浓度c,1.0×10-5 mol·L-1时,可认为该离子沉淀完全)。 Ⅱ.CO(g)+2H 2 (g) CH 3 OH(g)ΔH=-90.4 kJ·mol-1
2
Ⅲ.CO (g)+H(g) CO(g)+HO(g) ΔH
2 2 2 3
回答下列问题: Ⅱ.
(1)ΔH=________ kJ·mol-1。
3
(2)一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,容器中
2 2
CHOH(g)为a mol,CO为b mol,此时HO(g)的浓度为__________ mol·L-1
3 2
Ⅲ.
(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为__________。
Ar为芳基;X=Cl,Br;Z或Z′=COR,CONHR,COOR等。
(3)不同压强下,按照n(CO)∶n(H )=1∶3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温度的变
2 2 2 3
回答下列问题:
化关系如下图所示。
(1)实验室制备 A 的化学方程式为________________________________________,提高 A 产率的方法是
______________________________________;A的某同分异构体只有一种化学环境的碳原子,其结构简式为
________________。
(2)C→D的反应类型为____________;E中含氧官能团的名称为____________。
(3)C的结构简式为____________,F的结构简式为____________。
n(CO ) -n(CO )
已知:CO 的平衡转化率= 2 初始 2 平衡×100%
2 n(CO ) (4)Br 和 的反应与Br 和苯酚的反应类似,以 和 为原料合
2 初始 2 2
n(CH OH)
CHOH的平衡产率= 3 平衡×100%
3 n(CO )
2 初始
成 ,写出能获得更多目标产物的较优合成路线(其他试剂任选)。
其中纵坐标表示CO 平衡转化率的是图__________(填“甲”或“乙”);压强p 、p 、p 由大到小的顺序为
2 1 2 3
__________ ; 图 乙 中 T 温 度 时 , 三 条 曲 线 几 乎 交 于 一 点 的 原 因 是
1
_______________________________________________________________________________。
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为_____(填标号)。
2 3
A.低温、高压 B.高温、低压
20.(12分)某同学利用Cl 氧化KMnO 制备KMnO 的装置如下图所示(夹持装置略):
2 2 4 4
C.低温、低压 D.高温、高压
19.(12分)化合物F是合成吲哚2酮类药物的一种中间体,其合成路线如下:
已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO2-+2HO===2MnO-+MnO ↓+4OH-
4 2 4 2
回答下列问题:
知:Ⅰ.
(1)装置A中a的作用是________________________;装置C中的试剂为______________;装置A中制备Cl 的
2化学方程式为__________________________________。
(2)上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是________________。
4
(3)KMnO 常作氧化还原滴定的氧化剂,滴定时应将KMnO 溶液加入__________(填“酸式”或“碱式”)滴定管
4 4
中;在规格为50.00 mL的滴定管中,若KMnO 溶液起始读数为15.00 mL,此时滴定管中KMnO 溶液的实际体
4 4
积为______________(填标号)。
A.15.00 mL B.35.00 mL
C.大于35.00 mL D.小于15.00 mL
(4)某FeC O·2H O样品中可能含有的杂质为Fe (C O) 、HC O·2H O,采用KMnO 滴定法测定该样品的组成,
2 4 2 2 2 4 3 2 2 4 2 4
实验步骤如下:
Ⅰ.称取m g样品于锥形瓶中,加入稀HSO 溶解,水浴加热至75 ℃。用c mol·L-1的KMnO 溶液趁热滴定至溶
2 4 4
液出现粉红色且30 s内不褪色,消耗KMnO 溶液V mL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀HSO 酸化后,在75 ℃继续用KMnO 溶液滴
2 4 4
定至溶液出现粉红色且30 s内不褪色,又消耗KMnO 溶液V mL。
4 2
样品中所含HC O·2H O(M=126 g·mol-1)的质量分数表达式为________________。
2 2 4 2
下列关于样品组成分析的说法,正确的是__________(填标号)。
V
A.
1=3时,样品中一定不含杂质
V
2
V
B. 1越大,样品中HC O·2H O含量一定越高
V 2 2 4 2
2
C.若步骤Ⅰ中滴入KMnO 溶液不足,则测得样品中Fe元素含量偏低
4
D.若所用KMnO 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
4