文档内容
化学试题
可能用到的相对原子质量:H 1 O 16 Na 23 Mg 24 S 32
一、选择题:本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 建盏是久负盛名的陶瓷茶器,承载着福建历史悠久的茶文化。关于建盏,下列说法错误的是
A. 高温烧结过程包含复杂的化学变化 B. 具有耐酸碱腐蚀、不易变形的优点
C. 制作所用的黏土原料是人工合成的 D. 属硅酸盐产品,含有多种金属元素
2. 豆甾醇是中药半夏中含有的一种天然物质,其分子结构如下图所示。关于豆甾醇,下列说法正确的是
A. 属于芳香族化合物 B. 含有平面环状结构
C. 可发生取代反应和加成反应 D. 不能使酸性 溶液褪色
3. 设 为阿伏加德罗常数的值.下列说法正确的是
A. 所含极性共价键的数目为
B. 晶体中阴、阳离子总数为
C. 与足量 反应生成 的分子数为
D. 电解熔融 制 ,电路中通过的电子数为
4. 明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:下列说法错误的是
A. FeSO 的分解产物X为FeO B. 本流程涉及复分解反应
4
C. HNO 的沸点比HSO 的低 D. 制备使用的铁锅易损坏
3 2 4
5. 实验室配制碘水时,通常将 溶于 溶液: 。关于该溶液,下列说法正确的
是
A. 的电子式为 B. 滴入淀粉溶液,不变蓝
C. 加水稀释,平衡逆向移动 D. 加少量 固体平衡正向移动
6. 室温下,下列各组离子一定能与指定溶液共存的是
A. 的 溶液: 、 、 、
B. 的 溶液: 、 、 、
C. 的 溶液: 、 、 、
D. 的 溶液: 、 、 、
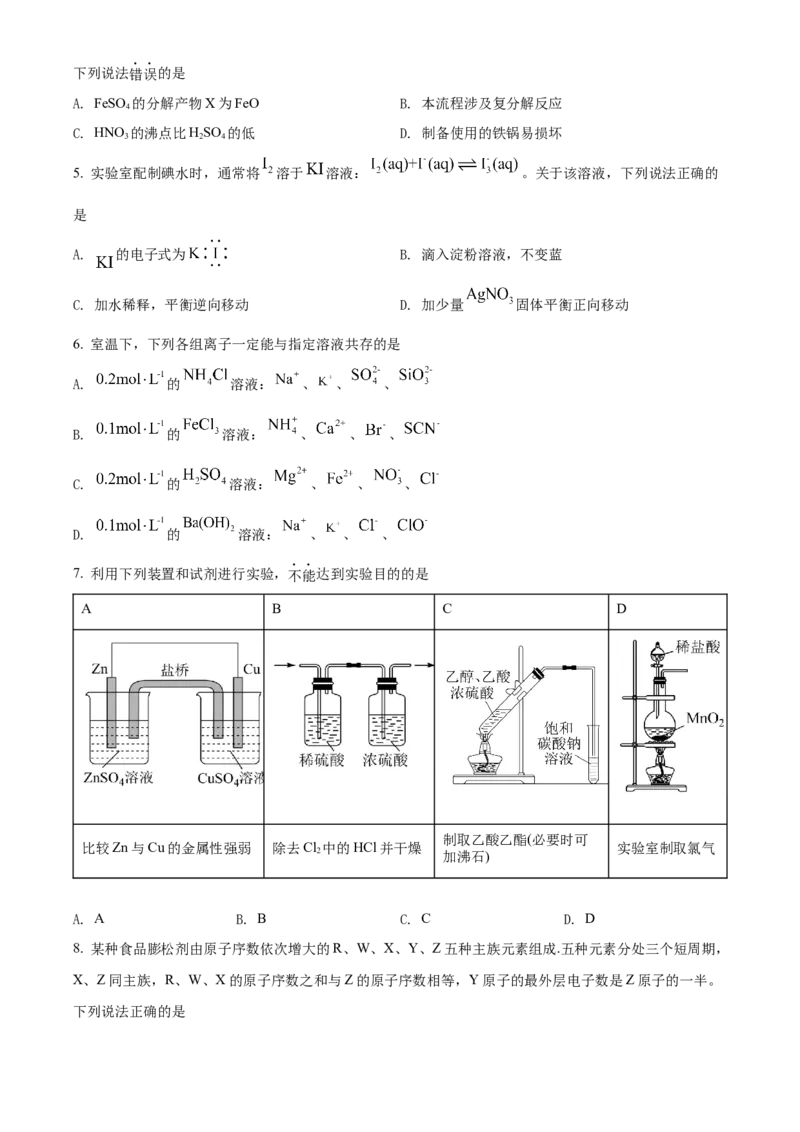
7. 利用下列装置和试剂进行实验,不能达到实验目的的是
A B C D
制取乙酸乙酯(必要时可
比较Zn与Cu的金属性强弱 除去Cl 中的HCl并干燥 实验室制取氯气
2 加沸石)
A. A B. B C. C D. D
8. 某种食品膨松剂由原子序数依次增大的R、W、X、Y、Z五种主族元素组成.五种元素分处三个短周期,
X、Z同主族,R、W、X的原子序数之和与Z的原子序数相等,Y原子的最外层电子数是Z原子的一半。
下列说法正确的是A. 简单氢化物的稳定性: B. Y的氧化物是两性氧化物
.
C R、W、X只能组成共价化合物 D. 最高正价:
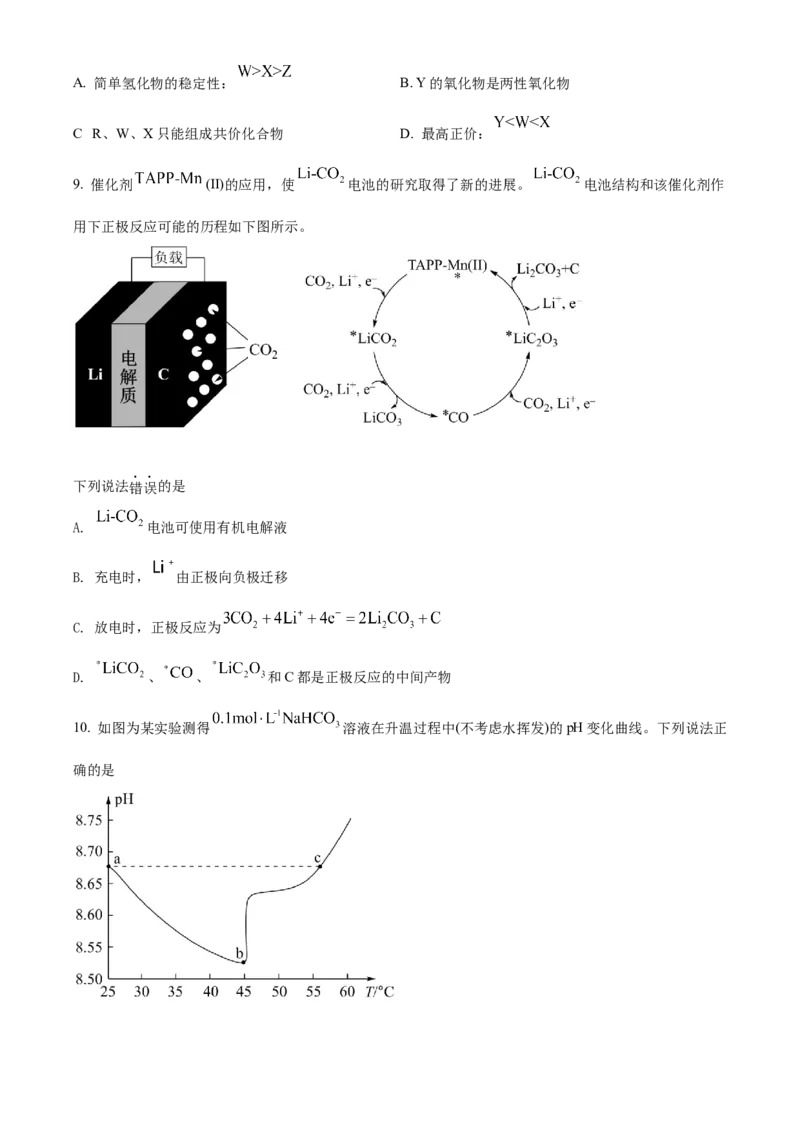
9. 催化剂 (Ⅱ)的应用,使 电池的研究取得了新的进展。 电池结构和该催化剂作
用下正极反应可能的历程如下图所示。
下列说法错误的是
A. 电池可使用有机电解液
B. 充电时, 由正极向负极迁移
C. 放电时,正极反应为
D. 、 、 和C都是正极反应的中间产物
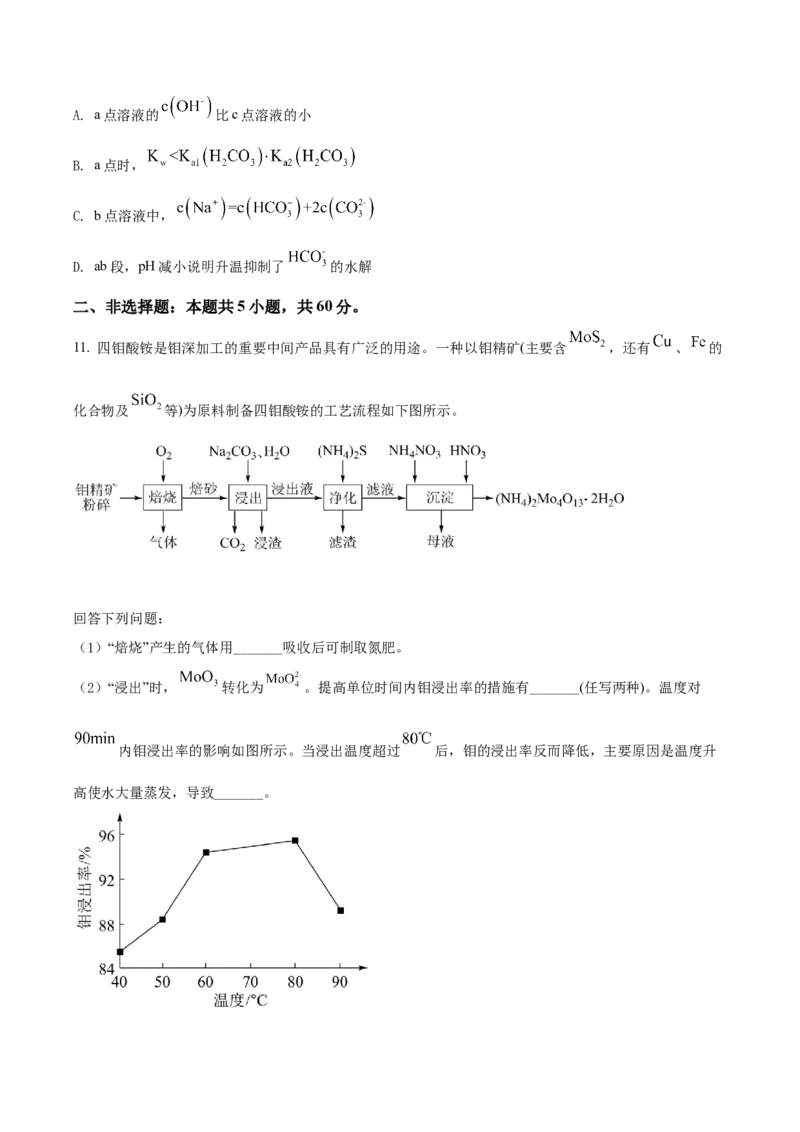
10. 如图为某实验测得 溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正
确的是A. a点溶液的 比c点溶液的小
B. a点时,
C. b点溶液中,
D. ab段,pH减小说明升温抑制了 的水解
二、非选择题:本题共5小题,共60分。
11. 四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含 ,还有 、 的
化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
回答下列问题:
(1)“焙烧”产生的气体用_______吸收后可制取氮肥。
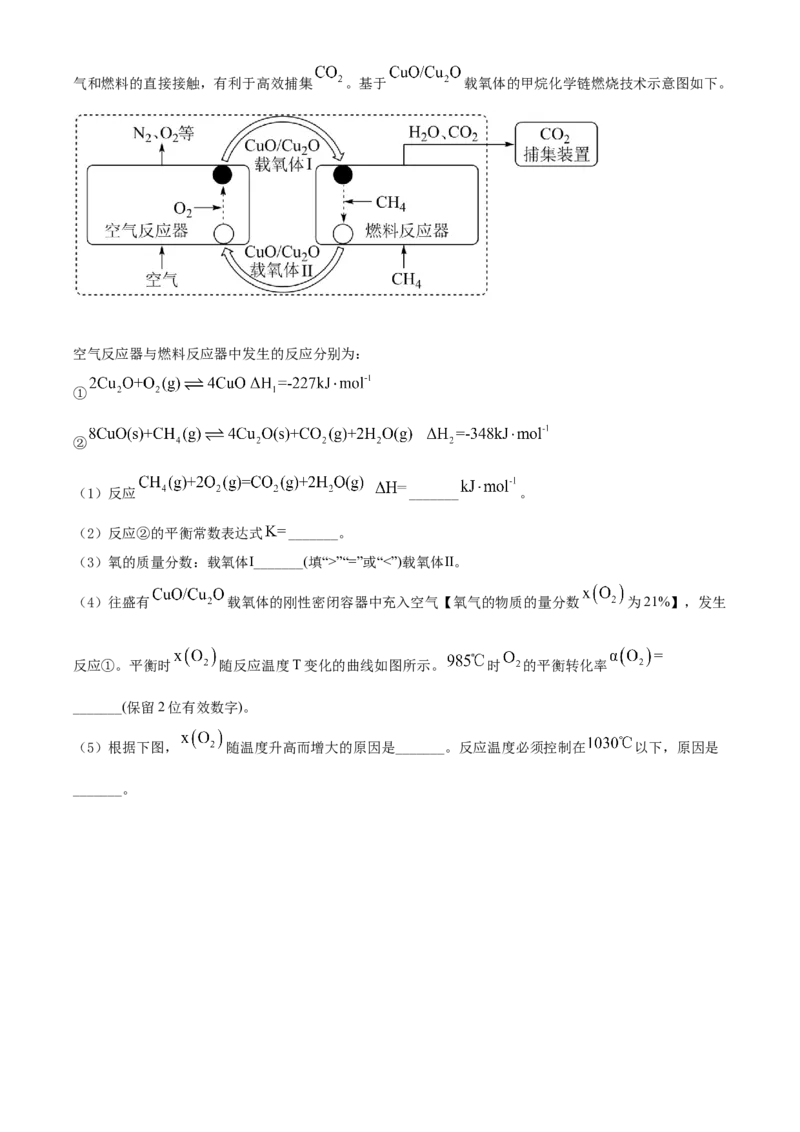
(2)“浸出”时, 转化为 。提高单位时间内钼浸出率的措施有_______(任写两种)。温度对
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升
高使水大量蒸发,导致_______。(3)“净化”时,浸出液中残留的 、 转化为沉淀除去。研究表明,该溶液中 和pH的关系
为: 。为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于
_______。(已知: ; 和 的 分别为35.2和17.2)
(4)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方
程式为_______。
(5)“沉淀”时,加入 的目的是_______。
(6)高温下用 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。【已知:(NH )MoO
4 2 4 13 4 2 4 13
受热分解生成 】
12. 溶液和 溶液可发生反应: 。为探究反应速率
与 的关系,利用下列装置(夹持仪器略去)进行实验。
实验步骤:往A中加入一定体积(V)的 溶液、 溶液和水,充分搅拌。
控制体系温度,通过分液漏斗往A中加入 醋酸。当导管口气泡均匀稳定冒出时,开始用排水法
收集气体。用秒表测量收集 所需的间,重复多次取平均值(t)。
回答下列问题:(1)仪器A的名称为_______。
(2)检验装置气密性的方法:关闭止水夹K,_______。
(3)若需控制体系的温度为 ,采取的合理加热方式为_______。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
实验编
号 醋
溶液 溶液 水
酸
1 4.0 4.0 8.0 334
2 4.0 4.0 150
.
3 8.0 4.0 40 4.0 83
4 12.0 4.0 4.0 0.0 38
① _______, _______。
②该反应 的速率方程为 ,k为反应速率常数。利用实验数据计算得
_______(填整数)。
③醋酸的作用是_______。
(5)如果用同浓度的盐酸代替醋酸进行实验1, 与盐酸反应生成 , 分解产生等物质
的量的两种气体.反应结束后,A中红棕色气体逐渐变浅装置中还能观察到的现象有_______。 分解
的化学方程式为_______。
13. 化学链燃烧( )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于 载氧体的甲烷化学链燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
②
(1)反应 _______ 。
(2)反应②的平衡常数表达式 _______。
(3)氧的质量分数:载氧体Ⅰ_______(填“>”“=”或“<”)载氧体Ⅱ。
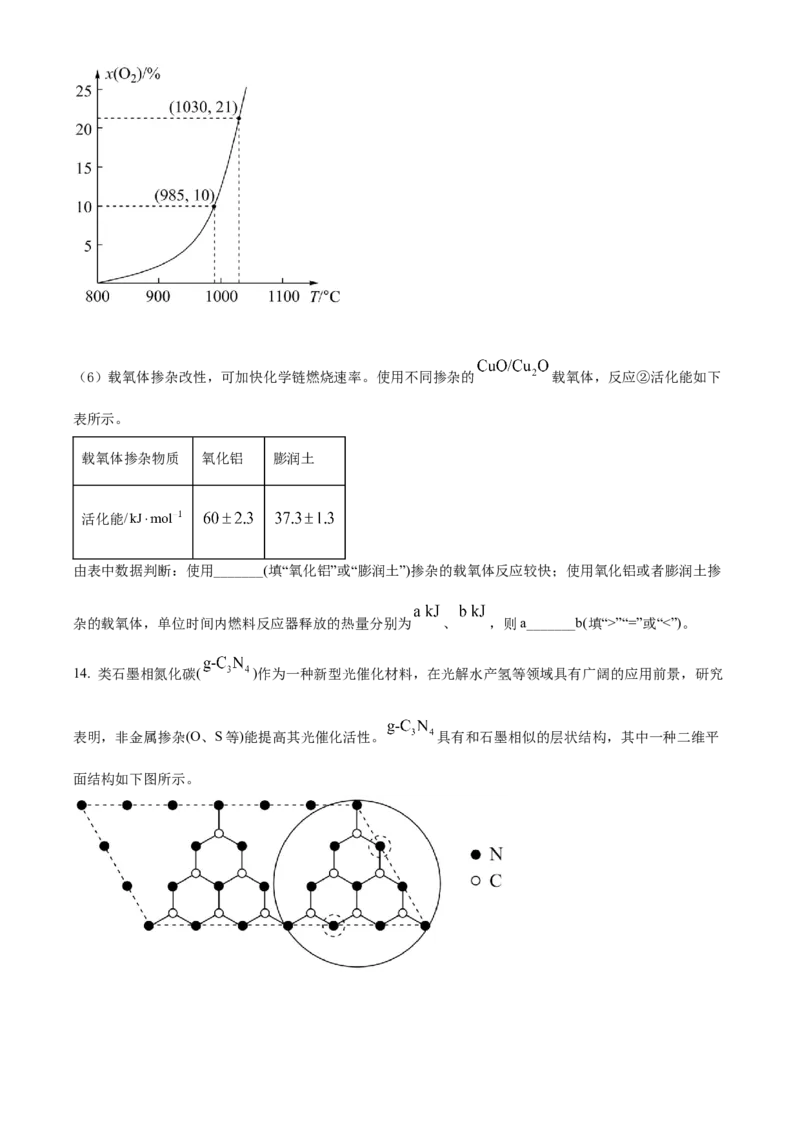
(4)往盛有 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生
反应①。平衡时 随反应温度T变化的曲线如图所示。 时 的平衡转化率
_______(保留2位有效数字)。
(5)根据下图, 随温度升高而增大的原因是_______。反应温度必须控制在 以下,原因是
_______。(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下
表所示。
载氧体掺杂物质 氧化铝 膨润土
活化能/
由表中数据判断:使用_______(填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺
杂的载氧体,单位时间内燃料反应器释放的热量分别为 、 ,则a_______b(填“>”“=”或“<”)。
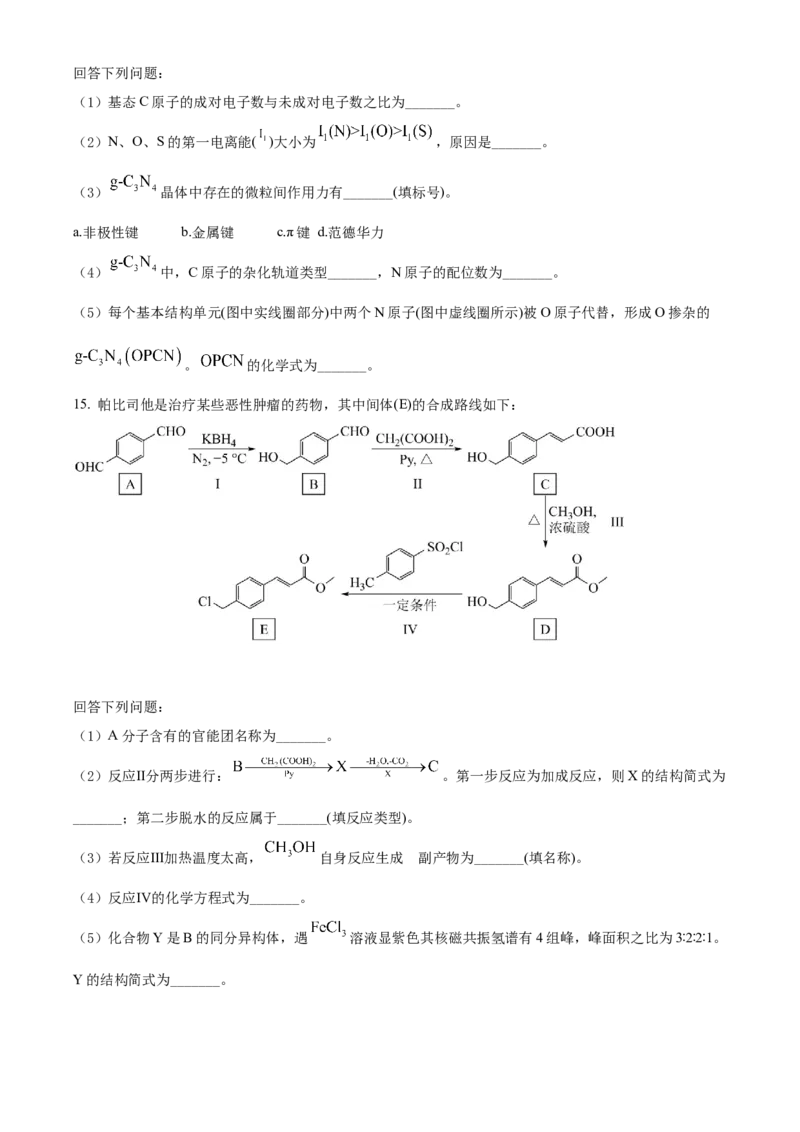
14. 类石墨相氮化碳( )作为一种新型光催化材料,在光解水产氢等领域具有广阔的应用前景,研究
表明,非金属掺杂(O、S等)能提高其光催化活性。 具有和石墨相似的层状结构,其中一种二维平
面结构如下图所示。回答下列问题:
(1)基态C原子的成对电子数与未成对电子数之比为_______。
(2)N、O、S的第一电离能( )大小为 ,原因是_______。
(3) 晶体中存在的微粒间作用力有_______(填标号)。
a.非极性键 b.金属键 c.π键 d.范德华力
(4) 中,C原子的杂化轨道类型_______,N原子的配位数为_______。
(5)每个基本结构单元(图中实线圈部分)中两个N原子(图中虚线圈所示)被O原子代替,形成O掺杂的
。 的化学式为_______。
15. 帕比司他是治疗某些恶性肿瘤的药物,其中间体(E)的合成路线如下:
回答下列问题:
(1)A分子含有的官能团名称为_______。
(2)反应Ⅱ分两步进行: 。第一步反应为加成反应,则X的结构简式为
_______;第二步脱水的反应属于_______(填反应类型)。
的
(3)若反应Ⅲ加热温度太高, 自身反应生成 副产物为_______(填名称)。
(4)反应Ⅳ的化学方程式为_______。
(5)化合物Y是B的同分异构体,遇 溶液显紫色其核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。
Y的结构简式为_______。