文档内容
2024 年新课标卷理综化学试题(网络版)
的
1. 文房四宝是中华传统文化 瑰宝。下列有关叙述错误的是
A. 羊毛可用于制毛笔,主要成分为蛋白质
B. 松木可用于制墨,墨的主要成分是单质碳
C. 竹子可用于造纸,纸的主要成分是纤维素
D. 大理石可用于制砚台,主要成分为硅酸盐
【答案】D
【解析】
【详解】A.动物的毛、皮、角等的主要成分都是蛋白质,羊毛的主要成分为蛋白质,A正确;
B.墨的主要成分是炭黑,炭黑是碳元素的一种单质,碳的单质在常温下的化学性质很稳定,不易与其他物
质发生化学反应,故用墨汁书写的字画历经千年仍不褪色,B正确;
C.竹子可用于造纸,竹子的主要成分是纤维素,用其造的纸的主要成分也是纤维素,C正确;
D.大理石可用于制砚台,大理石主要成分为碳酸钙,不是硅酸盐,D错误;
故选D。
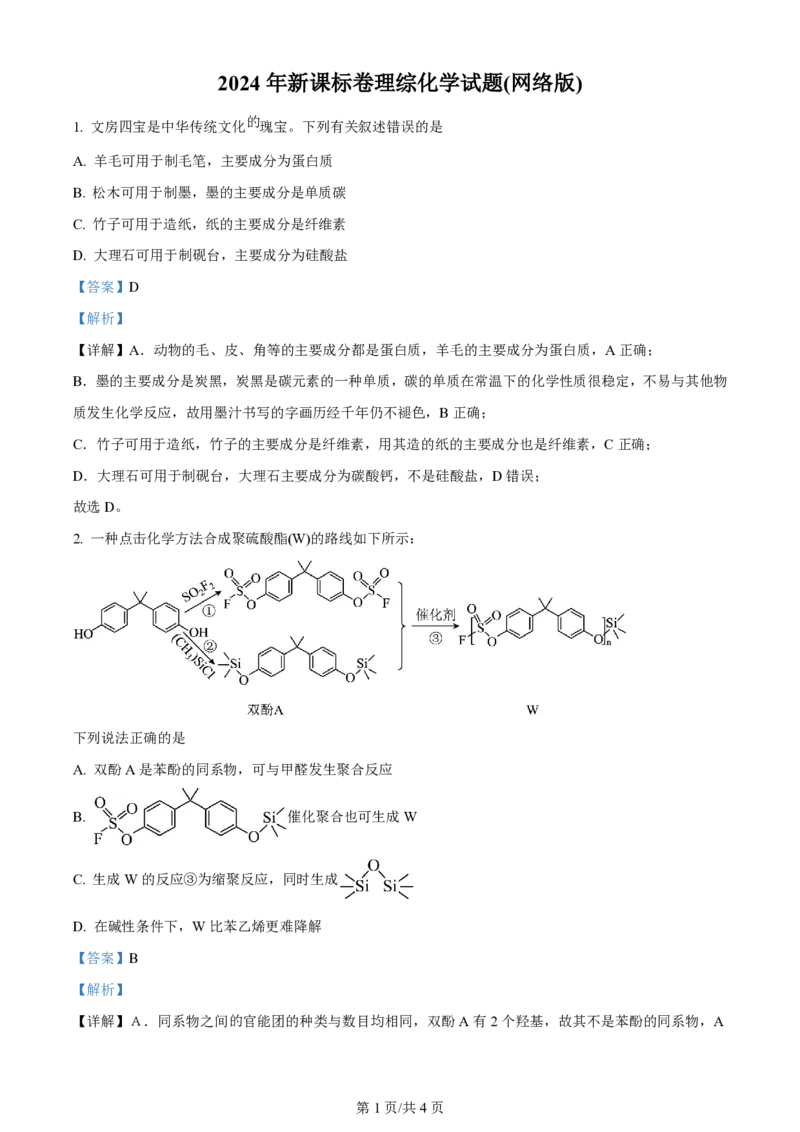
2. 一种点击化学方法合成聚硫酸酯(W)的路线如下所示:
下列说法正确的是
A. 双酚A是苯酚的同系物,可与甲醛发生聚合反应
B. 催化聚合也可生成W
C. 生成W的反应③为缩聚反应,同时生成
D. 在碱性条件下,W比苯乙烯更难降解
【答案】B
【解析】
【详解】A.同系物之间的官能团的种类与数目均相同,双酚A有2个羟基,故其不是苯酚的同系物,A
第1页/共4页
学科网(北京)股份有限公司不正确;
B . 题 干 中 两 种 有 机 物 之 间 通 过 缩 聚 反 应 生 成 W , 根 据 题 干 中 的 反 应 机 理 可 知 ,
也可以通过缩聚反应生成W,B正确;
C.生成W的反应③为缩聚反应,同时生成(CH ) SiF,C不正确;
3 3
D.W为聚硫酸酯,酯类物质在碱性条件下可以发生水解反应,因此,在碱性条件下,W比苯乙烯易降解,
D不正确;
综上所述,本题选B。
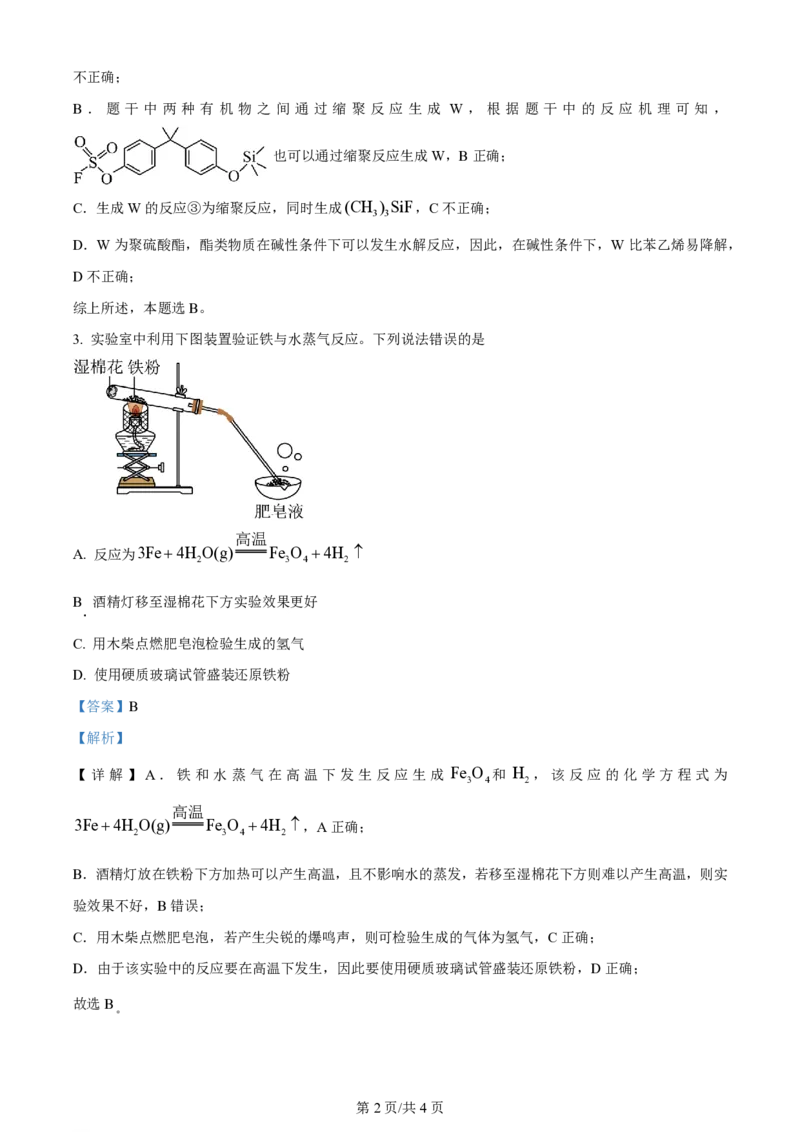
3. 实验室中利用下图装置验证铁与水蒸气反应。下列说法错误的是
高温
A. 反应为3Fe+4H O(g) Fe O +4H
2 3 4 2
B 酒精灯移至湿棉花下方实验效果更好
.
C. 用木柴点燃肥皂泡检验生成的氢气
D. 使用硬质玻璃试管盛装还原铁粉
【答案】B
【解析】
【详解】A.铁和水蒸气在高温下发生反应生成 Fe O 和 H ,该反应的化学方程式为
3 4 2
高温
3Fe+4H O(g) Fe O +4H ,A正确;
2 3 4 2
B.酒精灯放在铁粉下方加热可以产生高温,且不影响水的蒸发,若移至湿棉花下方则难以产生高温,则实
验效果不好,B错误;
C.用木柴点燃肥皂泡,若产生尖锐的爆鸣声,则可检验生成的气体为氢气,C正确;
D.由于该实验中的反应要在高温下发生,因此要使用硬质玻璃试管盛装还原铁粉,D正确;
故选B
。
第2页/共4页
学科网(北京)股份有限公司4. 对于下列过程中发生的化学反应,相应离子方程式正确的是
A. 试管壁上的银镜用稀硝酸清洗:Ag+2H+ +NO- =Ag+ +NO +H O
3 2 2
B. 工业废水中的Pb2+用FeS去除:Pb2+ +S2-= PbS¯
C. 海水提溴过程中将溴吹入SO 吸收塔:Br +SO +2H O=2Br- +SO2- +4H+
2 2 2 2 4
D. 用草酸标准溶液测定高锰酸钾溶液的浓度:2MnO- +5C O2- +16H+ =2Mn2+ +10CO +8H O
4 2 4 2 2
【答案】C
【解析】
【详解】A.试管壁上的银镜用稀硝酸清洗,银溶于稀硝酸生成硝酸银和一氧化氮 气体,该反应的离子方
程式为3Ag +4H++NO-= 3Ag++NO+2H O,A不正确;
3 2
B.由于PbS的溶解度远远小于FeS,因此,工业废水中的Pb2+用FeS去除,该反应的离子方程式为
Pb2++FeS=PbS+Fe2+,B不正确;
C.海水提溴过程中将溴吹入SO 吸收塔,SO 在水溶液中将Br 还原为Br-,该反应的离子方程式为
2 2 2
Br +SO +2H O =2Br-+ SO2-+4H+,C正确;
2 2 2 4
D.用草酸标准溶液测定高锰酸钾溶液的浓度,H C O 被氧化为CO ,H C O 属于弱酸,该反应的离
2 2 4 2 2 2 4
子方程式为2MnO-+ 5H C O +6H+=2Mn2++10CO +8H O,D不正确;
4 2 2 4 2 2
综上所述,本题选C。
5. 我国科学家最近研究的一种无机盐Y Z(WX) 纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能
3 6 2
力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内
层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错
误的是
A. W、X、Y、Z四种元素的单质中Z的熔点最高
B. 在X的简单氢化物中X原子轨道杂化类型为sp3
C. Y的氢氧化物难溶于NaCl溶液,可以溶于NH Cl溶液
4
D. Y Z(WX) 中WX-提供电子对与Z3+形成配位键
3 6 2
【答案】A
【解析】
第3页/共4页
学科网(北京)股份有限公司【分析】W、X 、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是
其内层电子数的2倍,则W为C元素;每个周期的ⅡA和ⅤA的元素的第一电离能都比左右相邻元素的高,
由于配合物Y[Z(WX) ] 中Y在外界,Y可形成简单阳离子,则Y属于金属元素,故X和Y分别为N和
3 6 2
Mg;Z的M层未成对电子数为4,则其3d轨道上有4个不成对电子,其价电子排布式为3d64s2,Z为Fe
元素,Y[Z(WX) ] 为Mg [Fe(CN) ] 。
3 6 2 3 6 2
【详解】A.W、X、 Y、Z四种元素的单质中,N元素的单质形成分子晶体,Mg和Fe均形成金属晶体,
C元素既可以形成金刚石又可以形成石墨,石墨的熔点最高,A不正确;
B.在X的简单氢化物是CH ,其中C原子轨道杂化类型为sp3,B正确;
4
C.Y的氢氧化物是Mg(OH) ,其属于中强碱,其难溶于水,难溶于NaCl溶液,但是,由于NH Cl电离
2 4
产生的NH+可以破坏Mg(OH) 的沉淀溶解平衡,因此Mg(OH) 可以溶于NH Cl溶液,C正确;
4 2 2 4
D.Mg [Fe(CN) ] 中CN-提供电子对与Fe3+形成配位键,D正确;
3 6 2
综上所述,本题选A。
第4页/共4页
学科网(北京)股份有限公司