文档内容
1.化学与生产和生活密切相关。下列过程中没有发生化学变化的是
A.氯气作水杀菌消毒剂
B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂
D.肥皂水作蚊虫叮咬处的清洗剂
2.根据下列实验操作和现象得出的结论正确的是
选项 实验操作 现象 结论
[来源:学科网ZXXK]
A 将某溶液与稀盐酸反应产生的 石灰水变浑浊 该溶液中一定含有CO 2-
3
气体通入澄清石灰水
B 常温下,将铁片浸入足量浓硫 铁片不溶解 常温下,铁与浓硫酸钠一
酸中 定没有发生化学反应
C 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 该食盐中一定没有添加
碘酸钾
D 向苯酚钠溶液中滴加乙酸溶液 溶液变浑浊 相同条件下,乙酸的酸性
一定比苯酚强
3.下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在H+、Cl-、MnO -
4
B.pH=2的溶液中可能大量存在Na+、NH +、SiO 2-
4 3
C.Fe2+与H O 在酸性溶液中的反应:2Fe2++H O +2H+=2Fe3++2H O
2 2 2 2 2
D.稀硫酸和氢氧化钡溶液反应:H++SO 2-+Ba2++OH-=BaSO ↓+H O
4 4 2
4. N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.2.4g镁在足量的氧气中燃烧,转移的电子数为0.1N
A
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5N
A
C.氢原子数为0.4N 的甲醇分子中含有的σ键数为0.4N
A A
D.0.1L0.5mol/LCH COOH溶液中含有的氢离子数为0.05N
3 A
5.某电动汽车配载一种可充放电的锂离子电池。学.科网.放电时电池的总反应为:Li CoO +Li C =LiCoO +
1-x 2 x 6 2
第1页 | 共5页C (x<1)。下列关于该电池的说法不正确的是
6
A.放电时,Li+在电解质中由负极向正极迁移
B.放电时,负极的电极反应式为Li C -xe-= xLi++ C
x 6 6
C.充电时,若转移1mole-,石墨C 电极将增重7xg
6
D.充电时,阳极的电极反应式为LiCoO -xe-=Li CoO +Li+
2 1-x 2
n(H O)
6.一定条件下,CH 与H O(g)发生反应:CH (g)+H O(g) CO(g)+3H (g),设起始 2 =Z,在恒压
4 2 4 2 2
n(CH )
4
下,平衡时j (CH )的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
4
A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
n(H O)
C.图中X点对应的平衡混合物中 2 =3
n(CH )
4
D.温度不变时,图中X点对应的平衡在加压后j (CH )减小
4
7.向1L含0.01molNaAlO 和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO )增大,先后发生三个不
2 2
同的反应,当0.01molc(AlO -)+c(OH-)
2
B 0.01 c(Na+)>c(AlO -)> c(OH-)>c(CO 2-)
2 3
C 0.015 c(Na+)> c(HCO -)>c(CO 2-)> c(OH-)
3 3
D 0.03 c(Na+)> c(HCO -)> c(OH-)>c(H+)
3
8.(13分)M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中
第2页 | 共5页p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨
的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是① ,X和Y中电负性较大的是 ② (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________。
(3)X与M形成的XM 分子的空间构型是__________。
3
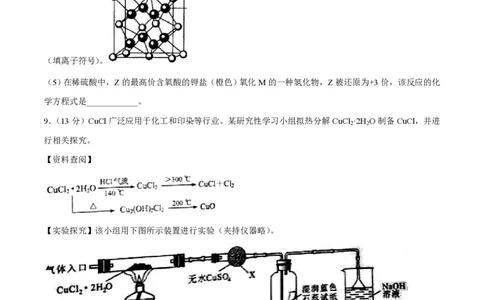
(4)M和R所形成的一种离子化合物R M晶体的晶胞如右图所示,则图中黑球代表的离子是_________
2
(填离子符号)。
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化
学方程式是____________。
9.(13分)CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl ·2H O制备CuCl,并进
2 2
行相关探究。
【资料查阅】
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
请回答下列问题:
(1)仪器X的名称是__________。
(2)实验操作的先后顺序是a→______→c(填操作的编号)
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
第3页 | 共5页c.在“气体入口”处干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N
2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是_______。
(4)装置D中发生的氧化还原反应的离子方程式是________________。
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl 或CuO杂质,根据资料信息分析:
2
①若杂质是CuCl ,则产生的原因是________________。
2
②若杂质是CuO,则产生的原因是________________。
§网]
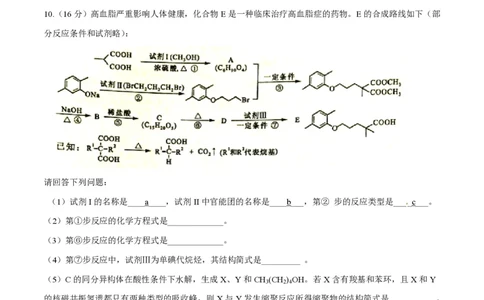
10.(16分)高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部
分反应条件和试剂略):
请回答下列问题:
(1)试剂I的名称是____a____,试剂II中官能团的名称是____b___,第② 步的反应类型是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH (CH ) OH。若X含有羧基和苯环,且X和Y
3 2 4
的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________。
11. (16分)资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主要含Ca (PO ) F
5 4 3
和CaCO ·MgCO 。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业用途的CaCO 、
3 3 3
Mg(OH) 、P 和H ,其简化流程如下:
2 4 2
第4页 | 共5页已知:①Ca (PO ) F在950℃不分解;
5 4 3
②4Ca (PO ) F+18SiO +30C 2CaF +30CO+18CaSiO +3P
5 4 3 2 2 3 4
请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是___________。
(2)实验室过滤所需的玻璃仪器是_____________。
(3)NH NO 溶液能从磷矿I中浸取出Ca2+的原因是__________。
4 3
(4)在浸取液II中通入NH ,发生反应的化学方程式是____________。
3
(5)工业上常用磷精矿[Ca (PO ) F]和硫酸反应制备磷酸。已知25℃,101kPa时:
5 4 3
CaO(s)+H SO (l)=CaSO4(s)+H O(l) △H=-271kJ/mol
2 4 2
5 CaO(s)+H PO (l)+HF(g)= Ca (PO ) F (s)+5H O(l) △H=-937kJ/mol
3 4 5 4 3 2
则Ca (PO ) F和硫酸反应生成磷酸的热化学方程式是_________________。
5 4 3
(6)在一定条件下CO(g)+H O(g) CO (g)+H (g),当CO与H O(g)的起始物质的量之比为1:5,达平衡
2 2 2 2
时,CO转化了5/6.若akg含Ca (PO ) F(相对分子质量为504)的质量分数为10%的磷尾矿,在上述过程
5 4 3
中有b%的Ca (PO ) F转化为P ,将产生的CO与H O(g)按起始物质的量之比1:3混合,则相同条件下达平
5 4 3 4 2
衡时能产生H ________kg。
2
]
第5页 | 共5页