文档内容
必做实验提升(一) 用化学沉淀法去除粗盐中的杂质离子
1.粗食盐水中常含有的杂质离子:Ca2+、Mg2+、SO。
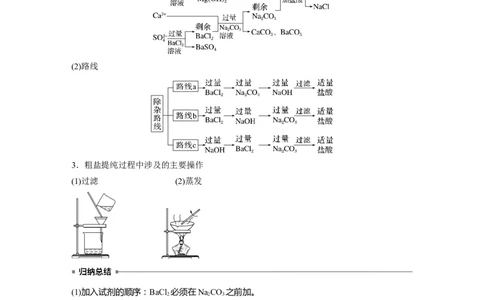
2.粗盐的除杂原理及规律
(1)原理
(2)路线
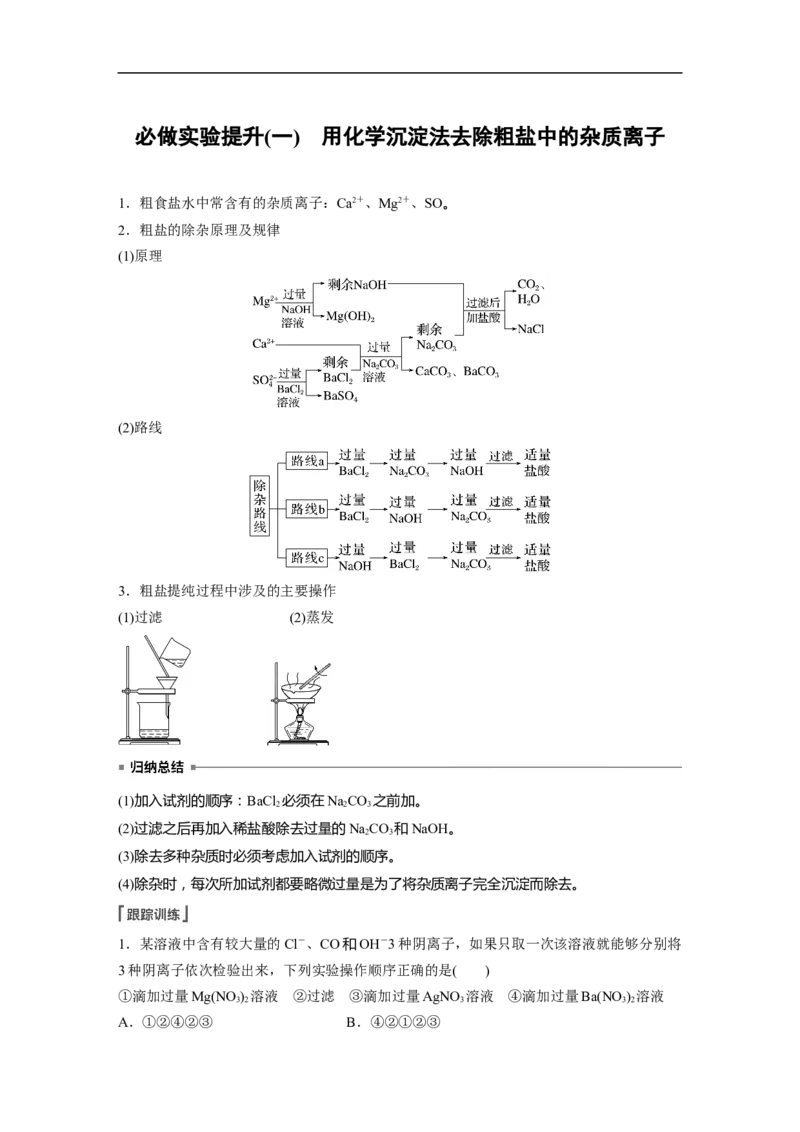
3.粗盐提纯过程中涉及的主要操作
(1)过滤 (2)蒸发
(1)加入试剂的顺序:BaCl 必须在NaCO 之前加。
2 2 3
(2)过滤之后再加入稀盐酸除去过量的NaCO 和NaOH。
2 3
(3)除去多种杂质时必须考虑加入试剂的顺序。
(4)除杂时,每次所加试剂都要略微过量是为了将杂质离子完全沉淀而除去。
1.某溶液中含有较大量的Cl-、CO和OH-3种阴离子,如果只取一次该溶液就能够分别将
3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加过量Mg(NO) 溶液 ②过滤 ③滴加过量AgNO 溶液 ④滴加过量Ba(NO ) 溶液
3 2 3 3 2
A.①②④②③ B.④②①②③C.①②③②④ D.④②③②①
答案 B
解析 某溶液中含有较大量的Cl-、CO和OH-3种阴离子,如果只取一次该溶液就能够分
别将3种阴离子依次检验出来,应该先滴加过量Ba(NO ) 溶液检验CO,过滤,再向滤液中
3 2
滴加过量Mg(NO) 溶液检验OH-,过滤,最后向滤液中滴加过量AgNO 溶液检验Cl-。
3 2 3
2.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为
98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO等杂质,提纯工艺线路如下:
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
请回答下列问题:
(1)试剂A是________,“母液”中除了含有Na+、CO、OH-外,还含有________等离子,
过滤要“趁热”的目的是________。
(2)检验试剂级NaCO 中Cl-和SO是否除尽,选用的试剂及加入的先后次序是___(填字母)。
2 3
a.HCl、BaCl 、AgNO
2 3
b.AgNO、HNO、Ba(NO )
3 3 3 2
c.HNO、Ba(NO )、AgNO
3 3 2 3
d.AgNO、HCl、BaCl
3 2
答案 (1)氢氧化钠溶液(或NaOH溶液) Cl-、SO 提高NaCO·H O的含量 (2)c
2 3 2
解析 (1)试剂A是氢氧化钠溶液,“母液”中除了含有Na+、CO、OH-外,还含有Cl-、
SO等离子,过滤要“趁热”的目的是提高NaCO·H O的含量。
2 3 2
(2)检验试剂级NaCO 中Cl-和SO是否除尽,需要用硝酸除去CO,防止生成Ag CO 和
2 3 2 3
BaCO 带来干扰,再加入过量Ba(NO ) 检验并除尽SO,最后加入AgNO 检验Cl-。
3 3 2 3