文档内容
[复习目标] 1.理解影响电离平衡、水解平衡及沉淀溶解平衡的因素。2.掌握电离平衡、水
解平衡及沉淀溶解平衡的应用。
正误判断,正确的打“√”,错误的打“×”
(1)常温下,pH为2的盐酸由HO电离出的c(H+)=1.0×10-12 mol·L-1( )
2
(2)同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7( )
(3)室温下,pH=3的CHCOOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7( )
3
(4)25 ℃时,等体积、等浓度的硝酸与氨水混合后,溶液pH=7( )
(5)用热的纯碱溶液洗去油污,是因为NaCO 可直接与油污反应( )
2 3
(6)NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
(7)施肥时,草木灰(有效成分为KCO)不能与NH Cl混合施用,是因为KCO 与NH Cl反应
2 3 4 2 3 4
生成氨气,会降低肥效( )
(8)向NaCl、NaI的混合稀溶液中滴入少量稀AgNO 溶液,有黄色沉淀生成,则K (AgCl)>
3 sp
K (AgI)( )
sp
(9)常温下,K [Mg(OH) ]=5.6×10-12,pH=10的含 Mg2+的溶液中,c(Mg2+)≤5.6×10-4
sp 2
mol·L - 1
( )
(10)室温下,向浓度均为0.1 mol·L-1的BaCl 和CaCl 混合溶液中滴加NaSO 溶液,出现白
2 2 2 4
色沉淀,所以K (BaSO)<K (CaSO)( )
sp 4 sp 4
答案 (1)√ (2)× (3)× (4)× (5)× (6)× (7)√ (8)× (9)√ (10)×
1.对比剖析“三大”平衡
水解平衡CHCOO-+
3
电离平衡CHCOOH 沉淀溶解平衡AgCl(s)Ag+
3
平衡类型 HOCHCOOH +
2 3
CHCOO-+H+ (aq)+Cl-(aq)
3
OH-
研究对象 弱电解质溶液 能水解的盐溶液 难溶电解质
影 若难溶物的 若难溶物的溶解
响 升温 促进电离 K a 增大 促进水解 K h 增大 溶解度与温 度与温度成正
因 度成正比, 比,K 增大;
sp促进溶解;
反之,则 K 减
sp
反之,则抑
小
制溶解
加水 促进电离 K 不变 促进水解 K 不变 促进溶解 K 不变
a h sp
加 入
加 入 加 入 加 入
相 应
CHCOONa CHCOOH AgNO 或
3 3 3
离 子 K 不变 K 不变 K 不变
a h sp
素 或HCl,抑 或 NaOH, NaCl , 抑
(或物
制电离 抑制水解 制溶解
质)
加 入
反 应 加 入 OH
加入 H+, 加入氨水,
离 子 -,促进电 K 不变 K 不变 K 不变
a h sp
促进水解 促进溶解
(或物 离
质)
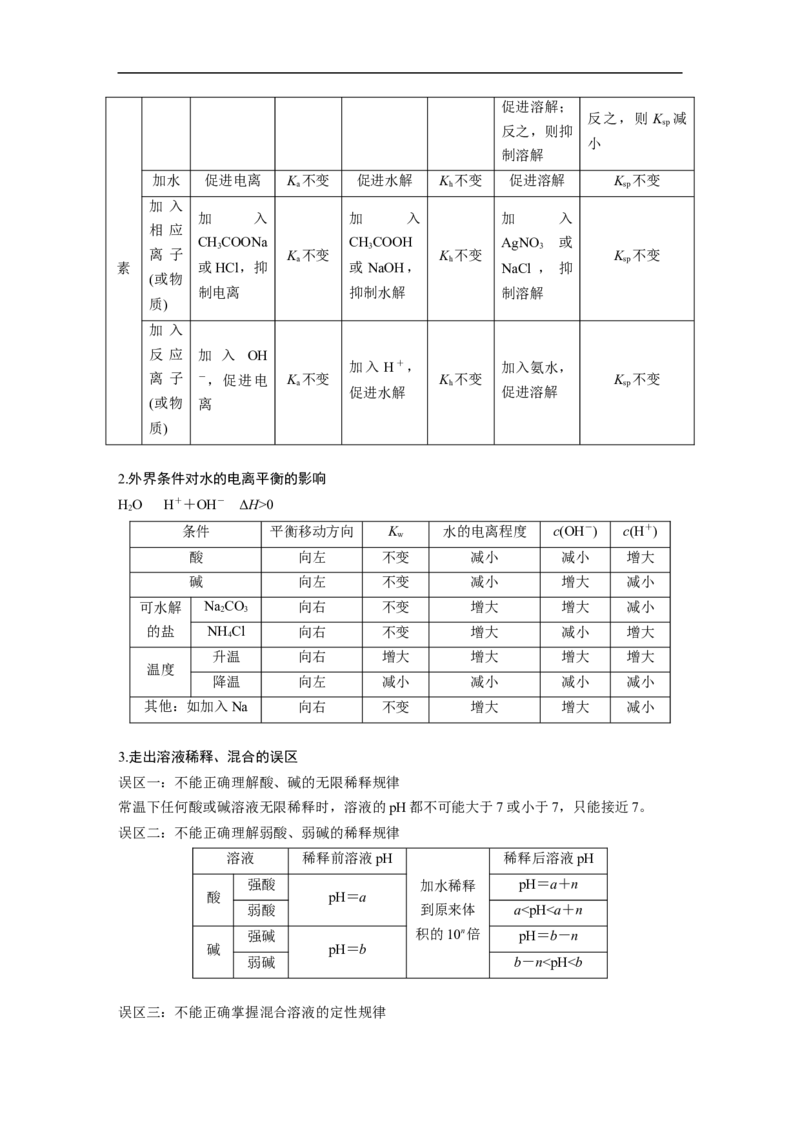
2.外界条件对水的电离平衡的影响
HOH++OH- ΔH>0
2
条件 平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
酸 向左 不变 减小 减小 增大
碱 向左 不变 减小 增大 减小
可水解 NaCO 向右 不变 增大 增大 减小
2 3
的盐 NH Cl 向右 不变 增大 减小 增大
4
升温 向右 增大 增大 增大 增大
温度
降温 向左 减小 减小 减小 减小
其他:如加入Na 向右 不变 增大 增大 减小
3.走出溶液稀释、混合的误区
误区一:不能正确理解酸、碱的无限稀释规律
常温下任何酸或碱溶液无限稀释时,溶液的pH都不可能大于7或小于7,只能接近7。
误区二:不能正确理解弱酸、弱碱的稀释规律
溶液 稀释前溶液pH 稀释后溶液pH
强酸 加水稀释 pH=a+n
酸 pH=a
弱酸 到原来体 a7。
角度一 电离平衡及影响因素
1.(2022·全国乙卷,13)常温下,一元酸HA的K(HA)=1.0×10-3。在某体系中,H+与A-
a
不能穿过隔膜,未电离的HA可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度[]为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
答案 B
解析 常温下,溶液Ⅰ的pH=7.0,则溶液Ⅰ中c(H+)=c(OH-)=1×10-7 mol·L-1,c(H+)
<c(OH-)+c(A-),A错误;常温下溶液Ⅱ的pH=1.0,溶液中c(H+)=0.1 mol·L-1,K(HA)
a
==1.0×10-3,c (HA)=c(HA)+c(A-),则=1.0×10-3,解得=,B正确;根据题意,未
总
电离的HA可自由穿过隔膜,故溶液Ⅰ和Ⅱ中的c(HA)相等,C错误;常温下溶液Ⅰ的pH=
7.0,溶液Ⅰ中c(H+)=1×10-7 mol·L-1,K(HA)==1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
=1.0×10-3,溶液Ⅰ中c (HA)=(104+1)c(HA),溶液Ⅱ中c (HA)=1.01c(HA),未电离的
总 总
HA可自由穿过隔膜,故溶液Ⅰ和Ⅱ中的c(HA)相等,溶液Ⅰ和Ⅱ中c (HA)之比为[(104+
总
1)c(HA)]∶[1.01c(HA)]=(104+1)
∶1.01≈104,D错误。
2.(2019·全国卷Ⅲ,11)设N 为阿伏加德罗常数的值。关于常温下pH=2的HPO 溶液,下
A 3 4
列说法正确的是( )
A.每升溶液中的H+数目为0.02N
A
B.c(H+)=c(H PO)+2c(HPO)+3c(PO)+c(OH-)
2
C.加水稀释使电离度增大,溶液pH减小
D.加入NaH PO 固体,溶液酸性增强
2 4
答案 B
解析 pH=2的HPO 溶液中c(H+)=10-2mol·L-1,每升溶液中所含N(H+)=0.01N ,A错
3 4 A
误;由电荷守恒知,该HPO 溶液中存在c(H+)=c(H PO)+2c(HPO)+3c(PO)+c(OH-),B
3 4 2正确;加水稀释能促进HPO 的电离,使其电离度增大,由于以增大溶液体积为主,导致溶
3 4
液中 c(H+)减小,溶液 pH 增大,C 错误;向 HPO 溶液中加入 NaH PO 固体,溶液中
3 4 2 4
c(H PO)增大,促使平衡HPO H++HPO逆向移动,抑制HPO 电离,溶液酸性减弱,
2 3 4 2 3 4
D错误。
角度二 水解平衡及影响因素
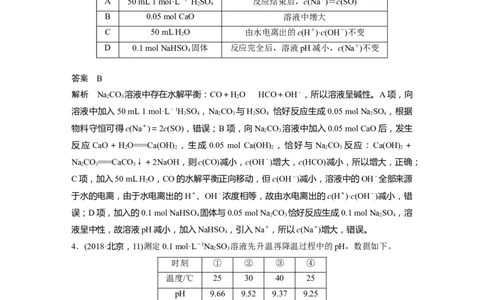
3.(2015·天津理综,5)室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中
2 3
加入下列物质,有关结论正确的是( )
加入物质 结论
A 50 mL 1 mol·L-1 HSO 反应结束后,c(Na+)=c(SO)
2 4
B 0.05 mol CaO 溶液中增大
C 50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D 0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
答案 B
解析 NaCO 溶液中存在水解平衡:CO+HOHCO+OH-,所以溶液呈碱性。A项,向
2 3 2
溶液中加入50 mL 1 mol·L-1HSO ,NaCO 与HSO 恰好反应生成0.05 mol Na SO ,根据
2 4 2 3 2 4 2 4
物料守恒可得c(Na+)=2c(SO),错误;B项,向NaCO 溶液中加入0.05 mol CaO后,发生
2 3
反应 CaO+HO===Ca(OH) ,生成 0.05 mol Ca(OH) ,恰好与 NaCO 反应:Ca(OH) +
2 2 2 2 3 2
NaCO===CaCO ↓+2NaOH,则c(CO)减小,c(OH-)增大,c(HCO)减小,所以增大,正确;
2 3 3
C项,加入50 mL H O,CO的水解平衡正向移动,但c(OH-)减小,溶液中的OH-全部来源
2
于水的电离,由于水电离出的H+、OH-浓度相等,故由水电离出的c(H+)·c(OH-)减小,错
误;D项,加入的0.1 mol NaHSO 固体与0.05 mol Na CO 恰好反应生成0.1 mol Na SO ,溶
4 2 3 2 4
液呈中性,故溶液pH减小,加入NaHSO,引入Na+,所以c(Na+)增大,错误。
4
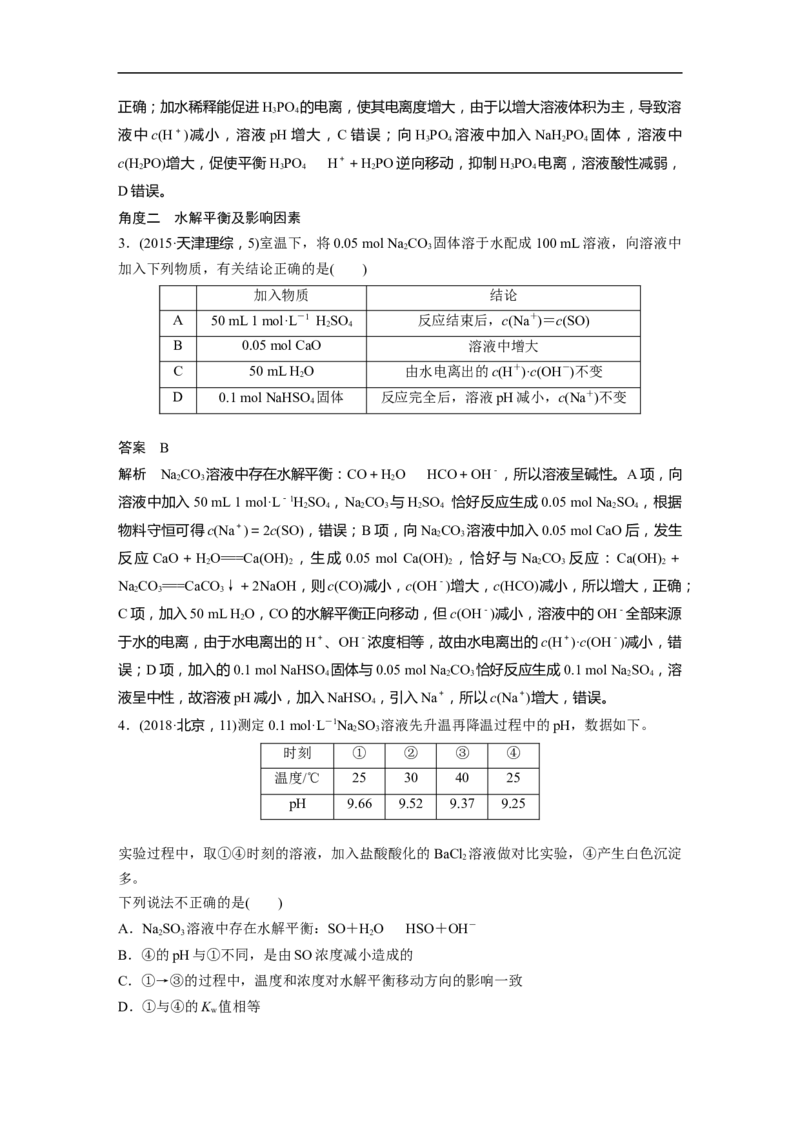
4.(2018·北京,11)测定0.1 mol·L-1NaSO 溶液先升温再降温过程中的pH,数据如下。
2 3
时刻 ① ② ③ ④
温度/℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀
2
多。
下列说法不正确的是( )
A.NaSO 溶液中存在水解平衡:SO+HOHSO+OH-
2 3 2
B.④的pH与①不同,是由SO浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的K 值相等
w答案 C
解析 ①→③的过程中,pH变小,说明SO水解产生的c(OH-)减小;升高温度,SO的水解
平衡正向移动,溶液中SO水解产生的c(OH-)应增大,pH应增大,而实际上溶液的pH减
小,其主要原因是实验过程中部分SO被空气中的O 氧化生成SO,溶液中c(SO)减小,水
2
解平衡逆向移动,则溶液中c(OH-)减小,pH减小;①→③的过程中,温度升高,SO的水
解平衡正向移动,而c(SO)减小,水解平衡逆向移动,二者对水解平衡移动方向的影响不一
致,C错;NaSO 是强碱弱酸盐,在水溶液中发生水解,存在水解平衡:SO+HOHSO
2 3 2
+OH-,A对;实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,
2
④产生白色沉淀多,说明④中SO的数目大于①中SO的数目,④中SO的数目小于①中SO
的数目,所以④中OH-的数目小于①中OH-的数目,pH不同,B对;K 只与温度有关,D
w
对。
(1)盐类水解易受温度、浓度、溶液的酸碱性等因素的影响。以氯化铁水解为例,当改变条
件,如升温、通入HCl气体、加水、加铁粉、加碳酸氢钠等时,应从平衡移动方向、pH的
变化、水解程度、现象等方面去归纳总结,加以分析掌握。
(2)多元弱酸的酸式盐问题。酸式盐一般既存在水解,又存在电离。如果酸式盐的电离程度
大于其水解程度,溶液显酸性,如NaHSO 溶液;如果酸式盐的水解程度大于其电离程度,
3
则溶液显碱性,如NaHCO 溶液。
3
角度三 沉淀溶解平衡及影响因素
5.(2016·海南,5)向含有MgCO 固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值
3
变小的是( )
A.c(CO) B.c(Mg2+)
C.c(H+) D.K (MgCO )
sp 3
答案 A
解析 含有MgCO 固体的溶液中存在沉淀溶解平衡:MgCO (s)Mg2+(aq)+CO(aq),滴加
3 3
少许浓盐酸与CO反应生成CO 气体,促使平衡向右移动,则c(Mg2+)和c(H+)增大,c(CO)
2
减小,温度不变,K (MgCO )不变,故A正确。
sp 3
(1)沉淀溶解平衡与化学平衡、电离平衡一样,具有动态平衡的特征,平衡时溶液中各离子
浓度保持恒定,平衡常数只受温度的影响,与浓度无关。
(2)溶度积(K )的大小只与难溶电解质的性质和溶液的温度有关,相同类型的难溶电解质的
sp
K 越小,溶解度越小,越难溶。
sp考向一 电离平衡及应用
1.将浓度为0.1 mol·L-1的HF溶液加水稀释,下列各量增大的是( )
①c(H+) ②c(F-) ③c(OH-) ④K(HF) ⑤K ⑥ ⑦
a w
A.①⑥ B.②④
C.③⑦ D.④⑤
答案 C
解析 HF是弱电解质,加水稀释促进HF的电离,但c(H+)、c(F-)、c(HF)都减小;温度不
变,K 不变,c(H+)减小,则c(OH-)增大;温度不变,K(HF)不变,=,c(F-)减小,则增
w a
大;根据电荷守恒知,c(H+)=c(OH-)+c(F-),则==1-, 因为增大,故减小。
2.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
答案 C
解析 由图可知,a、b、c三点对应的平衡常数不变,该曲线上的点温度相等,升高温度,
不能引起由c向b的变化,故A项错误;b点c(H+)=c(OH-)=1.0×10-7 mol·L-1,故K =
w
1.0×10-14,故B项错误;FeCl 为强酸弱碱盐,Fe3+结合水电离出的OH-,促进水的电离平
3
衡右移,c(H+)增大,c(OH-)减小,可能引起由b向a的变化,故C项正确;由c点到d点,
水的离子积常数减小,但温度不变,K 不变,则稀释溶液不能引起由c向d的变化,故D
w
项错误。
3.浓度均为0.1 mol·L-1、体积均为V 的HX、HY溶液,分别加水稀释至体积为V,pH随
0
lg 的变化关系如图所示。下列叙述正确的是( )
A.HX、HY都是弱酸,且HX的酸性比HY的弱B.相同温度下,电离常数K(HX):a>b
C.常温下,c (H+)·c (OH-):a<b
水 水
D.lg =3时,若同时加热两种溶液,则减小
答案 C
解析 由图像可知,HY溶液加水稀释104倍,溶液的pH也随之增加了4,而HX溶液加水
稀释104倍后,溶液的pH变化小于4,因此HY为强酸,HX为弱酸,A项错误;电离常数
只与温度有关,因此在相同温度下,电离常数K(HX):a=b,B项错误;a、b两点对应溶液
中水的电离都因HX的电离而受到抑制,在a点时,溶液中HX电离出的c(H+)较大,对水
的电离抑制更强,因此在a点时溶液中c (H+)、c (OH-)都比b点的小,则c (H+)·c (OH
水 水 水 水
-):a<b,C项正确;一般情况下,升高温度,促进弱电解质的电离,因此加热两溶液时,
HY是强酸,c(Y-)不变,而HX是弱酸,c(X-)增大,则增大,D项错误。
考向二 水解平衡及应用
4.下列实验中,均产生白色沉淀。
下列分析不正确的是( )
A.NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低
答案 B
解析 NaCO 溶液、NaHCO 溶液中均存在Na+、CO、HCO、HCO 、H+、OH-、HO,
2 3 3 2 3 2
故含有的微粒种类相同,A正确;HCOH++CO,加入Ca2+后,Ca2+和CO反应生成沉
淀,促进HCO的电离,且抑制CO的水解,B错误;Al3+与CO、HCO都能发生相互促进的
水解反应,C正确;Al3+与CO、HCO发生相互促进的水解反应,都生成Al(OH) 和CO ,
3 2
导致溶液酸性增强,pH减小,CaCl 与NaCO 反应生成CaCO ,c(CO)减小,溶液pH减小,
2 2 3 3
HCOH++CO,Ca2+与CO结合促进HCO的电离平衡正向移动,c(H+)增大,溶液pH减
小,D正确。
5.BiOCl是一种具有珍珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
下列说法错误的是( )
A.酸浸工序中分次加入稀HNO 可降低反应的剧烈程度
3B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CHCOONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
答案 D
解析 硝酸为强氧化剂,可与金属铋反应,酸浸工序中分次加入稀HNO ,可降低反应的剧
3
烈程度,A正确;金属铋与硝酸反应生成的硝酸铋会发生水解反应生成 BiONO ,水解的离
3
子方程式为Bi3++NO+HOBiONO +2H+,转化工序中加入稀HCl,使氢离子浓度增大,
2 3
硝酸铋水解平衡左移,可抑制生成BiONO ,B正确;氯化铋水解生成BiOCl的离子方程式
3
为Bi3++Cl-+HOBiOCl+2H+,水解工序中加入少量CHCOONa(s),醋酸根离子会结
2 3
合氢离子生成弱电解质醋酸,使氢离子浓度减小,氯化铋水解平衡右移,促进 Bi3+水解,C
正确;结合C项分析水解工序中加入少量NH NO (s),铵根离子水解生成氢离子,使氢离子
4 3
浓度增大,氯化铋水解平衡左移,不利于生成BiOCl,且部分铋离子与硝酸根离子、水也会
发生反应:Bi3++NO+HOBiONO +2H+,也不利于生成BiOCl,D错误。
2 3
考向三 沉淀溶解平衡及应用
6.室温下,通过下列实验探究Ca(ClO) 溶液的性质。
2
实验1:向0.1 mol·L-1 Ca(ClO) 溶液中滴加酚酞试剂,溶液先变红后褪色
2
实验2:向0.1 mol·L-1 Ca(ClO) 溶液中通入少量CO 气体,出现白色沉淀
2 2
实验3:向0.1 mol·L-1 Ca(ClO) 溶液中通入少量SO 气体,出现白色沉淀
2 2
实验4:将0.1 mol·L-1 Ca(ClO) 溶液与0.1 mol·L-1 NaHCO 溶液等体积混合,出现白色沉
2 3
淀
下列说法不正确的是( )
A.实验1说明Ca(ClO) 溶液中存在反应ClO-+HOHClO+OH-
2 2
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO)=K (CaCO)
sp 3
C.实验3中生成的白色沉淀主要成分是CaSO
4
D.由实验4可得出:K (H CO)>K(HClO)
a2 2 3 a
答案 D
解析 实验1酚酞变红说明Ca(ClO) 水解显碱性,故存在ClO-+HOHClO+OH-,A项
2 2
正确;实验 2出现白色沉淀,说明上层清液是饱和溶液,存在沉淀溶解平衡,有 c(Ca2
+)·c(CO)=K (CaCO),B项正确;SO 气体被Ca(ClO) 氧化为硫酸根离子生成CaSO 沉淀,
sp 3 2 2 4
C项正确;实验4生成的碳酸钙是难溶固体,不能得出K (H CO)>K(HClO),D项错误。
a2 2 3 a
7.向10.00 mL 0.50 mol·L-1 NaHCO 溶液中滴加不同浓度的CaCl 溶液,观察到明显产生浑
3 2
浊时,停止滴加;取少量所得浑浊液加热,记录实验现象。下列说法不正确的是( )
滴加CaCl 溶液时的实 加热浑浊液时的
2
实验 序号 c(CaCl ) /(mol·L-1)
2
验现象 实验现象至1.32 mL时产生明显
① 0.05 有较多气泡生成
浑浊,但无气泡产生
至 15.60 mL 时产生明
② 0.005 显浑浊,但无气泡产 有少量气泡生成
生
③ 0.000 5 至20 mL未见浑浊 —
A.①中产生浑浊的原因是c(Ca2+)·c(CO)>K (CaCO)
sp 3
B.未加热前①和②中发生了反应:2HCO+Ca2+===CaCO ↓+HCO
3 2 3
C.加热浊液产生气泡主要是因为CaCO 受热分解产生了更多的CO
3 2
D.向上述NaHCO 溶液中加入足量0.5 mol·L-1 CaCl 溶液,可能同时产生浑浊和气泡
3 2
答案 C
解析 ①中能产生碳酸钙沉淀,说明c(Ca2+)·c(CO)>K (CaCO),A项正确;未加热前①和
sp 3
②不放出二氧化碳,说明碳酸未饱和,加热后二氧化碳溶解度减小,放出二氧化碳气体,所
以未加热前①和②中发生反应:2HCO+Ca2+===CaCO ↓+HCO ,B项正确;结合B项分
3 2 3
析知,加热浊液产生气泡主要是因为 HCO 受热分解生成了 CO ,C 项错误;向上述
2 3 2
NaHCO 溶液中加入足量0.5 mol·L-1 CaCl 溶液,发生反应CaCl +2NaHCO ===CaCO ↓+
3 2 2 3 3
2NaCl+CO↑+HO,能同时产生浑浊和气泡,D项正确。
2 2
专题强化练
1.石蕊是一种有机弱酸,石蕊分子(HZ)及其酸根离子(Z-)在水溶液中呈现不同的颜色。则
Z-的颜色是( )
A.蓝色 B.紫色
C.红色 D.由溶液酸碱性确定
答案 A
解析 根据石蕊是一种弱酸可知,石蕊分子HZ在溶液中存在电离平衡:HZH++Z-,
酸性溶液中滴入石蕊溶液显红色,酸性溶液中氢离子浓度增大,则HZ的电离平衡逆向移动,
HZ的浓度增大,溶液变成红色,则HZ为红色;碱性溶液中石蕊溶液显蓝色,碱性溶液中
氢离子浓度减小,Z-的浓度增大,则Z-的颜色应该为蓝色。
2.常温下,将pH均为3,体积均为V 的HA溶液和HB溶液,分别加水稀释至体积为V,
0
pH随lg 的变化如图所示。下列说法正确的是( )A.稀释相同倍数时:c(A-)>c(B-)
B.水的电离程度:b=c>a
C.溶液中离子总物质的量:b>c>a
D.溶液中离子总浓度:a>b>c
答案 B
解析 根据图像,当lg =2时,HA溶液:pH=5,HB溶液:3<pH<5,故HA为强酸,
HB为弱酸。稀释相同倍数时,溶液的pH:HA溶液>HB溶液,溶液中c(A-)<c(B-),A
项错误;酸抑制水的电离,酸中c(H+)越大,其抑制水电离程度越大,c(H+)∶a>b=c,则
水的电离程度:b=c>a,B项正确;a、c点溶液体积相同,c点pH大于a点,c点溶液中
c(A-)<a点溶液中c(B-),溶液中离子总物质的量:a>c,b点相对于a点加水稀释,促进
HB的电离,溶液中离子总物质的量:b>a,故溶液中离子总物质的量:b>a>c,C项错误;
结合C项分析知,溶液中离子总浓度:a>c,b、c点溶液的pH相等,b、c点两溶液中的电
荷守恒分别为c(H+)=c(B-)+c(OH-)、c(H+)=c(A-)+c(OH-),溶液中离子总浓度:b=c,
故溶液中离子总浓度:a>b=c,D错误。
3.化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+
Mn2+(aq)。下列有关叙述正确的是( )
A.该反应的平衡常数K=
B.MnS的K 小于CuS的K
sp sp
C.达到平衡时c(Mn2+)=c(Cu2+)
D.向溶液中加入少量NaS固体后,溶液中c(Cu2+)、c(Mn2+)均保持不变
2
答案 A
解析 反应的平衡常数K===,故A正确;化学式相似的物质,溶度积小的沉淀可以转化
为溶度积更小的沉淀,故MnS的K 比CuS的K 大,故B错误;该反应达到平衡时各离子
sp sp
的浓度保持不变,但不一定相等,故C错误;增大硫离子的浓度,平衡向左移动,所以
c(Cu2+)、c(Mn2+)均减小,故D错误。
4.以菱镁矿(主要成分为MgCO ,含少量SiO 、Fe O 和Al O)为原料制备高纯镁砂的工艺
3 2 2 3 2 3
流程如图:已知浸出时产生的废渣中有SiO、Fe(OH) 和Al(OH) 。
2 3 3
下列说法错误的是( )
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.沉镁的操作不能在较高温度下进行
C.流程中可循环使用的物质只有NH
3
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
答案 C
解析 高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根离子水解产生的氢离
子反应,促进铵根离子的水解,得到氯化镁、氨气和水,所以浸出镁的反应为 MgO+
2NH Cl===MgCl +2NH ↑+HO,A项正确;一水合氨受热易分解,沉镁时在较高温度下
4 2 3 2
进行会造成一水合氨大量分解,挥发出氨气,降低利用率,故沉镁的操作不能在较高温度下
进行,B项正确;在浸出的操作中,NH 可以回收制备氨水,用于沉镁,在沉镁的滤液中含
3
有NH Cl,可用于浸出时的反应液,流程中可循环使用的物质有 NH 、NH Cl,C项错误;
4 3 4
Mg2+与Al3+、Fe3+的氢氧化物的K 相差较大,因此分离Mg2+与Al3+、Fe3+是利用了它们
sp
氢氧化物K 的不同,D项正确。
sp
5.某含锰废水中主要含有MnSO ,另含H+、Fe2+、Ca2+、Mg2+、Cu2+、Al3+等,某同学
4
为了回收Mn单质设计如下工艺流程,下列说法不正确的是( )
已知25 ℃时,K (CaF )=1.5×10-10、K (MgF )=7.5×10-11。
sp 2 sp 2
A.滤渣1主要含Fe(OH) 和Al(OH)
3 3
B.除钙镁步骤中,当Ca2+、Mg2+沉淀完全时,溶液中=2
C.滤液4主要含(NH )CO
4 2 3
D.反应①中Si可用铝替代
答案 C
解析 含锰废水中加入 HO 把Fe2+氧化为Fe3+,加入氢氧化钠调节 pH生成Fe(OH) 和
2 2 3
Al(OH) 沉淀,所以滤渣1主要含Fe(OH) 和Al(OH) ,故A正确;除钙镁步骤中,当Ca2
3 3 3
+、Mg2+沉淀完全时,溶液中====2,故B正确;“沉锰过程”是硫酸锰与NH HCO 反
4 3
应生成MnCO 沉淀、二氧化碳气体、水和硫酸铵,滤液4主要含硫酸铵,故C错误;MnO
3能和Al发生铝热反应生成Mn,所以反应①中Si可用铝替代,故D正确。
6.常温下,通过下列实验探究HS、NaS溶液的性质。
2 2
实验1:向0.1 mol·L-1 HS溶液中通入一定体积的NH ,测得溶液pH为7。
2 3
实验2:向0.1 mol·L-1 HS溶液中滴加等体积同浓度的NaOH溶液,充分反应后再滴入2滴
2
酚酞,溶液呈红色。
实验3:向5 mL 0.1 mol·L-1 Na S溶液中滴入1 mL 0.1 mol·L-1 ZnSO 溶液,产生白色沉淀;
2 4
再滴入几滴0.1 mol·L-1 CuSO 溶液,立即出现黑色沉淀。
4
实验4:向0.1 mol·L-1 Na S溶液中逐滴滴加等体积同浓度的盐酸,无明显现象。
2
下列说法正确的是( )
A.实验1得到的溶液中存在c(NH)=2c(S2-)
B.由实验2可得出:K <K (H S)·K (H S)
w a1 2 a2 2
C.由实验3可得出:K (ZnS)>K (CuS)
sp sp
D.实验4得到的溶液中存在c(H+)-c(OH-)=c(S2-)-c(H S)
2
答案 D
解析 实验1得到的中性溶液中存在电荷守恒:c(NH)+c(H+)=2c(S2-)+c(HS-)+c(OH-),
溶液中氢离子浓度与氢氧根离子浓度相等,则 c(NH)=2c(S2-)+c(HS-),A项错误;实验2
得到的溶液为硫氢化钠溶液,溶液呈碱性说明溶液中HS-的水解程度大于其电离程度,则
HS-的水解常数K =大于电离常数K (H S),则K >K (H S)·K (H S),B项错误;实验3中
h a2 2 w a1 2 a2 2
硫化钠溶液与硫酸锌溶液反应时,硫化钠溶液过量,再加入硫酸铜溶液时,只有硫化铜沉淀
的生成反应,没有硫化锌沉淀转化为硫化铜沉淀的转化反应,无法比较硫化锌和硫化铜溶度
积的大小,C项错误;实验4得到的溶液为硫氢化钠和氯化钠的混合溶液,溶液中存在质子
守恒:c(H+)+c(H S)=c(S2-)+c(OH-),则溶液中存在c(H+)-c(OH-)=c(S2-)-c(H S),D
2 2
项正确。