文档内容
重点题空热练(一) 物质的分离、提纯 反应条件的控制
1.某矿渣的成分为Cu O、Al O 、Fe O 、SiO ,工业上用该矿渣获取铜和胆矾的操作流程
2 2 3 2 3 2
如下:
请回答下列问题:操作 1 主要包括:________、____________、________。洗涤
CuSO ·5H O 粗 产 品 不 能 用 大 量 水 洗 , 而 用 冰 水 洗 涤 , 原 因 是
4 2
________________________________
________________________________________________________________________。
答案 蒸发浓缩 冷却结晶 过滤 冰水既可以洗去晶体表面的杂质离子,又可以减少晶体
的损失
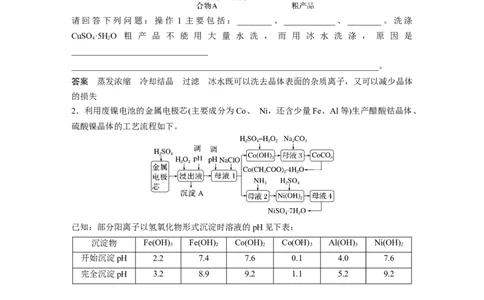
2.利用废镍电池的金属电极芯(主要成分为Co、 Ni,还含少量Fe、Al等)生产醋酸钴晶体、
硫酸镍晶体的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Co(OH) Al(OH) Ni(OH)
3 2 2 3 3 2
开始沉淀pH 2.2 7.4 7.6 0.1 4.0 7.6
完全沉淀pH 3.2 8.9 9.2 1.1 5.2 9.2
(1)用硫酸浸取金属电极芯时,提高浸取率的方法有________________(写出一种合理方法即
可)。
(2)沉淀A的主要成分是Fe(OH) 、________,“浸出液”调节pH的范围为______________,
3
调节pH选用的试剂可以是_____________________________________________(填字母)。
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸
(3)由“母液4”获取NiSO ·7H O的操作是____________,________,过滤,洗涤。
4 2
答案 (1)适当的升高温度(或将金属电极芯研成粉末) (2)Al(OH) 5.2≤pH<7.6 bc (3)蒸
3
发浓缩 冷却结晶
解析 (2)金属电极芯中的主要成分是Co、Ni,还含少量Fe、Al等,加入稀硫酸酸浸时,金属单质都转化为金属离子(Ni2+、Co2+、Fe2+、Al3+),浸出液中加入过氧化氢的作用是氧化
亚铁离子为铁离子,由流程图中最终产物可知,调节 pH的作用是除去溶液中的Fe3+、Al3
+,故沉淀A的主要成分是Fe(OH) 、Al(OH) ;为了保证Fe3+、Al3+沉淀完全而Ni2+、Co2+
3 3
不沉淀,由表格数据可知,要调节pH的范围为5.2≤pH<7.6;调节pH时不能加入铁,因为
铁能还原铁离子为亚铁离子,不能加入稀硫酸,因为要将溶液的pH调大,由流程图中后续
所加试剂可知,调节pH选用的试剂可以是氨水、碳酸钠溶液。
3.绿矾(FeSO ·7H O)可用于色谱分析剂、净水、照相制版等方面。下面是以铁屑(含少量锡
4 2
等杂质)生产绿矾的一种方法:
已知:在HS饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为
2
3.0,沉淀完全时溶液的pH为5.5。
(1)操作Ⅳ的顺序依次为________________、冷却结晶、__________________。
(2)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是①除去晶体表面附着的硫酸等杂质;
②________________________________________________________________________。
答案 (1)蒸发浓缩 过滤、洗涤、干燥 (2)降低绿矾的溶解度,减少绿矾的损失
4.二草酸合铜(Ⅱ)酸钾晶体{K [Cu(C O)]·2H O}制备流程如下:
2 2 4 2 2
(已知:HC O=====CO↑+CO↑+HO)
2 2 4 2 2
制备CuO:CuSO 溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤。
4
(1)用双层滤纸过滤的原因是__________________________________________________
________________________________________________________________________。
(2)用蒸馏水洗涤氧化铜时,如何证明氧化铜已洗涤干净?
________________________________________________________________________
________________________________________________________________________。
答案 (1)防止CuO颗粒穿过滤纸(或防止滤纸破损)
(2)取少量最后一次洗涤液于试管中,滴加BaCl 溶液,若无白色沉淀产生,说明已洗涤干净
2
解析 (1)过滤的目的是为了除尽不溶的固体,过滤时滤纸易破损,用双层滤纸的可能原因
是防止滤纸破损或防止CuO颗粒穿过滤纸。(2)可以检验是否存在硫酸根离子来检验是否洗
涤干净,具体方法:取少量最后一次洗涤液于试管中,滴加 BaCl 溶液,若无白色沉淀生成,
2
说明已洗涤干净。
5.工业上利用铬铁矿(FeO·Cr O)冶炼铬的工艺流程如下:
2 3(1)操作Ⅰ包括过滤与洗涤,简述实验室中洗涤沉淀的操作:______________________
________________________________________________________________________。
(2)Cr(OH) 和Al(OH) 类似,也是两性氢氧化物,写出Cr(OH) 溶于浓氢氧化钠溶液的离子
3 3 3
方程式:________________________________________________________________________
________________________________________________________________________。
答案 (1)将蒸馏水沿玻璃棒慢慢倒入漏斗中至浸没沉淀,待水自然流尽后,再重复操作 2~
3次
(2)Cr(OH) + OH- === CrO+2HO
3 2