文档内容
重点题空热练(三) 化工流程题中的曲线分析应用
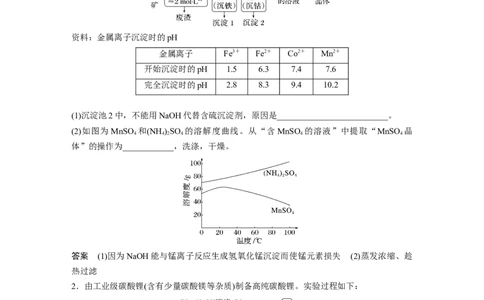
1.MnSO 是一种重要的化工产品。以菱锰矿(主要成分为MnCO ,还含有Fe O 、FeO、
4 3 3 4
CoO等)为原料制备MnSO 的工艺流程如下:
4
资料:金属离子沉淀时的pH
金属离子 Fe3+ Fe2+ Co2+ Mn2+
开始沉淀时的pH 1.5 6.3 7.4 7.6
完全沉淀时的pH 2.8 8.3 9.4 10.2
(1)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是__________________________。
(2)如图为MnSO 和(NH )SO 的溶解度曲线。从“含MnSO 的溶液”中提取“MnSO 晶
4 4 2 4 4 4
体”的操作为____________,洗涤,干燥。
答案 (1)因为NaOH能与锰离子反应生成氢氧化锰沉淀而使锰元素损失 (2)蒸发浓缩、趁
热过滤
2.由工业级碳酸锂(含有少量碳酸镁等杂质)制备高纯碳酸锂。实验过程如下:
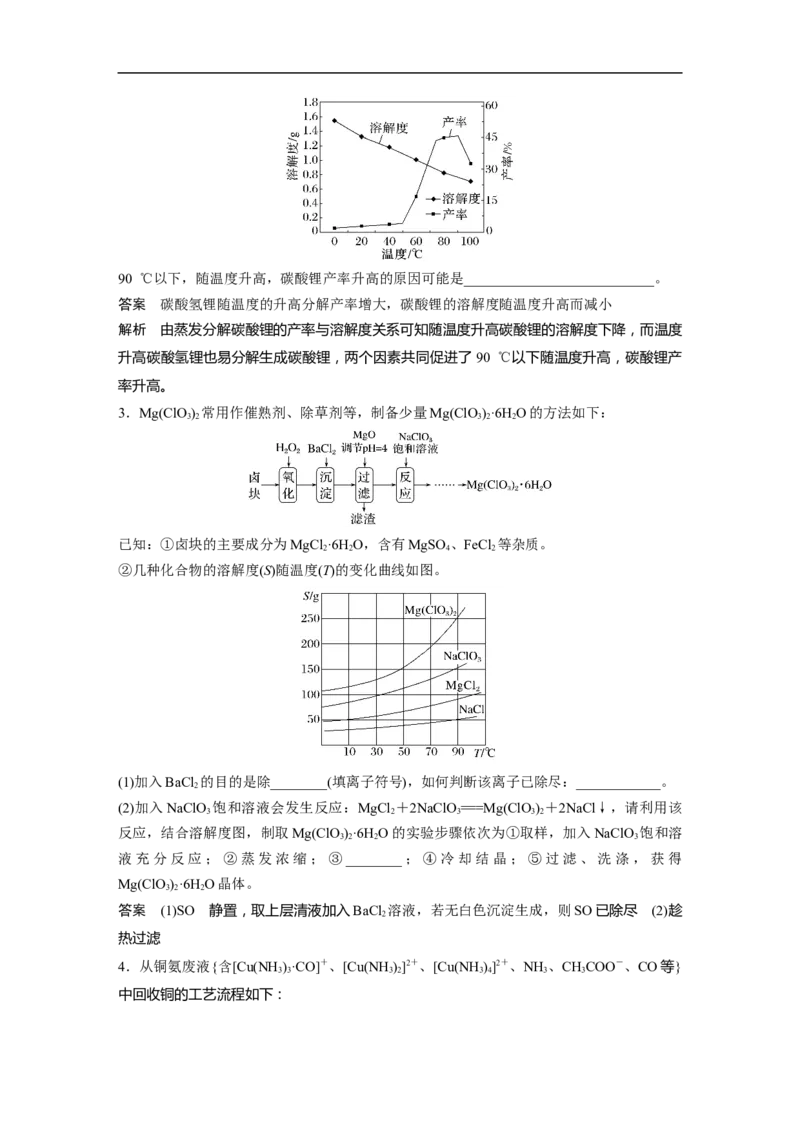
已知在不同温度下蒸发分解碳酸锂的产率与溶解度关系如图:90 ℃以下,随温度升高,碳酸锂产率升高的原因可能是___________________________。
答案 碳酸氢锂随温度的升高分解产率增大,碳酸锂的溶解度随温度升高而减小
解析 由蒸发分解碳酸锂的产率与溶解度关系可知随温度升高碳酸锂的溶解度下降,而温度
升高碳酸氢锂也易分解生成碳酸锂,两个因素共同促进了 90 ℃以下随温度升高,碳酸锂产
率升高。
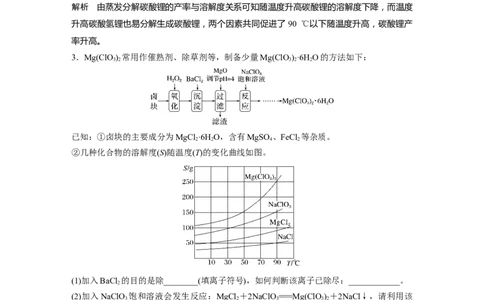
3.Mg(ClO) 常用作催熟剂、除草剂等,制备少量Mg(ClO)·6H O的方法如下:
3 2 3 2 2
已知:①卤块的主要成分为MgCl ·6H O,含有MgSO 、FeCl 等杂质。
2 2 4 2
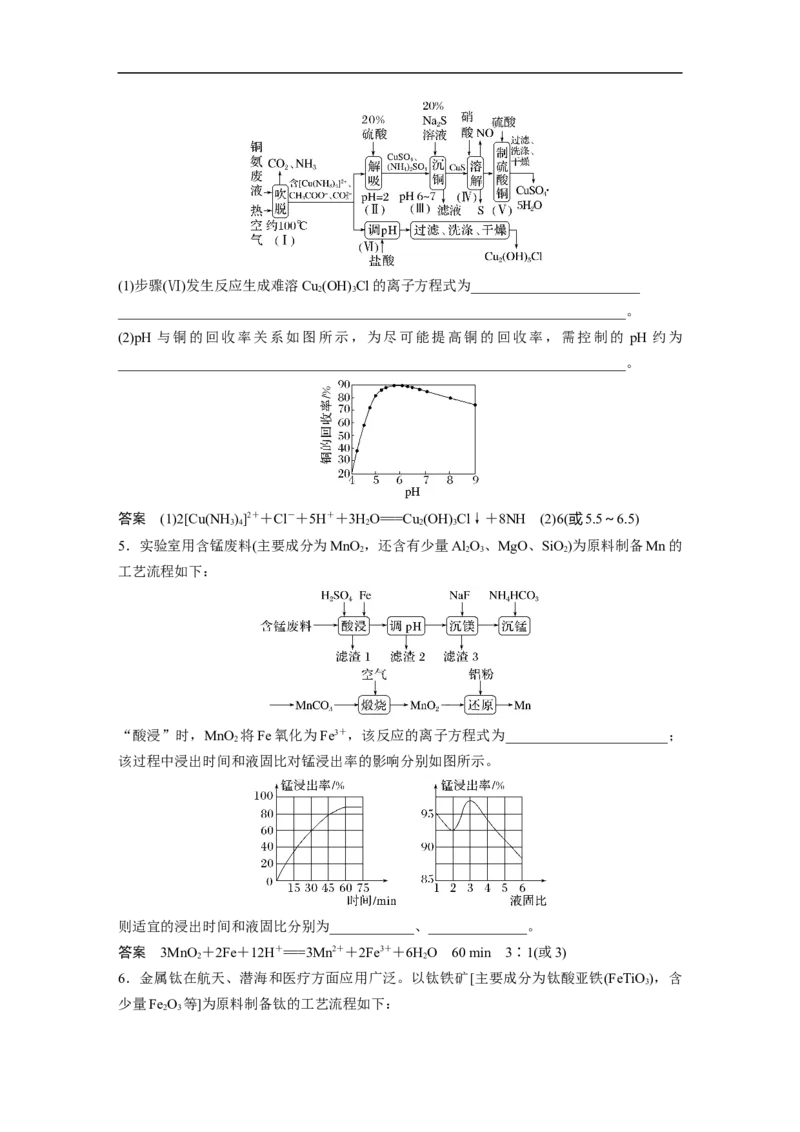
②几种化合物的溶解度(S)随温度(T)的变化曲线如图。
(1)加入BaCl 的目的是除________(填离子符号),如何判断该离子已除尽:____________。
2
(2)加入NaClO 饱和溶液会发生反应:MgCl +2NaClO===Mg(ClO) +2NaCl↓,请利用该
3 2 3 3 2
反应,结合溶解度图,制取Mg(ClO)·6H O的实验步骤依次为①取样,加入NaClO 饱和溶
3 2 2 3
液充分反应;②蒸发浓缩;③________;④冷却结晶;⑤过滤、洗涤,获得
Mg(ClO)·6H O晶体。
3 2 2
答案 (1)SO 静置,取上层清液加入BaCl 溶液,若无白色沉淀生成,则SO已除尽 (2)趁
2
热过滤
4.从铜氨废液{含[Cu(NH )·CO]+、[Cu(NH )]2+、[Cu(NH )]2+、NH 、CHCOO-、CO等}
3 3 3 2 3 4 3 3
中回收铜的工艺流程如下:(1)步骤(Ⅵ)发生反应生成难溶Cu (OH) Cl的离子方程式为________________________
2 3
________________________________________________________________________。
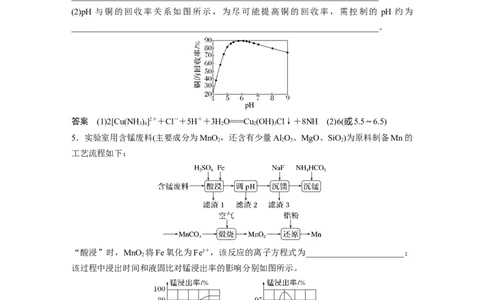
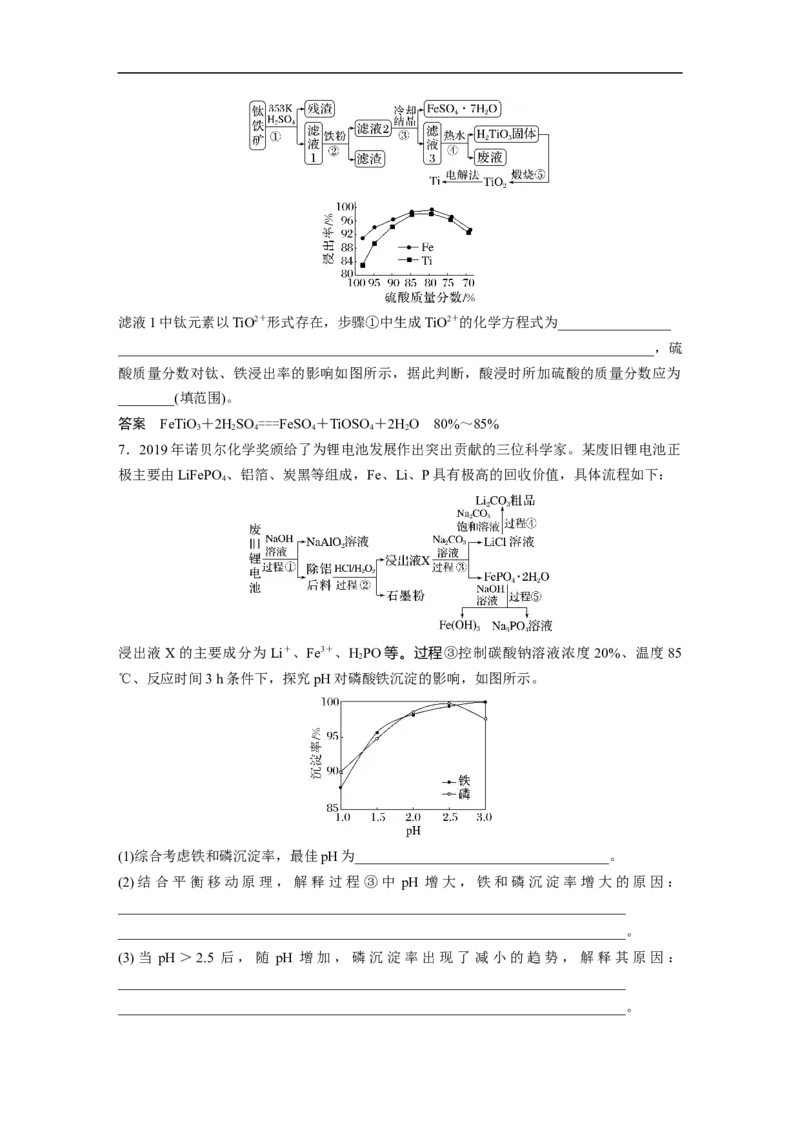
(2)pH 与铜的回收率关系如图所示,为尽可能提高铜的回收率,需控制的 pH 约为
________________________________________________________________________。
答案 (1)2[Cu(NH )]2++Cl-+5H++3HO===Cu (OH) Cl↓+8NH (2)6(或5.5~6.5)
3 4 2 2 3
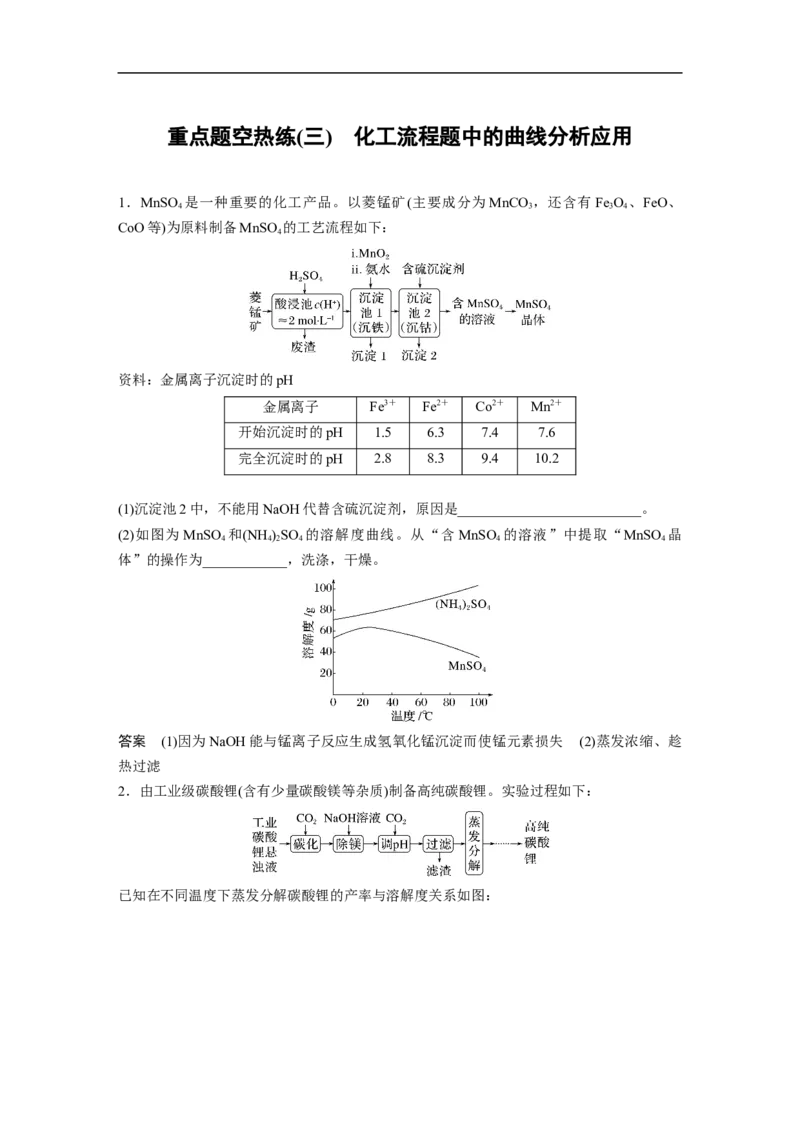
5.实验室用含锰废料(主要成分为MnO ,还含有少量Al O、MgO、SiO)为原料制备Mn的
2 2 3 2
工艺流程如下:
“酸浸”时,MnO 将Fe氧化为Fe3+,该反应的离子方程式为_______________________;
2
该过程中浸出时间和液固比对锰浸出率的影响分别如图所示。
则适宜的浸出时间和液固比分别为____________、______________。
答案 3MnO +2Fe+12H+===3Mn2++2Fe3++6HO 60 min 3∶1(或3)
2 2
6.金属钛在航天、潜海和医疗方面应用广泛。以钛铁矿[主要成分为钛酸亚铁(FeTiO),含
3
少量Fe O 等]为原料制备钛的工艺流程如下:
2 3滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为________________
____________________________________________________________________________,硫
酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸的质量分数应为
________(填范围)。
答案 FeTiO+2HSO ===FeSO +TiOSO +2HO 80%~85%
3 2 4 4 4 2
7.2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正
极主要由LiFePO 、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下:
4
浸出液X的主要成分为Li+、Fe3+、HPO等。过程③控制碳酸钠溶液浓度20%、温度85
2
℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。
(1)综合考虑铁和磷沉淀率,最佳pH为____________________________________。
(2)结合平衡移动原理,解释过程 ③中 pH 增大,铁和磷沉淀率增大的原因:
________________________________________________________________________
________________________________________________________________________。
(3)当 pH>2.5 后,随 pH 增加,磷沉淀率出现了减小的趋势,解释其原因:
________________________________________________________________________
________________________________________________________________________。答案 (1)2.5 (2)H POHPO+H+,HPOPO+H+,加入NaCO 后,CO结合H+使
2 2 3
c(H+)减小,促进上述电离平衡正向移动,c(PO)增大,与Fe3+结合形成磷酸铁沉淀 (3)pH
>2.5时,沉淀中的磷酸铁会有部分开始转变生成Fe(OH) ,使得部分PO释放,导致磷沉淀
3
率下降
解析 (3)已知FePO (s)Fe3+(aq)+ PO(aq),当pH>2.5后,随pH增大,溶液中c(OH-)
4
增大,Fe3+开始转变生成Fe(OH) ,促进溶解平衡正向移动,使得部分PO释放,导致磷沉
3
淀率下降。