文档内容
(二)化工工艺流程
1.锂辉石矿(主要含有LiAlSi O ,还含有少量Fe2+、Mg2+)是主要锂源,现利用锂辉石矿制
2 6
取LiBr,用于高级电池的电解质、医用镇静剂等。工艺流程如下:
(1)锂辉石中主要成分LiAlSi O 改写为氧化物形式为__________________。
2 6
(2)工业选择石灰石进行“中和”而不选择纯碱主要考虑的是__________;在“除镁除铁(调
节pH≈11)”步骤中得到的滤渣中含铁成分是__________;写出“除铝”所发生反应的离子
方程式:________________________________________________________________________
________________________________________________________________________。
(3)碳酸锂在水中的溶解度较小,其-lg K 与温度t关系如下表:
sp
t/℃ 0 10 20 30 40 50 60 70 80
-lg K 1.44 1.53 1.63 1.71 1.80 1.90 2.00 2.21 2.43
sp
由此可知碳酸锂在水中的溶解热效应 ΔH______(填“>”或“<”)0;加入纯碱试剂进行
“沉锂”后,依次进行保温静置、________(填序号)。
①洗涤 ②趁热过滤 ③离心分离
(4)在“合成”中,碳酸锂粉末分次少量加入冰水中溶解,再加入尿素搅拌得到“料液”,
料液中徐徐加入溴,控制pH=5.0,反应生成LiBr和两种无色无味气体,写出化学方程式:
________________________________________________________________________
________________________________________________________________________。
答案 (1)Li O·Al O·4SiO (2)石灰石价廉易得 Fe(OH) AlO+H++HO===Al(OH) ↓
2 2 3 2 3 2 3
(3)< ③②① (4)3Li CO+CO(NH)+3Br ===6LiBr+4CO↑+N↑+2HO
2 3 2 2 2 2 2 2
解析 (2)工业选择石灰石进行“中和”而不选择纯碱是因为石灰石价廉易得,生产成本低;
“除镁除铁”发生的反应为加入氢氧化钠溶液将溶液中铁离子、镁离子转化为氢氧化铁、氢
氧化镁沉淀,铝离子转化为偏铝酸根离子;除铝发生的反应为加入适量稀硫酸,将溶液中的
偏铝酸根离子转化为氢氧化铝沉淀,反应的离子方程式为AlO+H++HO===Al(OH) ↓。
2 3
(3)由表格数据可知,碳酸锂的溶解度随着温度的升高而减小,说明碳酸锂在水中的溶解为
放热过程,热效应ΔH<0;加入纯碱试剂进行沉锂后,为减少碳酸锂沉淀的损失,得到碳酸锂沉淀的操作为进行保温静置、离心分离、趁热过滤、洗涤。(4)由题意可知合成中发生的
反应为碳酸锂粉末在低温条件下与尿素和溴反应生成溴化锂、二氧化碳和氮气,反应的化学
方程式为3LiCO+CO(NH)+3Br ===6LiBr+4CO↑+N↑+2HO。
2 3 2 2 2 2 2 2
2.五氧化二钒(V O)广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼
2 5
用的催化剂等。从废钒催化剂(含有KSO 、VO 、VO 、SiO 、Fe O 、NiO等)中回收钒,
2 4 2 5 2 4 2 2 3
既能避免对环境的污染,又能节约宝贵的资源,回收工艺流程如下:
已知:①“酸浸”时VO 和VO 与稀硫酸反应分别生成VO和VO2+。
2 5 2 4
②溶液中VO与VO可相互转化:VO+HOVO+2H+,且NH VO 为沉淀。
2 4 3
(1)“酸浸”前,需对废钒催化剂进行粉碎预处理,其目的是______________________
________________________________________________________________________。
(2)“还原转化”中加入FeSO 的目的是将VO转化为VO2+,写出反应的离子方程式:
4
________________________________________________________________________
________________________________________________________________________。
(3)加入HO 的目的是将过量的Fe2+转化为Fe3+。“氧化1”后,溶液中含有的金属阳离子
2 2
主要有Fe3+、Ni2+、VO2+,调节pH使离子沉淀,若溶液中c(Ni2+)=0.2 mol·L-1,则调节溶
液的pH最小值为________可使Fe3+沉淀完全(离子浓度≤1.0×10-5 mol·L-1时沉淀完全),
此时__________(填“有”或“无”)Ni(OH) 沉淀生成{假设溶液体积不变,lg 6≈0.8,
2
K [Fe(OH) ]=2.16×10-39,K [Ni(OH) ]=2×10-15}。
sp 3 sp 2
(4)“氧化2”过程中发生反应的离子方程式为__________________________________
________________________________________________________________________。
(5)“沉钒”时,通入氨气的作用是___________________________________________
________________________________________________________________________。
(6)若该废钒催化剂中VO 的含量为10%(原料中所有的钒已换算成VO)。取100 g待处理
2 5 2 5
样品,按照上述流程进行实验。当加入 150 mL 0.1 mol·L-1 KClO 溶液时,溶液中的钒元素
3
恰好完全反应,则该工艺中钒的回收率是________%。(假设与KClO 反应后的操作步骤中
3
钒元素无损失)
答案 (1)增大接触面积,加快反应速率 (2)VO+Fe2++2H+===VO2++Fe3++HO (3)2.8
2
无 (4)3H O+ClO+6VO2+===6VO+Cl-+6H+ (5)使VO+HOVO+2H+平衡正向移
2 2
动,将VO转化为VO,同时增大NH的浓度 (6)81.9
解析 向废钒催化剂中加入稀硫酸进行“酸浸”,VO 和VO 与稀硫酸反应分别生成VO
2 5 2 4和VO2+,Fe O 转化为Fe (SO ) ,NiO转化为NiSO ,过滤后的滤渣1主要成分为SiO ,加
2 3 2 4 3 4 2
入FeSO 将VO转化为VO2+,加入HO 将过量的Fe2+全部转化为Fe3+,便于后续“调
4 2 2
pH”步骤中除去,过滤得滤渣2,主要成分为Fe(OH) ,滤液2中加入萃取剂,“萃取”出
3
含钒微粒,再进行“反萃取”后得到含钒的溶液,加入HSO 和KClO 的目的是将低价态的
2 4 3
钒氧化为+5价的钒,经过加入NH Cl和NH 后析出NH VO 沉淀,最后“煅烧”得VO ,
4 3 4 3 2 5
据此分析解题。(3)当c(Fe3+)=1.0×10-5 mol·L-1时,根据K 的公式可知,溶液中的c(OH
sp
-)== mol·L-1=6×10-12 mol·L-1,计算可得pH=2.8,Q[Ni(OH) ]=c(Ni2+)·c2(OH-)=
2
0.2×(6.0×10-12)2=7.2×10-24,因为Q[Ni(OH) ]” “<”或 “=”)K FeO
2 4 2 4
(3)将NaFeO 粗品[含有Fe(OH) 、NaCl等杂质]转化为KFeO 的实验方案为
2 4 3 2 4
a.在不断搅拌下,将NaFeO 粗品溶于冷的3 mol·L-1 KOH溶液中,快速过滤除去Fe(OH)
2 4 3
等难溶的物质。
b.将滤液置于__________中,向滤液中加入________________,过滤。
c.对产品进行洗涤时使用乙醇,其目的是________________________________________
_____________________________________________________________________(答两点)。
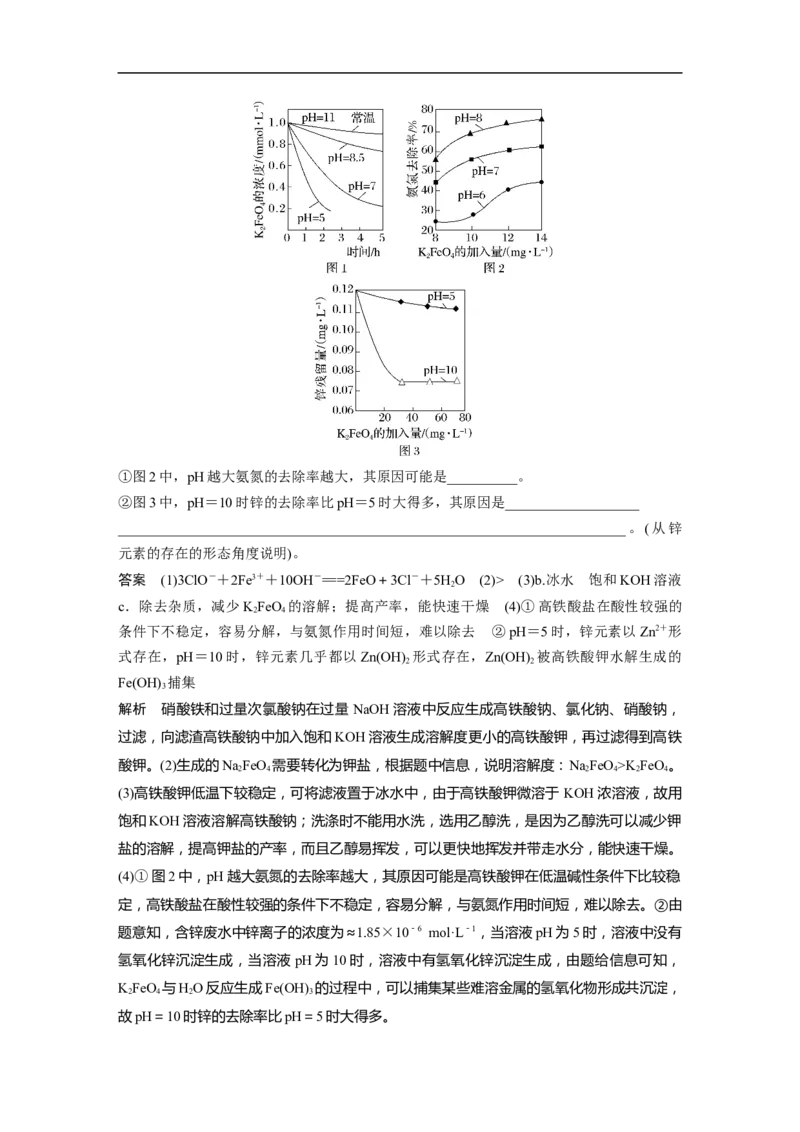
(4)高铁酸盐具有强氧化性,溶液pH越小氧化性越强,可用于除去废水中的氨、重金属等。
KFeO 的浓度与pH关系如图1所示;用KFeO 除去某氨氮(NH -N)废水,氨氮去除率与pH
2 4 2 4 3
关系如图2所示;用KFeO 处理Zn2+浓度为0.12 mg·L-1的含锌废水{K [Zn(OH) ]=1.2×10-
2 4 sp 2
17},锌残留量与pH关系如图3所示[已知: KFeO 与HO反应生成Fe(OH) 的过程中,可
2 4 2 3
以捕集某些难溶金属的氢氧化物形成共沉淀]。①图2中,pH越大氨氮的去除率越大,其原因可能是__________。
②图3中,pH=10时锌的去除率比pH=5时大得多,其原因是___________________
________________________________________________________________________。(从锌
元素的存在的形态角度说明)。
答案 (1)3ClO-+2Fe3++10OH-===2FeO+3Cl-+5HO (2)> (3)b.冰水 饱和KOH溶液
2
c.除去杂质,减少KFeO 的溶解;提高产率,能快速干燥 (4)①高铁酸盐在酸性较强的
2 4
条件下不稳定,容易分解,与氨氮作用时间短,难以除去 ②pH=5时,锌元素以Zn2+形
式存在,pH=10时,锌元素几乎都以Zn(OH) 形式存在,Zn(OH) 被高铁酸钾水解生成的
2 2
Fe(OH) 捕集
3
解析 硝酸铁和过量次氯酸钠在过量NaOH溶液中反应生成高铁酸钠、氯化钠、硝酸钠,
过滤,向滤渣高铁酸钠中加入饱和KOH溶液生成溶解度更小的高铁酸钾,再过滤得到高铁
酸钾。(2)生成的NaFeO 需要转化为钾盐,根据题中信息,说明溶解度:NaFeO>K FeO。
2 4 2 4 2 4
(3)高铁酸钾低温下较稳定,可将滤液置于冰水中,由于高铁酸钾微溶于 KOH浓溶液,故用
饱和KOH溶液溶解高铁酸钠;洗涤时不能用水洗,选用乙醇洗,是因为乙醇洗可以减少钾
盐的溶解,提高钾盐的产率,而且乙醇易挥发,可以更快地挥发并带走水分,能快速干燥。
(4)①图2中,pH越大氨氮的去除率越大,其原因可能是高铁酸钾在低温碱性条件下比较稳
定,高铁酸盐在酸性较强的条件下不稳定,容易分解,与氨氮作用时间短,难以除去。②由
题意知,含锌废水中锌离子的浓度为≈1.85×10-6 mol·L-1,当溶液pH为5时,溶液中没有
氢氧化锌沉淀生成,当溶液pH为10时,溶液中有氢氧化锌沉淀生成,由题给信息可知,
KFeO 与HO反应生成Fe(OH) 的过程中,可以捕集某些难溶金属的氢氧化物形成共沉淀,
2 4 2 3
故pH=10时锌的去除率比pH=5时大得多。4.铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿石[主要含Ru(CO) ,还含少量的
3 2
FeO、MgO、RuO、CaO、SiO]为原料制备钌(Ru)的流程如图。回答下列问题:
4 2
(1)Na Fe (SO )(OH) 中Fe的化合价为____________。
2 4 4 6 2
(2)“酸浸”时,NaSO 的作用是_____________________________________________。
2 3
“滤渣”的主要成分有SiO 和____________(填化学式)。“酸浸”中钌的浸出率与浸出温度、
2
pH的关系如图所示,“酸浸”的最佳条件是___________________________________。
(3)“除铁”的离子方程式为________________________________________________
________________________________________________________________________
(提示:1 mol NaClO 参与反应,转移6 mol电子)。
3
(4)从“滤液2”中可提取一种化肥,其电子式为____________。
(5)“灼烧”时Ar的作用是__________________________________________________
________________________________________________________________________。
(6)某工厂用10 t钌矿石[含8.84 t Ru(CO ) 、165 kg RuO ],最终制得3 636 kg Ru,则Ru的
3 2 4
产率为____________(结果保留三位有效数字)。
答案 (1)+3价 (2)溶解RuO CaSO 温度为65 ℃、pH为1.0 (3)6Na++12Fe2++
4 4
2ClO+18SO+6HO===3NaFe (SO )(OH) ↓+2Cl-+6OH- (4) (5)作
2 2 4 4 6 2
保护气,防止钌与空气中的氧气反应 (6)87.8%
解析 由题给流程可知,钌矿石中加稀硫酸和亚硫酸钠“酸浸”时,钌元素转化为硫酸钌,
氧化亚铁、氧化镁转化为硫酸亚铁、硫酸镁,氧化钙与稀硫酸反应生成硫酸钙,二氧化硅与
硫酸不反应,过滤得到含有二氧化硅、硫酸钙的滤渣和含有硫酸钌的滤液;向滤液中加入氯
酸钠溶液、碳酸钠溶液将铁元素转化为NaFe (SO )(OH) 沉淀,过滤,向滤液中加入氟化钠
2 4 4 6 2溶液将镁元素转化为氟化镁沉淀,过滤,向滤液中加入浓碳酸钠溶液将钌元素转化为碳酸钌
沉淀,碳酸钌溶于盐酸得到氯化钌,向氯化钌溶液中加入草酸铵溶液将氯化钌转化为草酸钌
沉淀,在氩气氛围中灼烧草酸钌制得钌。(3)由分析可知,加入氯酸钠溶液、碳酸钠溶液的
目的是将铁元素转化为NaFe (SO )(OH) 沉淀,反应的离子方程式为6Na++12Fe2++2ClO
2 4 4 6 2
+18SO+6HO===3NaFe (SO )(OH) ↓+2Cl-+6OH-。(5)灼烧时氩气的作用是作保护气,
2 2 4 4 6 2
否则反应得到的钌会被空气中的氧气氧化。(6)若10 t钌矿石最终制得3 636 kg钌,由钌原子
个数守恒可知,钌的产率为×100%≈87.8%。