文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题01
1.下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归为一类的是
A.泰山墨玉 B.龙山黑陶 C.齐国刀币 D.淄博琉璃
2.下列物质中属于耐高温酸性氧化物的是
A. CO B. SiO C. MgO D. Na O
2 2 2
3. 关于反应2NH OH+4Fe3+=NO↑+4Fe2++4H++HO,下列说法正确的是
2 2 2
A. 生成1molN O,转移4mol电子 B.NH OH是还原产物
2 2
C.NH OH既是氧化剂又是还原剂 D. 若设计成原电池,Fe2+为负极产物
2
4.下列反应的离子方程式不正确的是
A. Cl 通入氢氧化钠溶液:Cl+2OH-=Cl-+ClO-+HO
2 2 2
B. 氧化铝溶于氢氧化钠溶液:Al O+2OH-=2AlO+HO
2 3 2
C. 过量CO 通入饱和碳酸钠溶液:2Na++CO CO+HO =2NaHCO ↓
2 + 2 2 3
D. H SO 溶液中滴入氯化钙溶液:SO Ca2+=CaSO↓
2 3 + 3
5.材料是人类赖以生存和发展的物质基础,下列材料主要成分属于有机物的是
A. 石墨烯 B. 不锈钢 C. 石英光导纤维 D. 聚酯纤维
6.下列化学用语表示正确的是
A. H S分子的球棍模型:
2
B. AlCl 的价层电子对互斥模型:
3
C. KI的电子式:
D. CH CH(CH CH) 的名称:3−甲基戊烷
3 2 3 2
7.下列反应的离子方程式正确的是
A. 碘化亚铁溶液与等物质的量的氯气:2Fe2++2I-+2Cl=2Fe3++I+4Cl-
2 2
B. 向次氯酸钙溶液通入足量二氧化碳:ClO-+CO+HO=HClO+HCO
2 2
C. 铜与稀硝酸:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
D. 向硫化钠溶液通入足量二氧化硫:S2-+2SO +2HO=HS+2HSO
2 2 2
8.化学与生活密切相关,下列说法正确的是
A. 苯甲酸钠可作为食品防腐剂是由于其具有酸性B. 豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C. SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D. 维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
9.下列应用中涉及到氧化还原反应的是
A. 使用明矾对水进行净化 B. 雪天道路上撒盐融雪
C. 暖贴中的铁粉遇空气放热 D. 荧光指示牌被照发光
10.化学在文物的研究和修复中有重要作用。下列说法错误的是
A. 竹简的成分之一纤维素属于天然高分子
B. 龟甲的成分之一羟基磷灰石属于无机物
C. 古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
D. 古壁画颜料中所用的铁红,其成分为Fe O
2 3
11.【任务一】某小组研究NaCO 和NaHCO 的性质,实验如下:
2 3 3
现象
序号 操作
NaCO NaHCO
2 3 3
在两支试管中加入1g Na CO 或
2 3 温度由17.6℃变为 温度由17.6℃变为17.2℃;
1g NaHCO 固体,再加入5mL
① 3 23.2℃;放置至室温时, 放置至室温时,试管内有少
水,振荡;将温度计分别插入其
试管内无固体 量固体残留
中
室温时,分别向①所得溶液中滴
② 溶液变红 溶液微红
入2滴酚酞溶液
(1)室温下,NaCO 的溶解度大于NaHCO 的实验证据是___________________________。
2 3 3
(2)该实验不能说明NaCO 溶液的碱性强于NaHCO 溶液,理由是___________________。
2 3 3
【任务二】为进一步探究NaCO 和NaHCO 的性质,利用传感器继续做如下实验:
2 3 3编号 实验操作 实验数据
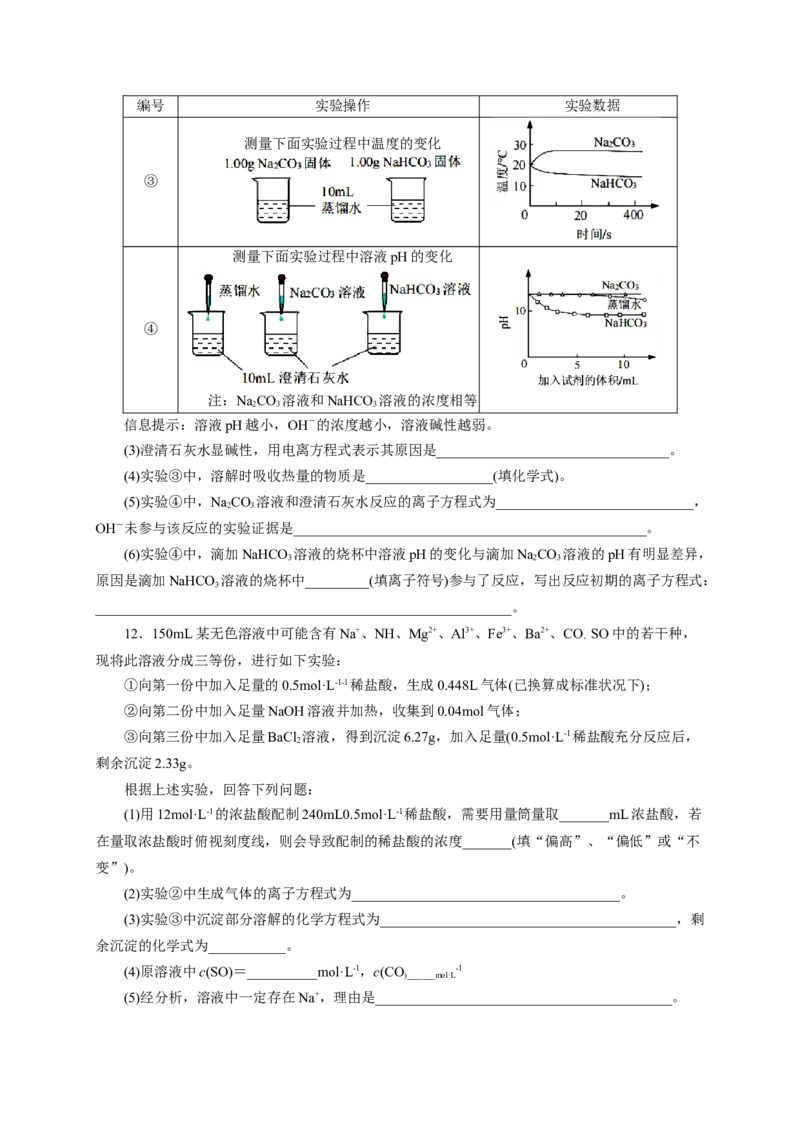
测量下面实验过程中温度的变化
③
测量下面实验过程中溶液pH的变化
④
注:NaCO 溶液和NaHCO 溶液的浓度相等
2 3 3
信息提示:溶液pH越小,OH-的浓度越小,溶液碱性越弱。
(3)澄清石灰水显碱性,用电离方程式表示其原因是_________________________________。
(4)实验③中,溶解时吸收热量的物质是__________________(填化学式)。
(5)实验④中,NaCO 溶液和澄清石灰水反应的离子方程式为____________________________,
2 3
OH-未参与该反应的实验证据是__________________________________________________。
(6)实验④中,滴加NaHCO 溶液的烧杯中溶液pH的变化与滴加NaCO 溶液的pH有明显差异,
3 2 3
原因是滴加NaHCO 溶液的烧杯中_________(填离子符号)参与了反应,写出反应初期的离子方程式:
3
___________________________________________________________。
12.150mL某无色溶液中可能含有Na+、NH、Mg2+、Al3+、Fe3+、Ba2+、CO SO中的若干种,
、
现将此溶液分成三等份,进行如下实验:
①向第一份中加入足量的0.5mol·L-1-1稀盐酸,生成0.448L气体(已换算成标准状况下);
②向第二份中加入足量NaOH溶液并加热,收集到0.04mol气体;
③向第三份中加入足量BaCl 溶液,得到沉淀6.27g,加入足量(0.5mol·L-1稀盐酸充分反应后,
2
剩余沉淀2.33g。
根据上述实验,回答下列问题:
(1)用12mol·L-1的浓盐酸配制240mL0.5mol·L-1稀盐酸,需要用量筒量取_______mL浓盐酸,若
在量取浓盐酸时俯视刻度线,则会导致配制的稀盐酸的浓度_______(填“偏高”、“偏低”或“不
变”)。
(2)实验②中生成气体的离子方程式为______________________________________。
(3)实验③中沉淀部分溶解的化学方程式为__________________________________________,剩
余沉淀的化学式为___________。
(4)原溶液中c(SO)=__________mol·L-1,c(CO -1
)_______mol·L
(5)经分析,溶液中一定存在Na+,理由是__________________________________________。