文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题05
1.祝融号火星车主体部件采用新型铝基碳化硅材料制造。铝基碳化硅材料属于
A.金属材料 B.无机非金属材料 C.有机合成材料 D.复合材料
答案:D
解析:铝基碳化硅材料是由铝和碳化硅复合而成的材料,属于符合材料;
2.CN-结合H+能力弱于CO
。下列化学反应表示正确的是
A.NaCN溶液通入少量的CO:CN-+CO+HO=HCN+HCO
2 2 2
B.Fe与HCN溶液反应:Fe+2HCN=Fe2++CN-+H↑
2
C.KCO 水解:CO HO HCO+OH-
2 3 + 2 2 3
D.Cl 处理含氰废水:5Cl+2CN-+4OH-=10Cl-+N↑+4H++2CO↑
2 2 2 2
答案:A
解析:A.因为CN-结合H+能力弱于CO HCO>HCN>HCO NaCN溶液通入少量的
,酸性: 2 3 ,所以
CO:CN-+CO+HO=HCN+HCO A正确;
2 2 2 ,
B.HCN酸性很弱,常温下很难与铁反应置换氢气,即使反应,亚铁离子和氢氰酸根离子会生
成配合离子,B错误;
C.CO CO HO HCO OH-,C错误;
水解是分步水解,主要为第一步水解: + 2 +
D.Cl 处理含氰废水,反应方程式为:5Cl+2CN-+8OH-=10Cl-+N↑+4HO+2CO↑,D
2 2 2 2 2
错误;
3.下列解释实验现象或用途的离子方程式书写不正确的是
A.用硫化钠处理含汞废水:S2-+Hg2+=HgS↓
B.将Cl 通入氢氧化钠溶液中制消毒液:Cl+2OH-=ClO-+Cl-+HO
2 2 2
C.FeCl 溶液腐蚀铜板:2Fe3++Cu=2Fe2++Cu2+
3
D.CaCO 溶于稀盐酸:CO 2H+=HO+CO↑
3 + 2 2
答案:D
解析:A.硫化钠和汞离子生成硫化汞,故离子方程式为S2-+Hg2+=HgS↓,故A正确;
B.氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,离子方程式为Cl+2OH-=ClO-+
2
Cl-+HO,故B正确;
2
C.氯化铁和铜反应生成氯化铜和氯化亚铁,离子方程式为2Fe3++Cu=2Fe2++Cu2+,故C正确;
D.碳酸钙为难溶盐,不能拆开写,故离子方程式为CaCO +2H+=Ca2++HO+CO↑,故D错
3 2 2
误;
4.下列指定反应的离子方程式正确的是
A.锅炉除垢中将CaSO 转化为CaCO :CaSO(s)+CO =CaCO (s)+SO(aq)
4 3 4 (aq) 3
B.硫酸酸化的淀粉碘化钾溶液久置后变蓝:2I-+O+4H+=I+2HO
2 2 2
C.用惰性电极电解饱和MgCl 溶液:2Cl-+2HO=====Cl↑+H↑+2OH-
2 2 2 2
D.CuSO 溶液中加入过量浓氨水:Cu2++2NH ∙HO=Cu(OH) ↓+2NH
4 3 2 2
答案:A解析:A.碳酸钙的溶度积比硫酸钙的溶度积更小,故CaSO 转化为CaCO 的离子方程式为:
4 3
CaSO(s)+CO (s)+SO(aq),A正确;
4 (aq)=CaCO3
B.硫酸酸化的淀粉碘化钾溶液久置后变蓝:4I−+O +4H+=2I +2H O,B错误;
2 2 2
C.用惰性电极电解饱和MgCl 溶液:Mg2++2Cl−+2H O=====Cl↑+H ↑+2Mg(OH) ↓,C错误;
2 2 2 2 2
D.CuSO 溶液中加入过量浓氨水:Cu2++4NH∙HO=[Cu(NH )]2++4H O,D错误;
4 3 2 3 4 2
5.下列化学变化不涉及氧化还原反应的是
A.含氯消毒剂用于环境消毒 B.水壶使用时间久后产生水垢
C.酸性重铬酸钾用于检验酒驾 D.谷物发酵酿醋
答案:B
解析:A.含氯消毒剂用于环境消毒,含氯消毒剂被还原,故不选A;
B.水壶使用时间久后产生水垢,发生反应Ca(HCO )===CaCO ↓+CO ↑+H O,没有元素化合
3 2 3 2 2
价改变,属于非氧化还原反应,故选B;
C.酸性重铬酸钾用于检验酒驾,重铬酸钾被乙醇还原,故不选C;
D.谷物发酵酿醋,淀粉水解为葡萄糖,葡萄糖被氧化为醋酸,故不选D;
6.下列反应的离子方程式书写正确的是
A.铜与浓硝酸反应:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
B.将Cl 通入石灰乳中制漂白粉:Cl +2OH-=ClO-+Cl-+HO
2 2 2
C.CaCO 溶于稀盐酸:CO 2H+=HO+CO↑
3 + 2 2
D.过量氨水与硫酸铝溶液反应:4NH ∙HO+Al3+=AlO+4NH+2HO
3 2 2
答案:A
解析:A.铜与浓硝酸反应生成二氧化氮和硝酸铜和水,A正确;
B.石灰乳主要成分Ca(OH) ,不可拆,B错误;
2
C.CaCO 不可拆,C错误;
3
D.NH ∙HO是弱碱,只能与Al3+生成Al(OH) ,不能生成偏铝酸盐,D错误;
3 2 3
7.下列解释实验事实的离子方程式书写正确的是
A.钠投入氯化铜溶液中:2Na+Cu2+=2Na++Cu
B.氯气通入水中:Cl+HO=2H++Cl-+ClO-
2 2
C.二氧化硫与酸性高锰酸钾溶液反应:5SO +2HO+2MnO 2Mn2++5SO+4H+
2 2 =
D.硫酸溶液中加入氢氧化钡溶液:Ba2++SO=BaSO↓
4
答案:C
解析:A.钠投入氯化铜溶液中,先和水反应生成氢氧化钠和氢气,氢氧化钠再和氯化铜反应
生成氢氧化铜沉淀和氯化钠,A错误;
B.氯气和水反应生成盐酸和次氯酸,盐酸能拆成离子形式,但次氯酸不能拆,B错误;
C.二氧化硫和高锰酸钾反应生成硫酸钾和硫酸锰和硫酸,反应的离子方程式为5SO +2HO+
2 2
2MnO 2Mn2++5SO+4H+,C正确;
=
D.硫酸溶液中加入氢氧化钡溶液:Ba2++2OH-+2H++SO=BaSO↓+2HO,D错误;
4 2
8.ClO 是一种常用的消毒剂,可通过反应2NaClO+SO +HSO =2ClO +2NaHSO 制取,下
2 3 2 2 4 2 4列有关说法正确的是
A.还原性:ClO >SO
2 2
B.每消耗1molSO ,转移4mol电子
2
C.氧化剂与还原剂的物质的量之比为2∶1
D.若该反应通过原电池来实现,则ClO 是负极产物
2
答案:C
解析:A.2NaClO+SO +HSO =2ClO +2NaHSO 反应中,SO 是还原剂、ClO 是还原产物,
3 2 2 4 2 4 2 2
还原性ClO <SO ,故A错误;
2 2
B.SO 中S元素化合价由+4升高为+6,每消耗1molSO ,转移2mol电子,故B错误;
2 2
C.NaClO 中Cl元素化合价降低,NaClO 是氧化剂,SO 中S元素化合价升高,SO 是还原剂,
3 3 2 2
氧化剂与还原剂的物质的量之比为2∶1,故C正确;
D.若该反应通过原电池来实现,负极发生氧化反应,正极发生还原反应,则ClO 是正极产物,
2
故D错误;
9.下列指定反应的离子方程式正确的是
A.用NaOH溶液吸收少量SO :OH-+SO =HSO
2 2
B.向稀FeSO 溶液中滴加稀硝酸:3Fe2++4H++NO 3Fe3++NO↑+2HO
4 = 2
C.向AlCl 溶液中加入过量氨水:Al3++4NH ∙HO=AlO+4NH+2HO
3 3 2 2
D.用盐酸、淀粉KI溶液检验含碘盐中的IO IO -+6H+=I+3HO
: +I 2 2
答案:B
解析:A.用NaOH溶液吸收少量SO ,反应产生NaSO 、HO,反应的离子方程式为:
2 2 3 2
SO +2OH-=SO O,A错误;
2 +H2
B.向稀FeSO 溶液中滴加稀硝酸,会发生氧化还原反应产生Fe3+、NO、HO,反应符合事实,
4 2
遵循物质的拆分原则,B正确;
C.向AlCl 溶液中加入过量氨水,反应产生Al(OH) 沉淀和NH Cl,反应的离子方程式为:
3 3 4
Al3++3NH·H O=Al(OH) ↓+3NH,C错误;
3 2 3
D.电子不守恒,电荷不守恒,反应的离子方程式应该为:IO -+6H+=3I+3HO,D错误;
+5I 2 2
10.含硫化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是
A.用NaSO 溶液吸收SO 废气:SO +HO=2HSO
2 3 2 +SO2 2
B.海水提溴工艺中用SO 还原Br :Br +SO +2HO=2H++SO+2HBr
2 2 2 2 2
C.用NaCO 溶液处理锅炉水垢中的CaSO:CaSO(s)+CO (s)+SO(aq)
2 3 4 4 (aq)=CaCO3
D.将S与NaSO 溶液混合加热制备NaSO:S+SO SO
2 3 2 2 3 === 2
答案:B
解析:A.用NaSO 溶液吸收SO 废气过程中,SO 和NaSO 溶液反应生成NaHSO,离子方
2 3 2 2 2 3 3
程式为:SO +HO=2HSO
+SO2 2 ,故A正确;
B.HBr是强酸,在离子方程式中要拆,故B错误;
C.CaCO 的溶解度小于CaSO,用NaCO 溶液处理锅炉水垢中的CaSO,CaSO 可以转化为
3 4 2 3 4 4CaCO ,离子方程式为:SO +HO=2HSO
3 +SO2 2 ,故C正确;
D.S与NaSO 溶液反应生成NaSO,离子方程式为:S+SO SO
2 3 2 2 3 === 2 ,故D正确;
11.SiCl 是生产多晶硅的副产物。利用SiCl 对废弃的锂电池正极材料LiCoO 进行氯化处理以
4 4 2
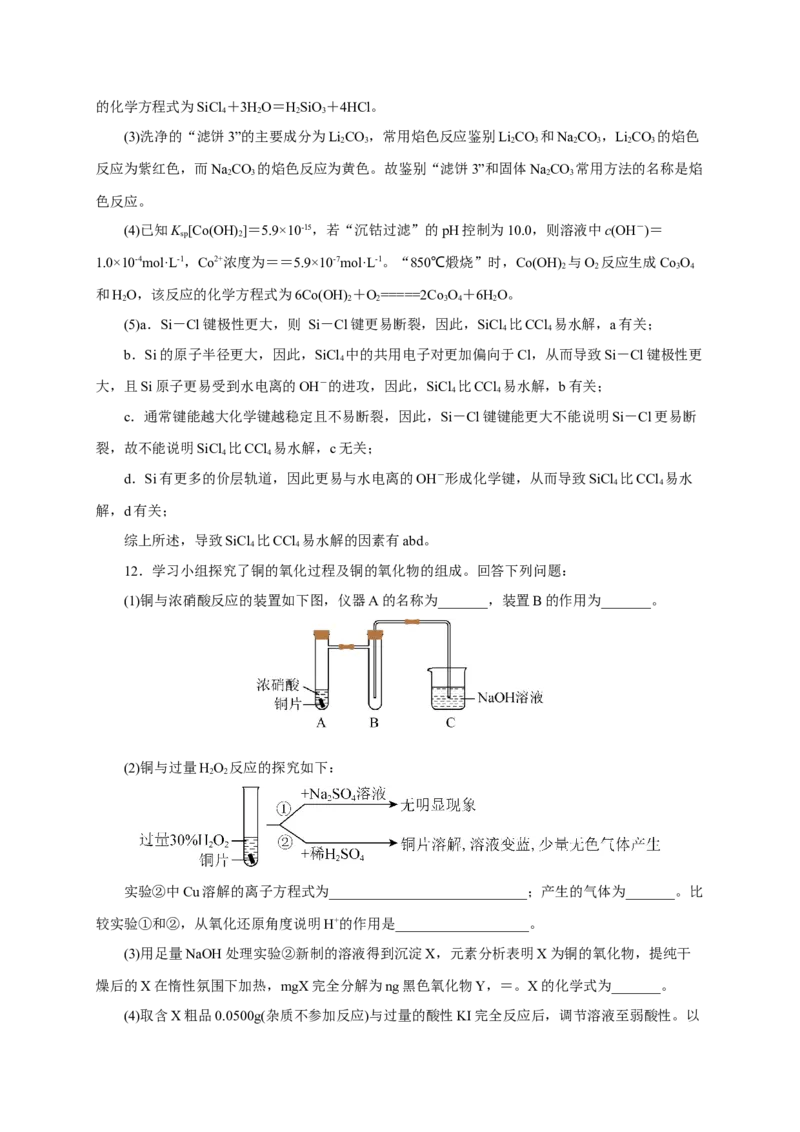
回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、CoCl 和SiO 的混合物,“500℃焙烧”后剩余的SiCl 应先除去,否则水浸时
2 2 4
会产生大量烟雾,用化学方程式表示其原因______________________________________________。
(3)鉴别洗净的“滤饼3”和固体NaCO 常用方法的名称是_______。
2 3
(4)已知K [Co(OH) ]=5.9×10-15,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+浓度为
sp 2
_______mol·L-1。“850℃煅烧”时的化学方程式为________________________________________。
(5)导致SiCl 比CCl 易水解的因素有_______(填标号)。
4 4
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
答案:(1) 4 Ⅷ (2) SiCl +3HO=HSiO+4HCl (3)焰色反应
4 2 2 3
(4)5.9×10-7 6Co(OH) +O=====2Co O+6HO (5)abd
2 2 3 4 2
解析:由流程和题中信息可知,LiCoO 粗品与SiCl 在500℃焙烧时生成氧气和烧渣,烧渣是
2 4
LiCl、CoCl 和SiO 的混合物;烧渣经水浸、过滤后得滤液1和滤饼1,滤饼1的主要成分是SiO 和
2 2 2
HSiO;滤液1用氢氧化钠溶液沉钴,过滤后得滤饼2[主要成分为Co(OH) ]和滤液2(主要溶质为
2 3 2
LiCl));滤饼2置于空气中在850℃煅烧得到Co O;滤液2经碳酸钠溶液沉锂,得到滤液3和滤
3 4
饼3,滤饼3为LiCO。
2 3
(1)Co是27号元素,其原子有4个电子层,其价电子排布为3d74s2,元素周期表第8、9、10三
个纵行合称第Ⅷ族,因此,其位于元素周期表第4周期、第Ⅷ族。
(2)“500℃焙烧”后剩余的SiCl 应先除去,否则水浸时会产生大量烟雾,由此可知,四氯化硅
4
与可水反应且能生成氯化氢和硅酸,故其原因是:SiCl 遇水剧烈水解,生成硅酸和氯化氢,该反应
4的化学方程式为SiCl +3HO=HSiO+4HCl。
4 2 2 3
(3)洗净的“滤饼3”的主要成分为LiCO,常用焰色反应鉴别LiCO 和NaCO,LiCO 的焰色
2 3 2 3 2 3 2 3
反应为紫红色,而NaCO 的焰色反应为黄色。故鉴别“滤饼3”和固体NaCO 常用方法的名称是焰
2 3 2 3
色反应。
(4)已知K [Co(OH) ]=5.9×10-15,若“沉钴过滤”的pH控制为10.0,则溶液中c(OH-)=
sp 2
1.0×10-4mol·L-1,Co2+浓度为==5.9×10-7mol·L-1。“850℃煅烧”时,Co(OH) 与O 反应生成Co O
2 2 3 4
和HO,该反应的化学方程式为6Co(OH) +O=====2Co O+6HO。
2 2 2 3 4 2
(5)a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此,SiCl 比CCl 易水解,a有关;
4 4
b.Si的原子半径更大,因此,SiCl 中的共用电子对更加偏向于Cl,从而导致Si-Cl键极性更
4
大,且Si原子更易受到水电离的OH-的进攻,因此,SiCl 比CCl 易水解,b有关;
4 4
c.通常键能越大化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断
裂,故不能说明SiCl 比CCl 易水解,c无关;
4 4
d.Si有更多的价层轨道,因此更易与水电离的OH-形成化学键,从而导致SiCl 比CCl 易水
4 4
解,d有关;
综上所述,导致SiCl 比CCl 易水解的因素有abd。
4 4
12.学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。
(2)铜与过量HO 反应的探究如下:
2 2
实验②中Cu溶解的离子方程式为____________________________;产生的气体为_______。比
较实验①和②,从氧化还原角度说明H+的作用是___________________。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干
燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,=。X的化学式为_______。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000mol·L-1NaSO 标准溶液滴定,滴定终点时消耗NaSO 标准溶液
2 2 3 2 2 3
15.00mL。(已知:2Cu2++4I-=CuI↓+I,I+2SO 2I-+SO
2 2 2 = 4 )标志滴定终点的现象是_______,粗品中X的相对含量为_______。
答案:(1)具支试管 防倒吸
(2)Cu+HO+2H+=Cu2++2HO O 既不是氧化剂,又不是还原剂
2 2 2 2
(3)CuO (4)溶液蓝色消失,且半分钟不恢复原来的颜色 72%
2
解析:(1)由图可知,仪器A的名称为具支试管;铜和浓硝酸反应生成硝酸铜和二氧化氮,其
中二氧化氮易溶于水,需要防倒吸,则装置B的作用为防倒吸;
(2)根据实验现象,铜片溶解,溶液变蓝,可知在酸性条件下铜和过氧化氢发生反应,生成硫酸
铜,离子方程式为:Cu+HO+2H+=Cu2++2HO;硫酸铜可以催化过氧化氢分解生成氧气,则产
2 2 2
生的气体为O;在铜和过氧化氢的反应过程中,氢元素的化合价没有发生变化,故从氧化还原角
2
度说明H+的作用是:既不是氧化剂,又不是还原剂;
(3)在该反应中铜的质量m(Cu)=n×=,因为=,则m(O)=n×+(m-n)=,则X的化学式中铜
原子和氧原子的物质的量之比为:==,则X为CuO;
2
(4)滴定结束的时候,单质碘消耗完,则标志滴定终点的现象是:溶液蓝色消失,且半分钟不恢
复原来的颜色;在CuO 中铜为+2价,氧为-1价,根据2Cu2++4I-=CuI↓+I,I+2SO 2I-+
2 2 2 2 =
SO ~2I~4SO )=×0.1mol/L×0.015L=0.000375mol,粗品中X的相对含量为
4 ,可以得到关系式:CuO2 2 2 ,则n(CuO2
×100%=72%。